Какие свойства у ртути

Ртуть в количестве 17 килограммов 322 грамма случайно найдена на дамбе реки Днестр между селом Карагаш и городом Слободзея, сообщил в пятницу местный телеканал со ссылкой на министерство госбезопасности (МГБ) непризнанной республики.
Ртуть (Hg) – химический элемент II группы периодической системы Менделеева, атомный номер 80, атомная масса 200,59; серебристо-белый тяжелый металл, жидкий при комнатной температуре.
Ртуть – один из семи металлов, известных с древнейших времен. Несмотря на то, что ртуть относится к рассеянным элементам и в природе ее очень мало (примерно столько же, сколько и серебра), она встречается в свободном состоянии в виде вкраплений в горные породы.
Кроме того, ее очень легко выделить при обжиге из основного минерала – сульфида (киновари). Пары ртути легко конденсируются в блестящую, как серебро, жидкость. Ее плотность настолько велика (13,6 г/куб. см), что ведро с ртутью обычный человек даже не оторвет от пола.
Ртуть широко применяется при изготовлении научных приборов (барометры, термометры, манометры, вакуумные насосы, нормальные элементы, полярографы, капиллярные электрометры и др.), в ртутных лампах, переключателях, выпрямителях; как жидкий катод в производстве едких щелочей и хлора электролизом, в качестве катализатора при синтезе уксусной кислоты, в металлургии для амальгамации золота и серебра, при изготовлении взрывчатых веществ; в медицине (каломель, сулема, ртутьорганические и другие соединения), в качестве пигмента (киноварь), в сельском хозяйстве в качестве протравителя семян и гербицида, а также как компонент краски морских судов (для борьбы с обрастанием их организмами).
В домашних условиях ртуть может оказаться в дверном звонке, лампах дневного света, медицинском термометре.
Металлическая ртуть высокотоксична для любых форм жизни. Основную опасность представляют пары ртути, выделение которых с открытых поверхностей возрастает при повышении температуры воздуха. При вдыхании ртуть попадает в кровь. В организме ртуть циркулирует в крови, соединяясь с белками; частично откладывается в печени, в почках, селезёнке, ткани мозга и др.
Токсическое действие связано с блокированием сульфгидрильных групп тканевых белков, нарушением деятельности головного мозга (в первую очередь, гипоталамуса). Из организма ртуть выводится через почки, кишечник, потовые железы и др.
Острые отравления ртутью и ее парами встречаются редко. При хронических отравлениях наблюдаются эмоциональная неустойчивость, раздражительность, снижение работоспособности, нарушение сна, дрожание пальцев рук, снижение обоняния, головные боли. Характерный признак отравления – появление по краю десен каймы сине-черного цвета; поражение десен (разрыхленность, кровоточивость) может привести к гингивиту и стоматиту.
При отравлениях органическими соединениями ртути (диэтилмеркурфосфатом, диэтил-ртутью, этилмеркурхлоридом) преобладают признаки одновременного поражения центральной нервной (энцефало-полиневрит) и сердечно-сосудистой систем, желудка, печени, почек.
Основная мера предосторожности при работе с ртутью и ее соединениями – исключение попадания ртути в организм через дыхательные пути или поверхность кожи.
Пролитую в помещении ртуть надо собирать самым тщательным образом. Особенно много паров образуется в том случае, если ртуть рассыпалась на множество мельчайших капелек, которые забились в различные щели, например, между плитками паркета. Все эти капельки необходимо собрать.
Лучше всего это сделать с помощью оловянной фольги, к которой ртуть легко прилипает, или же промытой азотной кислотой медной проволочкой. А те места, где ртуть еще могла бы задержаться, заливают 20%-ным раствором хлорного железа. Хорошая профилактическая мера против отравления парами ртути – тщательно и регулярно, в течение многих недель или даже месяцев, проветривать помещение, где была пролита ртуть.
Экологические последствия заражения парами ртути проявляются, прежде всего, в водной среде – подавляется жизнедеятельность одноклеточных морских водорослей и рыб, нарушается фотосинтез, ассимилируются нитраты, фосфаты, соединения аммония и т. д. Пары ртути фитотоксичны, ускоряют старение растений.
Ртуть является чрезвычайно важным металлом, который используется практически во всех производственных отраслях. Поэтому многие страны стремительно развивают ртутную промышленность и расширяют поиски ее месторождений. Какое место занимает применение ртути в современной промышленности – попробуем разобраться в этой статье.
Что представляет собой ртуть
Это химический элемент и единственный металл, который находится в жидком состоянии при нормальной температуре. Текучее вещество серого цвета – вот как выглядит ртуть, фото которой приведено ниже.

Затвердеть ртуть может только при очень низкой температуре. Средневековые алхимики никак не могли добиться отвердения этого металла. И только в 1759 году российские академики М. В. Ломоносов и И. А. Браун сумели сделать это. Дело в том, что в тот год в России были сильные морозы, и с помощью специальных смесей ученые понизили температуру до -56ºС. В таких условиях ртуть замерзла и стала похожа на металл. Спустя длительное время другие алхимики обнаружили у ртути сверхпроводимый эффект, когда понизили температуру до -270ºС.
Ртуть в истории человечества
Ртуть известна человеку еще с древних времен. Первые упоминания о ней встречаются в записях V века до н. э. Очень много исследовали ртуть в Индии и Китае. Самая древняя индийская школа по алхимии известна как «расаяна» или «путь ртути». Она занималась разработками лечебных препаратов и разных снадобий.
Древние люди находили ртуть в природе в виде киновари. Они использовали ее в качестве красного красителя. Название «киноварь» связано с древней легендой и переводится как «кровь дракона». Такая характеристика ртути связана с религиозными верованиями. В то время люди верили, что это кровь убитого в горах священного существа – дракона. Поэтому ртуть считали целебным веществом, способным лечить больных. Одним из таких лечебных средств была ртутная мазь.
Древние алхимики считали ртуть основой всех металлов и их жизненной силой. Они были убеждены, что из ртути и серы можно получить золото. Но после многочисленных опытов и экспериментов стало понятно, что ничего из этой идеи не выйдет. Сколько ученых погибло, пытаясь открыть формулу создания золота. И эти исследования продолжались до 30-х годов XX века, пока наука не начала стремительно развиваться. В результате применения радиоактивного распада, ученые получили из ртути стабильные изотопы золота, но их было очень мало. И цена такого металла очень высока.

Как добывают ртуть
Основным и практически единственным промышленным источником ртути является минерал киноварь. Он состоит на 86% из сульфида ртути, остальные составляющие – примеси других минералов. Обычно киноварь имеет вид сплошных выделений, богатых примесями, и внешне напоминает зерна неправильной формы. Редко встречаются сформированные кристаллы ромбоэдрического, бипирамидального облика. Иногда обнаруживаются двойники.

Металлическую ртуть из киновари получают путем нагрева в открытой трубке, которая обеспечивает контакт с кислородом. Во время нагревания маленькие капельки ртути стекают по холодным стенкам. Обычно рудные тела залегают на небольших глубинах и приурочены к кварцитам, известнякам, доломитам и сланцам. Самые крупные в мире месторождения ртути находятся в Испании, США, Югославии, Словении, Таджикистане, Кыргызстане. Большие кристаллы ртутной руды добывают в южной части Китая.
Основные свойства ртути
Этот минерал имеет уникальные свойства, которые сделали применение ртути в современной промышленности важным ее элементом. Ртуть считается ядовитым и опасным металлом. Но его физические и химические свойства во многих сферах человеческой деятельности незаменимы.
Физические свойства
Ртуть относится к диамагнетикам, так как может образовывать твердые сплавы с другими металлами и жидкие соединения – амальгамы. Температура затвердевания ртути составляет -38,83ºС, а кипит металл при 356,73 ºС. Испаряется она при комнатной температуре. Еще одна важная характеристика ртути – она диамагнитна. Это значит, что собрать жидкие шарики металла обычным магнитом невозможно.
Химические свойства
Как и благородные металлы, ртуть устойчива в сухом воздухе. Она взаимодействует с кислотами, солями, неметаллами. С водой, щелочами и неокисляющими кислотами ртуть не реагирует. При температуре выше 300ºС она вступает в реакцию с кислородом, образуя оксид ртути.
Применение ртути в современной промышленности
Еще в средние века жидкий металл активно применяли в медицине для амальгамирования и изготовления разных приборов. В наше время невозможно найти отрасль народного хозяйства, которая не использует ртуть. Свойства и применение этого минерала описаны учеными со всего мира в многочисленных научных трудах.
Так, ртуть используется в сельском хозяйстве для протравы семян. В химической промышленности ее применяют в качестве катализатора для получения из ацетилена уксусного альдегида. Использование ртутных катодов позволяет выделить из поваренной соли едкий натр и хлор.
Ртуть является незаменимым компонентом в производстве красок для подводной части морских судов. Дело в том, что обитающие в морской воде микроорганизмы прикрепляются к днищам судов и способствуют коррозии и износу металлических деталей. Содержащая в краске ртуть под воздействием морского хлора образует сулему, которая отравляет вредные бактерии.
Ртуть применяют даже в производстве фетра. Имеющиеся в ее составе соли отлично обезжиривают пух. Более безопасных заменителей, которые бы давали такой же эффект, пока не нашли. Также ртуть служит катализатором во время органического синтеза в процессе дубления кожи.
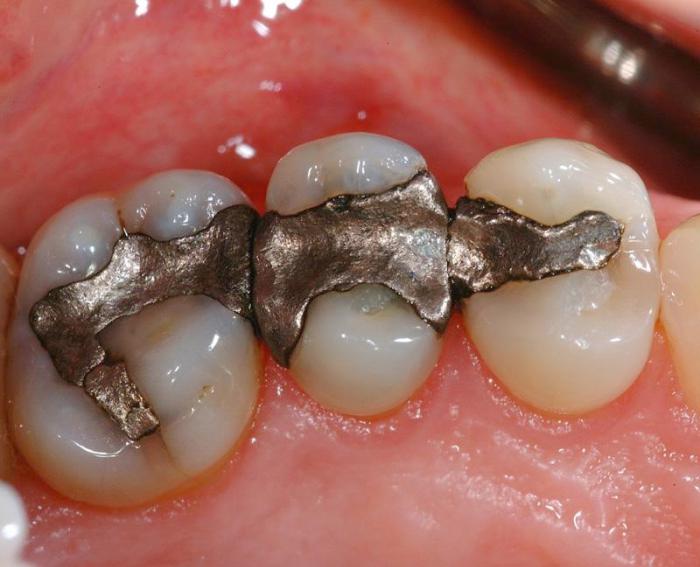
Как уже упоминалось, ртуть всегда использовалась в медицине. В наши дни на ее основе выпускают антисептические и мочегонные препараты. А ртутная мазь готовилась еще в древней Индии, рецепт которой сохранился до наших дней. Из-за свойства растворять другие металлы (олово, серебро) ртуть используют для изготовления зубных пломб.
Применение ртути в промышленности связано также с ее способностью испаряться при комнатной температуре. Например, для очистки нефти. Так, выпаривание металла способствует регулировке температуры нефтеперерабатывающих процессов.

Ртутные приборы
Физико-химические свойства являются главной причиной, по которой происходит применение ртути в разных приборах и машинах. Пары металла используются в ртутных турбинах. Такие установки особенно выгодны, когда в агрегате мало воды и охлаждение механизма происходит исключительно воздухом.
В электротехнике применяют выпрямители с жидким ртутным катодом. Они позволяют преобразовать трехфазный электрический ток в постоянный. Даже в астрономических целях применяют ртутные приборы – горизонты. Они имеют специальный сосуд с жидким металлом, поверхность которого служит зеркалом во время наблюдений за космосом. Также применение ртути в современной промышленности проявляется в производстве разных диффузионных насосов, прерывателей, термометров.
Во многих отраслях медицины используют ртутно-кварцевые лампы, которые облучают ультрафиолетовыми лучами. Также незаменимым медицинским инструментом является всем известный градусник для измерения температуры тела.
Сколько стоит ртуть: цена на мировом рынке
Цена на ртуть формируется по тому же принципу, что и на другие металлы. Так, стоимость этого минерала зависит от объема поставок и чистоты предлагаемой ртути. На мировом рынке цена на ртуть за последние полгода значительно упала. Так, если ее средняя цена в конце 2014 года составляла 75 долларов США/кг, то в марте 2015 года — 55 долларов США/кг. Но свободно купить жидкий металл практически невозможно, поскольку ртуть относится к химически-опасным веществам. Даже за утилизацию разлитой ртути необходимо заплатить определенную сумму.
Что касается изделий, которые содержат ртуть, их стоимость зависит от количества используемого металла и от других производственных издержек. Например, очень дешево стоит градусник ртутный. Цена в аптеках колеблется от 25 до 50 рублей.
Опасность ртути для здоровья
Несмотря на широкое применение ртути в промышленности, она считаются довольно опасным химическим веществом. По критериям вреда для жизни и здоровья ртуть относится к первому классу опасности. Обычно ртуть попадает в организм путем вдыхания ее паров, которые не имеют запаха. Именно ртутные испарения представляют наибольшую опасность.
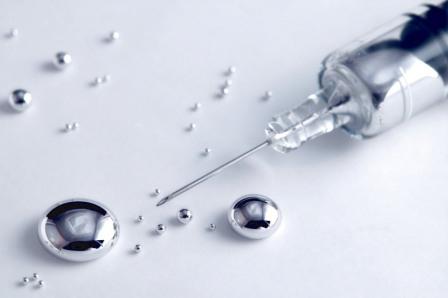
Чтобы вызвать тяжелое отравление и проблемы со здоровьем, достаточно воздействия небольшого количества минерала. Во время токсикации в наибольшей степени поражаются легкие, почки, иммунная, нервная, пищеварительная системы, глаза и кожа.
В зависимости от причин и характера отравления различают легкую, острую и хроническую формы. Легкая токсикация возникает при пищевом отравлении. После аварий на предприятиях химической промышленности или вследствие нарушения техники безопасности проявляется острая форма отравления. В этом случае у больного наблюдается снижение умственной активности, истощение, могут появляться судороги, потеря зрения, облысение и даже полный паралич. В тяжелых случаях острое отравление может привести к летальному исходу. Хроническое отравление развивается в результате постоянного контакта с ртутью и может проявляться долгое время после прекращения работы с ней. У людей с этой формой патологии повышается риск развития гипертонии, туберкулеза и атеросклероза. Бывают случаи, когда хроническая токсикация вызывает психические отклонения.
Особенно внимательно с ртутными приборами следует обращаться беременным женщинам. Пары ртути представляют большую угрозу для развития плода. Если в доме есть дети, лучше обычные ртутные термометры заменить электронными.
Утилизация ртутьсодержащих отходов
Широкое применение ртути способствует высокой концентрации ее паров в атмосфере крупных городов. Сейчас повсюду используют люминесцентные лампы, которые содержат от 30 до 300 мг жидкого металла. А в некоторых лампах его в несколько раз больше. Согласно статистике, ежегодно около 100 млн. таких ламп становятся непригодными и требуют переработки. Лишь небольшая их часть проходит специальную утилизацию, а остальные сразу отправляются на свалку, где из-за разрушения целостности стекла ртуть попадает в атмосферу.
Кроме того, ртуть применяется в производстве аккумуляторов и батарей, которые в основном никак не перерабатываются. Таким путем за год на свалку попадает около 40 тонн ртути. Эта цифра очень большая, поэтому проблема утилизации ртутьсодержащих предметов стоит очень остро. Бесконтрольное обращение с ртутными отходами, безответственное отношение к приборам, содержащим этот жидкий металл, создает угрозу здоровью и жизни людей. Всем известно, какие неприятности может принести обычный градусник ртутный. Цена неумелого обращения с ним может стоить даже жизни.

Сейчас правительства всех стран работают над вопросом переработки ртутьсодержащих отходов. С этой целью создаются специальные компании, которые занимаются сбором непригодных к использованию приборов и ртутных предметов. Они разделяют их на компоненты (цоколи, стекло, металл) и перерабатывают. Из каждого вида отходов формируются блоки, которые упаковываются в специальную тару (чехлы, полиэтиленовые пакеты, канистры) и доставляются на место переработки.
 Ртуть — минерал, природная металлическая ртуть. Переходный металл, при комнатной температуре представляющий собой тяжёлую серебристо-белую жидкость, пары которой чрезвычайно ядовиты. Ртуть — один из двух химических элементов (и единственный металл), простые вещества которых при нормальных условиях находятся в жидком агрегатном состоянии (второй такой элемент — бром). Иногда содержит примесь серебра и золота.
Ртуть — минерал, природная металлическая ртуть. Переходный металл, при комнатной температуре представляющий собой тяжёлую серебристо-белую жидкость, пары которой чрезвычайно ядовиты. Ртуть — один из двух химических элементов (и единственный металл), простые вещества которых при нормальных условиях находятся в жидком агрегатном состоянии (второй такой элемент — бром). Иногда содержит примесь серебра и золота.
СТРУКТУРА
Сингония тригональная, гексагонально-скаленоэдрическая (ниже -39°С).
СВОЙСТВА
 Цвет оловянно-белый. Блеск сильный металлический. Температура кипения 357 °C. Единственный жидкий минерал при обычной температуре. Затвердевает, приобретая кристаллическое состояние при −38°С. Плотность 13,55. На огне легко испаряется с образованием ядовитых паров. В древности вдыхание этих паров было единственным доступным средством лечения сифилиса (по принципу: если больной не умрёт, то поправится. Является диамагнетиком.
Цвет оловянно-белый. Блеск сильный металлический. Температура кипения 357 °C. Единственный жидкий минерал при обычной температуре. Затвердевает, приобретая кристаллическое состояние при −38°С. Плотность 13,55. На огне легко испаряется с образованием ядовитых паров. В древности вдыхание этих паров было единственным доступным средством лечения сифилиса (по принципу: если больной не умрёт, то поправится. Является диамагнетиком.
ЗАПАСЫ И ДОБЫЧА
 Ртуть — относительно редкий элемент в земной коре со средней концентрацией 83 мг/т. Однако ввиду того, что ртуть слабо связывается химически с наиболее распространёнными в земной коре элементами, ртутные руды могут быть очень концентрированными по сравнению с обычными породами. Наиболее богатые ртутью руды содержат до 2,5 % ртути. Основная форма нахождения ртути в природе — рассеянная, и только 0,02 % её заключено в месторождениях. Содержание ртути в различных типах изверженных пород близки между собой (около 100 мг/т). Из осадочных пород максимальные концентрации ртути установлены в глинистых сланцах (до 200 мг/т). В водах Мирового океана содержание ртути — 0,1 мкг/л. Важнейшей геохимической особенностью ртути является то, что среди других халькофильных элементов она обладает самым высоким потенциалом ионизации. Это определяет такие свойства ртути, как способность восстанавливаться до атомарной формы (самородной ртути), значительную химическую стойкость к кислороду и кислотам.
Ртуть — относительно редкий элемент в земной коре со средней концентрацией 83 мг/т. Однако ввиду того, что ртуть слабо связывается химически с наиболее распространёнными в земной коре элементами, ртутные руды могут быть очень концентрированными по сравнению с обычными породами. Наиболее богатые ртутью руды содержат до 2,5 % ртути. Основная форма нахождения ртути в природе — рассеянная, и только 0,02 % её заключено в месторождениях. Содержание ртути в различных типах изверженных пород близки между собой (около 100 мг/т). Из осадочных пород максимальные концентрации ртути установлены в глинистых сланцах (до 200 мг/т). В водах Мирового океана содержание ртути — 0,1 мкг/л. Важнейшей геохимической особенностью ртути является то, что среди других халькофильных элементов она обладает самым высоким потенциалом ионизации. Это определяет такие свойства ртути, как способность восстанавливаться до атомарной формы (самородной ртути), значительную химическую стойкость к кислороду и кислотам.
Одно из крупнейших в мире ртутных месторождений находится в Испании (Альмаден). Известны месторождения ртути на Кавказе (Дагестан, Армения), в Таджикистане, Словении, Киргизии (Хайдаркан — Айдаркен) Украине (Горловка, Никитовский ртутный комбинат).
В России находятся 23 месторождения ртути, промышленные запасы составляют 15,6 тыс. тонн (на 2002 год), из них крупнейшие разведаны на Чукотке — Западно-Палянское и Тамватнейское.
Ртуть получают обжигом киновари (сульфида ртути(II)) или металлотермическим методом. Пары ртути конденсируют и собирают. Этот способ применяли ещё алхимики древности.
ПРОИСХОЖДЕНИЕ
 Ртуть присутствует в большинстве сульфидных минералов. Особенно высокие её содержания (до тысячных и сотых долей процента) устанавливаются в блёклых рудах, антимонитах, сфалеритах и реальгарах. Близость ионных радиусов двухвалентной ртути и кальция, одновалентной ртути и бария определяет их изоморфизм во флюоритах и баритах. В киновари и метациннабарите сера иногда замещается селеном или теллуром; содержание селена часто составляет сотые и десятые доли процента. Известны крайне редкие селениды ртути — тиманит (HgSe) и онофрит (смесь тиманита и сфалерита).
Ртуть присутствует в большинстве сульфидных минералов. Особенно высокие её содержания (до тысячных и сотых долей процента) устанавливаются в блёклых рудах, антимонитах, сфалеритах и реальгарах. Близость ионных радиусов двухвалентной ртути и кальция, одновалентной ртути и бария определяет их изоморфизм во флюоритах и баритах. В киновари и метациннабарите сера иногда замещается селеном или теллуром; содержание селена часто составляет сотые и десятые доли процента. Известны крайне редкие селениды ртути — тиманит (HgSe) и онофрит (смесь тиманита и сфалерита).
ПРИМЕНЕНИЕ
 Ртуть используется как рабочее тело в ртутных термометрах (особенно высокоточных), так как обладает довольно широким диапазоном, в котором находится в жидком состоянии, её коэффициент термического расширения почти не зависит от температуры и обладает сравнительно малой теплоёмкостью. Сплав ртути с таллием используется для низкотемпературных термометров.
Ртуть используется как рабочее тело в ртутных термометрах (особенно высокоточных), так как обладает довольно широким диапазоном, в котором находится в жидком состоянии, её коэффициент термического расширения почти не зависит от температуры и обладает сравнительно малой теплоёмкостью. Сплав ртути с таллием используется для низкотемпературных термометров.
Парами ртути заполняют люминесцентные лампы, поскольку пары светятся в тлеющем разряде. В спектре испускания паров ртути много ультрафиолетового света и, чтобы преобразовать его в видимый, стекло люминесцентных ламп изнутри покрывают люминофором. Без люминофора ртутные лампы являются источником жёсткого ультрафиолета (254 нм), в каковом качестве и используются. Такие лампы делают из кварцевого стекла, пропускающего ультрафиолет, поэтому они называются кварцевыми.
Ртуть и сплавы на её основе используются в герметичных выключателях, включающихся при определённом положении.
Ртуть используется в датчиках положения.
Иодид ртути(I) используется как полупроводниковый детектор радиоактивного излучения.
Фульминат ртути(II) («гремучая ртуть») издавна применяется в качестве инициирующего ВВ (Детонаторы).
Бромид ртути(I) применяется при термохимическом разложении воды на водород и кислород (атомно-водородная энергетика).
Перспективно использование ртути в сплавах с цезием в качестве высокоэффективного рабочего тела в ионных двигателях.
До середины 20 века ртуть широко применялась в барометрах, манометрах и сфигмоманометрах (отсюда традиция измерять давление в миллиметрах ртутного столба).
Соединения ртути использовались в шляпном производстве для выделки фетра.
Ртуть (англ. Mercury) — Hg
| Молекулярный вес | 200.59 г/моль |
| Происхождение названия | от латинского алхимического названия этого элемента hydrargyrum (от др.-греч. ὕδωρ «вода» и ἄργυρος «серебро») |
| IMA статус | действителен, описан впервые до 1959 (до IMA) |
КЛАССИФИКАЦИЯ
| Strunz (8-ое издание) | 1/A.02-10 |
| Nickel-Strunz (10-ое издание) | 1.AD.05 |
| Dana (7-ое издание) | 1.1.10.1 |
| Dana (8-ое издание) | 1.1.7.1 | Hey’s CIM Ref | 1.12 |
ФИЗИЧЕСКИЕ СВОЙСТВА
| Цвет минерала | оловянный белый |
| Цвет черты | не может быть взята |
| Прозрачность | непрозрачный |
| Блеск | металлический |
| Спайность | нет |
| Твердость (шкала Мооса) | не может быть измерена |
| Излом | нет |
| Плотность (измеренная) | 13.596 г/см3 |
| Радиоактивность (GRapi) | |
| Магнетизм | диамагнетик |
ОПТИЧЕСКИЕ СВОЙСТВА
| Люминесценция в ультрафиолетовом излучении | не флюоресцентный |
КРИСТАЛЛОГРАФИЧЕСКИЕ СВОЙСТВА
| Точечная группа | 3m (3 2/m) — гексагональная-скаленоэдрическая |
| Пространственная группа | R3m |
| Сингония | тригональная |
| Параметры ячейки | a = 3.463Å, c = 6.706Å |
| Морфология | жидкие глобулы или сферы |
mineralpro.ru
04.08.2016
