Свойства каких химических элементов были предсказаны менделеевым
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 11 июля 2019;
проверки требуют 4 правки.
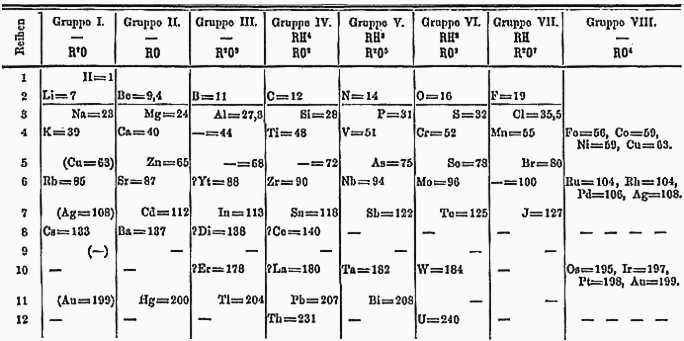
Периодическая система Д. И. Менделеева (1871 год)
В 1869 году Дмитрий Иванович Менделеев опубликовал Периодическую таблицу элементов, в которой химические элементы были расположены в соответствии с наличием у них сходных свойств в порядке возрастания атомного веса[1].
В отличие от работ предшественников Менделеев исходил из допущения существования еще не открытых элементов на основе периодического изменения физических и химических свойств известных элементов. Им были оставлены в таблице пустые ячейки для ещё не открытых элементов и предсказаны их свойства. Чтобы дать предсказанным элементам «временные» названия, Менделеев использовал приставки «эка», «дви» и «три» (от санскритских слов «один», «два» и «три»), в зависимости от того, на сколько позиций вниз от уже открытого элемента с похожими свойствами находился предсказанный элемент. Так, германий до своего открытия в 1886 году носил название «экасилиций», а рений, открытый в 1926 году, назывался «двимарганец».
Первоначальные предсказания (1869—1870 годы)[править | править код]
Уже в первом варианте Периодической таблицы, опубликованном Д. И. Менделеевым в 1869 году, включено больше элементов, чем их было открыто на тот момент. В нём оставлены четыре свободные ячейки для еще неизвестных элементов и указаны их атомные веса (в «паях», близких по значению к массе атома водорода).
Развивая в 1869—1871 годах идеи периодичности, Д. И. Менделеев ввёл понятие о месте элемента в периодической системе как совокупности его свойств в сопоставлении со свойствами других элементов. Для предсказания свойств простых веществ и соединений он исходил из того, что свойства каждого элемента являются промежуточными между соответствующими свойствами двух соседних элементов в группе периодической таблицы, двух соседних элементов в периоде и элементов по диагонали — так называемое «правило звезды». На этой основе, в частности, опираясь на результаты изучения последовательности изменения стеклообразующих оксидов, исправил значения атомных масс 9 элементов. Предсказал в 1870 году существование, вычислил атомные массы и описал свойства трёх ещё не открытых тогда элементов — «экаалюминия», «экабора» и «экасилиция»[2]. Затем предсказал существование ещё восьми элементов, в том числе «двителлура» — полония, «экаиода» — астата, «экамарганца» — технеция, «экацезия» — франция.
Предсказания Менделеева вызвали в научном мире скепсис и острую критику. Так, немецкий физикохимик Вильгельм Оствальд, будущий лауреат Нобелевской премии, утверждал, что открыт не закон, а принцип классификации «чего-то неопределенного». Роберт Бунзен, первооткрыватель рубидия и цезия, писал, что Менделеев увлекает химиков «в надуманный мир чистых абстракций», а Герман Кольбе в 1870 г. назвал работу Менделеева спекулятивной. Правота Менделеева была убедительно доказана, когда были открыты предсказанные им элементы: галлий (Поль Лекок де Буабодран, 1875), скандий (Ларс Нильсон, 1879) и германий (Клеменс Винклер, 1886) — соответственно экаалюминий, экабор и экасилиций.
Триумф Периодического закона[править | править код]
В 1875 г. французский химик Поль Эмиль Лекок де Буабодран открыл в минерале вюртците — сульфиде цинка ZnS — предсказанный Менделеевым «экаалюминий» и назвал его в честь своей родины галлием Ga (латинское название Франции — Галлия). Он писал: «Я думаю, нет необходимости настаивать на огромном значении подтверждения теоретических выводов господина Менделеева». Менделеев точно предсказал свойства галлия: его атомную массу, плотность металла, формулу оксида, хлорида, сульфата. Менделеев предугадал, что это будет очень легкоплавкий металл. Ниже в таблице сравниваются свойства, предсказанные Менделеевым, с действительными характеристиками галлия.
| Свойство | Экаалюминий | Галлий |
|---|---|---|
| Атомная масса | 68 | 69,72 |
| Плотность (г/см³) | 6,0 | 5,904 |
| Температура плавления (°C) | низкая | 29,78 |
| Формула оксида | Ea2O3 (плотность 5,5 г см−3, растворяется и в кислотах, и в основаниях) | Ga2O3 (плотность 5,88 г см−3, растворяется и в кислотах, и в основаниях) |
| Формула хлорида | Ea2Cl6 (летучий) | Ga2Cl6 (летучий) |
В 1879 г. шведский химик Ларс Нильсон открыл в сложном минерале гадолините скандий. Позже Пер Теодор Клеве доказал совпадение свойств предсказанного экабора и только что открытого скандия и известил об этом Менделеева. Менделеев предсказал для экабора атомную массу 44, а атомная масса скандия оказалась равна 44,955910. Нильсон писал: «Не остается никакого сомнения, что в скандии открыт экабор… Так подтверждаются нагляднейшим образом соображения русского химика, которые не только дали возможность предсказать существование скандия и галлия, но и предвидеть заранее их важнейшие свойства».
По поводу элемента экасилиция Менделеев писал: «Мне кажется, наиболее интересным из несомненно недостающих металлов будет тот, который принадлежит к IV группе аналогов углерода, а именно к III ряду. Это будет металл, следующий тотчас же за кремнием, и потому назовем его экасилицием». Германий был впервые выделен в 1886 году во Фрейбурге немецким химиком Клеменсом Винклером при анализе редкого минерала аргиродита. Его открытие оказалось лучшим на то время подтверждением теории Менделеева, поскольку германий по своим свойствам значительно резче отличается от соседних элементов, чем два предсказанных ранее элемента.
| Свойство | Экасилиций | Германий |
|---|---|---|
| Атомная масса | 72 | 72,61 |
| Плотность (г/см³) | 5,5 | 5,35 |
| Температура плавления (°C) | высокая | 947 |
| Цвет | серый | серый |
| Тип оксида | тугоплавкий диоксид | тугоплавкий диоксид |
| Плотность оксида (г/см³) | 4,7 | 4,7 |
| Реакция оксида | слабое основание | слабое основание |
| Температура кипения хлорида | ниже 100 °C | 86 °C (GeCl4) |
| Плотность хлорида (г/см³) | 1,9 | 1,9 |
Триумф предсказательной силы открытия Менделеева был настолько силён, что Винклер натолкнулся на неприятие со стороны некоторых химиков предложенного им названия «германий». Они стали обвинять Винклера в национализме и в присвоении открытия, которое сделал Менделеев, уже давший элементу имя «экасилиций». Обескураженный Винклер обратился за советом к самому Дмитрию Ивановичу. Тот объяснил, что именно первооткрыватель нового элемента должен дать ему название. Позже Винклер писал: «Едва ли можно найти иное более поразительное доказательство справедливости учения о периодичности, как во вновь открытом элементе. Это не просто подтверждение смелой теории, здесь мы видим очевидное расширение химического кругозора, мощный шаг в области познания».
Менделеев включил присланные ему портреты Лекока де Буабодрана, Нильсона и Винклера в общую рамку, озаглавив ее «Укрепители периодического закона». С конца 1880-х годов Периодический закон был окончательно признан в качестве одной из теоретических основ химии.
Никто из учёных, занимавшихся до Менделеева или одновременно с ним исследованиями соотношений между атомными весами и свойствами элементов, не смог сформулировать эту закономерность так ясно, как это сделал он. В частности, это относится к Дж. Ньюлендсу и Л. Мейеру. Предсказание ещё неизвестных элементов, их свойств и свойств их соединений является исключительно заслугой Д. И. Менделеева. …Наилучшим образом он смог применить свой метод горизонтальной, вертикальной и диагональной интерполяции в открытой им периодической системе для предсказания свойств…
— Анорганикум : В 2-х т. / [Блументаль Г., Энгельс З., Фиц И. и др.] ; Ред. Л. Кольдиц. — М. : Мир, 1984
Предсказания тяжёлых элементов[править | править код]
В 1871 году Менделеев предсказал существование элемента, расположенного между торием и ураном. Тридцатью годами позже, в 1900 году, Уильям Крукс выделил протактиний как неизвестную радиоактивную примесь в образце урана. Различные изотопы протактиния затем выделяли в Германии в 1913 и 1918 годах[3], но современное название элемент получил только в 1948 году.
Версия Периодической таблицы, изданная в 1869, предсказывала существование более тяжёлого аналога титана и циркония, но в 1871 году Менделеев поместил на это место лантан. Открытие в 1923 году гафния подтвердило первоначальное предположение Менделеева.
В период создания первых вариантов периодической таблицы свойства редкоземельных элементов были изучены плохо и недостоверно. Кроме того, для тяжелых элементов периодическое изменение свойств имеет более сложный характер: критерий аналогии атомов не мог помочь Менделееву, как в случае экабора, экаалюминия и экасилиция; в этом случае этот критерий был лишен по крайней мере предсказательной силы, что снижало его научную ценность. Это объясняет, почему предсказания Менделеева для более тяжёлых элементов сбылись не так точно, как для лёгких, и почему эти предсказания не так широко известны.
Гипотеза об трансводородных элементах[править | править код]
В 1902 году после открытия гелия и аргона Менделеев поместил их в нулевую группу таблицы[4]. Сомневаясь в правильности атомной теории, объясняющей закон постоянства состава, он не мог априори считать водород легчайшим из элементов и полагал, что ещё более лёгкий член химически инертной нулевой группы мог оказаться незамеченным. Существованием этого элемента Менделеев пытался объяснить радиоактивность.
Более тяжёлый из двух гипотетических трансводородных элементов Менделеев отождествлял с коронием, получившим название по ассоциации с необъяснённой спектральной линией солнечной короны. Ошибочная калибровка прибора дала длину волны 531,68 нм, которая позже была исправлена на 530,3 нм. Эту длину волны Гротриан и Эдлен в 1939 году соотнесли с линией железа[5].
Легчайшему из газов нулевой группы, первому в Периодической таблице, приписывалась теоретическая атомная масса между 5,3·10−11 и 9,6·10−7. Частицам этого газа, названного им ньютонием, Менделеев приписал кинетическую скорость порядка 2,5·106 м/с. Почти невесомые, частицы обоих этих газов, по Менделееву, должны были легко проходить через толщу материи, практически не вступая в химические реакции. Высокая подвижность и очень малая атомная масса трансводородных газов приводила бы к тому, что они могли быть очень разреженными, по внешним признакам оставаясь при этом плотными.
Позже Менделеев опубликовал теоретическую разработку об эфире. Книга, называвшаяся «Химическая концепция эфира», вышла в 1904 году, и в ней вновь содержалось упоминание о двух гипотетических инертных газах легче водорода, коронии и ньютонии[6]. Под «эфирным газом» Менделеев понимал межзвёздную атмосферу, состоящую из двух трансводородных газов с примесями других элементов и образовавшуюся в результате внутренних процессов, идущих на звёздах.
Примечания[править | править код]
- ↑ Kaji, Masanori. D.I.Mendeleev’s concept of chemical elements and The Principles of Chemistry (англ.) // Bulletin for the History of Chemistry (англ.)русск. : journal. — 2002. — Vol. 27, no. 1. — P. 4—16. Архивировано 17 декабря 2008 года.
- ↑ Менделеев Д. И. Естественная система элементов и применение её к указанию свойств неоткрытых элементов // Журнал Русского химического общества. — 1871. — Т. III. — С. 25—56. Архивировано 17 марта 2014 года.
- ↑ Emsley, John. Nature’s Building Blocks (англ.). — (Hardcover, First Edition). — Oxford University Press, 2001. — P. 347. — ISBN 0198503407.
- ↑ Менделеев, Д. Основы химии (рус.). — 7-е издание. — 1902.
- ↑ Swings, P. Edlén’s Identification of the Coronal Lines with Forbidden Lines of Fe X, XI, XIII, XIV, XV; Ni XII, XIII, XV, XVI; Ca XII, XIII, XV; a X, XIV (англ.) // The Astrophysical Journal : journal. — IOP Publishing, 1943. — July (vol. 98, no. 119). — P. 116—124. — doi:10.1086/144550. и [1]
- ↑ Менделеев, Д. Попытка химического понимания мирового эфира (рус.). — Санкт-Петербург, 1903.
Английский перевод:
Mendeléeff, D. (англ.)русск.. An Attempt Towards A Chemical Conception Of The Ether (англ.) / G. Kamensky (translator). — Longmans, Green & Co., 1904.
См. также
Bensaude-Vincent, Bernadette. L’éther, élément chimique: un essai malheureux de Mendéleev en 1904 (фр.) // British Journal for the History of Science (англ.)русск. : magazine. — 1982. — Vol. 15. — P. 183—188. — doi:10.1017/S0007087400019166.
Литература[править | править код]
- Scerri Eric. The Periodic Table: Its Story and Its Significance (англ.). — New York: Oxford University Press, 2007. — ISBN 0195305736.
Анонимный вопрос · 6 сентября 2018
2,1 K
Экабор (Eb), экаалюминий (Ea), экамарганец (Em) и экасилиций (Es) — эти 4 элемента были предсказаны Менделеевым, специально для них он оставил в пустые ячейки в своей таблице. Их свойства совпадали с некоторыми уже хорошо изученными элементами, однако отличались от них.
Когда в будущем произойдёт очередное научное открытие, которое изменит представление о мире?
phd @ princeton astro | haykh.github.io
Ну они происходят постоянно, просто вместо того, чтобы следить за ними, основная серая масса людей смотрит дурацкие фильмы с деГрассом Тайсоном или читает бесполезные книжки Хокинга с красивыми картинками и «объяснениями на пальцах» вместо того, чтобы реально сесть и потратить время, попытавшись разобраться в том, что на самом деле происходит в науке.
Давайте посмотрим.
Всего лишь каких-то 20 лет назад люди доказали, что наша Вселенная расширяется с ускорением. Из этого следовало что 70% энергии во Вселенной имеют абсолютно нематериальную природу и никак не объясняется никакой из существующих гипотез.
15 лет назад появились первые серьёзные предпосылки (а спустя несколько лет и очень точные доказательства) того, что у нейтрино есть масса. Это противоречило мнению большинства физиков за последние 70 лет.
За последние 5-10 лет было огромное количество событий космических лучей и внегалактических нейтрино (в том числе на IceCube) ультравысоких энергий (до сотен EeV). Более-менее понятно, что они ускоряются в активных ядрах галактик, но эти энергии никак не вписываются ни в какие теории ускорения.
За последние годы открыли такое количество экзотических астрофизических объектов, что вам даже и не снилось: тут вам и объекты со сверх-эддингтоновской светимостью, и аномальные x-ray пульсары (магнитары) с рекордно высокими магнитными полями (1e+15 Г), и экзопланету с огромными кольцевыми системами, и древние галактики, образовавшиеся задолго до периода, когда по идее должны были образовываться галактики и т.д. Каждое такое открытие просто диаметрально переворачивает любые существующие астрофизические теории. Но большинство их как-то даже не замечает.
Всего каких-то 6 лет назад группа Fermi/LAT нашла огромные «пузыри» излучающие в гамма и жестком рентгене прямо над нашей галактикой. Природа их до сих пор не ясна, но предварительно это означает, что наша чёрная дыра в центре Млечного Пути до сих пор активна.
Из будущих открытий, которые нас ожидают в ближайшие годы.
Есть инсайдерская информация, что в LHC есть статистически значимый двухфотонный пик на энергии 750 ГэВ (будет объявлено точно в августе). Вот об этом уже много где спекулируют. Если это правда, то скорее всего это подтверждение суперсимметрии и, возможно, это решит проблему с тёмной материей.
Чувствительность гравитационного детектора advLIGO уже по идее хватает, чтобы наблюдать первичные гравитационные волны. Поэтому сейчас активно занимаются и этим. Если их найдут — то это самое что ни на есть прямое подтверждение первичных флуктуаций и теории инфляции.
Плюс ещё куча всяких клёвых телескопов и детекторов собираются делать на Земле или посылать в космос. Так что в ближайшие годы вас ждёт куча новых открытий, главное не проморгать их, сидя перед экраном с попкорном и слушая голос какого-нибудь очередного популяризатора.
Прочитать ещё 1 ответ
Кто такой Менделеев?
Читаю и пишу. Иногда разговариваю и слушаю музыку.
Дмитрий Иванович Менделеев — российский ученый, живший в конце 19-начале 20 века, известный, прежде всего, как автор периодической системы химических элементов, ставшей краеугольным камнем всей современной химии. Однако его научные интересы не ограничивались только физикой и химией. Менделеев занимался метеорологией, геологией, воздухоплаванием и даже экономикой.
Могут ли на других планетах, в Солнечной системе и за ее пределами, существовать абсолютно новые металлы, отличные от земных железа, меди, золота? Или все металлы во Вселенной одни и те же?
Инженер, немного пилот. Физик, химик, электронщик-любитель. Независимый звукореж…
Все химические элементы, в том числе металлы, подчиняются Периодическому закону Д.И.Менделеева, который, в свою очередь, обусловлен устройством атомов, а точнее, их электронных оболочек. Поскольку в таблице Менделеева нет пустых ячеек, то и новых элементов, по крайней мере, при условиях как в Солнечной системе, ожидать не приходится.
Если же условия будут существенно отличаться от условий в Солнечной системе (например, внутри или в окрестностях «чёрной дыры»), то конфигурация электронных оболочек в атомах может быть другой, что приведёт к «неведомым» элементам. Но в этом случае и «таблица Менделеева» там будет выглядеть совсем по-другому.
Кстати, во времена Менделеева, в его таблице были пустые ячейки, например, под номером 43. «Эко-марганец» (в последствии названный «технеций»), предсказанный Менделеевым, самый лёгкий элемент, не имеющий стабильных изотопов, был получен искусственно только в 1937 году.
Прочитать ещё 4 ответа
Могут ли в бесконечности действовать законы?
Нет. В рамках бесконечности любой закон превращается в фикцию, так как любое статистическое отклонение становится вероятностно равным стандартной модели.
Если вы имеете ввиду законы физики — они действую либо в рамках замкнутой системы, либо в конечных рамках взаимодейтсвующих систем.
Прочитать ещё 1 ответ
Существует ли научное обоснование магии?
мои ответы не являются «глубокомысленными» статьями для ЯДзен
Это как мёд. Если объяснено наукой, значит не магия )
И процитирую:
Нет, волшебство это другое. Во всех культурах более менее одинаково принято считать волшебством такое воздействие на природу, которое меняет естественный ход вещей. Происходит это либо за счет тайных знаний о природе (здесь принципиально понятие «тайный», когда эти знания становятся общими, то они перестают действовать), либо за счет тайных же знаний того, как вступить в связь с некими потусторонними силами, причем якобы знания дают возможность почти что принуждать эти силы действовать.
Знания, которые нельзя передавать свободно другим или они перестанут действовать, это принципиально противоречит науке. Естественные науки это воспроизводимость опытов вне зависимости от личности экспериментатора.
Прочитать ещё 7 ответов
Дмитрий Менделеев опубликовал периодическую таблицу из химических элементов , в 1869 году на основе свойств , которые появились с некоторой регулярностью , когда он выложил элементы от легких до самых тяжелых. Когда Менделеев предложил свою периодическую таблицу, он отметил , пробела в таблице и предсказал , что , как-то, неизвестные элементы существовали со свойствами соответствующих для заполнения этих пробелов. Он назвал их эка-бор, эка-алюминий и эка-кремний, с соответствующими атомными массами 44, 68 и 72.
Приставки
Чтобы дать временные имена его предсказанных элементов, Менделеев использовал префиксы EKA -, дви — и три -, от санскритских названий цифр 1, 2 и 3, в зависимости от того, был ли предсказанный элемент один, два или три места вниз от известного элемента той же самой группы в его таблице. Например, германий называли эка-кремний до его открытия в 1886 году, и рений называли DVI- марганца до его открытия в 1926 году.
Ека приставка использовалась другими теоретиками, а не только в собственных предсказаний Менделеева. Перед открытием, франций был передан как эка-цезий , и астатина как эка-йод . Иногда, Ека по — прежнему используются для обозначения некоторых трансурановых элементов , например, эка-актиний (или дви-лантан ) для unbiunium . Но текущие официальная IUPAC практика заключается в использовании систематического имени элемента на основе атомного номера элемента в качестве временного названия, вместо того , чтобы на основе его положения в периодической таблице , поскольку эти префиксы требуют.
Оригинальные предсказания
Четыре предсказали элементы легче , чем редкоземельные элементы , эка-бор ( Eb , под бором, B, 5), эка-алюминий ( Ео или El , под Al, 13), эка-марганец ( Em под Mn, 25 ), и эка-кремний ( Es , под Si, 14), оказались хорошими предикторами свойств скандия (Sc, 21), галлий (Ga, 31), технеций (Tc, 43), и германий (Ge, 32) соответственно, которые заполняют место в периодической таблице Менделеева , присвоенной.
Имена были написаны Менделеевым , как экаборъ (ekabor), экаалюминій (ekaalyuminiy), экамарганецъ (ekamarganets) и экасилицій (ekasilitsiy) соответственно, после предварительной 1917 года орфографией .
Первоначальные версии таблицы Менделеева не различали редкоземельные элементы из переходных элементов , помогают объяснить и почему предсказания Менделеева для более тяжелых неизвестных элементов не так хорошо , как и для более легких и почему они не так хорошо известны или документально.
Оксид скандия был выделен в конце 1879 г. Lars Fredrick Nilson ; Пер Теодор Клеве признал соответствие и уведомление Менделеева в конце этого года. Менделеев предсказал атомную массу от 44 для ekaboron в 1871 году, в то время как скандий имеет атомную массу 44.955908.
В 1871 году Менделеев предсказал существование еще неоткрытых-элемента он назвал эка-алюминий (из — за его близости к алюминию в периодической таблице). В приведенной ниже таблице сравниваются свойства элемента предсказанный Менделеевым с фактическими характеристиками галлия (обнаруженных в 1875 году Поль Эмиль Лекок де Буабодрана ).
| Имущество | Эка-алюминий | галлий |
|---|---|---|
| атомная масса | 68 | 69,723 |
| Плотность (г / см 3 ) | 6,0 | 5,91 |
| Температура плавления (° С) | низкий | 29,76 |
| Формула оксида в | Еа 2 O 3 (плотность: 5,5 г / см 3 ) (растворимый в обоих щелочей и кислот) | Ga 2 O 3 (плотность: 5,88 г / см 3 ) (растворимый в обоих щелочей и кислот) |
| Формула компании Chloride | Еа 2 Cl 6 (летучий) | Ga 2 Cl 6 (летучий) |
Технеций был выделен Карло Перье и Эмилио Сегре в 1937 году, а после жизни Менделеева, из образцов молибдена , которые были бомбардировке дейтерия ядрами в циклотроне с помощью Эрнест Лоуренс . Менделеев предсказал атомную массу 100 для ekamanganese в 1871 году, а наиболее стабильный изотоп технеция является 98 Tc.
Германий был выделен в 1886 году и обеспечил лучшее подтверждение теории до того времени, из-за его более четко с соседними элементами, чем два ранее подтвержденных предсказания Менделеева делают с их контрастными.
| Имущество | Эка-кремний | германий |
|---|---|---|
| атомная масса | 72 | 72,630 |
| Плотность (г / см 3 ) | 5,5 | 5,323 |
| Температура плавления (° С) | высоко | +938 |
| цвет | серый | серый |
| оксида типа | Огнеупорный диоксид | Огнеупорный диоксид |
| Плотность оксида (г / см 3 ) | 4,7 | 4,228 |
| оксид активность | основной слабо | основной слабо |
| Точка кипения хлорида | при 100 ° C | 86,5 ° С (GeCl 4 ) |
| Плотность хлорида (г / см 3 ) | 1,9 | 1,879 |
Другие прогнозы
Существование элемента между торием (90) и ураном (92) было предсказано Менделеевым в 1871. В 1900 годе Крукс изолированный протактиний (91) в качестве радиоактивного материала из урана , что он не мог определить. Различные изотопы протактиния были обнаружены в Германии в 1913 году и в 1918 году, но имя протактиний не был дан до 1948 г. После принятия Сиборг «s концепции актиноидов в 1945 году, торий, уран и протактиний были классифицированы как актиноиды ; следовательно, протактиний не занимает место Ека тантала (по 93) в том, что теперь называется группой 5 . Эка-тантал фактически является синтетическим сверхтяжелый элемент дубний (105).
1869 таблицы Менделеева был неявно предсказал более тяжелый аналог титана (22) и циркония (40), но в 1871 году он поместил лантан (57) в этом месте. 1923 Открытие гафния (72) подтверждено оригинальный 1869. предсказание Менделеева.
Более поздние предсказания
В 1902 году, приняв доказательства элементов гелия и аргона , Менделеев поместил эти благородные газы в группе 0 в его расположении элементов. Как Менделеев сомневался в атомной теории , чтобы объяснить закон определенных пропорций , у него не было априорным основания полагать , что водород был самым легким из элементов, и предположил , что гипотетическая зажигалку членом эту химически инертной группы 0 элементов могли бы незамеченные и быть ответственность за радиоактивностью . В настоящее время некоторые периодические таблицы элементов поместить одиночка нейтронов в этом месте, и это соответствует предсказаниям Менделеева достаточно хорошо.
Чем тяжелее гипотетических элементов прото-гелиевых Менделеевы , идентифицированные с коронией , названного по ассоциации с необъяснимой спектральной линией в Солнцах короны . Дефектные калибровки дали длину волны 531.68 нма, который был в конечном счете скорректированного на 530,3 нм, Гротриан и Эдлены идентифицированных как происходящие из Fe XIV в 1939 году.
Легкая из группы 0 газов, первые в периодической таблице, была присвоена теоретической атомной масса между 5,3 × 10 -11 и 9,6 × 10 -7 . Кинетическая скорость этого газа была рассчитана Менделеевым быть 2500000 метров в секунду. Почти безмассово эти газы предполагались Менделеев пронизывает весь материал, редко взаимодействуя химически. Высокая подвижность и очень малая масса транс-водородных газов приведет к тому , что они могут быть разрежен, но кажутся очень плотными.
Менделеева позднее опубликовала теоретическое выражение эфира в небольшой брошюре , озаглавленной химическое вещество Концепции Эфира (1904). Его публикация 1904 снова содержала два атомных элементов меньше и легче , чем водород. Он рассматривал «эфир» газ в качестве межзвездной атмосферы , состоящей по меньшей мере из двух элементов , более легких , чем водород. Он отметил , что эти газы , образующиеся в результате ожесточенных бомбежек внутренних к звездам, Солнце является наиболее плодовитым источником таких газов. Согласно брошюре Менделеева, межзвездная атмосфера, вероятно , состоит из нескольких дополнительных элементарных видов.
Заметки
Рекомендации
дальнейшее чтение
- Шерри, Эрик (2007). Периодическая таблица: его история и его значение . Нью — Йорк: Oxford University Press. ISBN 0-19-530573-6 .
