Какое свойство оксидов и гидроксидов называется амфотерностью

Это занятие мы посвятим изучению амфотерных оксидов и гидроксидов. На нем мы поговорим о веществах, имеющих амфотерные (двойственные) свойства, и особенностях химических реакций, которые протекают с ними. Но сначала повторим, с чем реагируют кислотные и основные оксиды. После рассмотрим примеры амфотерных оксидов и гидроксидов.
Тема: Введение
Урок: Амфотерные оксиды и гидроксиды
1. Характеристика амфотерных соединений
Рис. 1. Вещества, проявляющие амфотерные свойства
Основные оксиды реагируют с кислотными оксидами, а кислотные оксиды – с основаниями. Но существуют вещества, оксиды и гидроксиды которых в зависимости от условий, будут реагировать и с кислотами и с основаниями. Такие свойства называются амфотерными.
Вещества, обладающие амфотерными свойствами приведены Рис.1.. Это соединения, образованные бериллием, цинком, хромом, мышьяком, алюминием, германием, свинцом, марганцем, железом, оловом.
Примеры их амфотерных оксидов приведены в таблице 1.
2. Химические свойства амфотерных оксидов цинка и алюминия
Рассмотрим амфотерные свойства оксидов цинка и алюминия. На примере их взаимодействия с основными и кислотными оксидами, с кислотой и щелочью.
— Взаимодействие с основными оксидами и основаниями:
ZnO + Na2O → Na2ZnO2 (цинкат натрия). Оксид цинка ведет себя как кислотный.
ZnO + 2NaOH → Na2ZnO2+ H2O
— Взаимодействие с кислотными оксидами и кислотами. Проявляет свойства основного оксида.
3ZnO + P2O5 → Zn3(PO4)2 (фосфат цинка)
ZnO + 2HCl → ZnCl2 + H2O
Аналогично оксиду цинка ведет себя и оксид алюминия:
— Взаимодействие с основными оксидами и основаниями:
Al2O3 + Na2O → 2NaAlO2 (метаалюминат натрия). Оксид алюминия ведет себя как кислотный.
Al2O3 + 2NaOH → 2NaAlO2+ H2O
— Взаимодействие с кислотными оксидами и кислотами. Проявляет свойства основного оксида.
Al2O3 + P2O5 → 2AlPO4(фосфат алюминия)
Al2O3 + 6HCl → 2AlCl3 + 3H2O
Рассмотренные реакции происходят при нагревании, при сплавлении. Если взять растворы веществ, то реакции пойдут несколько иначе.
3. Химические свойства амфотерных оксидов цинка и алюминия в растворах
ZnO + 2NaOH + H2O → Na2[Zn(OH)4] (тетрагидроксоцинкат натрия) Al2O3 + 2NaOH + 3H2O → 2Na[Al(OH)4] (тетрагидроксоалюминат натрия)
В результате этих реакций получаются соли, которые относятся к комплексным.
Рис. 2. Минералы на основе оксида алюминия
Оксид алюминия.
Оксид алюминия чрезвычайно распространенное на Земле вещество. Он составляет основу глины, бокситов, корунда и других минералов. Рис.2.
В результате взаимодействия этих веществ с серной кислотой, получается сульфат цинка или сульфат алюминия.
ZnO + H2SO4 → ZnSO4 + H2O
Al2O3 + 3H2SO4→ Al2 (SO4)3 + 3H2O
4. Химические свойства амфотерных гидроксидов цинка и алюминия
Реакции гидроксидов цинка и алюминия с оксидом натрия происходят при сплавлении, потому что эти гидроксиды твердые и не входят в состав растворов.
Zn(OН)2 + Na2O → Na2ZnO2 + Н2О соль называется цинкат натрия.
2Al(OН)3 + Na2O → 2NaAlO2 + 3Н2О соль называется метаалюминат натрия.
Рис. 3. Гидроксид алюминия
Реакции амфотерных оснований со щелочами характеризует их кислотные свойства. Данные реакции можно проводить как при сплавлении твердых веществ, так и в растворах. Но при этом получатся разные вещества, т.е. продукты реакции зависят от условий проведения реакции: в расплаве или в растворе.
Zn(OH)2 + 2NaOH тв. Na2ZnO2 + 2Н2О
Al(OH)3 + NaOH тв. NaAlO2+ 2H2O
Zn(OH)2 + 2NaOH раствор → Na2[Zn(OH)4] Al(OH)3 + NaOH раствор → Na[Al(OH)4] тетрагидроксоалюминат натрия Al(OH)3 + 3NaOH раствор→ Na3[Al(OH)6] гексагидроксоалюминат натрия.
Получается тетрагидроксоалюминат натрия или гексагидроксоалюминат натрия зависит от того, сколько щелочи мы взяли. В последней реакции щелочи взято много и образуется гексагидроксоалюминат натрия.
5. Химические свойства амфотерных цинка и алюминия
Элементы, которые образуют амфотерные соединения, могут сами проявлять амфотерные свойства.
Zn + 2NaOH + 2H2O → Na2[Zn(OH)4] + Н2↑(тетрагидроксоцинкат натрия)
2Al + 2NaOH + 6H2O → 2Na[Al(OH)4] + 3Н2↑( (тетрагидроксоалюминат натрия)
Zn + H2SO4(разб.)→ ZnSO4 + H2↑
2Al + 3H2SO4(разб.)→ Al2 (SO4)3 + 3H2↑
Напомним о том, что амфотерные гидроксиды являются нерастворимыми основаниями. И при нагревании разлагаются , образуя оксид и воду.
Разложение амфотерных оснований при нагревании.
2Al(OH)3 Al2O3 + 3H2O
Zn(OH)2 ZnO + H2O
Подведение итога урока.
Вы узнали свойства амфотерных оксидов и гидроксидов. Эти вещества, имеют амфотерные (двойственные) свойства. Химические реакции, которые протекают с ними, имеют особенности. Вы рассмотрели примеры амфотерных оксидов и гидроксидов.
Список рекомендованной литературы
1. Рудзитис Г.Е. Неорганическая и органическая химия. 8 класс: учебник для общеобразовательных учреждений: базовый уровень/ Г. Е. Рудзитис, Ф.Г. Фельдман.М.: Просвещение. 2011 г.176с.:ил.
2. Попель П.П.Химия:8 кл.: учебник для общеобразовательных учебных заведений/П.П. Попель, Л.С.Кривля. -К.: ИЦ «Академия»,2008.-240 с.: ил.
3. Габриелян О.С. Химия. 9 класс. Учебник. Издательство: Дрофа.:2001. 224с .
Рекомендованные ссылки на ресурсы интернет
1. Chemport.ru (Источник).
1. Химик (Источник).
Рекомендованное домашнее задание
1. №№ 6,10 (с.130) Рудзитис Г.Е. Неорганическая и органическая химия. 9 класс: учебник для общеобразовательных учреждений: базовый уровень/ Г. Е. Рудзитис, Ф.Г. Фельдман.М.: Просвещение. 2008 г.170с.: ил.
2. Напишите формулу гексагидроксоалюмината натрия. Как получают это вещество?
3. К раствору сульфата алюминия понемногу приливали раствор гидроксида натрия до избытка. Что наблюдали? Напишите уравнения реакций.
Анонимный вопрос · 30 мая 2019
29,2 K
Амфотерными называются элементы, которые в соединениях проявляют свойства металлов и неметаллов. К ним относятся элементы А-групп Периодической системы — Be, Al, Ga, Ge, Sn, Pb, Sb, Bi, Po и др., а также большинство элементов Б-групп — Cr, Mn, Fe, Zn, Cd, Au и др.
Оксиды и гидроксиды этих соединений, соотвественно, будут амфотерными.
Подготовила к ЕГЭ по химии 5000 учеников. С любого уровня до 100 в режиме… · vk.com/mendo_him
☘️Амфотерные оксиды — это оксиды, у которых элемент в степени окисления +3 или +4
Например, Al2O3, ТiO2, Cr2O3, Fe2O3, PbO2
☘️Но☝️
ZnO, BeO тоже амфотерные, хотя Zn и Be в степени окисления +2. Это нужно запомнить)
☘️Гидроксиды, которые соответствуют амфотерными оксидам, тоже амофотерны ????
Эффективный репетитор по математике, физике, химии. Автор книг и консультант по… · repetitor-5.ru
Из #викивпечку : Амфоте́рность (от др.-греч. ἀμφότεροι «двойственный; обоюдный») — способность некоторых химических веществ и соединений проявлять в зависимости от условий как кислотные, так и осно́вные свойства.
Похожее слово есть в биологии: «амфибия» — животное, которое может жить и в воде, и на суше. Амфи — и тот, и другой, био — жизнь. Живёт и там, и тут.
Амфотер… Читать далее
V2O5? Какой оксид?
Подготовила к ЕГЭ по химии 5000 учеников. С любого уровня до 100 в режиме… · vk.com/mendo_him
☘️V2O5-оксид ванадия (V)
☘️V в степени окисления +5➡️оксид кислотный, соответствует ванадиевой кислоте HVO3
H2O+V2O5=2HVO3
☘️Имеет те же химические свойства, что и другие кислотные оксиды
Прочитать ещё 3 ответа
Почему оксиды имеют разный характер и от чего это зависит?
Химия, кулинария, математика.
Характер оксида зависит от элемента оксида. Если это оксид металла, то это основный оксид ( пример Al2O3 ), если это оксид не металла, то это кислотный оксид ( пример NO2), если степень окисления переходит, то это амфотерный оксид ( пример ZnO ), еще существуют несолеобразующие оксиды ( пример NO ).
Что такое «оляция» и «оксоляция»?
Researcher, Institute of Physics, University of Tartu
Возьмем обычный гидроксид. Ну, скажем, гидроксид титана или ортотитановая кислота, кому как нравится. Формула Ti(OH)4. Т.е. условная молекула этого соединения содержит четыре ОН-группы, присоединенные к атому титана. Каждая из этих ОН-групп присоединена к титану так: Ti-OH. Это обычный вариант, обычная концевая («терминальная») ОН-группа, которая присоединена сигма-связью только к одному атому, как ей и положено.
Однако, у кислорода есть неподеленная электронная пара, которая может «сесть» на чью-нибудь незаполненную орбиталь по донорно-акцепторному механизму, а у титана есть куда ей сесть. При этом происходит образование мостиковой ОН-группы между двумя молекулами гидроксида титана (т.е. ОН-группа уже была по обычной сигма-связи соеденина с одним атомом титана, а теперь присоединилась неподеленной парой к еще одному. Выглядит это так: (HO)3Ti-O(H)-Ti(OH)4 . При этом мы видим, что мостиковый кислород имеет три связи, а один из атомов титана — пять. Такая мостиковая ОН-группа называется «ол-группа«, а процесс ее образования, которыя я описал выше — оляцией.
Это структура с формально трехвалентным кислородом и пятивалентным титаном является неустойчивой и довольно быстро переходит в более удобоваримую структуру с мостиковым атомом кислорода: (HO)3Ti-O(H)-Ti(OH)4 -> (HO)3Ti-O-Ti(OH)3 + H2O. Теперь, как мы видим, у всех всё в порядке — кислород двухвалентный, оба титана четырехвалентны, всё как обычно. Этот процесс называется оксоляцией, поскольку ол-группа превращается в мостиковую оксо-группу (-O-). Можно заметить, что отщепилась молекула воды и гидроксид как бы стал на шажок ближе к оксиду. Это будет совершенно справедливое замечание, поскольку конечным результатом оксоляции (далеко не всегда достигаемым, конечно) и будет оксид, у которого ОН-группы остались только на поверхности.
Процессы оляции-оксоляции характерны для амфотерных гидроксидов, а также для слабых кислот и оснований. Обычно происходят после их образования в результате гидролиза, то есть сначала из какой-то соли в результате гидролиза получается гидроксид чего-то, а потом постепенно он претерпевает процессы оляции-оксоляции, при этом из индивидуальных молекул этого гидроксида с одним центральным атомом получаются многоатомные (конденсированные) оксо-гидроксосоединения (это называют поликонденсацией). Именно в связи с этим процессом свежеосажденные гидроксиды гораздо более реакционно способны, чем состарившиеся. У преподавателей есть садистический эксперимент для первокурсников или старших школьников — всем известно, что гидроксид алюминия растворяется в избытке щелочи. Так вот надо аккуратно осадить его, потом оставить на некоторое время, а потом попросить студента растворить его в NaOH. Если студент не в курсе дела, то он будет его растворять до позеленения и навсегда потом запомнит, что такое оляция-оксоляция 🙂
Какими свойствами обладает кремний материаловедение?
Мои интересы: разнообразны, но можно выделить следующие: литература, история…
Кремний это неметалл. Степени окисления: +4, -4, -2. Валентность – 2, 4. Взаимодействует со фтором: Si + 2F2 = SiF4. При 1000 °C реагирует с неметаллами: с CL2, N2, C, S. Реагирует со смесью азотной и плавиковой кислот. Хорошо растворяется в расплавленных металлах Zn, Al, Sn, Pb но не реагирует с ними. С Mg, Cu, Fe кремний взаимодействует с образованием силицидов: Si + 2Mg = Mg2Si. Горит в кислороде.
Ключевые слова конспекта: амфотерность, амфотерные оксиды, амфотерные гидроксиды,
ГИДРОКСИДЫ
Гидроксиды – это неорганические соединения, образованные тем или иным элементом, кислородом и водородом. В гидроксидах обязательно имеется водород, связанный с кислородом (связь О–Н). В некоторых гидроксидах водород может непосредственно соединяться с атомами элемента. Например, в H3РO3 два атома водорода связаны с атомами кислорода, а один – с атомом фосфора.
В ряде случаев гидроксиды являются продуктами гидратации (соединения с водой) соответствующих оксидов, хотя многие оксиды непосредственно с водой не взаимодействуют. В результате дегидратации гидроксидов образуются соответствующие оксиды.
Гидроксиды могут быть основными (основания), кислотными (кислородсодержащие кислоты) и амфотерными. Примерами основных гидроксидов являются NaOH, Ва(ОН)2, Mg(OH)2. Примерами кислотных гидроксидов являются НСlO4 (хлорная кислота, высший гидроксид хлора), H3РO4 (ортофосфорная кислота, высший гидроксид фосфора), H2SO4 (серная кислота, высший гидроксид серы).
Графические формулы перечисленных гидроксидов приведены ниже. Во всех гидроксидах имеется связь О–Н:
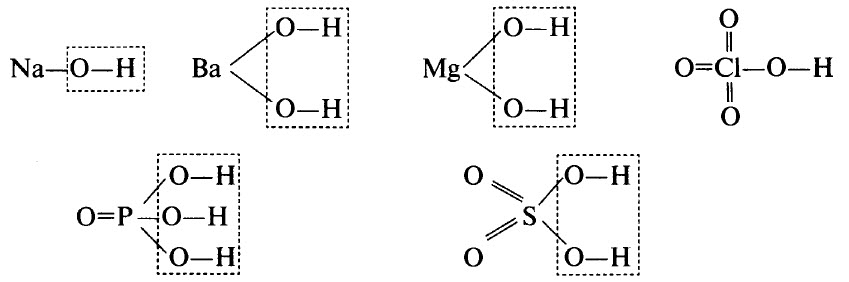
ПОНЯТИЕ ОБ АМФОТЕРНЫХ ОКСИДАХ И ГИДРОКСИДАХ
Амфотерность (от греч. amphoteros – и тот, и другой) – способность химических соединений проявлять и кислотные, и основные свойства в зависимости от природы реагента, с которым амфотерное вещество вступает в кислотно-основное взаимодействие.
Амфотерные оксиды и гидроксиды – оксиды и гидроксиды, проявляющие как основные, так и кислотные свойства. Они реагируют как с кислотами, так и с основаниями. Амфотерным оксидам соответствуют амфотерные гидроксиды, например: ВeО – Вe(ОН)2, Сr2O3 – Сr(ОН)3.
Амфотерные гидроксиды практически нерастворимы в воде. Их основные и кислотные свойства выражены слабо, они являются слабыми кислотами и слабыми основаниями.
Амфотерными оксидами и гидроксидами являются, как правило, оксиды и гидроксиды металлов, в которых степень окисления металла +3, +4, иногда +2.
Среди оксидов элементов главных подгрупп амфотерными являются: BeO, Al2O3, SnO, SnO2, PbO, Sb2O3.
Амфотерными гидроксидами являются следующие гидроксиды элементов главных подгрупп: Ве(ОН)2, Al(ОН)3, Рb(ОН)2 и некоторые другие.
Оксиды и гидроксиды элементов побочных подгрупп, соответствующие высоким степеням окисления, как правило, являются кислотными, например: СrO3 (ему соответствует H2СrO4), Мn2O7 (ему соответствует НМnO4).
Для низших оксидов и гидроксидов характерно преобладание основных свойств, например: СrO и Сr(ОН)2, МnО и Мn(ОН)2.
Оксиды и гидроксиды, в которых степени окисления элементов +3 и +4, являются, как правило, амфотерными: Сг2O3 и Cr(OH)3, Fe2O3 и Fe(OH)3. Однако последние элементы в декадах d–элементов (например, Zn) образуют амфотерные оксиды и гидроксиды даже в низких степенях окисления, например ZnO и Zn(OH)2.
ХИМИЧЕСКИЕ СВОЙСТВА АМФОТЕРНЫХ ОКСИДОВ И ГИДРОКСИДОВ
Рассмотрим амфотерные свойства оксида и гидроксида цинка – ZnO и Zn(OH)2. Оба вещества реагируют с кислотами:
ZnO + 2HNO3 = Zn(NO3)2 + H2O
Zn(OH)2 + H2SO4 = ZnSO4 + 2H2O
Оксид и гидроксид цинка реагируют также и со щелочами:
В результате реакций со щелочами в растворах образуются комплексные ионы – тетрагидроксоцинкаты (например, Na2[Zn(OH)4]), а при сплавлении – цинкаты (например, Na2ZnO2). Чтобы составить формулы цинкатов, запишите формулу гидроксида цинка Zn(OH)2 как формулу кислоты – H2ZnO2. Кислотным остатком такой кислоты является ион ZnO22–.
При диссоциации этих солей в растворах образуются ионы, в которых цинк входит в состав анионов, поэтому говорят, что в этих соединениях «цинк в анионной форме».
Докажем амфотерность оксида и гидроксида алюминия Al(ОН)3. Он растворяется в кислотах с образованием солей, где алюминий находится в катионной форме:
Al(ОН)3 + 3Н+ = Al3+ + 3H2O
Но гидроксид алюминия взаимодействует и со щелочами. При сплавлении со щелочами образуются алюминаты (метаалюминаты):
Al(ОН)3 + NaOH = NaAlO2 + 2H2O
Чтобы составить формулы алюминатов, запишите формулу гидроксида алюминия Al(ОН)3 как H3AlO3. Теперь представьте, что от 1 моль этого соединения отщепляется 1 моль воды. Образуется соединение НАlO2, в котором кислотным остатком будет ион AlO2–.
В образовавшейся соли алюминий образует анион AlO2– (алюминий в анионной форме). В растворах в результате реакции со щёлочью образуется комплексный тетрагидроксоалюминат-ион [Al(ОН)4]–:
Al(ОН)3 + NaOH = Na[Al(OH)4] (тетрагидроксоалюминат натрия)
Некоторые амфотерные оксиды и гидроксиды не проявляют амфотерность в обычных условиях и в растворах ведут себя как основные. Амфотерность таких соединений проявляется в более жёстких условиях. Например, гидроксид железа (III) Fe(OH)3 легко реагирует с кислотами:
Fe(OH)3 + 3НCl = FeCl3 + 3H2O
Fe(OH)3 + NaOH = NaFeO2 + 2H2O
Признаком этой реакции будет растворение бурого осадка. А вот при добавлении раствора щёлочи гидроксид железа (III) не растворяется. Тогда, может быть, считать его основанием, не растворимым в воде? Дело в том, что в данном случае соль образуется при плавлении со щёлочью.
Естественно, что в ходе плавления происходит разложение гидроксида на оксид и воду, и в действительности реакция идёт между оксидом и щёлочью:
Fe2O3 + 2NaOH = 2NaFeO2 + H2O
Таким образом, гидроксид железа (III) можно отнести к амфотерным гидроксидам, хотя основные свойства у него преобладают.
Конспект урока «Амфотерные оксиды и гидроксиды».
Следующая тема: «».
Анонимный вопрос · 5 марта 2019
4,7 K
Подготовила к ЕГЭ по химии 5000 учеников. С любого уровня до 100 в режиме… · vk.com/mendo_him
Амфотерные гидроксиды — это гидроксиды, которые повторяют свойства кислот и оснований ⚗️
????К амфотерным относятся следующие гидроксиды:
????большинство гидроксидов d-элементов (хрома(III), железа, цинка, и др.);
????ряд гидроксидов p-элементов (алюминия, галлия, олова, свинца и др.);
????из гидроксидов s-элементов амфотерным является гидроксид бериллия;
????ХИМИЧЕСКИЕ СВОЙСТВА, СОВПАДАЮЩИЕ С ОСНОВАНИЯМИ
????Реагируют с кислотами
▫️Al(OH)3 + 3HCl = AlCl3 + 3H2O
????Реагируют с кислотными оксидами
▫️2Al(OH)3 + 3SiO2 = Al2(SiO3)3 + 3H2O
????ХИМИЧЕСКИЕ СВОЙСТВА, СОВПАДАЮЩИЕ С КИСЛОТАМИ
????Реагируют со щелочами
1) В растворе:
▫️Al(OH)3 + NaOH = Na[Al(OH)4]
2) При сплавлении:
▫️Al(OH)3 + NaOH = NaAlO2 + 2H2O
????Реагируют с основными оксидами
▫️2Al(OH)3 + Na2O = 2NaAlO2 + 3H2O
????Реагируют с солями
▫️2Al(OH)3 + Na2CO3 = 2NaAlO2 + CO2 + 3H2O
????Одно из общих свойств — разложение при нагревании:
▫️2Fe(OH)3 = Fe2O3 + 3H2O
Какими способами доказывается амфотерный характер соединений?
Подготовила к ЕГЭ по химии 5000 учеников. С любого уровня до 100 в режиме… · vk.com/mendo_him
☘️Амфотерные соединения — это вещества, которые ведут себя, как кислоты и как основания????
Возьмем Al(OH)3. Как доказать, что он амфотерный? ????
????Добавим в него кислоту HCl
Al(OH)3+3HCl=3H2O+AlCl3
Гидроксид алюминия реагирует с кислотой подобно основаниям)
????Теперь возьмём щёлочь NaOH
Al(OH)3+NaOH=Na[Al(OH)4]
Мы видим, что он реагирует основаниями, как кислоты)
Делаем вывод, что он амфотерный
Как найти высшей оксид и гидроксид Астата(At)?
Ну, если есть таблица Менделеева, то просто нужно посмотреть в самый низ группы Астата. Там будет формула высшего оксида
Высший гидроксид можно найти, исходя из высшей степени окисления вещества (как, собственно, и оксид). У Астата — 7 (номер группы). Итак, получается, что высший гидроксид — HAtO4
Как определить растворимость кислых солей?
Есть такая таблица растворимости. Это справочный материал его выдают на ЕГЭ экзаменах и тд.
Допустим нужно определить растворимости следующих кислых солей, это соли в которых есть катион, анион и катион водорода: гидрокарбонат натрия ( сода пищевая), дигидрофосфат стронция и гидросульфат свинца. Для этого запишем их формулы и посмотрим какие у них анионы и катионы:
NaHCO3 => Na+ и HCO3-
Sr(H2PO4)2=> Sr2+ и 2H2PO4-
Pb(HSO4)2 => Pb2+ и 2HSO4-
Теперь смотрим в волшебную таблицу
Ищем катион ( это тот что с плюсиком) Na+ и потом смотрим анион( с минусом) HCO3- там стоит буква Р значит растворимо. А вот дигидрофосфат стронция, не растворим, там стоит буква Н. Со свинцом аналогично. Вообще по этой таблице можно посмотреть растворимость как и кислот ( там катион H+), так и оснований (OH-), да и вообще любых солей.
Какими свойствами обладает апатит?
Обожаю точные науки и испытываю огромный интерес к творчеству. При таком…
Различают три вида апатитов:
1) гидроксоапатит;
2) фторапатит;
3) хлорапатит.
Апатит — полигенный минерал, образующий скопления в щелочных, магматических породах карбонатитах, нефелиновых и гранитных пегматитах и т. д.
Химический состав: оксид калия, фтор, хлор и многочисленные примеси.
В зависимости от состава цвет апатита также меняется. Апатиты бывают с зелеными, голубыми, розовыми и желтыми оттенками.
Апатит применяют в сельскохозяйственной промышленности для производства удобрений, а также на металлургическом, стекольном и керамическом производстве.
Приведите примеры реакций декарбоксилирования?
Подготовила к ЕГЭ по химии 5000 учеников. С любого уровня до 100 в режиме… · vk.com/mendo_him
????Реакция декарбоксилирования????
✅Это реакция отщепления CO2 от органических кислот,их солей,аминокислот
✅При этом необходима температура
✅Пример:
R-CH(NH2)-COOH➡️R-CH2-NH2+CO2
Для солей органических кислот сплавление с NaOH:
CH3-CH2-COONa+NaOH➡️CH3-CH3+Na2CO3
