Какими общими физическими свойствами обладают металлы
Общие физические свойства мекталлов:
1) Пластичность — способность изменять форму при ударе, вытягиваться в проволоку, прокатываться в тонкие листы. В ряду — Au, Ag, Cu, Sn, Pb, Zn, Fe уменьшается.
2) Блеск, обычно серый цвет и непрозрачность. Это связано со взаимодействием свободных электронов с падающими на металл квантами света.
3) Электропроводность. Объясняется направленным движением свободных электронов от отрицательного полюса к положительному под влиянием небольшой разности потенциалов. В ряду — Ag, Cu, Al, Fe уменьшается. При нагревании электропроводность уменьшается, т. к. с повышением температуры усиливаются колебания атомов и ионов в узлах кристаллической решетки, что затрудняет направленное движение «электронного газа».
4) Теплопроводность. Закономерность та же. Обусловлена высокой подвижностью свободных электронов и колебательным движением атомов, благодаря чему происходит быстрое выравнивание температуры по массе металла. Наибольшая теплопроводность — у висмута и ртути.
5) Твердость. Самый твердый – хром (режет стекло) ; самые мягкие – щелочные металлы – калий, натрий, рубидий и цезий – режутся ножом.
6) Плотность. Она тем меньше, чем меньше атомная масса металла и чем больше радиус его атома (самый легкий — литий (r=0,53 г/см3); самый тяжелый – осмий (r=22,6 г/см3).
Металлы, имеющие r < 5 г/см3 считаются «легкими металлами».
7) Температуры плавления и кипения. Самый легкоплавкий металл – ртуть (т. пл. = -39°C), самый тугоплавкий металл – вольфрам (t°пл. = 3390°C).
Металлы с t°пл. выше 1000°C считаются тугоплавкими, ниже – низкоплавкими.
Все металлы являются восстановителями. Для металлов главных подгрупп восстановительная активность (способность отдавать электроны) возрастает сверху вниз и справа налево. Например, Натрий и кальций вытесняют водород из воды уже при обычных условиях:
Ca + 2H2O Ca(OH)2 + H2¬ ; 2Na + 2H2O 2NaOH + H20
А магний при повышении температуры:
Mg + H2O –t MgO + H2
Восстановительная способность и химическая активность элементов побочных подгрупп увеличивается снизу вверх по группе (например, серебро на воздухе окисляется, а золото нет; медь вытесняет серебро из его соли) :
Cu + 2AgNO3 → 2Ag ↓ + Cu(NO3)2
Cu0 -2 ē → Cu+2 1 О. О. В.
Ag+ + ē → Ag0 2 В. В. О.
Высшая положительная степень окисления для металлов главных подгрупп в их соединениях равна номеру группы (например, NaCl, MgCl2, AlCl3, SnCl4), а для металлов побочных подгрупп в их кислородосодержащих соединениях также часто совпадает с номером группы (например, ZnO, TiO2, V2O5, CrO3, KMnO4).
Свойства оксидов металлов слева направо по периоду и снизу вверх по группе изменяются от основных к амфотерным для металлов главных подгрупп (Na2O и MgO – основные оксиды, Al2O3 и BeO – амфотерные) . Для металлов побочных подгрупп свойства оксидов, в которых металлы проявляют свою высшую степень окисления, изменяются от основных через амфотерные к кислотным ( CuO — основной, ZnO — амфотерный, CrO3 — кислотный) .
Сила оснований, образуемых металлами главных подгрупп увеличивается справа налево по периоду и сверху вниз по группе ( Be(OH)2 и Al(OH)3– амфотерные гидроксиды, Mg(OH)2 — слабое основание, NaOHи – Ca(OH)2 сильные основания) . Гидраты оксидов металлов побочных подгрупп с высшими степенями окисления металла вдоль периода слева направо меняют свои свойства от оснований через амфотерные гидроксиды к кислотам ( Cu(OH)2 — основание, Zn(OH)2 — амфотерный гидроксид, H2CrO4 — кислота) .
В природе металлы встречаются в основном в виде соединений – оксидов или солей. Исключение составляют такие малоактивные металлы, как серебро, золото, платина, которые встречаются в самородном состоянии.
Все способы получения металлов основаны на процессах их восстановления из природных соединений.
Общие физические свойства металлов
Благодаря наличию свободных электронов (“электронного газа”) в кристаллической решетке все металлы проявляют следующие характерные общие свойства:
1) Пластичность – способность легко менять форму, вытягиваться в проволоку, прокатываться в тонкие листы.
2) Металлический блеск и непрозрачность. Это связано со взаимодействием свободных электронов с падающими на металл светом.
3) Электропроводность. Объясняется направленным движением свободных электронов от отрицательного полюса к положительному под влиянием небольшой разности потенциалов. При нагревании электропроводность уменьшается, т.к. с повышением температуры усиливаются колебания атомов и ионов в узлах кристаллической решетки, что затрудняет направленное движение “электронного газа”.
4) Теплопроводность. Обусловлена высокой подвижностью свободных электронов, благодаря чему происходит быстрое выравнивание температуры по массе металла. Наибольшая теплопроводность – у висмута и ртути.
5) Твердость. Самый твердый – хром (режет стекло); самые мягкие – щелочные металлы – калий, натрий, рубидий и цезий – режутся ножом.
6) Плотность. Она тем меньше, чем меньше атомная масса металла и больше радиус атома. Самый легкий – литий (ρ=0,53 г/см3); самый тяжелый – осмий (ρ=22,6 г/см3). Металлы, имеющие плотность менее 5 г/см3 считаются “легкими металлами”.
7) Температуры плавления и кипения. Самый легкоплавкий металл – ртуть (т.пл. = -39°C), самый тугоплавкий металл – вольфрам (t°пл. = 3390°C). Металлы с t°пл. выше 1000°C считаются тугоплавкими, ниже – низкоплавкими.
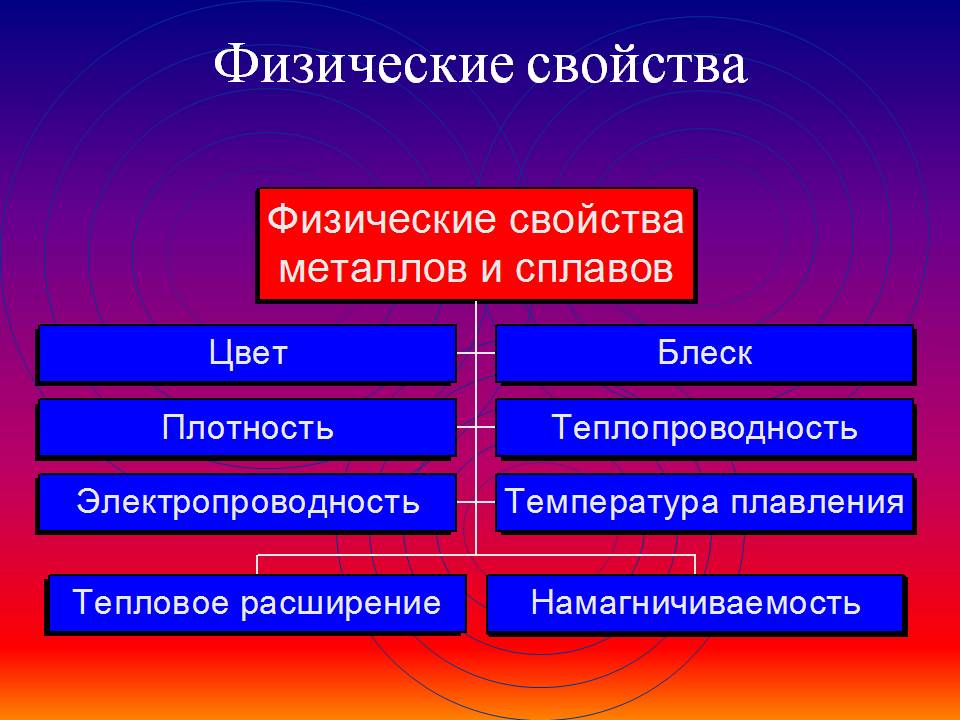
Общие химические свойства металлов
Сильные восстановители: Me0 – nē → Men+
Ряд напряжений характеризует сравнительную активность металлов в окислительно-восстановительных реакциях в водных растворах.
1. Реакции металлов с неметаллами
1) С кислородом:
2Mg + O2 → 2MgO
2) С серой:
Hg + S → HgS
3) С галогенами:
Ni + Cl2 –t°→ NiCl2
4) С азотом:
3Ca + N2 –t°→ Ca3N2
5) С фосфором:
3Ca + 2P –t°→ Ca3P2
6) С водородом (реагируют только щелочные и щелочноземельные металлы):
2Li + H2 → 2LiH
Ca + H2 → CaH2
2. Реакции металлов с кислотами
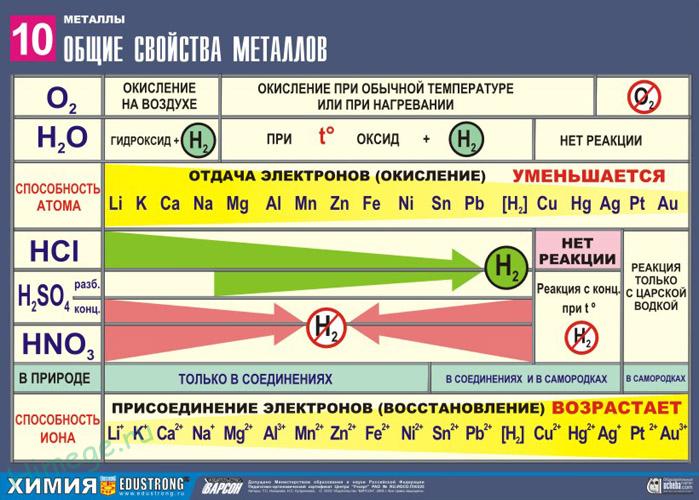
1) Металлы, стоящие в электрохимическом ряду напряжений до H восстанавливают кислоты-неокислители до водорода:
Mg + 2HCl → MgCl2 + H2
2Al+ 6HCl → 2AlCl3 + 3H2
6Na + 2H3PO4 → 2Na3PO4 + 3H2
2) С кислотами-окислителями:
При взаимодействии азотной кислоты любой концентрации и концентрированной серной с металлами водород никогда не выделяется!

Zn + 2H2SO4(К) → ZnSO4 + SO2 + 2H2O
4Zn + 5H2SO4(К) → 4ZnSO4 + H2S + 4H2O
3Zn + 4H2SO4(К) → 3ZnSO4 + S + 4H2O
2H2SO4(к) + Сu → Сu SO4 + SO2 + 2H2O
10HNO3 + 4Mg → 4Mg(NO3)2 + NH4NO3 + 3H2O
4HNO3(к) + Сu → Сu (NO3)2 + 2NO2 + 2H2O
3. Взаимодействие металлов с водой
1) Активные (щелочные и щелочноземельные металлы) образуют растворимое основание (щелочь) и водород:
2Na + 2H2O → 2NaOH + H2
Ca+ 2H2O → Ca(OH)2 + H2
2) Металлы средней активности окисляются водой при нагревании до оксида:
Zn + H2O –t°→ ZnO + H2
3) Неактивные (Au, Ag, Pt) – не реагируют.
4. Вытеснение более активными металлами менее активных металлов из растворов их солей:
Cu + HgCl2 → Hg+ CuCl2
Fe+ CuSO4 → Cu+ FeSO4
В промышленности часто используют не чистые металлы, а их смеси — сплавы, в которых полезные свойства одного металла дополняются полезными свойствами другого. Так, медь обладает невысокой твердостью и малопригодна для изготовления деталей машин, сплавы же меди с цинком (латунь) являются уже достаточно твердыми и широко используются в машиностроении. Алюминий обладает высокой пластичностью и достаточной легкостью (малой плотностью), но слишком мягок. На его основе готовят сплав с магнием, медью и марганцем – дуралюмин (дюраль), который, не теряя полезных свойств алюминия, приобретает высокую твердость и становится пригодным в авиастроении. Сплавы железа с углеродом (и добавками других металлов) – это широко известные чугун и сталь.
Металлы в свободном виде являются восстановителями. Однако реакционная способность некоторых металлов невелика из-за того, что они покрыты поверхностной оксидной пленкой, в разной степени устойчивой к действию таких химических реактивов, как вода, растворы кислот и щелочей.
Например, свинец всегда покрыт оксидной пленкой, для его перехода в раствор требуется не только воздействие реактива (например, разбавленной азотной кислоты), но и нагревание. Оксидная пленка на алюминии препятствует его реакции с водой, но под действием кислот и щелочей разрушается. Рыхлая оксидная пленка (ржавчина), образующаяся на поверхности железа во влажном воздухе, не мешает дальнейшему окислению железа.
Под действием концентрированных кислот на металлах образуется устойчивая оксидная пленка. Это явление называется пассивацией. Так, в концентрированной серной кислоте пассивируются (и после этого не реагируют с кислотой) такие металлы, как Ве, Вi, Со, Fе, Мg и Nb, а в концентрированной азотной кислоте – металлы А1, Ве, Вi, Со, Сг, Fе, Nb, Ni, РЬ, Тh и U.
При взаимодействии с окислителями в кислых растворах большинство металлов переходит в катионы, заряд которых определяется устойчивой степенью окисления данного элемента в соединениях (Nа+, Са2+,А13+,Fе2+ и Fе3+)
Восстановительная активность металлов в кислом растворе передается рядом напряжений. Большинство металлов переводится в раствор соляной и разбавленной серной кислотами, но Сu, Аg и Нg – только серной (концентрированной) и азотной кислотами, а Рt и Аи – «царской водкой».
Коррозия металлов
Нежелательным химическим свойством металлов является их коррозия, т. е. активное разрушение (окисление) при контакте с водой и под воздействием растворенного в ней кислорода (кислородная коррозия). Например, широко известна коррозия железных изделий в воде, в результате чего образуется ржавчина, и изделия рассыпаются в порошок.
Коррозия металлов протекает в воде также из-за присутствия растворенных газов СО2 и SО2; создается кислотная среда, и катионы Н+ вытесняются активными металлами в виде водорода Н2 (водородная коррозия).
Особенно коррозионно-опасным может быть место контакта двух разнородных металлов (контактная коррозия). Между одним металлом, например Fе, и другим металлом, например Sn или Сu, помещенными в воду, возникает гальваническая пара. Поток электронов идет от более активного металла, стоящего левее в ряду напряжений (Ре), к менее активному металлу (Sn, Сu), и более активный металл разрушается (корродирует).
Именно из-за этого ржавеет луженая поверхность консервных банок (железо, покрытое оловом) при хранении во влажной атмосфере и небрежном обращении с ними (железо быстро разрушается после появления хотя бы небольшой царапины, допускающей контакт железа с влагой). Напротив, оцинкованная поверхность железного ведра долго не ржавеет, поскольку даже при наличии царапин корродирует не железо, а цинк (более активный металл, чем железо).
Сопротивление коррозии для данного металла усиливается при его покрытии более активным металлом или при их сплавлении; так, покрытие железа хромом или изготовление сплава железа с хромом устраняет коррозию железа. Хромированное железо и сталь, содержащая хром (нержавеющая сталь), имеют высокую коррозионную стойкость.
Анонимный вопрос · 3 апреля 2018
14,3 K
Свойства металлов делятся на несколько групп: физические, химические, механические и технологические.
1) Физические свойства: цвет, удельный вес, плавкость, электропроводность, магнитные свойства, теплопроводность.
2) Химические свойства: окисляемость, растворимость и коррозионная стойкость.
3) Механические свойства: прочность, твердость, упругость, пластичность.
4) Технологические свойства: прокаливаемость, жидкотекучесть, ковкость, обрабатываемость резанием.
Слишком примитивно, кое-что неверно, что-то устарело (терминология). Не советую использовать.
Какой самый прочный металл?
Эксперт в области популяризации науки.
Твёрдость чистых металлов зависит от многих физических факторов и может быть разной в зависимости от условий взаимодействия при измерениях. Лидерами по твёрдости среди известных металлов являются два металла, иридий и осмий, однако, на нашей планете этих металлов очень мало. Самый доступный твёрдый на Земле металл, это титан, поэтому он занимает первую позицию, для использования его человеком.
Значение металлов и сплавов и применение их в машиностроение?
TutorOnline — одна из крупнейших онлайн-школ. Мы преподаем более 150 предметов. Наша цель… · tutoronline.ru
Материалы, используемые в машиностроении В машиностроении любое изделие, оборудование, деталь из которых они состоят, изготавливают из материалов, которые удовлетворяют техническим, экологическим, экономическим, эксплуатационным и другим требованиям, обеспечивая при этом выполнение их назначения. Такие материалы называются конструкционными. Такие детали несомненно должны выдерживать как внешнее, так и внутреннее физическое воздействие (шумоизоляция, теплоизоляция, герметизация и т.п.). Данные способности материалов проверяются при анализе их свойств. Существует довольно широкий спектр конструкционных материалов, выбором наиболее подходящего для того или иного изделия материала, удовлетворяющего все требования и себестоимость, занимаются конструкторы. Металлы и сплавы В машиностроении под металлами может пониматься как химический элемент, так и его примеси, или сплавы, которые различаются рядом свойств: Металлический блеск Высокая тепло- и электропроводность Непрозрачность Способность подвергаться обработке в холодном и горячем состоянии Металлы хорошо образуют химические соединения с неметаллами (оксиды, нитриды, бориды и т.п.), а также с другими металлами (интерметаллиды). Машиностроительные предприятия активно используют более 60 видов металлов, на их основе более 5000 сплавов. Сплав – это твердый материал, образованный путем смешивание двух и более компонентов Сплавы могут создаваться как при чистом физическом процессе (плавка, растворение, перемешивание), так и химическими воздействиями между элементами. Сплавы на основе металлов называются черными, на основе других элементов – цветными. Легкие цветные металлы сделаны на основе алюминия, магния, титана и имеют малую плотность, тяжелые же, с высокой плотностью изготовлены на основе олова, свинца, меди. Чугун Один из наиболее распространенных металлов в машиностроении. Чугун подразделяется на белый, серый, ковкий, высокопрочный. Белый чугун используется в основном для переделки в сталь, он получается при быстром охлаждении при заливки металла в форму. Имеет уменьшенное количество кремния или повышенное содержание магния. При долгом отжиге белого чугуна получают ковкий чугун, он довольно хрупкий и применяется при производстве зубчатых колес, звеньев цепей, хомуты, муфты и т.п., так как не предусматривает механического воздействия. Серый чугун имеет повышенное содержание кремния, и является основным материалом для изготовления отливок. Со временем путем воздействия на графит в момент нахождения в жидком состоянии, удалось вывести модифицированный чугун, который имеет повышенную прочность. Сталь Сталь наиболее распространенный материал в машиностроении. Он обладает ковкостью, высокой прочностью, вязкостью, хорошо обрабатывается. Стали разделяются на углеродистые и легированные. Из стали изготавливаются такие изделия как: прокат, штамповые болты, штыри, свариваемые детали, сверла, зубила, валу, зубчатые колеса и т.п. Твердые сплавы Свое место твердые сплавы нашли в горнодобывающей, металлообрабатывающей и других отраслях промышленности. Режущие инструменты, изготовленные из твердых сплавов могут работать в несколько раз более производительнее, чем простые режущие сплавы. Одним из самых прочных, но довольно молодых сплавов считается титан. К тому же такие сплавы вдвое легче. Такие сплавы применяются в изготовлении сверхзвуковых самолетов, так как титан способен выдерживать температуры превышающие 500 градусов. К тому же титан обладает коррозийной стойкостью, не окисляясь в агрессивной среде. Алюминий и алюминиевые сплавы Алюминиевые сплавы широко применяются при производстве автомобилей, самолетов, приборостроении, тракторной промышленности, многие отрасли промышленности используют алюминий на производстве. Алюминий наиболее распространенный химический элемент после кислорода. Отлично поддается штамповки, ковке, и отливу. К тому же он гораздо легче чугуна и стали. Обладает хорошей электропроводностью. Другие металлы Медь широко применяется в производстве токопроводящих деталей. Медь тяжелее стали и чугуна. Обладает хорошей пластичностью. Свинец плохой проводник тепла и тока. В промышленности применяется при производстве аккумуляторов, кабеля и т.п. Он очень мягкий и пластичный. Часто используется в соединении с другими металлами. Цинк, своего рода тяжелый металл с сильным металлическим блеском. Большое количество цинка используется для шинкования деталей. В основном цинк применяется в сплавах. Так же цинк применяют при производстве белил. Олово, довольно мягкий металл, широко применяемы в быту и промышленности, за счет устойчивости к воздуху, воды, слабым кислотам. Так же олово входит в состав припоев, антифрикционных сплавов и бронз. Баббиты – это сплав на основе меди, цинка и олова, алюминия. В основном применяются для заливки подшипников в двигателях, турбин, насосов и т.п. Бронза, разделяется на оловянную бронзу и без оловянную. Оловянные бронзы обладают высокой антикоррозийностью, а также высокими литейными свойствами. Но широкого применения они не нашли, так как олово достаточно дорогой и дефицитный металл. Зато без оловянные бронзы нашли широкое применение в промышленности. Неметаллические материалы, используемые в машиностроении Основой машиностроения служат металлы, но также свое применение находят и ряд неметаллических материалов. Практически все они плохо передают тепло, прочные, легкие, а также на порядок дешевле металлов. Примеры неметаллических материалов: Стекло органическое Пресс-материал, используется для изготовления различных деталей путем прессования. Текстолит конструкционный Гетинакс, применяется для изготовления подшипников, маховиков и тп. Паронит, служит для выпуска прокладок между неподвижными металлическими деталями Пластины резиновые и резинотканевые Войлок технический Водостойкий, обивочный картон Ткань асбестовая
Прочитать ещё 1 ответ
Какой металл самый твёрдый?
Ну довольно твердые металлы — хром, молибден, осмий.
Практического значения измерение твердости сверхчистых металлов не имеет абсолютно. Если в каком-то применении нужен именно сверхчистый металл, то твердость 63я или 117я характеристика, которая может интересовать инженера или исследователя.
А в случае сплавов данная характеристика очень резко и нелинейно меняется, даже 0.1% посторонних включений может очень резко поднять или опустить твердость.
Достаточно сказать что для различных стандартных сталей, в каждой из которых более 80% составляет очень мягкий металл железо, твердость отличается в 12-13 раз.
Какие металлы принято называть активными?
Увлекаюсь всем на свете: от моды до путешествий. Работаю помощником главного…
Активные металлы отличаются мягкостью, легкостью и невысокой температурой плавления. Как правило, у активных металлов 1-2 валентных электрона, находящихся на достаточном удалении от ядра. Наиболее активными считаются литий, натрий, калий, цезий, рубидий.
Степень активности металла можно посмотреть в электрохимическому ряду напряжений металлов. Чем левее от водорода расположен элемент, тем более он активен.
Как обозначается металл в химии?
Невское Оборудование поставщик металлообрабатывающего оборудования и станков · spbstanki.ru
Возможно, что под обозначением вы имеете в виде «Ме», так обозначают металлы в химии на общих схемах различных химических реакций (окисления, восстановления и т.д..) Но у каждого металла, как у простого вещества, есть свое принятое обозначение в таблице Менеделева: Fe (железо); Na (натрий) и т.д..
