Какие свойства фермента характеризуются константой михаэлиса
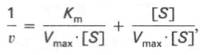
Константа Михаэлиса Км — весьма удобный количественный параметр, помогающий установить, каким образом данный фермент будет реагировать при тех условиях, которые имеются в живой клетке.
Иными словами, Км представляет собой концентрацию субстрата, при которой скорость реакции равна половине максимальной. Если фермент характеризуется высоким значением Км, то это означает, что потребуется много субстрата для того, чтобы увеличить скорость катализируемой этим ферментом реакции до половины максимальной; низкая величина Км указывает на то, что для насыщения фермента достаточно небольшого количества субстрата. Из этих положений следует также, что фермент-субстратные пары с низким значением Км характеризуются высоким сродством друг к другу и наоборот.
Кроме того, величина Км помогает решить вопрос о том, какие из групп субстратов будут наиболее эффективно связываться с данным ферментом. Если фермент не обладает строгой специфич ностью, то в присутствии обычных концентраций реагентов, имею щихся в клетке, он будет предпочтительно катализировать реакцию, протекающую при участии того субстрата, для которого характерна наиболее низкая величина /См при взаимодействии с данным ферментом. Знание концентраций различных субстратов в клетке и величин /См при взаимодействии этих субстратов с ферментами позволяет оценить вклад отдельных реакций в процесс обмена веществ в организме в целом, а также установить, какая из этих реакций лимитирует скорость всего процесса. Выяснение этих вопросов совершенно необходимо для понимания воздействия физиологических регуляторных факторов, таких, как гормоны, на скорость метаболических реакций.
Влияние концентрации фермента на реакцию
Хотя величина Км характерна и постоянна для каждой фермент-субстратной пары, величина Vmax прямо пропорциональна количеству имеющегося в системе фермента. Действительно, можно показать алгебраически, что Vmаx=k [Е], где [Е] — концентрация фермента, a k — константа скорости для реакций, описанных выше при рассмотрении этапов (3) и (4). Измерение Vmax» или скорости ферментативной реакции в присутствии насыщающей концентрации субстрата, фактически служит мерой числа имеющихся в клетке молекул фермента. Хотя не всегда удается выразить [Е] в молях на литр, поскольку величина k не всегда известна, можно допустить, что измерение активности фермента при оптимальных условиях дает истинное представление об относительных количествах фермента.
В число условий, оптимальных для действия фермента, включают, кроме обеспечения достаточной для насыщения фермента концентрации субстрата, соответствующие физические параметры (температура, рН среды, степень ионизации), а также наличие любых дополнительных факторов, которые могли бы способствовать каталитическому процессу.
— Читать «Влияние температуры на реакцию. Оптимальная температура ферментной реакции»
Оглавление темы «Ферментативные реакции в организме»:
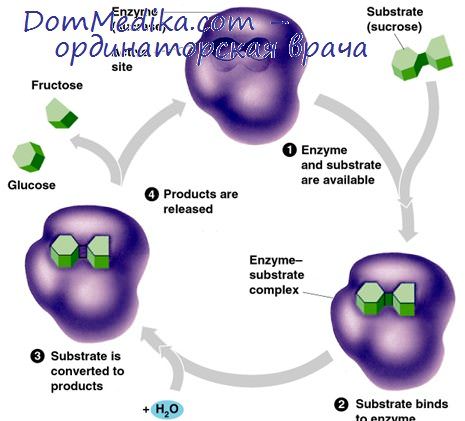
1. Ферментный катализ. Механизмы ферментного катализа
2. Соединение субстрата с ферментом. Конкурентное торможение
3. Концентрация субстрата. Влияние концентрации субстрата на ферментативную реакцию
4. Константа Михаэлиса. Влияние концентрации фермента на реакцию
5. Влияние температуры на реакцию. Оптимальная температура ферментной реакции
6. Оптимальная температура человека. Влияние pH на реакции в организме
7. Влияние ионов на химические реакции. Кофакторы и коферменты
8. Ингибиторы ферментов. Механизмы действия ингибиторов ферментов
9. Аллостерические модификаторы. Механизм действия модификаторов
10. Положительные модификаторы. Активация зимогенов
Большая Советская энциклопедия
один из важнейших параметров кинетики ферментативных реакций, введённый немецкими учёными Л. Михаэлисом (L. Michaelis) и М. Ментен в 1913; характеризует зависимость скорости ферментативного процесса от концентрации субстрата. Согласно теории Михаэлиса — Ментен, первым этапом любого ферментативного процесса является обратимая реакция между ферментом (Е) и субстратом (S), приводящая к образованию промежуточного фермент-субстратного комплекса (ES), который затем подвергается практически необратимому расщеплению на продукт реакции (Р) и исходный фермент:
Реакции образования и распада комплекса ES характеризуются константами скорости k1, k-1, k2. Если концентрация субстрата значительно превышает концентрацию фермента ([S] >> [E]) и, следовательно, концентрация ES становится постоянной, скорость ферментативной реакции (υ) выражается уравнением:
где V — максимальная скорость реакции, достигаемая при полном насыщении фермента субстратом. Соотношение констант скорости
также является константой (Кm), получившей название М. к. Подставляя в уравнение (2) М. к., получаем уравнение Михаэлиса — Ментен:
Из уравнения (3) следует, что М. к. численно равна концентрации субстрата, при которой скорость реакции составляет половину максимально возможной (см. рис.). В ряде случаев, когда величина k1 мала и ею можно пренебречь, М. к. становится равной
и может служить мерой сродства субстрата к ферменту. М. к. имеет размерность концентрации. Практически величину М. к. находят различными графическими методами, исследуя зависимость скорости ферментативной реакции от концентрации субстрата. См. также Ферментативный катализ.
Лит.: Яковлев В. А., Кинетика ферментативного катализа, М., 1965; Уэбб Л., Ингибиторы ферментов и метаболизма, пер. с англ., М., 1966. Д.
Д. М. Беленький.
Зависимость скорости ферментативной реакции (υ)от концентрации субстрата [S].
- константа Михаэлиса — Michaelis constant, Km — .Kинетический параметр ферментативной реакции, численно равный концентрации субстрата, при которой скорость реакции составляет половину максимальной…
Молекулярная биология и генетика. Толковый словарь
- Константа — постоянная величина. Постоянство величины х обозначается символически записью х = const…
Начала современного Естествознания
- Михаэлиса синдром — Наблюдается при патологии промежуточного мозга и включает в себя явления депрессии, повышенной сонливости и прожорливости либо мании, осложненной дисфориями и параноидными эпизодами…
Толковый словарь психиатрических терминов
- Прибор Михаэлиса — лабораторный прибор рычажного типа для определения предела прочности при изгибе образцов-балочек из цементного раствора с нагружением образца ведерком с дробью из бункера прибора…
Строительный словарь
- КОНСТАНТА — в математике и других науках — величина или коэффициент, не подвергающийся изменению. Константа может быть универсальной, как число , или конкретной, как коэффициенты, введенные в алгебраическое уравнение…
Научно-технический энциклопедический словарь
- КОНСТАНТА — остающееся неизменным при всех изменениях и расчетах…
Философская энциклопедия
- КОНСТАНТА — постоянная величина. Постоянство величины х символически записывают х = const…
Естествознание. Энциклопедический словарь
- аппарат Михаэлиса — см. Михаэлиса аппарат…
Большой медицинский словарь
- Михаэлиса аппарат — комплект для определения концентрации водородных ионов колориметрическим методом, состоящий из простейшего колориметра и набора эталонов — пробирок с жидкостью, окрашенной индикаторами…
Большой медицинский словарь
- Михаэлиса ромб — см. Крестцовый…
Большой медицинский словарь
- Фульда-Гросса-Михаэлиса метод — метод измерения активности трипсина в панкреатическом соке, основанный на определении максимальной степени разведения, при которой он способен переварить определенное количество казеина…
Большой медицинский словарь
- КОНСТАНТА — пост. величина. Постоянство величины х записывают: х = const…
Большой энциклопедический политехнический словарь
- Константа — постоянная величина в математике, физике, химии и других отраслях науки и техники, часто обозначаемая буквами С или К. К физическим константам относятся: c ≈ 3 • 108 м/с — скорость света в вакууме…
Энциклопедический словарь по металлургии
- Константа — I Конста́нта постоянная величина в математических, физических и химических исследованиях. Постоянство величины х символически записывают х = const…
Большая Советская энциклопедия
- Михаэлиса константа — один из важнейших параметров кинетики ферментативных реакций, введённый немецкими учёными Л. Михаэлисом и М. Ментен в 1913…
Большая Советская энциклопедия
- КОНСТАНТА — постоянная величина. Постоянство величины х символически записывают х=const…
Большой энциклопедический словарь
«Михаэлиса константа» в книгах
7. КОНСТАНТА ЛИВАНОВА
Существует множество эмпирических зависимостей, называемых законами. В качестве примеров можно назвать основной психофизический закон, устанавливающий зависимость силы ощущения от физической интенсивности стимула, закон постоянства скорости
7. КОНСТАНТА ЛИВАНОВА
Существует множество эмпирических зависимостей, называемых законами. В качестве примеров можно назвать основной психофизический закон, устанавливающий зависимость силы ощущения от физической интенсивности стимула, закон постоянства скорости
Константа разума
— Ну, хорошо, — согласился Скептик. — Не получается — подсмотрим у соседей. А они где берут? Где подсмотреть самое первое — то, что нет ни у кого? Ведь должно же быть что-нибудь самое первое?!Нас губит «одна, но пламенная страсть» — к упрощению. Упрощаем
Сакральная константа
Что-то здесь должно свидетельствовать об универсальной константе, геометрической модели. Хорошо известно, что Vesica Piscis создавалась с помощью сакральной геометрии, а сейчас современная наука обнаружила такую же удивительную форму в коррелированных
12. КОНСТАНТА ЖИЗНИ
Августин Блаженный невесело пошутил: «Я прекрасно знаю, что такое время, пока меня об этом не спросят». За полторы тысячи лет ничего не изменилось: о природе времени мы знаем не больше, чем рыба о воде. Время может тянуться, идти и лететь, — но мы
«Образец веры» Константа II
Церковная политика после смерти Ираклия, при Константе II, сводилась к следующему: после потери Египта, перешедшего в сороковых годах VII века к арабам, император, оставаясь сторонником монофелитства, несмотря на то, что этот вопрос потерял уже
«Образец веры» Константа II
Церковная политика после смерти Ираклия, при Константе II, сводилась к следующему: после потери Египта, перешедшего в сороковых годах VII века к арабам, император, оставаясь сторонником монофелитства, несмотря на то, что этот вопрос потерял уже
Некая константа
«Кто был в Италии, тот скажет «прощай» другим землям. Кто был на небе, тот не захочет на землю». Эти слова принадлежат классику русской литературы Николаю Гоголю.Когда солнечная Италия стала для обитателей снежной Московии земным воплощением рая,
Константа RES_USE_INET6
Поскольку функция gethostbyname не имеет аргумента для указания нужного семейства адресов (подобного hints.ai_family для getaddrinfo), в первом варианте API использовалась константа RES_USE_INET6, которая должна была добавляться к флагам распознавателя посредством внутреннего
14.2.2. Константа ARGF
Глобальная константа ARGF представляет псевдофайл, получающийся в результате конкатенации всех имен файлов, заданных в командной строке. Во многих отношениях она ведет себя так же, как объект IO.Когда в программе встречается «голый» метод ввода (без
Психическая константа
Вот есть мозг. Центральная нервная система. Кора и подкорка. Нейроны и сосуды.И вот есть мощность человеческого организма. Которую в сущности можно измерить. Надо взять потребляемую энергию на килограмм веса – и суммарную производимую работу на
Константа правды
Людям вообще трудно что-то предвидеть. В частности, то, что стало происходить с нашим телевидением, его федеральными каналами. Вот две цитаты, первая из статьи 2008 года «Суверенный экран» («ЛГ», № 36): «Вопрос о создании хотя бы одного телеканала, который
Одним из
характерных проявлений жизни является удивительная способность живых организмов
кинетически регулировать химические реакции, подавляя стремление к достижению
термодинамического равновесия. Ферментативная кинетика занимается исследованием
закономерностей влияния химической природы реагирующих веществ (ферментов,
субстратов) и условий их взаимодействия (концентрация, рН среды, температуры,
присутствие активаторов или ингибиторов) на скорость ферментативной реакции.
Главной целью изучения кинетики ферментативных реакций является получение
информации, которая может способствовать выяснению молекулярного механизма
действия фермента.
Общие
принципы кинетики химических реакций применимы и к ферментативным реакциям.
Известно, что любая химическая реакция характеризуется константой
термодинамического равновесия. Она выражает состояние химического равновесия,
достигаемого системой, и обозначается Кр.
Так, для реакции:
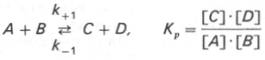
константа
равновесия равна произведению концентраций образующихся веществ, деленному на
произведение концентрации исходных веществ. Значение константы равновесия
обычно находят из соотношения констант скоростей прямой (k+1) и
обратной (k–1 ) реакций, т.е. Кp = k+1/k–1. В
состоянии равновесия скорость прямой реакции: v+1
= k +1[ А ]
• [ B ] равна
скорости обратной реакции: v–1
= k –1 [ С ]
• [ D ] , т.
е. v+1 = v–1 соответственно k+1[А]•[B] = k–1[С]•[D], или
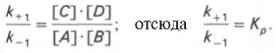
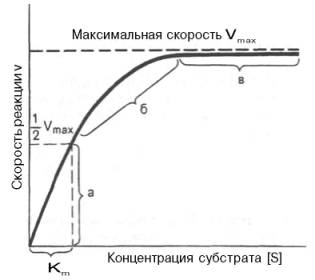
Рис. 4.12. Теоретический график зависимости скорости
ферментативной реакции от концентрации субстрата при постоянной концентрации
фермента.
а — реакция
первого порядка (при [ S ] < Кm скорость реакции
пропорциональна концентрации субстрата); б — реакция смешанного порядка; в —
реакция нулевого порядка, когда v = Vmaxи
скорость реакции не зависит от концентрации субстрата.
Таким
образом, константа равновесия равна отношению констант скоростей прямой и
обратной реакций. Величину, обратную константе равновесия, принято называть
субстратной константой, или, в случае ферментативной реакции, константой
диссоциации фермент–субстратного комплекса, и обозначать символом KS. Так,
в реакции
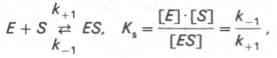
т.е. KSравна
отношению произведения концентрации фермента и субстрата к концентрации
фермент-субстратного комплекса или отношению констант скоростей обратной и
прямой реакций. Следует отметить, что константа KSзависит
от химической природы субстрата и фермента и определяет степень их сродства.
Чем ниже значение KS, тем
выше сродство фермента к субстрату.
При изучении
кинетики ферментативных реакций следует учитывать одну важную особенность этих
реакций (не свойственную обычным химическим реакциям), связанную с явлением
насыщения фермента субстратом. При низкой концентрации субстрата зависимость
скорости реакции от концентрации субстрата (рис. 4.12) является почти линейной
и подчиняется кинетике первого порядка. Это означает, что скорость реакции S —> Р прямо пропорциональна концентрации
субстрата S и в любой момент времени t определяется следующим кинетическим уравнением:
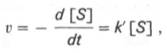
где [S] – молярная концентрация
субстрата S; –d[S]/dt – скорость убыли субстрата; k’ – константа скорости реакции, которая в данном случае имеет
размерность, обратную единице времени
(мин–1 или с–1).
При высокой концентрации
субстрата скорость реакции максимальна, становится постоянной и не зависящей от
концентрации субстрата [ S ] . В
этом случае реакция подчиняется кинетике нулевого порядка v = k»
(при полном
насыщении фермента субстратом) и целиком определяется концентрацией фермента.
Различают, кроме того, реакции второго порядка, скорость
которых пропорциональна произведению концентраций двух реагирующих веществ. В
определенных условиях при нарушении пропорциональности говорят иногда о
реакциях смешанного порядка (см. рис. 4.12).
Изучая
явление насыщения, Л. Михаэлис и М. Ментен разработали общую теорию
ферментативной кинетики. Они исходили из предположения, что ферментативный
процесс протекает в виде следующей химической реакции:
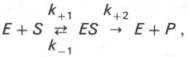
т.е. фермент Е вступает во взаимодействие с субстратом S с образованием промежуточного комплекса ES, который далее распадается
на свободный фермент и продукт реакции Р.
Математическая обработка на основе закона действующих масс дала возможность
вывести уравнение, названное в честь авторов уравнением Михаэлиса–Ментен,
выражающее количественное соотношение между концентрацией субстрата и скоростью
ферментативной реакции:
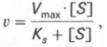
где v – наблюдаемая скорость реакции при
данной концентрации субстрата [S]; KS– константа
диссоциации фермент-субстратного комплекса, моль/л; Vmax–
максимальная скорость реакции при полном насыщении фермента субстратом.
Из уравнения
Михаэлиса–Ментен следует, что при высокой концентрации субстрата и низком
значении KSскорость реакции является
максимальной, т.е. v = Vmax(реакция нулевого порядка, см. рис. 4.12). При низкой концентрации
субстрата, напротив, скорость реакции оказывается пропорциональной концентрации
субстрата в каждый данный момент (реакция первого порядка).
Следует
указать, что уравнение Михаэлиса–Ментен в его классическом виде не учитывает
влияние на скорость ферментативного процесса продуктов реакции, например в
реакции
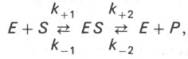
и носит
несколько ограниченный характер. Поэтому были предприняты попытки
усовершенствовать его. Так, было предложено уравнение Бриггса-Холдейна:
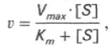
где Кm представляет собой константу
Михаэлиса, являющуюся экспериментально определяемой величиной. Она может быть
представлена следующим уравнением:
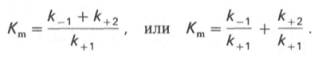
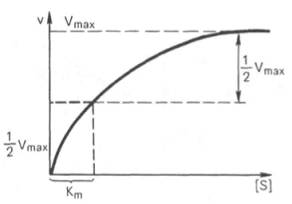
Рис. 4.13. Кривая
уравнения Михаэли-са-Ментен: гиперболическая зависимость начальных скоростей
катализируемой ферментом реакции от концентрации субстрата.
В числителе
представлены константы скоростей распада комплекса ES в
двух направлениях (в сторону исходных Е и S и в сторону
конечных продуктов реакции Е и Р). Отношение k–1/ k+1представляет собой константу диссоциации ферментсубстратного комплекса KS,
тогда:
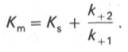
Отсюда
вытекает важное следствие: константа Михаэлиса всегда больше константы
диссоциации фермент-субстратного комплекса KSна
величину
k+2/k+1.
Для
определения численного значения Кm
обычно находят ту концентрацию субстрата, при которой скорость ферментативной
реакции v составляет половину от
максимальной Vmax, т.е.
если v = 1/2
Vmaх. Подставляя
значение v в уравнение
Бриггса–Холдейна, получаем:
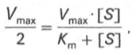
разделив обе
части уравнения на Vmах,
получим
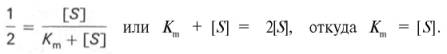
Таким
образом, константа Михаэлиса численно равна концентрации субстрата (моль/л),
при которой скорость данной ферментативной реакции составляет половину от
максимальной.
Определение
величины Кm имеет важное значение при выяснении механизма действия
эффекторов на активность ферментов и т.д. Константу Михаэлиса можно вычислить
по графику (рис. 4.13). Отрезок на абсциссе, соответствующий скорости, равной
половине максимальной, будет представлять собой Кm.
Пользоваться
графиком, построенным в прямых координатах зависимости начальной скорости
реакции v0 от
начальной концентрации субстрата [S0], неудобно,
поскольку максимальная скорость Vmaxявляется в данном случае асимптотической
величиной и определяется недостаточно точно.
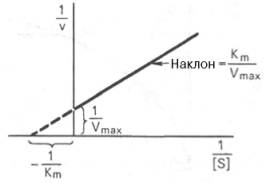
Рис. 4.14. График Лайнуивера-Бэрка.
Для более
удобного графического представления экспериментальных данных Г. Лайнуивер и Д.
Бэрк преобразовали уравнение Бриггса–Хол-дейна по методу двойных обратных
величин исходя из того принципа, что если существует равенство между двумя
какими-либо величинами, то и обратные величины также будут равны. В частности,
если
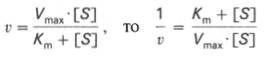
или
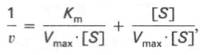
то после
преобразования получаем уравнение:
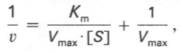
которое
получило название уравнения Лайнуивера–Бэрка. Это уравнение прямой линии: у = ах +
b. Если теперь в соответствии с этим
уравнением построить график в координатах 1/v
(y) от
l/[S] (x),
то получим прямую линию (рис. 4.14), тангенс угла наклона который будет
равен величине Km/Vmax; отрезок,
отсекаемый прямой от оси ординат, представляет собой l/Vmax(обратная величина
максимальной скорости). Если продолжить прямую линию за ось ординат, тогда на
абсциссе отсекается отрезок, соответствующий обратной величине константы
Михаэлиса – 1/Кm (см.
рис. 4.14). Таким образом, величину Кm
можно вычислить из данных наклона прямой и длины отрезка, отсекаемого от оси
ординат, или из длины отрезка, отсекаемого от оси абсцисс в области
отрицательных значений.
Следует
подчеркнуть, что значения Vmax, как и
величину Кm, более
точно, чем по графику, построенному в прямых координатах, можно определить по
графику, построенному по методу двойных обратных величин. Поэтому данный метод
нашел широкое применение в современной энзимологии. Предложены также
аналогичные графические способы определения Кm и Vmaxв координатах зависимости v от
v/[S] и [S]/v от [S].
Следует
отметить некоторые ограничения применения уравнения Ми-хаэлиса–Ментен,
обусловленные множественными формами ферментов и аллостерической природой
фермента. В этом случае график зависимости начальной скорости реакции от
концентрации субстрата (кинетическая
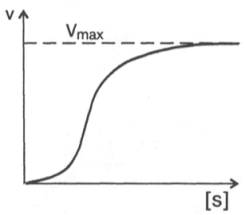
Рис. 4.15. Сигмоидная кинетическая кривая насыщения
субстратом.
кривая) имеет
не гиперболическую форму, а сигмоидный характер (рис. 4.15) наподобие кривой
насыщения гемоглобина кислородом. Это означает, что связывание одной молекулы
субстрата в одном каталитическом центре повышает связывание субстрата с другим
центром, т.е. имеет место кооперативное взаимодействие, как и в случае
присоединения кислорода к 4 субъединицам гемоглобина. Для оценки концентрации
субстрата, при которой скорость реакции составляет половину максимальной, в
условиях сигмоидного характера кинетической кривой обычно применяют
преобразованное уравнение Хилла:
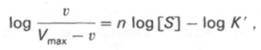
где К’ – константа
ассоциации; n – число субстратсвязывающих центров.
Еще по теме:
- ФЕРМЕНТАТИВНЫХ РЕАКЦИЙ КИНЕТИКА — химическая энциклопедия
- Кинетика ферментативных реакций — Наглядная биохимия
