В какой строке перечислены свойства веществ твердое жидкое газообразное
Описание презентации по отдельным слайдам:
1 слайд

Описание слайда:
Что учёные называют телами? А) Все предметы, которые окружают нас. Б) Только живые существа. В) Части животных организмов. А Б В
2 слайд

Описание слайда:
Продолжи. Вещество-это то,… А) из чего состоят тела. Б) что может изменять форму. В) что люди используют в пищу. Г) из чего делают вещи. А Б В Г
3 слайд

Описание слайда:
В какой строке перечислены состояния веществ? А) Хрупкое, пластичное, прозрачное. Б) Большое, маленькое, длинное. В) Твердое, жидкое, газообразное. Г) Овальное, круглое, квадратное. А Б В Г
4 слайд

Описание слайда:
Какими свойствами обладают жидкости? А) Сохраняют форму. Б) Сохраняют свой объём. В) Летучи. Г) Текучи. А Б В Г
5 слайд

Описание слайда:
Какой из материалов создан человеком? А) Полиэтилен. Б) Древесина. В) Мрамор. А Б В
6 слайд

Описание слайда:
Какой прибор поможет разглядеть, что находится в капле болотной воды? А) Лупа. Б) Телескоп. В) Термометр. Г) Микроскоп. А Б В Г
7 слайд

Описание слайда:
Какие материалы являются природными? А) Пластмасса. Б) Глина. В) Пластилин. Г) Резина А Б В Г
8 слайд

Описание слайда:
Что является главной частью лупы и микроскопа? А) Объектив. Б) Окуляр. В) Линза. Г) Ручка. А Б В Г
9 слайд

Описание слайда:
Почему становится невидимым кусочек сахара в горячем чае? А) Молекулы сахара улетучились. Б) Его скрывает коричневый цвет чая. В) Он растворяется на отдельные молекулы, а они не видимы. А Б В
10 слайд

Описание слайда:
Из чего состоит всё живое? А) Из живого вещества. Б) Из клеток. В) Из ящиков. А Б В
11 слайд

Описание слайда:
Что НЕ относится к телам живой природы? А) растения Б) дождь В) животные Г) человек А Б В Г
12 слайд

Выберите книгу со скидкой:
БОЛЕЕ 58 000 КНИГ И ШИРОКИЙ ВЫБОР КАНЦТОВАРОВ! ИНФОЛАВКА
Инфолавка — книжный магазин для педагогов и родителей от проекта «Инфоурок»

Курс профессиональной переподготовки
Учитель начальных классов

Курс повышения квалификации

Курс повышения квалификации
Найдите материал к любому уроку,
указав свой предмет (категорию), класс, учебник и тему:
также Вы можете выбрать тип материала:
Общая информация
Номер материала:
ДВ-102083
Вам будут интересны эти курсы:
Оставьте свой комментарий
Учебник для 6 класса
ФИЗИКА
Притяжение и отталкивание частиц определяют их взаимное расположение в веществе. А от расположения частиц существенно зависят свойства веществ. Так, глядя на прозрачный очень твердый алмаз (бриллиант) (рис. 111, а) и на мягкий черный графит (рис. 111, б) (из него изготавливают стержни карандашей), мы не догадываемся, что оба вещества состоят из совершенно одинаковых атомов углерода. Просто в графите эти атомы расположены иначе, чем в алмазе.

Рис. 111
Заметим, что на рисунках изображены не сами атомы, а их модели — шарики и в действительности никаких соединительных стержней или проволочек между ними нет. Это — условное изображение расположения атомов в веществе.
Взаимодействие частиц вещества приводит к тому, что оно может находиться в трех состояниях: твердом, жидком и газообразном. Например, лед, вода, пар (рис. 112). В трех состояниях может находиться любое вещество, но для этого нужны определенные условия: давление, температура. Например, кислород в воздухе — газ, но при охлаждении ниже -193°С он превращается в жидкость, а при температуре -219°С кислород — твердое вещество. Железо при нормальном давлении и комнатной температуре находится в твердом состоянии. При температуре выше 1539°С железо становится жидким, а при температуре выше 3050°С — газообразным. Жидкая ртуть, используемая в медицинских термометрах, при охлаждении до температуры ниже -39°С становится твердой. При температуре выше 357°С ртуть превращается в пар (газ).

Рис. 112
Превращая металлическое серебро в газ, его напыляют на стекло и получают «зеркальные» очки.
Какими свойствами обладают вещества в различных состояниях?
Начнем с газов, в которых поведение молекул (рис. 113) напоминает движение пчел в рое. Однако пчелы в рое самостоятельно изменяют направление движения и практически не сталкиваются друг с другом. В то же время для молекул в газе такие столкновения не только неизбежны, но происходят практически непрерывно. В результате столкновений направления и значения скорости движения молекул изменяются.

Рис. 113
Результатом такого движения и отсутствия взаимодействия частиц при движении является то, что газ не сохраняет ни объема, ни формы, а занимает весь предоставленный ему объем. Каждый из вас посчитает сущей нелепицей утверждения: «Воздух занимает половину объема комнаты» и «Я накачал воздух в две трети объема резинового шарика». Воздух, как и любой газ, занимает весь объем комнаты и весь объем шарика.
А какие свойства имеют жидкости? Проведем опыт.

Рис. 114
Перельем воду из мензурки 1 в мензурку 2. Форма жидкости изменилась, но объем воды остался тем же (рис. 114). Молекулы не разлетелись по всему объему, как это было бы в случае с газом. Значит, взаимное притяжение молекул жидкости существует, но оно не удерживает жестко соседние молекулы. Они колеблются и перескакивают из одного места в другое (рис. 115), чем и объясняется текучесть жидкостей.

Рис.115
Наиболее сильным является взаимодействие частиц в твердом теле. Оно не дает возможности частицам разойтись. Частицы лишь совершают хаотические колебательные движения около определенных положений (рис. 116). Поэтому твердые тела сохраняют и объем, и форму. Резиновый мяч будет сохранять форму шара и объем, куда бы его не поместили: в банку, на стол и т. д.

Рис. 116
Подумайте и ответьте
- Какими основными свойствами обладает газ?
- Почему жидкость не сохраняет форму?
- Чем отличается твердое состояние вещества от жидкого и газообразного?
- Отличаются ли молекулы воды от молекул льда?
- Какие из перечисленных веществ в обычных условиях (при комнатной температуре и нормальном давлении) находятся в газообразном состоянии, а какие — в жидком или твердом: олово, бензин, кислород, железо, ртуть, воздух, стекло, пластмасса?
- Может ли ртуть находиться в твердом состоянии, а воздух — в жидком? При каких условиях?
Домашнее задание
- В пластмассовую бутылку (0,5 л) налейте доверху воду и закройте герметично крышкой. Попробуйте сжать в бутылке воду. Затем вылейте воду и снова закройте бутылку. Теперь сожмите в ней воздух. На основании результатов опыта выскажите гипотезу о строении газов и жидкостей.
- Задание-конкурс: составьте таблицу, в которой сравните характер движения, взаимодействия частиц, а также свойства вещества в газообразном, твердом и жидком состояниях. Победителем конкурса будет тот, чья таблица содержит наиболее полную и правильную информацию.
Повторим главное в изученном
- Все вещества состоят из отдельных частиц (атомов, молекул), между которыми имеются расстояния.
- Частицы веществ непрерывно и хаотически движутся.
- Скорость движения частиц тем больше, чем выше температура тела.
- Диффузией называется явление взаимного проникновения веществ друг в друга. Особенно быстро диффузия протекает в газах, медленнее — в жидкостях, очень медленно — в твердых телах. При увеличении температуры диффузия идет быстрее.
- На расстояниях, больших, чем размеры самих частиц, преобладает притяжение частиц. На расстояниях, меньших размеров самих частиц, — отталкивание. Притяжение частиц очень быстро ослабевает при их удалении друг от друга.
- Изменение размеров тела при его нагревании называется тепловым расширением.
- Тепловое расширение разных твердых и жидких веществ различно, а всех газов — одинаково.
Анонимный вопрос · 14 февраля 2018
1,2 K
Какое самое плотное газообразное вещество в мире?
Химик. Пытаюсь сделать мир немножко лучше. · koa.su
Если считать все рассматриваемые газы идеальными, то плотность газа зависит только от величины молярной массы соединения (на самом деле плотность газов, состоящих из сложных молекул, значительно отличается от рассчитанной для идеальных газов).
Вкратце говоря, поиск самого тяжелого газа ограничивается лишь информацией о существовании соединений и знанием агрегатного состояния вещества при необходимых условиях.
Вот что пришло мне на ум (комн. т.):
WF6 — 396 г/моль,
IF7 — 259 г/моль,
Rn — 222 г/моль,
список можно продолжать.
Как объясняют давление газа на основе учения о движении молекул?
Люблю фантастику, вязание, начинающий садовод
Давление газа на стенки сосудов вызывается ударами молекул газа.
У газов нет ни формы ни постоянного объема. Они могут заполнить любой объем.
Количество молекул в каждом кубическом сантиметре увеличивается при сжатии (уменьшается при расширении) от этого число ударов о стенки сосуда увеличивается (уменьшается). Поэтому чем больший сосуд газ заполняет, тем меньше давление и наоборот.
Газ одинаково давит по всем направлениям, как пример -когда надуваешь воздушный шар, то он надувается равномерно.
Если газ находиться в маленьком объеме, то давление на стенки становится огромным, поэтому газ удобнее и безопаснее заключать в специальные прочные стальные баллоны.
Прочитать ещё 1 ответ
Железо твёрдое, потому что в нём молекулы и атомы спрессованы ближе друг у другу или в чём причина?
Researcher, Institute of Physics, University of Tartu
Нужно сначала избежать путаницы — «твердое» может значить две вещи: 1) агрегатное состояние, как твердое-жидкое-газ, и 2) механическая характеристика — твердость, как алмаз твердый, а мел — мягкий. Эти вещи в принципе связаны, но связь сложна и неоднозначная, поэтому не будем о ней :). Вероятно, Вы имеете в виду второе, механическую твердость (хотя железо отнюдь не чемпион, а вполне себе средненький материал по твердости, скорее для него имеет смысл говорить о довольно высокой прочности и пластичности).
Вы правы в том, что чем ближе элементы (молекулы, атомы, ионы) решетки друг к другу, тем прочнее будет свзь между ними. Но ключевым параметром здесь является тип химической связи, поскольку расстояние между атомами (молекулами, ионами) в решетке во многом определяется именно типом связи. Для железа, как и для других металлов, характерен металлический тип связи, когда, ну скажем, ионы металла в узлах решетки, а вокруг них общее электронное облако (это не совсем точное описание, но сгодится). Это дает 1) пластичность, поскольку связь кулоновская, а значит ненаправленная + ослабевает не так быстро при изменении расстояния. То есть, при сдвиге ионов из позиций (при механическом воздействии) связи не рвутся сразу, а имеют некий «запас прочности», 2) прочность, поскольку кулоновское взаимодействие достаточно сильное. Вот металлы они такие и есть — пластичные и прочные. Степень прочности/пластичности/твердости будет определяться во многом симметрией решетки, параметрами электронного газа и т.д.
Это можно сравнить с атомными кристаллами (типа того же алмаза) с ковалентными связями между атомами в узлах решетки (твердость может быть и повыше, поскольку если расстояние между атомами короткие, то энергия связи может быть очень высока. Зато пластичности никакой — связь направленная, любое смещение атома ее рвет). Или с молекулярными кристаллами, где связь между молекулами в узлах решетки Ван-дер-ваальсова (прочность никакая, поскольку энергия связи маленькая, зато пластичность может быть неплохая, поскольку связь ненаправленная, вопрос только в том, чтобы механическое воздействие было не слишком сильное, поскольку независимо от пластичности предел прочности очень низкий). Решетки с одним и тем же типом химсвязи всегда будут иметь много общего, хотя и могут различаться между собой достаточно сильно по количественным критериям в зависимости от других параметров.
Существует три основные состояния вещества — газообразное, жидкое и твердое. В физике эти состояния называют агрегатными. Итак, агрегатное состояние вещества называют физическое состояние, которое напрямую зависит от таких основных характеристик как давление и температура.
Пребывая в том или ином состоянии, веществам свойственны разнообразные структуры. Кроме перечисленных трех основных агрегатных состояний существуют и другие, но мы в рамках статьи не будем в них углубляться.
- Влияние энергии движения частиц на свойства агрегатных состояний веществ
- Твердое агрегатное состояние
- Жидкое агрегатное состояние
- Газообразное агрегатное состояние
- Точка плавления
- Точка кипения
- Влияние давления и различных примесей на кипение или плавление

Влияние энергии движения частиц на свойства агрегатных состояний веществ
Как известно, любое вещество состоит из молекул, которые в свою очередь делятся на атомы. В качестве частиц кроме молекул могут рассматриваться и ионы, в которые превращаются атомы или их группы. На самом деле, ионы или молекулы имеют сложную форму построения, но для упрощения их построения и создания визуальной наглядности их представляют в сферическом виде.
Абсолютно во всех веществах сила взаимного притяжения между их частицами препятствуют их передвижению друг относительно друга. Однако с ростом температуры кинетическая энергия частиц начинает расти и тем создавая все большее противодействие силе притяжения между частицами. Агрегатное состояние вещества зависит от отношения приобретенной кинетической энергии частицы к силе их взаимного притяжения.

Проще говоря, от того, насколько свободно и дальше может «гулять» молекулы относительно других и зависит текущее физическое состояние вещества. Изменяя показатели температуры и давления можно наблюдать переход из одного состояния в другое.
Самый распространенный пример перехода из одного состояния в другое в жизни можно наблюдать на примере трех состояний молекулы воды: твердом в качестве льда при температуре ниже 0 0С, жидком при температуре выше 00С и газообразном паре, который образуется после закипания воды при температуре 100 0С и выше.
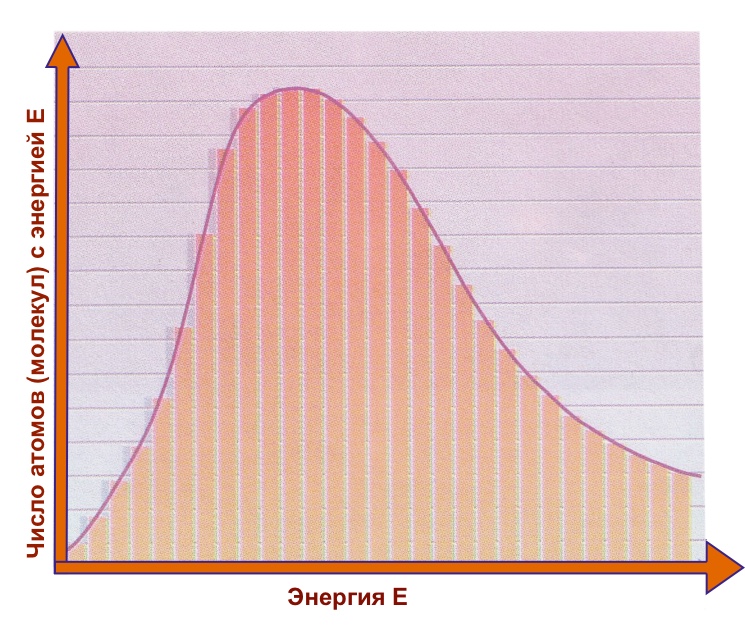
На этом графике показано, как изменяется энергия частиц вещества в твердом, жидком и газообразном состояниях. Чем больше энергия, тем быстрее частицы движутся или колеблются. Небольшая доля частиц обладает очень низкой или очень высокой энергией.
Твердое агрегатное состояние
В твердых веществах за счет сильного взаимного притяжения у частиц нет возможности развивать необходимую кинетическую энергию и тем самым передвигаться свободно от заданной позиции при условии сохранения текущей температуры и давления. Частицы твердых веществ располагаются тесно друг от друга и образуют определенную структуру, которую называют кристаллической решеткой.
В твердом веществе молекулы плотно «упакованы». Как правило они образуют регулярную структуру, называемую кристаллической решеткой.
Эталонным примером регулярной кристаллической решетки является кристалл.
Жидкое агрегатное состояние
Отличительным свойством жидкости является их текучесть, вследствие чего они способны менять свою форму. Жидкость, налитая в сосуд, моментально принимает его форму и под воздействием гравитационной силы Земли располагается на его дне. Граница верхней поверхности жидкости при этом образует гладкую плоскость. Кинетическая энергия движения молекул воды превосходит их взаимное притяжение, которое не способно в свою очередь удержать их не месте. Молекула воды словно перекатывается от одной к другой создавая видимую нашим глазом текучесть.
Молекулы жидкости могут свободно двигаться как и молекулы газ. Однако «упакованы» они плотнее, что больше похоже на твердое вещество.
Жидкость, в отличие от твердых тел, не имеет кристаллической решетки.
Газообразное агрегатное состояние
Газообразное вещество как и жидкость заполняет сосуд, только в отличии от жидкости — весь его объем. Прощу говоря, наполовину налитая жидкость в сосуд не может заполнить весь ее объем, а газ может. Это достигается благодаря очень высокой кинетической энергии молекул газа, которая в разы превосходит энергию их взаимного притяжения, а также гравитационную силу. Поэтому газ не скатывается как жидкость на дно сосуда. Газ, как и жидкость не имеет кристаллической решетки в отличии от твердого тела.
Молекулы газа расположены на значиельном расстояниии друг от друга. Они движутся с большой скоростью. Скорость около 300 км/ч, сталвикаясь при этом между собой и ударяяс о стенки сосуда, в котором находятся.
Взаимное расположения между молекулами газа свободно изменяется, что позволяет различным телам проходить сквозь его молекулы.
Точка плавления
Физические агрегатные состояния веществ способны переходить с одного вида в другие — из твердых в жидкие, из жидких в газообразные при изменении их температуры. Изменение температуры ведет к увеличению или к уменьшению кинетической энергии. Переход твердого вещества в жидкое называют плавлением.
Границу перехода из твердого состояния в жидкое задает так называемая точка плавления с температурой, способной возбудить кинетическую энергию в частице, которой будет достаточно, чтобы отделиться от своего стационарного положения кристаллической решетки. Чем больше температура, тем больше передаваемая кинетическая энергия частицам элемента. Чем сильнее сила притяжения между частицами, тем больше необходимо создать кинетической энергии для высвобождения частиц из кристаллической решетки.
К примеру, железо необходимо нагреть до 1538 0С для того, чтобы оно начало плавиться, а тугоплавкий вольфрам — до 3422 0С.
Во время литья расплавленное (раскаленное добела) железо выливается в приготовленную форму.

При температуре ниже 1535 0С железо затвердевает, принимая вид литейной формы.
Температура плавления вещества зависит от сил притяжения составляющих его частиц.

Для гелия эти силы настолько малы, что он становится твердым при давлении по крайней мере в 25 раз выше атмосферного.
Точка кипения
Пожалуй, самое распространенное явление перехода жидкого состояния в газообразное в быту — это кипение воды. Заваривая чай каждый из нас мог наблюдать рождение процесса кипения воды. Маленькие пузырьки пара в толще подогревающейся воды постепенно растут и достигая критических размеров начинают подниматься на поверхность, где лопаясь превращаются в газообразное состояние — пар.
Как и в случае с плавлением существует граничная температура, называемая точкой кипения, при которой кинетическая энергия становится достаточной для того, чтобы преодолеть силы взаимного притяжения частиц, не дающие оторваться друг от друга и покинуть занимаемый объем. Любой элемент таблицы Менделеева или вещество из нескольких элементов имеет свою точку кипения. Чистая дистиллированная вода (H2O) имеет температуру кипения 100 0С, этиловый спирт — (-79 0С), а высококонцентрированная серная кислота кипит при температуре 338 0С.
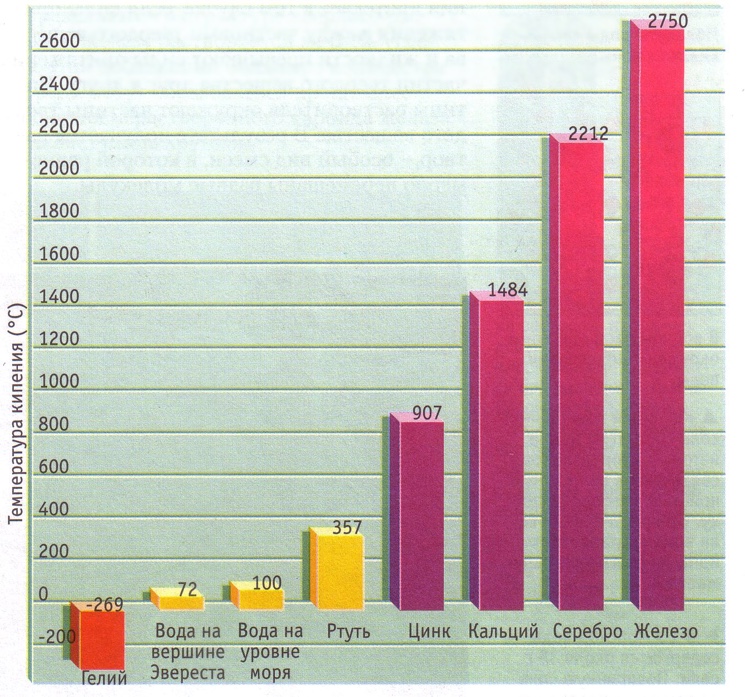
Температура кипения также зависит от давления и сил притяжения между частицами.
На вершине Эвереста температура кипения воды на 28 0С ниже, чем внизу, над уровнем моря.
Однако, существуют исключения, при котором вещества могут миновать при переходе из одного агрегатного состояния в другую целую фазу превращения — переходя из твердого сразу в газообразную. Этот эффект называют сублимацией или возгонкой.
Видео подборки опытов с сухим льдом
В качестве примера можно привести превращение сухого льда (диоксид углерода в твердом виде сразу в газообразное при температуре -78,5 0С.
Влияние давления и различных примесей на кипение или плавление
Вторым фактором, влияющим на агрегатное состояние вещества это давление. Повышая давление сила прижатия одной частицы вещества к другой растет, и таким образом необходимо для перехода из одного состояния в другое приложить большую кинетическую энергию (температуру). Образуется следующая взаимосвязь: температура кипения и плавления растет при повышении давления.
Примеси в частицах вещества также влияют на фактическую температуру плавления или кипения за чтоб того, что они влияют на существующие силы притяжения между частицами. Одним из ярких примеров влияние примесей — рассыпанные кристаллы соли на льду, которые заставляют лед превращаться в жидкость при температуре окружающей среды ниже нуля.
Загрузка…

