В каких клапанах содержится натрий

kalmuik 11.03.2011 — 12:55
Имеются дизельные клапана. Вопрос:
Как определить есть ли внутри заполнитель? (слышал якобы иногда заполняют натрием).
Мнения о качестве и пригодности клапановых сталей с удовольствием почитаю в ДРУГИХ темах.
Буду благодарен за советы по существу вопроса и тычки носом в ссылку
Сургутянин 11.03.2011 — 12:57
от какого именно дизеля?
впускные или выпускные?
без этого только наугад можно ответ дать ????
kalmuik 11.03.2011 — 13:04
Задача стоит в том чтобы определить в «полевых» условиях наличие/отсутствие заполнителя в имеющихся железках. Происхождение ХЗ. Есть кое какие варианты проверки, но сначала хочу послушать умных и/или ???? опытных людей. После некоторых способов проверки слышал бывает даже выживают ????
Тов. Сталин 11.03.2011 — 13:04
У меня был случай взорвался один клапан под молотом, с натрием видимо. Только не знаю от какой техники он был,теперь шляпки отпиливаю и если с натрием, выковыриваю и стамесочки полукруглые делаю.
ВладимирН 11.03.2011 — 13:55
Если
иногда заполняют натрием
тогда только распиливать,и подальше от огня и воды.
Сургутянин 11.03.2011 — 14:01
ВладимирН
тогда только распиливать,и подальше от огня и воды.
+1
Алмазный напильник/надфиль и вперед с песней ????
диверсант 11.03.2011 — 14:11
мы их пацанами ломали, крутили шарик и в воду )))
kalmuik 11.03.2011 — 14:52
Уточняю вопрос КАК определить по целому клапану, есть ли внутри натрий
Сургутянин 11.03.2011 — 15:04
Маркировка есть на них какая-нить?..
Если точно не знать от чего, то скорее всего никак.
Впрочем… Определить объем (с помощью мерной емкости с жидкостью например), точно взвесить, вычислить плотность. Сравнить с табличными данными сталей, применяемых для изготовления клапанов. Если плотность меньше, значит внутри есть полость с легким натрием.
Павел Быков 74 11.03.2011 — 15:41
Для верности обрезайте шляпы ведь бережёного бог бережёт сказала монашка надевая презерватив на свечку
Сургутянин 11.03.2011 — 15:51
Вот нашел примету клапанов с натрием: «Клапан должен иметь ПЛОСКУЮ шляпку, без всяких выемок и впадин, ну на Моём веку в клапанах с впадинами ничего не было»
За достоверность не ручаюсь.
диверсант 11.03.2011 — 15:58
ну да, там как то по шляпке определяли, плоская и с ямкой, попробуйте по одной надрезать или взвесить как тут советовали.
Древесный уголь 11.03.2011 — 21:08
Ярославские, барнаульские, харьковские, минские, точно, без натрия. Был в зиловских, а, чтобы где-то ещё- не видал и не слыхал.
Кирьян 12.03.2011 — 08:33
kalmuik
Уточняю вопрос КАК определить по целому клапану, есть ли внутри натрий
Сходить на флюрографию с клапаном в кармане ????
Serpentik 12.03.2011 — 09:12
Толщиномером ультразвуковым шляпку промерить))))). Натрий закладывался в клапана от ЗиЛ и Урал бензиновые. В дизельных клапанах не встречался. Так что если клапан от дизеля, 90% что без натрия.
KAR-KAR 12.03.2011 — 09:59
Натрий закладывался в клапана от ЗиЛ и Урал бензиновые. В дизельных клапанах не встречался.
+1. И то только в выпускные. У них шляпка меньшего диаметра. И плоская. У впускных бывает т.н. тюльпанообразная. Еще у впускных бывает меньше угол рабочей фаски. Т.е. если есть клапана с двигателя, одни больше, другие — меньше диаметром шляпки, наверняка берем те, что больше и с ямкой.
kalmuik 14.03.2011 — 09:49
Спасибо всем ответившим.
Теперь дурацкий вопрос: а по звуку (при ударе), или по цветам побежалости/каления (при нагреве) можно определить? (Приходилось видеть резкую границу побежалости на клапане.)
Burchitai 14.03.2011 — 10:00
kalmuik
Уточняю вопрос КАК определить по целому клапану, есть ли внутри натрий
мензурка и весы в помощь. Плотность стали — около 7,8 — с полостью и натрием — меньше.
AndYur 14.03.2011 — 10:32
Кмк,натрий же только на «выпускных клапанах»,они чуть отличаются,когда оба под рукой,можно определить…Или я не прав?
amaru 14.03.2011 — 15:01
Делали на выпускных клапанах ЗиЛа(отвод тепла), сейчас такого нет, на дизелях и не было.
aaaps 15.03.2011 — 21:17
Знаю точно, что на ГАЗ-66 И ГАЗ-69 выпускные клапана были с натрием.
Сам отуда выковыривал килограммами в детстве.

Для работы четырехтактного ДВС требуется как минимум по два клапана на цилиндр — впускной и выпускной. В настоящее время применяются клапаны тарельчатого типа со стержнем. Для улучшения наполнения цилиндра горючей смесью диаметр тарелки впускного клапана делается больше, чем у выпускного. Седла клапанов изготовленные из чугуна или стали, запрессовываются в головку блока цилиндров.
При работе двигателя клапаны подвергаются значительным механическим и тепловым нагрузкам, поэтому для их изготовления применяются специальные сплавы. Иногда для улучшения охлаждения клапанов высокофорсированных двигателей применяют клапаны с полым стержнем, который заполняется натрием. Натрий при рабочих температурах плавится и в расплавленном виде перетекает внутри клапана, перенося тепло от более нагретой тарелки клапана к стержню. Для лучшей очистки рабочей фаски от нагара и равномерной теплопередачи иногда применяются различные механизмы для вращения клапана.
ГРМ могут быть нижнеклапанными и верхнеклапанными, но в современных двигателях используются только верхнеклапанные ГРМ, когда клапаны располагаются в головке цилиндров. Клапан удерживается в закрытом состоянии с помощью пружины, а открывается при нажатии на стержень клапана. Клапанные пружины должны иметь определенную жесткость для гарантированного закрытия клапана при работе, но жесткость пружины не должна быть чрезмерной, чтобы не увеличивать ударной нагрузки на седло клапана. Иногда для уменьшения возможности резонансных колебаний используются пружины уменьшенной жесткости, но на один клапан устанавливается по две пружины.

При использовании двух пружин они должны быть навиты в разные стороны, чтобы не произошло заклинивания клапана в случае поломки одной из пружин и попадания ее витка между витками другой пружины. Для снижения потерь на трение в ГРМ сейчас широко применяются ролики, размещаемые на рычагах и толкателях привода клапанов.
Рис. Замена трения скольжения трением качения путем применения в клапанном механизме роликов дает возможность уменьшить потери на привод клапанов

При открытии (опускании) впускного клапана через кольцевой проход между тарелкой клапана и седлом проходит топливно-воздушная смесь (или воздух) и заполняет цилиндр. Чем больше будет площадь проходного сечения, тем полнее заполнится цилиндр, а следовательно, и выходные показатели этого цилиндра при рабочем ходе будут выше. Для лучшей очистки цилиндров от продуктов сгорания желательно также увеличить диаметр тарелки выпускного клапана. Размеры тарелок клапанов ограничены размером камеры сгорания, выполненной в головке цилиндров. Лучшее наполнение цилиндров и их очистка обеспечиваются при использовании большего, чем два, числа клапанов на один цилиндр. Встречаются трехклапанные (два впускных и один выпуск ной) системы и пятиклапанные (три впускных и два выпускных) системы.
Рис. Четырехклапанная камера сгорания. Применение газораспределительного механизма с четырьмя клапанами на цилиндр в дизельном двигателе
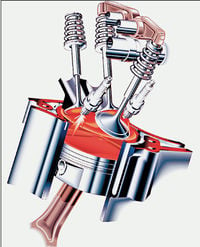
Впервые четыре клапана на цилиндр были использованы еще 1912 г. на двигателе автомобиля Peugeot Gran Prix. Широкое использование такой схемы на серийных легковых автомобилях началось только в 1970-е гг. Сейчас ГРМ с четырьмя клапанами на цилиндр стали практически стандартными для двигателей европейских и японских легковых автомобилей. Некоторые из двигателей Mercedes имеют по три клапана на цилиндр, два впускных и один выпускной, с двумя свечами зажигания (по одной с каждой стороны от выпускного клапана).
Двигатели некоторых автомобилей группы Volksvagen-Audi и ряд японских двигателей используют пять клапанов на цилиндр (три впускных и два выпускных), но при таком числе клапанов значительно усложняется их привод.
Рис. Трехклапанный ГРМ. Компания DaimlerChrysler утверждает, что ГРМ с двумя впускными, одним выпускным и двумя свечами зажигания обеспечивает снижение вредных веществ в отработавших газах
Назад
На сайте https://tvoiklas.ru/ представлены уроки географии, биологии и истории… · tvoiklas.ru
Кальций является составной частью клеточной стенки растений. У животных входит в состав костной ткани, эмали зубов, участвует в свёртывании крови и сокращении мышц .
Натрий в качестве иона (катиона) участвует в создании биоэлектрического потенциала мембран клеток, в синтезе гормонов и регуляции сердечного ритма.
Фосфор нужен для формирования зубной эмали и костной ткани. Входит в состав органических молекул, таких как ДНК, РНК, АТФ.
Фтор необходим для формирования костной ткани и зубной эмали.
Где кислород находится в химически связанном виде (вода, гранит, песок, известняк, металлическая руда, тело растений, животных и человека)?
Вопрос выглядит некорректным. Дело в том что в связанном виде кислород находится во всех практически упомянутых субстанциях. Есть конечно некоторые(очень редкие и мало распространенные) руды, кислород в связанном виде не содержащие, но этими исключениями стоит пренебречь.
Правильно вопрос следовало бы сформировать так — в каких из субстанций содержится несвязанный кислород — а тут вопрос очень прост, по крайней мере из перечисленных свободный кислород содержится только в живых(биологических) субстанциях, т.е. тела растений, животных и человека(кстати тело человека выделять бессмысленно — человек есть животное).
В каких органах (частях тела) рыб содержится фосфор?
Мои интересы: разнообразны, но можно выделить следующие: литература, история…
Основная масса кальция и фосфора в теле рыбы содержится в костях, образуя их твердый остов. Фосфор также входит в состав мышечных клеток, межклеточной жидкости, плазмы крови.
Как квантовые частицы человеческого тела взаимодействуют с квантами окружающей среды?
Занимаюсь разработкой игр.
Веду активный образ жизни, связанный с акробатикой и…
Самое очевидное для нас взаимодействие — это взаимодействие электронов в разных атомах — так и образуются различные соединения. Чтобы это взаимодействие произошло, необходимо иметь свободные электроны, которые образуют интерференцию волн электронов и таким образом сформируют ковалентную или другие связи. На поверхности кожи энергии электронов недостаточно, чтобы они провзаимодействовали с электронами неагрессивной окружающей среды.
Какой химический элемент произошел бы от соединения всех остальных элементов?
Researcher, Institute of Physics, University of Tartu
Химический элемент — это некоторая абстрактная совокупность атомов с одинаковым числом протонов в ядре. То есть, где бы такие атомы не находились, в состав чего бы они ни входили, они будут атомами данного элемента. Грубо говоря, химический элемент — это сорт атомов. Как «антоновка» — это сорт яблок. Яблоко может расти на дереве или лежать в ящике, но все равно будет «антоновкой».
Реальным выражением этой абстрактной совокупности являются так называемые «простые вещества», то есть, вещества состоящие только из атомов одного «сорта». Скажем, железо. Кусок железа состоит только из атомов железа. Как на дереве антоновки растут только яблоки антоновки.
Но если мы возьмем ржавчину, оксид железа, то атомы железа в нем все равно останутся атомами химического элемента «железо», хотя кусок ржавчины не будет куском железа, а будет куском оксида железа, сложного вещества, то есть, вещества, состоящего из атомов разных элементов. Это как в ящик сложить яблоки антоновки и, например, грушевки. Будет ящик с двумя сортами яблок. И нельзя будет назвать какого-то одного сорта для всех этих яблок.
В связи с этим вопрос «какой химический элемент произошел бы от соединения всех остальных элементов?» не имеет смысла. От соединения атомов разных элементов получаются сложные вещества, а не химические элементы. Атомы разных сортов по определению не могут составлять «химического элемента», это было бы логическим противоречием с определением понятия «химический элемент». Это то же самое, что спросить «какой сорт яблок получится, если сложить в один ящик яблоки антоновки, гольден, семеренко и т.д.?» Никакого сорта не получится, будет просто ящик с разными яблоками.
Польза и вред глутамата натрия — крайне спорный вопрос, волнующий всех, кто заботится о своем здоровье. Чтобы ответить на него, необходимо разобраться, что представляет из себя вещество, и каковы его свойства.
Что такое глутамат натрия и для чего он нужен
Глутамат натрия, или Е 621, — белое вещество, не обладающее никаким запахом. В состав глутамата натрия входит лишь натриевая соль, полученная из глутаминовой кислоты. Сама по себе она совершенно безвкусна, однако, в сочетании с другими продуктами проявляет уникальные свойства. А именно усиливает вкус, точнее, оказывает возбуждающее действие на рецепторы человека и заставляет чувствовать сладкие, кислые, горькие или соленые нотки привычных блюд намного острее.
Способы получения глутамата натрия
Химическое вещество, применяемое в пищевой промышленности, получают несколькими способами:
- кислотным гидролизом натурального глютена или клейковины;
- посредством переработки глутамина в пироглутаминовую кислоту, а затем − в глутаминовую кислоту;
- при помощи чисто химической переработки соединений акрилонитрила;
- микробиологическим способом — переработкой углеводов в глутаминовую кислоту посредством особых бактерий Corynebacterium glutamicum, а затем − очисткой и кристаллизацией полученного вещества.
На сегодняшний день в промышленности применяется в основном четвертый способ — микробиологический. Он позволяет получать натуральное вещество без примесей и лишних изомеров — польза от него максимальна.
В каких продуктах содержится глутамат натрия
Пищевая добавка представлена не только синтетическим соединением Е 621, которое сознательно применяется в пищевой промышленности для усиления вкуса. Этот компонент приносит как пользу, так и вред. Глутаминовая кислота присутствует во многих продуктах и сама по себе находится в свободном или связанном виде, когда для высвобождения требуется термическая обработка.
В частности, природную глутаминовую кислоту можно обнаружить:
- практически в любом мясе и ветчине;
- в раках, мидиях, креветках и других морепродуктах;
- в сырах — пармезане и рокфоре;
- в соевом соусе;
- в грибах и горохе;
- в грецких орехах;
- в томатном и виноградном соке;
- в кукурузе и брокколи;
- во многих других продуктах.
Внимание! Именно с глутаминовой кислотой связано изменение вкуса мясных и морских продуктов после жарки, варки или тушения. Свойства вещества высвобождаются из связанного состояния, и пища становится намного сочнее и вкуснее.
Разумеется, применение глутамата натрия в синтетической форме широко распространено в изготовлении полуфабрикатов, закусок и десертов. Добавку Е 621, свойства которой бывают довольно вредные, можно обнаружить в шоколаде и конфетах, сухариках и чипсах, замороженных продуктах, мороженом и напитках.
Чем опасен глутамат натрия
Очень часто свойства вещества упоминаются в негативном контексте — как откровенно вредные для организма. Какой именно вред пищевая добавка может нанести здоровью:
- в больших количествах свойства Е 621 оказывают отравляющее действие, излишне возбуждая и повреждая нервную систему;
- избыток вещества приводит к тому, что у человека формируется вредная привычка — пища без усилителей перестает его привлекать. В свою очередь, употребление еды исключительно с добавкой Е 621 повышает опасность передозировки;
- усилитель вкуса глутамат натрия может привести к ожирению. Дело в том, что пища с вредной добавкой плохо насыщает и способствует повышению аппетита, соответственно, увеличивается и риск набора веса.
Если эта статья оказалась вам полезной, ставьте лайк и подписывайтесь на наш канал. Не забывайте делиться информацией с друзьями в социальных сетях.
Читайте далее: https://poleznii-site.ru/pitanie/vreden-li-glutamat-glyutamat-natriya-dlya-zdorovya.html
Ñîåäèíåíèÿ íàòðèÿ ñòàëè èçâåñòíû ÷åëîâå÷åñòâó ñ ãëóáîêîé äðåâíîñòè.
Ñåé÷àñ, òàêæå, êàê è ðàíüøå íåâîçìîæíî âîîáðàçèòü ñâîþ æèçíü áåç ïðèñóòñòâèÿ â íåé ñîåäèíåíèé íàòðèÿ.
 íàøè äíè àáñîëþòíî âñå ëþäè åæåäíåâíî âñòðå÷àþò âîêðóã ñåáÿ îãðîìíîå êîëè÷åñòâî ñîåäèíåíèé íàòðèÿ, äàæå, ïîðîé, íå çíàÿ îá ýòîì. Ýòî è îáû÷íàÿ ïîâàðåííàÿ ñîëü, ïèùåâàÿ ñîäà, ùåëî÷íûå ÷èñòÿùèå ñðåäñòâà, ìûëî è ñðåäñòâà äëÿ ìûòüÿ ïîñóäû, ëåêàðñòâåííûå ñðåäñòâà (àñïèðèí, òåòðàáîðàò íàòðèÿ è äðóãèå), ñòåêëî, ëàìïû è ìíîæåñòâî äðóãèõ òîâàðîâ ìàññîâîãî ïîòðåáëåíèÿ.
Ñàìûì ðàñïðîñòðàíåííûì èñòî÷íèêîì íàòðèÿ íà ïëàíåòå ñ÷èòàåòñÿ êàìåííàÿ ñîëü (ãàëèò). Ãàëèò ýòî ïðàêòè÷åñêè ÷èñòûé NaCl.
Äåñÿòêè ñàìûõ ðàçíûõ ñîåäèíåíèé íàòðèÿ èñïîëüçóþòñÿ ñåãîäíÿ âî âñåõ ñôåðàõ íàøåé äåÿòåëüíîñòè.
Î íàèáîëåå âàæíûõ ñîåäèíåíèÿõ íàòðèÿ, à òàêæå îá èõ èñïîëüçîâàíèè â ïðîìûøëåííîñòè è ïîéäåò ðå÷ü íèæå.
Õëîðèä íàòðèÿ NaCl íàèáîëåå èçâåñòíîå âñåì ïðèìåíåíèÿ ïîëó÷èë â êà÷åñòâå óñèëèòåëÿ âêóñà. Âåäü õëîðèä íàòðèÿ íè ÷òî èíîå, êàê ïîâàðåííàÿ ñîëü. Êðîìå óëó÷øåíèÿ âêóñîâûõ êà÷åñòâ õëîðèä íàòðèÿ îáëàäàåò àíòèáàêòåðèàëüíûìè ñâîéñòâàìè, ïîýòîìó èñïîëüçóåòñÿ â êà÷åñòâå êîíñåðâàíòà.
Ïîä âîçäåéñòâèåì ýëåêòðè÷åñêîãî òîêà èç NaCl, ðàñòâîðåííîãî â âîäå, ïîëó÷àþò ñðàçó òðè âàæíåéøèõ äëÿ ïðîìûøëåííîñòè ýëåìåíòà. Ýòî ãàçîîáðàçíûé õëîð (Cl2), ãèäðîîêñèä íàòðèÿ (âòîðîå íàçâàíèå — êàóñòè÷åñêàÿ ñîäà) (NaOH) è ãàçîîáðàçíûé âîäîðîä (H2).
 ñâîþ î÷åðåäü õëîð ïðèìåíÿåòñÿ â ïðîèçâîäñòâå, êðàñîê, ðàñòâîðèòåëåé, ïëàñòìàññ, ïåñòèöèäîâ, èñïîëüçóåòñÿ â òåêñòèëüíîé è ôàðìàöåâòè÷åñêîé ïðîìûøëåííîñòè.
Ãèäðîîêñèä íàòðèÿ è ðàñòâîð ãèäðîîêñèäà íàòðèÿ íàøëè áîëüøîå ïðèìåíåíèå â ìåòàëëóðãè÷åñêîé, íåôòåïåðåðàáàòûâàþùåé, êîñìåòè÷åñêîé, òåêñòèëüíîé, à òàêæå ïèùåâîé ïðîìûøëåííîñòÿõ. Êðîìå òîãî ýòè ñîåäèíåíèÿ óñïåøíî ïðèìåíÿþòñÿ äëÿ îáðàáîòêè âîäû.
Êàðáîíàò íàòðèÿ( Na2CO3) âñåì èçâåñòíàÿ ñîäà. Ýòî ñîåäèíåíèå íàòðèÿ íàøëî ïðèìåíåíèå â ïðîèçâîäñòâå ñòåêëà, áóìàãè è öåëëþëîçû, ìûëà, ÷èñòÿùèõ è ìîþùèõ ñðåäñòâ, â ëåãêîé ïðîìûøëåííîñòè. Ïèùåâàÿ ñîäà âõîäèò â ñîñòàâ ïðîäóêòîâ ïèòàíèÿ. Òàêæå èñïîëüçóåòñÿ äëÿ î÷èñòêè ñòî÷íûõ âîä, êðîìå òîãî ÿâëÿåòñÿ îòïðàâíîé òî÷êîé äëÿ ïðîèçâîäñòâà äðóãèõ ñîåäèíåíèé íàòðèÿ.
Áèêàðáîíàò íàòðèÿ (NaHCO3) ïðè ðàñòâîðåíèè â âîäå âûçûâàåò ðåàêöèþ øèïåíèÿ. Íàïðèìåð, ãàçèðîâàííûå íàïèòêè, ðàçðûõëèòåëü äëÿ òåñòà, àñïèðèí â «øèïó÷èõ» òàáëåòêàõ çäåñü èñïîëüçóåòñÿ áèêàðáîíàò íàòðèÿ.
Ãèïîõëîðèò íàòðèÿ ( NaOCl) èñïîëüçóåòñÿ â ôàðìàöåâòè÷åñêîé ïðîìûøëåííîñòè, â êà÷åñòâå îäíîãî èç êîìïîíåíòîâ, âõîäÿùèõ â ñîñòàâ áûòîâîé õèìèè, òàêîé, êàê îòáåëèâàòåëè, îáåçæèðèâàòåëè , ÷èñòÿùèå ñðåäñòâà; ïðèìåíÿòñÿ äëÿ îáåççàðàæèâàíèÿ è äåçèíôåêöèè âîäû.
Íèòðèò íàòðèÿ (NaNO2) àçîòîñîäåðæàùåå óäîáðåíèå, ïèùåâîé êîíñåðâàíò è óëó÷øèòåëü îêðàñêè Å250. Íèòðèò íàòðèÿ øèðîêî èñïîëüçóåòñÿ â ìåäèöèíå è âåòåðèíàðèè êàê ñîñóäîðàñøèðÿþùåå ñðåäñòâî, áðîíõîëèòè÷åñêîå, ñëàáèòåëüíîå, ñðåäñòâî ïðîòèâ ñïàçìîâ è ïðîòèâîÿäèå ïðè îòðàâëåíèè öèàíèäàìè.  ôîòîãðàôèè íèòðèò íàòðèÿ íàøåë ïðèìåíåíèå êàê ðåàãåíò, ïðîòèâîìîðîçíàÿ äîáàâêà äëÿ áåòîíà, ïðèìåíÿåòñÿ ïðè èçãîòîâëåíèè êàó÷óêà è âçðûâ÷àòûõ âåùåñòâ.
Íèòðàò íàòðèÿ (NaNO3) — ýòî ñîåäèíåíèå íàòðèÿ òàêæå ïîëó÷èëî øèðî÷àéøåå ïðèìåíåíèå: êîíñåðâàíò Å251 (ïðîòèâîìèêðîáíàÿ äîáàâêà), óäîáðåíèå. Òàêæå èñïîëüçóåòñÿ ïðè èçãîòîâëåíèè ðàêåòíîãî òîïëèâà, âõîäèò â ñîñòàâ âçðûâ÷àòûõ âåùåñòâ, à òàêæå â ìåòàëëîîáðàáàòûâàþùåé è ñòåêîëüíîé ïðîìûøëåííîñòè.
Àëüãèíàò íàòðèÿ (NaC 6 H 7 O 6 ) ïðîèçâîäñòâî öåìåíòà, êðàñêè íà âîäíîé îñíîâå, çàãóñòèòåëü â ìîðîæåíîì è äðóãèõ ïðîäóêòàõ ïèòàíèÿ.
Áèôòîðèä íàòðèÿ (KHF 2 ) àíòèñåïòèê, íå ïèùåâîé êîíñåðâàíò, òàêæå èñïîëüçóåòñÿ ïðè ïðîèçâîäñòâå æåñòè è òðàâëåíèè ñòåêëà;
Äèóðàíàò íàòðèÿ, èëè « æåëòûé óðàí » (Na 2 U 2 O 7 ) èñïîëüçóåòñÿ äëÿ ïðîèçâîäñòâà îðàíæåâîé ãëàçóðè äëÿ êåðàìèêè;
Ôòîðñèëèêàò íàòðèÿ (Na 2 SiF 6 ) èñïîëüçóåòñÿ ïðè èçãîòîâëåíèè çóáíûõ ïàñò ñî ôòîðîì, õîçÿéñòâåííîãî ìûëà, òàêæå èñïîëüçóåòñÿ ïðè èçãîòîâëåíèè ñðåäñòâ äëÿ áîðüáû ñ êðûñàìè è íàñåêîìûìè. Êðîìå òîãî ôòîðñèëèêàò íàòðèÿ íàøåë ïðèìåíåíèå â êà÷åñòâå êîíñåðâàíòà äëÿ êîæè è äåðåâà.
Ìåòàáîðàò íàòðèÿ (NaBO 2 ) ãåðáèöèä, ïðèìåíÿåòñÿ äëÿ óíè÷òîæåíèÿ ðàñòèòåëüíîñòè.
Ñòåàðàò íàòðèÿ (NaOOCC 17 H 35 ) èñïîëüçóåòñÿ êàê äîáàâêà â êîñìåòè÷åñêèå ñðåäñòâà è çóáíûå ïàñòû. Ïðèìåíÿåòñÿ â êà÷åñòâå ãèäðîèçîëÿöèè è êàê êîìïîíåíò, ïðåäîòâðàùàþùèé ðàçðóøåíèå ïëàñòèêà.
Ãëèêîëÿò íàòðèÿ öèðêîíèÿ (NaZrH 3 (H 2 COCOO) 3 ) ýòî âåùåñòâî âõîäèò â ñîñòàâ äåçîäîðàíòîâ, ïðîòèâîìèêðîáíûõ ïðåïàðàòîâ, òàêæå ïðèìåíÿåòñÿ ïðè èçãîòîâëåíèè îãíåñòîéêèõ ìàòåðèàëîâ.
Ïàðàïåðèîäàò íàòðèÿ (Na 3 H 2 IO 6 ) — ýòî ñîåäèíåíèå ïîìîãàåò áóìàãå ñîõðàíÿòü ïðî÷íîñòü ïðè íàìîêàíèè.
Ãèäðîôòîðèä íàòðèÿ( NaHF2) àíòèñåïòèê, èñïîëüçóåòñÿ ïðè ïðîèçâîäñòâå ïëàâèêîâîé êèñëîòû, òàêæå íàøåë ïðèìåíåíèå äëÿ òðàâëåíèÿ ñòåêëà.
Âîëüôðàìèò íàòðèÿ (NaWO4) èçãîòîâëåíèå ïèãìåíòîâ.
Ãåêñàìåòàëôîñôàò íàòðèÿ (Na6P6O18) òåêñòèëüíàÿ, êîæåâåííàÿ, íåôòÿíàÿ ïðîìûøëåííîñòü, ñìÿã÷åíèå âîäû.
Äèòèîíèò íàòðèÿ (Na2S2O4) ïðîèçâîäñòâî êðàñèòåëåé
Ñàëèöèëàò íàòðèÿ C7H5NaO3 ôàðìàöåâòèêà.
Ìåòàñèëèêàò íàòðèÿ (Na2SiO3) ïðîèçâîäñòâî áåòîíà, öåìåíòíûõ ðàñòâîðîâ, ñòåêëà.
Ãèäðèä íàòðèÿ (NaH) c ïîìîùüþ ðàñòâîðà NaH â ãèäðîîêñèäå íàòðèÿ ñíèìàþò îêàëèíó ñî ñòàëåé è òóãîïëàâêèõ ìåòàëëîâ.
Áèñóëüôèò íàòðèÿ (NaHSO3) ôîòîãðàôèÿ, áóìàæíàÿ, òåêñòèëüíàÿ, êîæåâåííàÿ èíäóñòðèÿ, î÷èñòêà âîäû.
Ôîñôàò íàòðèÿ (Na3PO4) êîñìåòè÷åñêèå ïðåïàðàòû, çóáíàÿ ïàñòà, ïèùåâàÿ äîáàâêà.
Ñåëåíèò íàòðèÿ ( Na2SeO3) ìèíåðàëüíàÿ äîáàâêà, ôàðìàöåâòèêà, âåòåðèíàðèÿ.
Òèîñóëüôàò íàòðèÿ ôàðìàöåâòè÷åñêàÿ ïðîìûøëåííîñòü
Ñòàííèò íàòðèÿ (Na2SnO2) ñ åãî ïîìîùüþ îòêðûâàþò èîíû êîáàëüòà â ñòàëÿõ, äîáûâàþò ìåòàëëè÷åñêîå ñåðåáðî, áëàãîäàðÿ ñòàííèòó íàòðèÿ âîçìîæíî ïîëíîå âîññòàíîâëåíèå îðãàíè÷åñêèõ ñîåäèíåíèé ðòóòè.
Ìåòàñòàííàò íàòðèÿ Na2[Sn(OH)6] ãàëüâàíèêà, ëóæåíèå àëþìèíèÿ.
Òèîöèàíàò íàòðèÿ ( òðàäèöèîííîå íàçâàíèå -ðîäàíèò íàòðèÿ) (NaSCN) èñïîëüçóåòñÿ â êà÷åñòâå ðåàêòèâà äëÿ ôîòîìåòðè÷åñêîãî îïðåäåëåíèÿ æåëåçà, òàêæå èñïîëüçóåòñÿ â ôîòîãðàôèè è òåêñòèëüíîé ïðîìûøëåííîñòè.
Íàòðèé-áóòàäèåíîâûé êàó÷óê ñàìûé âîñòðåáîâàííûé èç âñåõ êàó÷óêîâ
Àìèä íàòðèÿ (NaNH2) — ó÷àñòâóåò â ñèíòåçå äðóãèõ õèìè÷åñêèõ âåùåñòâ, âêëþ÷àÿ âèòàìèí À.
Àöåòàò íàòðèÿ (C2H3O2Na) ëåãêàÿ, ïèùåâàÿ ïðîìûøëåííîñòü, òàêæå èñïîëüçóåòñÿ â áûòó.
Ïèðîñóëüôèò íàòðèÿ (Na2(SO2SO3)) ïèùåâîé êîíñåðâàíò, òàêæå íàøåë ïðèìåíåíèå â õèìè÷åñêîé è ôàðìàöåâòè÷åñêîé îòðàñëÿõ.
Êðåìíåôòîðèñòûé íàòðèé (Na2SiO6) è Ãåêñàôòîðîñèëèêàò íàòðèÿ (Na2[SiF6] ) íåîáõîäèìû ïðè ïîëó÷åíèè áåðèëëà è ìàðãàíöà, èñïîëüçóåòñÿ ïðè èçãîòîâëåíèè öåìåíòîâ, ñòåêîë, ýìàëåé, çàìàçîê.
Ìåòèëàò íàòðèÿ (CH3NaO) íåîáõîäèì äëÿ ñèíòåçà â ïðè èçãîòîâëåíèè ëåêàðñòâåííûõ ïðåïàðàòîâ è õèìèêàòîâ.
Ïåðåêèñü íàòðèÿ (Na2O2) âåëèêîëåïíûé îòáåëèâàòåë.ü
Ôåíîëÿò íàòðèÿ èñïîëüçóåòñÿ äëÿ äåçèíôåêöèè.
Ôòîðèä íàòðèÿ (NaF)- ïðè èçãîòîâëåíèè çóáíîé ïàñòû, êðîìå òîãî êîìïîíåíò ñîñòàâîâ ôëþñà äëÿ ñâàðêè, ïàéêè ìåòàëëîâ, ýìàëåé, ñòåêîë, êåðàìèêè, âõîäèò â ñîñòàâ ñðåäñòâ äëÿ î÷èñòêè ìåòàëëîâ è ò.ä.
Ðàäèîàêòèâíûå èçîòîïû íàòðèÿ èìåþò êàê ìåäèöèíñêîå, òàê è íå ìåäèöèíñêîå ïðèìåíåíèå (íàïðèìåð, ïðîâåðÿò íåôòåïðîâîäû íà ïðåäìåò óòå÷åê)
Áîëüøèíñòâî ëþäåé íèêîãäà íå âèäåëè ìåòàëëè÷åñêèé íàòðèé (Na). Äà è â âèäå ñâîáîäíîãî ýëåìåíòà â ïðèðîäå îí íèêîãäà íå âñòðå÷àåòñÿ. Îí íàñòîëüêî àêòèâåí, ÷òî îáû÷íî õðàíèòñÿ â æèäêîñòè, ñ êîòîðîé íå ðåàãèðóåò, ÷àùå âñåãî èñïîëüçóþò êåðîñèí. Òåì íå ìåíåå, è â âèäå ñâîáîäíîãî ýëåìåíòà íàòðèé íàøåë áîëüøîå ïðèìåíåíèÿ â ðàçëè÷íûõ îáëàñòÿõ ïðîìûøëåííîñòè. Ýòî è òåïëîîáìåííàÿ ñðåäà â àòîìíûõ ýëåêòðîñòàíöèÿõ, è ïðîèçâîäñòâî äðóãèõ ìåòàëëîâ, âêëþ÷àÿ òèòàí, ïðîèçâîäñòâî àêêóìóëÿòîðîâ, ýëåêòðè÷åñêèõ ïðîâîäîâ, íàòðèåâûõ ëàìï, èñêóññòâåííîãî êàó÷óêà è ïðî÷åå.
Ïîäâîäÿ èòîã âñåìó âûøåñêàçàííîìó, íåîáõîäèìî îòìåòèòü, ÷òî ïåðåîöåíèòü ðîëü òàêîãî õèìè÷åñêîãî ýëåìåíòà, êàê íàòðèé, êðàéíå ñëîæíî. Îäíàêî, âàæíåéøèì èç âñåõ ñîåäèíåíèé íàòðèÿ, ïî ïðàâó ìîæåò ñ÷èòàòüñÿ îáûêíîâåííàÿ ïèùåâàÿ ñîëü. Âåäü èìåííî õëîðèä íàòðèÿ èìååò îãðîìíîå âëèÿíèå íà ðÿä îñíîâíûõ ôóíêöèé ó ðàñòåíèé, æèâîòíûõ è ëþäåé. Èìåííî õëîðèä íàòðèÿ ïðèíèìàåò íåïîñðåäñòâåííîå ó÷àñòèå â âîäíî-ñîëåâîì îáìåíå, îäíîì èç âàæíåéøèõ ïðîöåññîâ, ïðîòåêàþùèõ â îðãàíèçìàõ æèâîòíûõ è ëþäåé.
