So2 какое свойство проявляет сера

Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 16 февраля 2020;
проверки требуют 2 правки.
У этого термина существуют и другие значения, см. Оксид серы.
| Оксид серы(IV) | |
|---|---|
| Систематическое наименование | Оксид серы(IV) |
| Хим. формула | SO2 |
| Рац. формула | SO2 |
| Состояние | бесцветный газ |
| Молярная масса | 64,054 г/моль |
| Плотность | 0,002927 г/см³ |
| Энергия ионизации | 12,3 ± 0,1 эВ[2] |
| Температура | |
| • плавления | −75,5 °C |
| • кипения | −10,01 °C |
| Энтальпия | |
| • образования | −296,90 кДж/моль |
| Давление пара | 3,2 ± 0,1 атм[2] |
| Растворимость | |
| • в воде | 11,5 г/100 мл |
| Рег. номер CAS | [7446-09-5] |
| PubChem | 1119 |
| Рег. номер EINECS | 231-195-2 |
| SMILES | O=S=O |
| InChI | 1S/O2S/c1-3-2 RAHZWNYVWXNFOC-UHFFFAOYSA-N |
| Кодекс Алиментариус | E220 |
| RTECS | WS4550000 |
| ChEBI | 18422 |
| ChemSpider | 1087 |
| Предельная концентрация | 10 мг/м³[1] |
| Токсичность | Класс опасности III |
| Пиктограммы ECB | |
| NFPA 704 | 2 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
| Медиафайлы на Викискладе | |
Окси́д се́ры(IV) (диокси́д се́ры, двуокись серы, серни́стый газ, серни́стый ангидри́д) — соединение серы с кислородом состава SO2. В нормальных условиях представляет собой бесцветный газ с характерным резким запахом (запах загорающейся спички). В высоких концентрациях токсичен. Под давлением сжижается при комнатной температуре. Растворяется в воде с образованием нестойкой серни́стой кислоты; растворимость 11,5 г/100 г воды при 20 °C, снижается с ростом температуры. Растворяется также в этаноле и се́рной кислоте. Один из основных компонентов вулканических газов.
Получение[править | править код]
Промышленный способ получения — сжигание серы или обжиг сульфидов, в основном — пирита:
В лабораторных условиях и в природе SO2 получают воздействием сильных кислот на сульфиты и гидросульфиты. Образующаяся сернистая кислота H2SO3 сразу разлагается на SO2 и H2O:
Химические свойства[править | править код]
Спектр поглощения SO2 в ультрафиолетовом диапазоне.
Относится к кислотным оксидам. Растворяется в воде с образованием сернистой кислоты (при обычных условиях реакция обратима):
С щелочами образует сульфиты:
Химическая активность SO2 весьма велика. Наиболее ярко выражены восстановительные свойства SO2, степень окисления серы в таких реакциях повышается:
Предпоследняя реакция является качественной реакцией на сульфит-ион SO32− и на SO2 (обесцвечивание фиолетового раствора).
В присутствии сильных восстановителей SO2 способен проявлять окислительные свойства. Например, для извлечения серы из отходящих газов металлургической промышленности используют восстановление SO2оксидом углерода(II):
Или для получения фосфорноватистой кислоты:
Применение[править | править код]
Большая часть оксида серы(IV) используется для производства сернистой кислоты. Используется также в виноделии в качестве консерванта (пищевая добавка E220). Так как этот газ убивает микроорганизмы, им окуривают овощехранилища и склады. Оксид серы(IV) используется для отбеливания соломы, шёлка и шерсти, то есть материалов, которые нельзя отбеливать хлором. Применяется он также и в качестве растворителя в лабораториях[3]. Оксид серы(IV) применяется также для получения различных солей сернистой кислоты.
Токсическое действие[править | править код]
Оксид серы (IV) SO2 (диоксид серы) в высоких дозах очень токсичен. Симптомы при отравлении сернистым газом — насморк, кашель, охриплость, сильное першение в горле и своеобразный привкус. При вдыхании сернистого газа более высокой концентрации — удушье, расстройство речи, затруднение глотания, рвота, возможен острый отёк лёгких.
При кратковременном вдыхании оказывает сильное раздражающее действие, вызывает кашель и першение в горле.
Длительное воздействие диоксида серы в малых концентрациях также может нести вред организму. Системное исследование, проведённое в 2011 году показывает связь между воздействием диоксида серы на организм и преждевременными родами у женщин.
- ПДК (предельно допустимая концентрация):
- в атмосферном воздухе максимально-разовая — 0,5 мг/м³, среднесуточная — 0,05 мг/м³;
- в помещении (рабочая зона) — 10 мг/м³.
По степени воздействия на человеческий организм сернистый ангидрид относится к III классу опасности («умеренно-опасное химическое вещество»)[4] согласно ГОСТ 12.1.007-76.
Интересно, что чувствительность по отношению к SO2 весьма различна у отдельных людей, животных и растений. Так, среди растений наиболее устойчивы по отношению к сернистому газу берёза и дуб, наименее — роза, сосна и ель.
По данным исследования[5] средний порог восприятия запаха может превышать ПДК (21 мг/м3), а у части людей порог был значительно выше среднего значения.
Биологическая роль[править | править код]
Роль эндогенного сернистого газа в физиологии организма млекопитающих ещё окончательно не выяснена.[6] Сернистый газ блокирует нервные импульсы от рецепторов растяжения лёгких и устраняет рефлекс, возникающий в ответ на перерастяжение лёгких, стимулируя тем самым более глубокое дыхание.
Показано, что эндогенный сернистый газ играет роль в предотвращении повреждения лёгких, уменьшает образование свободных радикалов, оксидативный стресс и воспаление в лёгочной ткани, в то время как экспериментальное повреждение лёгких, вызываемое олеиновой кислотой, сопровождается, наоборот, снижением образования сернистого газа и активности опосредуемых им внутриклеточных путей и повышением образования свободных радикалов и уровня оксидативного стресса. Что ещё более важно, блокада фермента, способствующего образованию эндогенного сернистого газа, в эксперименте способствовала усилению повреждения лёгких, оксидативного стресса и воспаления и активации апоптоза клеток лёгочной ткани. И напротив, обогащение организма подопытных животных серосодержащими соединениями, такими, как глютатион и ацетилцистеин, служащими источниками эндогенного сернистого газа, приводило не только к повышению содержания эндогенного сернистого газа, но и к уменьшению образования свободных радикалов, оксидативного стресса, воспаления и апоптоза клеток лёгочной ткани.[7]
Считают, что эндогенный сернистый газ играет важную физиологическую роль в регуляции функций сердечно-сосудистой системы, а нарушения в его метаболизме могут играть важную роль в развитии таких патологических состояний, как лёгочная гипертензия, гипертоническая болезнь, атеросклероз сосудов, ишемическая болезнь сердца, ишемия-реперфузия и др.[8]
Показано, что у детей с врождёнными пороками сердца и лёгочной гипертензией повышен уровень гомоцистеина (вредного токсичного метаболита цистеина) и снижен уровень эндогенного сернистого газа, причём степень повышения уровня гомоцистеина и степень снижения выработки эндогенного сернистого газа коррелировала со степенью выраженности лёгочной гипертензии. Предложено использовать гомоцистеин как маркер степени тяжести состояния этих больных и указано, что метаболизм эндогенного сернистого газа может быть важной терапевтической мишенью у этих больных.[9]
Также показано, что эндогенный сернистый газ понижает пролиферативную активность клеток гладких мышц эндотелия сосудов, угнетая активность MAPK-сигнального пути и одновременно активируя аденилатциклазный путь и протеинкиназу A.[10] А пролиферация гладкомышечных клеток стенок сосудов считается одним из механизмов гипертензивного ремоделирования сосудов и важным звеном патогенеза артериальной гипертензии, а также играет роль в развитии стеноза (сужения просвета) сосудов, предрасполагающего к развитию в них атеросклеротических бляшек.
Эндогенный сернистый газ оказывает эндотелий-зависимое вазодилатирующее действие в низких концентрациях, а в более высоких концентрациях становится эндотелий-независимым вазодилататором, а также оказывает отрицательное инотропное действие на миокард (понижает сократительную функцию и сердечный выброс, способствуя снижению артериального давления). Этот вазодилатирующий эффект сернистого газа опосредуется через АТФ-чувствительные кальциевые каналы и кальциевые каналы L-типа («дигидропиридиновые»). В патофизиологических условиях эндогенный сернистый газ оказывает противовоспалительное действие и повышает антиоксидантный резерв крови и тканей, например при экспериментальной лёгочной гипертензии у крыс. Эндогенный сернистый газ также снижает повышенное артериальное давление и тормозит гипертензивное ремоделирование сосудов у крыс в экспериментальных моделях гипертонической болезни и лёгочной гипертензии. Последние (на 2015 год) исследования показывают также, что эндогенный сернистый газ вовлечён в регуляцию липидного метаболизма и в процессы ишемии-реперфузии.[11]
Эндогенный сернистый газ также уменьшает повреждение миокарда, вызванное экспериментальной гиперстимуляцией адренорецепторов изопротеренолом, и повышает антиоксидантный резерв миокарда.[12]
Воздействие на атмосферу[править | править код]
Из-за образования в больших количествах в качестве отходов диоксид серы является одним из основных газов, загрязняющих атмосферу.
Наибольшую опасность представляет собой загрязнение соединениями серы, которые выбрасываются в атмосферу при сжигании угольного топлива, нефти и природного газа, а также при выплавке металлов и производстве серной кислоты.
Антропогенное загрязнение серой в два раза превосходит природное[13][14]. Серный ангидрид образуется при постепенном окислении сернистого ангидрида кислородом воздуха с участием света. Конечным продуктом реакции является аэрозоль серной кислоты в воздухе, раствор в дождевой воде (в облаках). Выпадая с осадками, она подкисляет почву, обостряет заболевания дыхательных путей, скрыто угнетающе воздействует на здоровье человека. Выпадение аэрозоля серной кислоты из дымовых факелов химических предприятий чаще отмечается при низкой облачности и высокой влажности воздуха. Растения около таких предприятий обычно бывают густо усеяны мелкими некротическими пятнами, образовавшимися в местах оседания капель серной кислоты, что доказывает присутствие её в окружающей среде в существенных количествах. Пирометаллургические предприятия цветной и чёрной металлургии, а также ТЭЦ ежегодно выбрасывают в атмосферу десятки миллионов тонн серного ангидрида.
Необходимо отметить также, что диоксид серы имеет максимум в спектре поглощения света в ультрафиолетовой области (190—220 нм), что совпадает с максимумом в спектре поглощения озона. Это свойство диоксида серы позволяет утверждать, что наличие этого газа в атмосфере имеет также положительный эффект, предотвращая возникновение и развитие онкологических заболеваний кожи человека. Диоксид серы в атмосфере Земли существенно ослабляет влияние парниковых газов (диоксид углерода, метан) на рост температуры атмосферы[15].
Наибольших концентраций сернистый газ достигает в северном полушарии, особенно над территорией США, Европы, Китая, европейской части России и Украины. В южном полушарии содержание его значительно ниже[16].
Примечания[править | править код]
- ↑ Ошибка в сносках?: Неверный тег <ref>; для сносок onx.distant.ru не указан текст
- ↑ 1 2 https://www.cdc.gov/niosh/npg/npgd0575.html
- ↑ Гордон А., Форд Р. Спутник химика / Пер. на русск. Е. Л. Розенберга, С. И. Коппель. — М.: Мир, 1976. — 544 с.
- ↑ Ошибка в сносках?: Неверный тег <ref>; для сносок xumuk.ru не указан текст
- ↑ Mary O. Amdur, Walter W. Melvin, Philip Drinker. Effects of Inhalation of Sulphur Dioxide by Man (англ.) // The Lancet. — Elsevier B.V, 1953. — 1 October (vol. 262 (iss. 6789). — P. 758—759. — ISSN 0140-6736. — doi:10.1016/S0140-6736(53)91455-X.
- ↑ Liu, D.; Jin, H; Tang, C; Du, J. Sulfur dioxide: a novel gaseous signal in the regulation of cardiovascular functions (англ.) // Mini-Reviews in Medicinal Chemistry (англ.)русск. : journal. — 2010. — Vol. 10, no. 11. — P. 1039—1045. — PMID 20540708. Архивировано 26 апреля 2013 года.
- ↑ Chen S, Zheng S, Liu Z, Tang C, Zhao B, Du J, Jin H. Endogenous sulfur dioxide protects against oleic acid-induced acute lung injury in association with inhibition of oxidative stress in rats. // Lab Invest.. — Feb 2015. — Т. 95, вып. 95(2), № 2. — С. 142—156. — doi:10.1038/labinvest.2014.147. — PMID 25581610.
- ↑ Tian H. Advances in the study on endogenous sulfur dioxide in the cardiovascular system. // Chin Med J. — Nov 2014. — Т. 127, вып. 127(21), № 21. — С. 3803—3807. — PMID 25382339.
- ↑ Yang R, Yang Y, Dong X, Wu X, Wei Y. Correlation between endogenous sulfur dioxide and homocysteine in children with pulmonary arterial hypertension associated with congenital heart disease (кит.) // Zhonghua Er Ke Za Zhi. — Aug 2014. — 第52卷, 第52(8)期, 第8数. — 第625—629 页. — PMID 25224243.
- ↑ Liu D, Huang Y, Bu D, Liu AD, Holmberg L, Jia Y, Tang C, Du J, Jin H. Sulfur dioxide inhibits vascular smooth muscle cell proliferation via suppressing the Erk/MAP kinase pathway mediated by cAMP/PKA signaling. // Cell Death Dis.. — May 2014. — Т. 5, вып. 5(5), № 5. — С. e1251. — doi:10.1038/cddis.2014.229.. — PMID 24853429.
- ↑ Wang XB, Jin HF, Tang CS, Du JB. The biological effect of endogenous sulfur dioxide in the cardiovascular system. // Eur J Pharmacol.. — 16 Nov 2011. — Т. 670, вып. 670(1), № 1. — doi:10.1016/j.ejphar.2011.08.031. — PMID 21925165.
- ↑ Liang Y, Liu D, Ochs T, Tang C, Chen S, Zhang S, Geng B, Jin H, Du J. Endogenous sulfur dioxide protects against isoproterenol-induced myocardial injury and increases myocardial antioxidant capacity in rats. // Lab Invest.. — Jan 2011. — Т. 91, вып. 91(1), № 1. — С. 12—23. — doi:10.1038/labinvest.2010.156. — PMID 20733562.
- ↑ Серный ангидрид, его воздействие на окружающую среду. Дата обращения 21 ноября 2013.
- ↑ Основы расчета нормативов пдв. Дата обращения 21 ноября 2013.
- ↑ Проблемы загрязнения атмосферы. Парниковый эффект.. Дата обращения 21 ноября 2013.
- ↑ Экологические кризисы. Дата обращения 21 ноября 2013.
Литература[править | править код]
- Ахметов Н. С. Общая и неорганическая химия. — М.: Высшая школа, 2001.
- Карапетьянц М. Х., Дракин С. И. Общая и неорганическая химия. — М.: Химия, 1994.
Ссылки[править | править код]
- Global map of sulfur dioxide distribution (англ.)
- United States Environmental Protection Agency Sulfur Dioxide page (англ.)
- International Chemical Safety Card 0074 (англ.)
- IARC Monographs. «Sulfur Dioxide and some Sulfites, Bisulfites and Metabisulfites» v54. 1992. p131. (англ.)
- Sulfur Dioxide, Molecule of the Month (англ.)
Сера — элемент VIa группы 3 периода периодической таблицы Д.И. Менделеева. Относится к
группе халькогенов — элементов VIa группы.
Сера — S — простое вещество имеет светло-желтый цвет. Использовалась еще до нашей эры в составе священных курений при
религиозных обрядах.

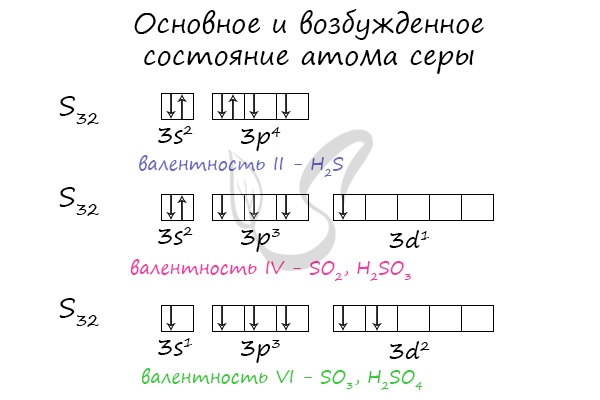
Основное и возбужденное состояние атома серы
Электроны s- и p-подуровня способны распариваться и переходить на d-подуровень. Как и всегда, количество валентных
электронов отражает количество возможных связей у атома.
В разных электронных конфигурациях сера способна принимать валентности: II, IV и VI.
Природные соединения
- FeS2 — пирит, колчедан
- ZnS — цинковая обманка
- PbS — свинцовый блеск (галенит), Sb2S3 — сурьмяный блеск, Bi2S3 — висмутовый блеск
- HgS — киноварь
- CuFeS2 — халькопирит
- Cu2S — халькозин
- CuS — ковеллин
- BaSO4 — барит, тяжелый шпат
- CaSO4 — гипс
В местах вулканической активности встречаются залежи самородной серы.

Получение
В промышленности серу получают из природного газа, который содержит газообразные соединения серы: H2S,
SO2.
H2S + O2 = S + H2O (недостаток кислорода)
SO2 + C = (t) S + CO2
Серу можно получить разложением пирита
FeS2 = (t) FeS + S
В лабораторных условиях серу можно получить слив растворы двух кислот: серной и сероводородной.
H2S + H2SO4 = S + H2O
Химические свойства
- Реакции с неметаллами
- Реакции с металлами
- Реакции с кислотами
- Реакции с щелочами
На воздухе сера окисляется, образуя сернистый газ — SO2. Реагирует со многими неметаллами, без нагревания —
только со фтором.
S + O2 = (t) SO2
S + F2 = SF6
S + Cl2 = (t) SCl2
S + C = (t) CS2

При нагревании сера бурно взаимодействует со многими металлами с образованием сульфидов.
K + S = (t) K2S
Al + S = Al2S3
Fe + S = (t) FeS
При взаимодействии с концентрированными кислотами (при длительном нагревании) сера окисляется до сернистого газа или серной кислоты.
S + H2SO4 = (t) SO2 + H2O
S + HNO3 = (t) H2SO4 + NO2 + H2O
Сера вступает в реакции диспропорционирования с щелочами.
S + KOH = (t) K2S + K2SO3 + H2O
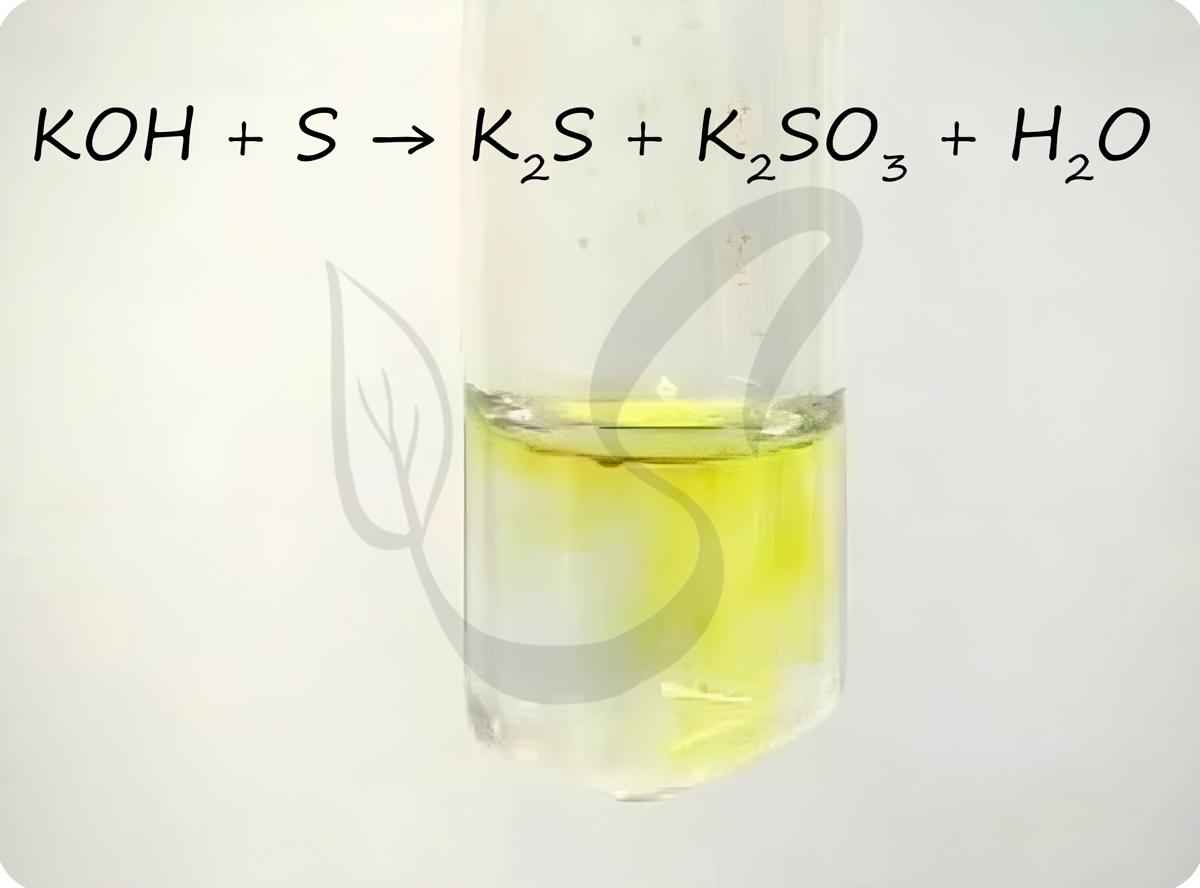
Сероводород — H2S
Бесцветный газ с характерным запахом тухлых яиц. Огнеопасен. Используется в химической промышленности и в лечебных целях (сероводородные
ванны).

Получение
Сероводород получают в результате реакции сульфида алюминия с водой, а также взаимодействия разбавленных кислот с сульфидами.
Al2S3 + H2O = (t) Al(OH)3↓ + H2S↑
FeS + HCl = FeCl2 + H2S↑

Химические свойства
- Кислотные свойства
- Восстановительные свойства
- Качественная реакция
Сероводород плохо диссоциирует в воде, является слабой кислотой. Реагирует с основными оксидами, основаниями с образованием средних и кислых солей (зависит
от соотношения основания и кислоты).
MgO + H2S = (t) MgS + H2O
KOH + H2S = KHS + H2O (гидросульфид калия, избыток кислоты)
2KOH + H2S = K2S + 2H2O
Металлы, стоящие в ряду напряжений до водорода, способны вытеснить водород из кислоты.
Ca + H2S = (t) CaS + H2
Сероводород — сильный восстановитель (сера в минимальной степени окисления S2-). Горит в кислороде синим пламенем, реагирует с кислотами.
H2S + O2 = H2O + S (недостаток кислорода)
H2S + O2 = H2O + SO2 (избыток кислорода)
H2S + HClO3 = H2SO4 + HCl

Качественной реакцией на сероводород является реакция с солями свинца, при котором образуется сульфид свинца.
H2S + Pb(NO3)2 = PbS↓ + HNO3
Оксид серы — SO2
Сернистый газ — SO2 — при нормальных условиях бесцветный газ с характерным резким запахом (запах загорающейся
спички).

Получение
В промышленных условиях сернистый газ получают обжигом пирита.
FeS2 + O2 = (t) FeO + SO2
В лаборатории SO2 получают реакцией сильных кислот на сульфиты. В ходе подобных реакций образуется сернистая кислота,
распадающаяся на сернистый газ и воду.
K2SO3 + H2SO4 = (t) K2SO4 + H2O + SO2↑
Сернистый газ получается также в ходе реакций малоактивных металлов с серной кислотой.
Cu + H2SO4(конц.) = (t) CuSO4 + SO2 + H2O
- Кислотные свойства
- Восстановительные свойства
- Как окислитель
С основными оксидами, основаниями образует соли сернистой кислоты — сульфиты.
K2O + SO2 = K2SO3
NaOH + SO2 = NaHSO3
2NaOH + SO2 = Na2SO3 + H2O

Химически сернистый газ очень активен. Его восстановительные свойства продемонстрированы в реакциях ниже.
Fe2(SO4)3 + SO2 + H2O = FeSO4 + H2SO4
SO2 + O2 = (t, кат. — Pt) SO3
В присутствии сильных восстановителей SO2 способен проявлять окислительные свойства (понижать степень окисления).
CO + SO2 = CO2 + S
H2S + SO2 = S + H2O
Сернистая кислота
Слабая, нестойкая двухосновная кислота. Существует лишь в разбавленных растворах.
Получение
SO2 + H2O ⇄ H2SO3
Химические свойства
- Диссоциация
- Кислотные свойства
- Окислительные свойства
- Восстановительные свойства
Диссоциирует в водном растворе ступенчато.
H2SO3 = H+ + HSO3-
HSO3- = H+ + SO32-
В реакциях с основными оксидами, основаниями образует соли — сульфиты и гидросульфиты.
CaO + H2SO3 = CaSO3 + H2O
H2SO3 + 2KOH = 2H2O + K2SO3 (соотношение кислота — основание, 1:2)
H2SO3 + KOH = H2O + KHSO3 (соотношение кислота — основание, 1:1)
С сильными восстановителями сернистая кислота принимает роль окислителя.
H2SO3 + H2S = S↓ + H 2O
Как и сернистый газ, сернистая кислота и ее соли обладают выраженными восстановительными свойствами.
H2SO3 + Br2 = H2SO4 + HBr

Оксид серы VI — SO3
Является высшим оксидом серы. Бесцветная летучая жидкость с удушающим запахом. Ядовит.
Получение
В промышленности данный оксид получают, окисляя SO2 кислородом при нагревании и присутствии катализатора
(оксид ванадия — Pr, V2O5).
SO2 + O2 = (кат) SO3
В лабораторных условиях разложением солей серной кислоты — сульфатов.
Fe2(SO4)3 = (t) SO3 + Fe2O3
Химические свойства
- Кислотные свойства
- Окислительные свойства
Является кислотным оксидом, соответствует серной кислоте. При реакции с основными оксидами и основаниями образует ее соли — сульфаты и
гидросульфаты. Реагирует с водой с образованием серной кислоты.
SO3 + 2KOH = K2SO4 + 2H2O (основание в избытке — средняя соль)
SO3 + KOH = KHSO4 + H2O (кислотный оксид в избытке — кислая соль)
SO3 + Ca(OH)2 = CaSO4 + H2O

SO3 + Li2O = Li2SO4
SO3 + H2O = H2SO4
SO3 — сильный окислитель. Чаще всего восстанавливается до SO2.
SO3 + P = SO2 + P2O5
SO3 + H2S = SO2 + H2O
SO3 + KI = SO2 + I2 + K2SO4

© Беллевич Юрий Сергеевич 2018-2020
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение
(в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов
без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования,
обратитесь, пожалуйста, к Беллевичу Юрию.
