Определите какие продукты образуются на катоде

Электролиз (греч. elektron — янтарь + lysis — разложение) — химическая реакция, происходящая при прохождении постоянного тока через
электролит. Это разложение веществ на их составные части под действием электрического тока.
Процесс электролиза заключается в перемещении катионов (положительно заряженных ионов) к катоду (заряжен отрицательно), и отрицательно
заряженных ионов (анионов) к аноду (заряжен положительно).
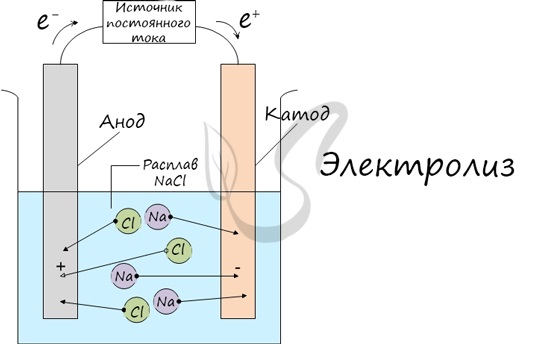
Итак, анионы и катионы устремляются соответственно к аноду и катоду. Здесь и происходит химическая реакция. Чтобы успешно решать задания
по этой теме и писать реакции, необходимо разделять процессы на катоде и аноде. Именно так и будет построена эта статья.
Катод
К катоду притягиваются катионы — положительно заряженные ионы: Na+, K+, Cu2+, Fe3+,
Ag+ и т.д.
Чтобы установить, какая реакция идет на катоде, прежде всего, нужно определиться с активностью металла: его положением в электрохимическом
ряду напряжений металлов.
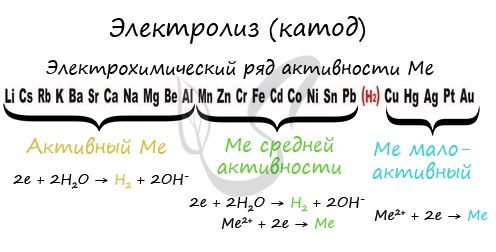
Если на катоде появился активный металл (Li, Na, K) то вместо него восстанавливаются молекулы воды, из которых выделяется водород. Если металл средней
активности (Cr, Fe, Cd) — на катоде выделяется и водород, и сам металл. Малоактивные металлы выделяются на катоде в чистом виде (Cu, Ag).
Замечу, что границей между металлами активными и средней активности в ряду напряжений считается алюминий. При электролизе на катоде металлы
до алюминия (включительно!) не восстанавливаются, вместо них восстанавливаются молекулы воды — выделяется водород.
В случае, если на катод поступают ионы водорода — H+ (например при электролизе кислот HCl, H2SO4) восстанавливается
водород из молекул кислоты: 2H+ — 2e = H2
Анод
К аноду притягиваются анионы — отрицательно заряженные ионы: SO42-, PO43-, Cl-, Br-,
I-, F-, S2-, CH3COO-.

При электролизе кислородсодержащих анионов: SO42-, PO43- — на аноде окисляются не анионы, а молекулы
воды, из которых выделяется кислород.
Бескислородные анионы окисляются и выделяют соответствующие галогены. Сульфид-ион при оксилении окислении серу. Исключением является фтор — если он
попадает анод, то разряжается молекула воды и выделяется кислород. Фтор — самый электроотрицательный элемент, поэтому и является исключением.
Анионы органических кислот окисляются особым образом: радикал, примыкающий к карбоксильной группе, удваивается, а сама карбоксильная группа (COO)
превращается в углекислый газ — CO2.
Примеры решения
В процессе тренировки вам могут попадаться металлы, которые пропущены в ряду активности. На этапе обучения вы можете пользоваться расширенным рядом
активности металлов.
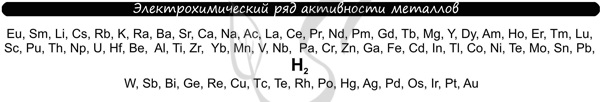
Теперь вы точно будете знать, что выделяется на катоде 😉
Итак, потренируемся. Выясним, что образуется на катоде и аноде при электролизе растворов AgCl, Cu(NO3)2, AlBr3,
NaF, FeI2, CH3COOLi.

Иногда в заданиях требуется записать реакцию электролиза. Сообщаю: если вы понимаете, что образуется на катоде, а что на аноде,
то написать реакцию не составляет никакого труда. Возьмем, например, электролиз NaCl и запишем реакцию:
NaCl + H2O → H2 + Cl2 + NaOH
Натрий — активный металл, поэтому на катоде выделяется водород. Анион не содержит кислорода, выделяется галоген — хлор. Мы пишем уравнение, так
что не можем заставить натрий испариться бесследно 🙂 Натрий вступает в реакцию с водой, образуется NaOH.
Запишем реакцию электролиза для CuSO4:
CuSO4 + H2O → Cu + O2 + H2SO4
Медь относится к малоактивным металлам, поэтому сама в чистом виде выделяется на катоде. Анион кислородсодержащий, поэтому в реакции выделяется
кислород. Сульфат-ион никуда не исчезает, он соединяется с водородом воды и превращается в серую кислоту.
Электролиз расплавов
Все, что мы обсуждали до этого момента, касалось электролиза растворов, где растворителем является вода.
Перед промышленной химией стоит важная задача — получить металлы (вещества) в чистом виде. Малоактивные металлы (Ag, Cu) можно легко получать
методом электролиза растворов.
Но как быть с активными металлами: Na, K, Li? Ведь при электролизе их растворов они не выделяются на катоде в чистом виде, вместо них восстанавливаются
молекулы воды и выделяется водород. Тут нам как раз пригодятся расплавы, которые не содержат воды.
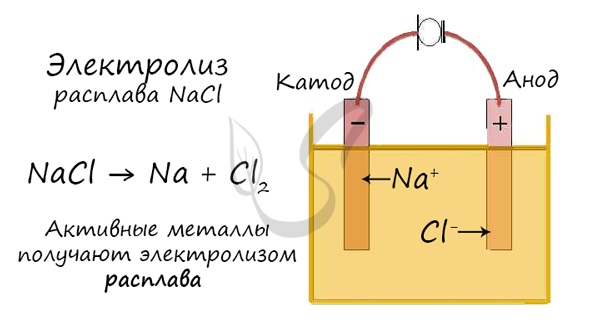
В безводных расплавах реакции записываются еще проще: вещества распадаются на составные части:
AlCl3 → Al + Cl2
LiBr → Li + Br2
© Беллевич Юрий Сергеевич 2018-2020
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение
(в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов
без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования,
обратитесь, пожалуйста, к Беллевичу Юрию.
Полный курс химии вы можете найти на моем сайте CHEMEGE.RU. Чтобы получать актуальные материалы и новости ЕГЭ по химии, вступайте в мою группу в ВКонтакте или на Facebook. Если вы хотите подготовиться к ЕГЭ по химии на высокие баллы, приглашаю на онлайн-курс «40 шагов к 100 баллам на ЕГЭ по химии«.
При электролизе расплавов или водных растворов солей протекают окислительно-восстановительные реакции на электродах (аноде и катоде). В статье рассмотрены расчетные задачи, в которых основной химической реакцией является электролиз — основные приемы и типы решения таких задач.
Какие именно процессы протекают при электролизе и как составлять уравнения химических реакций, протекающих при электролизе, вы можете узнать из статьи.
При решении задач на электролиз необходимо учитывать, что растворенное вещество может подвергнуться электролизу не полностью. Если вещество полностью разложилось под действием тока, далее может протекать электролиз воды по уравнению:
2H₂O → O₂ + 2H₂
При действии тока на растворы некоторых веществ (например, соли активных металлов и кислородсодержащих кислот, щелочи, кислородсодержащие кислоты) количество этих веществ фактически не меняется, т.к. протекающие на катоде и аноде процессы приводят к электролизу воды.
Электролиза с растворимыми электродами или электролиза растворов, в которых содержится несколько растворенных веществ, в ЕГЭ по химии пока нет.
Давайте рассмотрим несколько простых задач на электролиз, а затем перейдем к более сложным.
1. Провели электролиз водного раствора нитрата серебра с инертным анодом. Масса восстановленного на катоде серебра оказалась равной 2,16 г. Какой объём газа (н.у.) выделился на аноде? Вычислите массовую долю кислоты в полученном растворе, если масса раствора 250 г.
Решение и ответ:
Запишем уравнение электролиза раствора нитрата серебра:
4AgNO₃ + 2H₂O → 4Ag + 4HNO₃ + O₂
Количество вещества серебра, образовавшегося на катоде:
n(Ag) = m/M = 2,16 г/107 г/моль = 0,02 моль
На аноде выделился кислород. Количество кислорода можем определить из количества серебра по уравнению реакции:
n(O₂) = 1/4·n(Ag) = 1/4 · 0,02 = 0,005 моль
Объем кислорода:
V(O₂) = n·Vm = 0,005·22,4 = 0,112 л
Количество вещества азотной кислоты:
n(HNO₃) = n(Ag) = 0,02 моль
m(HNO₃) = n·M = 0,02 моль·63 г/моль = 1,26 г
Массовая доля азотной кислоты в полученном растворе:
ω(HNO₃) = m(HNO₃)/*mр-ра = 1,26/250 = 0,005 = 0,5%
Ответ: V(O₂) = 0,112 л, ω(HNO₃) = 0,5%
2. Провели полный электролиз 200 г раствора хлорида калия с ω(KCl) = 7,45%. К полученному раствору добавили 50 г раствора фосфорной кислоты с ω(H₃PO₄) = 19,6%. Определите формулу образовавшейся при этом соли.
Решение и ответ:
Запишем уравнение электролиза раствора хлорида калия:
2KCl + 2H₂O → 2KOH + Cl₂ + H₂
При полном электролизе вступит в реакцию весь хлорид калия. Определим массу и количество вещества хлорида калия:
m(KCl) = mр-ра(KCl) ·ω(KCl) = 200 г · 0,075 = 14,9 г
n(KCl) = m/M =14,9 г / 74,5 г/моль = 0,2 моль
Определим количество образовавшейся щелочи:
n(KOH) = n(KCl) = 0,2 моль
Определим количество фосфорной кислоты:
m(H₃PO₄) = mр-ра(H₃PO₄) ·ω(H₃PO₄) = 50 г · 0,196 = 9,8 г
n(H₃PO₄) = m/M =9,8 г / 98 г/моль = 0,1 моль
При взаимодействии фосфорной кислоты с щелочью возможно образование трех типов солей:
H₃PO₄ + KOH → KH₂PO₄ + H₂O
H₃PO₄ + 2KOH → K₂HPO₄ + 2H₂O
H₃PO₄ + 3KOH → K₃PO₄ + 3H₂O
При соотношении кислоты и щелочи n(H₃PO₄):n(KOH) = 0,1:0,2 или 1:2 протекает вторая реакция и образуется гидрофосфат калия. Количество вещества гидрофосфата калия равно:
n(K₂HPO₄) = n(H₃PO₄) = 0,1 моль
Ответ: K₂HPO₄
3. В процессе электролиза 500 мл раствора гидроксида натрия с ω(NaОН) = 4,6% (ρ = 1,05 г/мл) массовая доля NaОН в растворе увеличилась до 10%. Вычислите объёмы газов (н.у.), выделившихся на электродах.
Решение и ответ:
Уравнение реакции, которая протекает при электролизе раствора гидроксида натрия:
2H₂O → O₂ + 2H₂
Фактически, на катоде восстанавливается водород, на аноде окисляется кислород. Количество щелочи в растворе при этом не изменяется. Определим количество щелочи:
mр-ра(NaOH) = Vр-ра(NaOH) ·ρ(NaOH) = 500 мл · 1,05 г/мл = 525 г
m(NaOH) = mр-ра(NaOH) ·ω(NaOH) = 525 г · 0,046 = 24,15 г
n(NaOH) = m/M =24,15 г / 40 г/моль = 0,604 моль
За счет чего же меняется массовая доля? Все очень просто — за счет электролиза воды. Зная, что масса гидроксида натрия не изменилась, найдем массу конечного раствора:
mр-ра,₂(NaOH) = m(NaOH) / ω(NaOH) = 24,15 г / 0,1 = 241,5 г
Количество воды, которая подверглась электролизу:
m(H₂O) = mр-ра,1(NaOH) – mр-ра,₂ (NaOH) = 525 – 241,5 = 283,5 г
n(H₂O) = m/M =283,15 г / 18 г/моль = 15,75 моль
Из уравнения электролиза определим количество вещества водорода и кислорода и их массу:
n(H₂) = n(H2O) = 15,75 моль
V(H₂) = n·Vm =15,75 моль · 22,4 л/моль = 352,8 л
n(О₂) = 1/2·n(H2O) = 7,875 моль
V(O₂) = n·Vm = 7,875 моль · 22,4 л/моль = 176,4 л
Ответ: V(H₂) = 352,8 л, V(O₂) = 176,4 л
Задачи на электролиз встретились в ЕГЭ по химии в 2018 году. Вот одна из задач реального экзамена по химии:
4. При проведении электролиза 500 г 16% раствора сульфата меди (II) процесс прекратили, когда на аноде выделилось 1,12 л газа. Из полученного раствора отобрали порцию массой 98,4 г. Вычислите массу 20%-ного раствора гидроксида натрия, необходимого для полного осаждения ионов меди из отобранной порции раствора.
Решение.
Во-первых, составляем уравнение реакции электролиза раствора сульфата меди. Как это делать, подробно описано в статье Электролиз.
2CuSO₄ + 2H₂O → 2Cu + 2H₂SO₄ + O₂
Находим массу чистого сульфата меди:
m(CuSO₄) = mраствора*ω(CuSO₄) = 500*0,16 = 80 г
Количество вещества сульфата меди:
n(CuSO₄) = m/M = 80/160 = 0,5 моль
Видно, что на аноде должно выделиться 0,25 моль газа, или 5,6 л.
Однако, в условии сказано, что выделилось только 1,12 л газа. Следовательно, сульфат меди прореагировал не полностью, а только частично.
Находим количество и массу кислорода, который выделился на аноде:
n(O₂) = V/Vm = 1,12/22,4 = 0,05 моль,
m(O₂) = n*M = 0,05*32 = 1,6 г.
Следовательно, в электролиз вступило 0,1 моль сульфата меди.
В растворе осталось 0,4 моль сульфата меди. При этом образовалось 0,1 моль серной кислоты массой 9,8 г и 0,1 моль меди выпало в осадок (масса меди 6,4 г).
При этом масса полученного раствора после электролиза mр-ра₂ равна:
mр-ра₂ = 500 – 1,6 – 6,4 = 492 г
Из полученного раствора отобрали порцию массой 98,4 г. При этом количество растворенных веществ поменялось. Зато не поменялась их массовая доля.
Найдем массовую долю сульфата меди ω(CuSO₄)₂ и серной кислоты ω(H₂SO₄) в растворе, который остался после электролиза:
m(CuSO₄)ост = n*M = 0,4*160 = 64 г
ω(CuSO₄)₂ = m(CuSO₄)₂/*mр-ра₂ = 64/492 = 0,13 = 13%
ω(H₂SO₄) = m(H₂SO₄)/*mр-ра₂ = 9,8/492 = 0,02 = 2%
Найдем массу и количество серной кислоты и массу сульфата меди в порции массой mр-ра3 = 98,4 г, которую мы отобрали:
m(CuSO₄)3 = ω(CuSO₄)₂ *mр-ра3 = 0,13*98,4 = 12,79 г
m(H₂SO₄)₂ = ω(H₂SO₄)*mр-ра3 = 0,02*98,4 = 1,97 г
n(CuSO₄) = m/M = 12,79/160 = 0,08 моль
n(H₂SO₄) = m/M = 1,97/98 = 0,02 моль
Чтобы осадить ионы меди, гидроксид натрия должен прореагировать и с серной кислотой в растворе, и с сульфатом меди:
H₂SO₄ + 2NaOH = Na₂SO₄ + 2H₂O
CuSO₄ + 2NaOH = Cu(OH)₂ + 2H₂O
В первой реакции израсходуется 0,04 моль гидроксида натрия, во второй реакции 0,16 моль гидроксида натрия. Всего потребуется 0,2 моль гидроксида натрия. Или 8 г чистого NaOH, что соответствует 40 г 20%-ного раствора.
Ответ: mр-ра = 40 г.
Задача из досрочного ЕГЭ по химии-2020 на электролиз:
5. Через 640 г 15%-ного раствора сульфата меди(II) пропускали электрический ток до тех пор, пока на аноде не выделилось 11,2 л (н.у.) газа. К образовавшемуся раствору добавили 665,6 г 25%-ного раствора хлорида бария. Определите массовую долю хлорида бария в полученном растворе. В ответе запишите уравнения реакций, которые указаны в условии задачи, и приведите все необходимые вычисления (указывайте единицы измерения искомых физических величин).
Решение и ответ:
Уравнения реакций:
2CuSO₄ + 2H2O = 2Cu↓ + 2H2SO₄ + O2↑ (электролиз)
BaCl₂ + H₂SO₄ = BaSO₄↓ + 2HCl
Количество вещества реагентов и масса продуктов реакций:
m(CuSO₄) = 640 · 0,15 = 96 г
n(CuSO₄) = 96 / 160 = 0,6 моль
n(O₂) = 11,2 / 22,4 = 0,5 моль
n(Cu) = n(CuSO₄) = 0,6 моль
m(Cu) = 0,6 · 64 = 38,4 г
n(H₂SO₄) = n(CuSO₄) = 0,6 моль
При электролизе сульфата меди может выделится максимальное количество кислорода:
n(O₂ [1]) = 0,5n(CuSO₄) = 0,3 моль
Однако, по условию, на аноде всего выделилось 0,5 моль газа. Следовательно, дальше протекает электролиз воды:
2H₂O → O₂ + 2H₂ (электролиз)
Количество кислорода ,который выделится при электролизе воды:
n(O₂ [2]) = 0,5 – 0,3 = 0,2 моль
Отсюда можно найти массу воды, которая разложилась под действием тока:
n(H₂O прореаг.) = 2n(O₂ [2]) = 0,4 моль
m(H₂O прореаг.) = 0,4 · 18 = 7,2 г
m(O₂ [1]) = 32 · 0,3 = 9,6 г
m(BaCl₂) = 665,6 · 0,25 = 166,4 г
n(BaCl₂) = 166,4 / 208 = 0,8 моль
n(BaCl₂ прореаг.) = n(H₂SO₄) = 0,6 моль
n(BaCl₂ осталось) = 0,8 – 0,6 = 0,2 моль
m(BaCl₂ осталось) = 0,2 · 208 = 41,6 г
n(BaSO₄) = n(BaCl₂ прореаг.) = 0,6 моль
m(BaSO₄) = 0,6 · 233 = 139,8 г
Массовая доля хлорида бария в растворе:
m(р-ра) = 640 + 665,6 – 38,4 – 7,2 – 139,8 – 9,6 = 1110,6 г
ω(BaCl₂) = 41,6 / 1110,6 = 0,037, или 3,7 %
Ответ: ω(BaCl₂) = 3,7 %
Еще больше задач на электролиз вы можете найти в моей статье.
Задача 13 (ОВР-63)
Сформулировать правило разряда ионов для процессов анодного окисления. Растворимые и нерастворимые аноды.
Решение:
Правило разряда ионов (в соответствии с законами ТД): в тех случаях, когда на одном и том же электроде возможно протекание двух (нескольких) процессов, наиболее вероятен тот, осуществление которого требует меньшей затраты энергии.
Поэтому порядок разрядки ионов на электродах из смеси (раствора) при ее электролизе определяется потенциалом соответствующего электрода с учетом поляризации:
первым на катоде выделяется (разряжается) тот ион, потенциал которого больше;
на аноде в первую очередь разряжаются (окисляются) ионы, потенциал которых меньше.
Так как существует поляризация, то определять порядок разрядки ионов на электродах по стандартным значениям потенциалов нельзя, нужно знать экспериментальные значения потенциалов при определенных условиях. Перенапряжение при разрядке ионов металлов на катоде наименьшее, поэтому они ведут себя при электролизе приблизительно в соответствии с их стандартными потенциалами. Наибольшее перенапряжение имеет место при разрядке сложных ионов (NO3− , SO42− и др.), а также на газовых электродах (водородном, кислородном).
В соответствии с экспериментальными данными для катодного восстановления при электролизе водных растворов электролитов сформулированы качественные правила для электролиза разбавленных растворов солей, которые учитывают тот факт, что в растворе соли, кроме ее собственных ионов, имеются ионы и молекулы самой воды (Н2О. Н+, ОН−), которые также могут участвовать в электролизе.
Катодные процессы:
1. Катионы металлов, стоящих в ряду напряжений до Al (вкл.) не разряжаются на катоде; в этом случае на катоде восстанавливаются ионы водорода (в кислой среде) или молекулы воды (водородная деполяризация катода):
2Н+ + 2ē → Н2↑ , φ°= −0,00 В , φ = −0,059рН
2Н2О + 2ē → Н2↑ + 2ОН− , φ°= −0,826 В, φ(рН=7)=−0,413 В, φ=φ°+0,059рН
2. Катионы металлов, находящихся в ряду напряжений после Al,но до Cd (φ°= −0,41В), разряжаются параллельно с водородом:
Ме(n+) + nē → Ме ; 2Н2О + 2ē → Н2 + 2ОН− ; 2Н+ + 2ē → Н2↑ (в кислой среде)
3. Ионы благородных и малоактивных металлов, потенциал которых φ° > −0,41В, разряжаются в первую очередь, и разряд ионов водорода или молекул воды не происходит: Ме(n+) + nē → Ме
Анодные процессы:
Анионы также можно расположить в ряд по возрастанию восстановительной активности: F− , NO3− , SO42−, OH− , Cl−, Br−, I− , S2− .
Однако порядок разрядки также не полностью подчиняется этому ряду. Поэтому существуют следующие правила для инертного анода:
1. Простые анионы Cl−, Br−, S2− и др. (кроме F−) на аноде разряжаются сами, напр.:
2Cl− − 2ē → Cl2.
2. Сложные анионы (SO42−, NO3− и т.д.) и F− на аноде не разряжаются, происходит окисление воды: 2Н2О − 4ē = O2 + 4Н+ (φ° = +1,23 В).
Т.о. электролиз водных растворов щелочей и кислородсодержащих кислот приводит к образованию водорода на катоде и кислорода на аноде, т.е. к простому электролизу воды.
Электролиз с растворимым (активным) анодом: если анод выполнен из металла с потенциалом более отрицательным, чем потенциалы окисления других частиц, присутствующих в данной системе, в том числе ионов ОН–, то происходит анодное растворение:
Мео – nе – → Меn+
При этом в качестве электролита, как правило, берется соединение элемента, входящего в состав анода. Тогда на катоде и аноде происходит одна реакция в противоположных направлениях, поэтому Δφ° близко к 0.
