Какое свойство углерода выделяет его из совокупности других
Углерод — химический элемент № (6). Он расположен в IVА группе Периодической системы.
C6+6)2e)4e
На внешнем слое атома углерода содержатся четыре валентных электрона, и до его завершения не хватает четырёх электронов. Поэтому в соединениях с металлами углероду характерна степень окисления (–4), а при взаимодействии с более электроотрицательными неметаллами он проявляет положительные степени окисления: ( +2) или (+4).
В природе углерод встречается как в виде простых веществ, так и в виде соединений. В воздухе содержится углекислый газ. В земной коре распространены карбонаты (например, CaCO3 образует мел, мрамор, известняк). Горючие ископаемые (уголь, торф, нефть, природный газ) состоят из органических соединений, главным элементом которых является углерод.
Углерод относится к жизненно важным элементам, так как входит в состав молекул всех органических веществ.
Углерод образует несколько аллотропных видоизменений, из которых наиболее известны алмаз и графит.
Алмаз имеет атомную кристаллическую решётку. Каждый атом углерода в алмазе связан четырьмя прочными ковалентными связями с соседними атомами, расположенными в вершинах тетраэдра.
Благодаря такому строению алмаз — самое твёрдое из известных природных веществ. Все четыре валентных электрона каждого атома углерода участвуют в образовании связей, поэтому алмаз не проводит электрический ток. Это бесцветное прозрачное кристаллическое вещество, хорошо преломляющее свет.
Графит тоже имеет атомную кристаллическую решётку, но устроена она иначе. Решётка графита слоистая. Каждый атом углерода соединён прочными ковалентными связями с тремя соседними атомами. Образуются плоские слои из шестиугольников, которые между собой связаны слабо. Один валентный электрон у атома углерода остаётся свободным.
Графит представляет собой тёмно-серое вещество с металлическим блеском, жирное на ощупь. В отличие от алмаза графит непрозрачный, проводит электрический ток и оставляет серый след на бумаге. У графита очень высокая температура плавления ((3700) °С).
Алмаз и графит взаимопревращаемы. При сильном нагревании без доступа воздуха алмаз чернеет и превращается в графит. Графит можно превратить в алмаз при высокой температуре и большом давлении.
Из мельчайших частиц графита состоят сажа, древесный уголь и кокс. Сажа образуется при неполном сгорании топлива. Древесный уголь получают при нагревании древесины без доступа воздуха, а кокс — переработкой каменного угля.
Древесный уголь имеет пористое строение и обладает способностью поглощать газы и растворённые вещества. Такое свойство называется адсорбцией.
Аллотропные модификации углерода в химических реакциях могут проявлять и окислительные, и восстановительные свойства. Окислительные свойства углерода выражены слабее, чем у других неметаллов второго периода (азота, кислорода и фтора).
- Взаимодействие с металлами.
Углерод реагирует с металлами при высокой температуре с образованием карбидов:
4Al0+3C0=tAl+34C−43.
В этой реакции углерод выступает как окислитель.
- Взаимодействие с водородом.
Реакция происходит при сильном нагревании. Образуется метан. Углерод — окислитель.
C0+2H02=tC−4H+14.
- Взаимодействие с кислородом.
Углерод горит в кислороде с образованием углекислого газа и проявляет в этой реакции восстановительные свойства:
C0+O02=tC+4O−22.
- Взаимодействие с оксидами металлов.
Углерод способен восстанавливать металлы из их оксидов:
2Cu+2O+C0=t2Cu0+C+4O2.
Применение простых веществ
Алмаз применяется:
- для обработки твёрдых поверхностей;
- для резки стекла;
- для изготовления буров и свёрл;
- для изготовления ювелирных украшений.
Графит используется:
- при изготовлении карандашей;
- как твёрдая смазка в подшипниках;
- для изготовления электродов;
- в качестве замедлителя нейтронов в ядерных реакторах;
- для получения искусственных алмазов.
Сажа:
- входит в состав типографской краски, крема для обуви;
- используется как наполнитель для производства резины.
Уголь используется:
- в противогазах, промышленных и бытовых фильтрах;
- для очистки сахарного сиропа, спирта и т. д.;
- в медицине.
Кокс применяется в металлургической промышленности.
Вопрос 1. Каковы основные положения атомно — молекулярного учения?
1) Все вещества состоят из молекул.
2) Молекулы состоят из атомов. Атомы каждого вида (элемента) одинаковы между собой, но отличаются от атомов любого другого вида.
3) Частицы — молекулы и атомы — находятся в непрерывном движении. Тепловое состояние тел есть результат движения их частиц.
4) При взаимодействии атомов образуются молекулы: гомоядерные — при соединении атомов одного вида (например, H2, O2), образующиеся при этом вещества называются простыми; гетероядерные — при взаимодействии атомов разного вида (например, H2O, H2SO4), образующиеся при этом вещества называются сложными.
5) При физических явлениях молекулы сохраняются, при химических — разрушаются (или образуются новые). Атомы же и при физических, и при химических реакциях остаются неизменными.
6) Химические реакции заключаются в образовании новых веществ из тех же самых атомов, из которых состоят первоначальные вещества.
Вопрос 2. Что такое химические элементы? Как устроены атомы разных химических элементов?
Химический элемент — совокупность атомных частиц (электронейтральных атомов и одноатомных ионов) с одинаково положительным зарядом ядра.
Атомы чрезвычайно малы, их диаметр колеблется в пределах 0,2 — 0,5 нм (1 нм = 10 — 9 м). Массы атомов составляют порядка 10 — 24 — 10 — 22 г. Атомы имеют сложное строение и состоят из положительно заряженного ядра и вращающихся вокруг него отрицательно заряженных электронов.
Вопрос 3. Что такое валентные электроны?
Валентные электроны — это такие электроны, которые участвуют в образовании химических связей.
Вопрос 4. Чем различаются свойства химических элементов главных и побочных подгрупп из левой и правой частей таблицы Менделеева?
Главное отличие в особенности заполнения электронами орбиталей и, соответственно, различие химических свойств.
Химические свойства, например, у s — элементов 1 группы — валентность 1, степень окисления — +1. А у d — элементов — переменная валентность и степень окисления, т.к у них есть свободные орбитали для заполнения электронами. К примеру, представлены электронно — графические схемы Na и Fe.
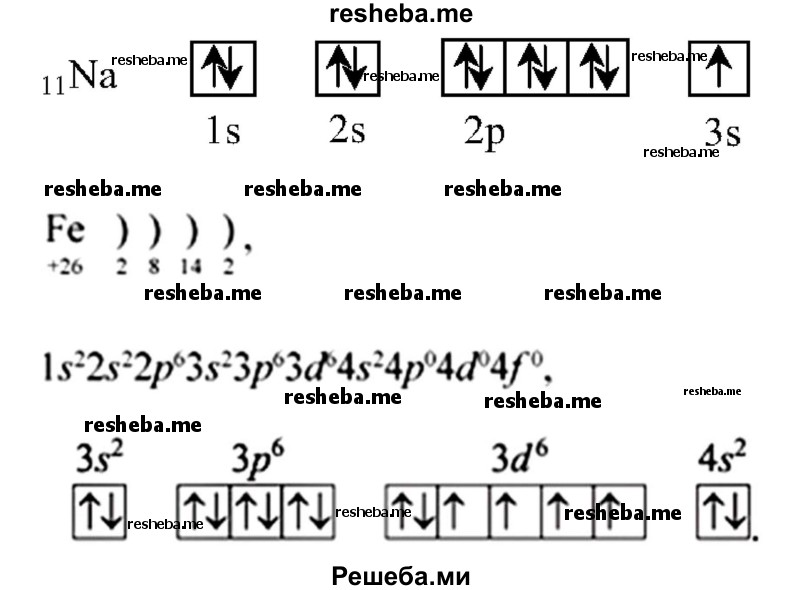
Вопрос 5. Какие химические элементы относят к группе макроэлементов и почему?
К группе макроэлементов относят химические элементы, содержание которых в живых организмах превышает 0,01 %. В значительных количествах встречаются 4 хим. элемента (кислород, углерод, водород и азот) (в сумме около 96 %) и ещё 8: кальций, фосфор, калий, сера, хлор, натрий, магний и железо.
Вопрос 6. Из чего состоят молекулы различных веществ? Что лежит в основе образования их структуры?
Молекулы состоят из атомов различных химических элементов. в основе образования их структуры обеспечивается возникновением химической связи между входящими в их состав атомами. Эти связи возникают вследствие объединения электронных оболочек атомов, которые образуют молекулу.
Вопрос 7. Что лежит в основе разделения веществ на органические и неорганические?
В основе разделения веществ на органические и неорганические лежит происхождение и наличие углерода в составе этих веществ (СО, СО2, Н2СО3 и карбонаты — это неорганические вещества).
Вопрос 8. Какие особенности атомов углерода обусловливают многообразие органических веществ в природе?
Очень важной особенностью атома углерода является его способность образовывать связи сразу с четырьмя другими такими же атомами. Благодаря этой способности атомы углерода могут образовывать каркасы огромного количества разнообразных биологических молекул, что способствует появлению многообразных органических веществ в природе.
Вопрос 9. Какие органические вещества являются биополимерами? Приведите примеры известных вам регулярных и нерегулярных полимеров, гомо — и гетерополимеров.
Биополимеры — высокомолекулярные органические соединения, входящие в состав живых организмов (белки, полисахариды, нуклеиновые кислоты).
Пример регулярных полимеров: крахмал, полисахариды, целлюлоза, гликоген.
Пример нерегулярных полимеров: белки, нуклеиновые кислоты.
Пример гомополимеров: крахмал, полисахариды, целлюлоза, гликоген.
Пример гетерополимеров: белки, нуклеиновые кислоты.
Вопрос 10. Используя данные таблицы 1, постройте диаграмму, отражающую содержание указанных в ней химических элементов в организме человека и в земной коре (% по массе).
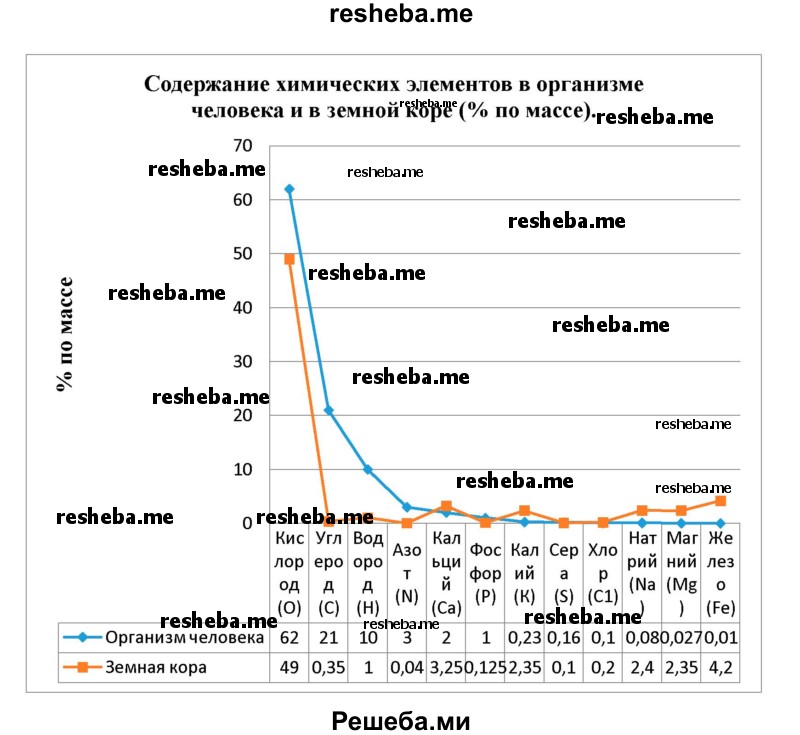
Вопрос 11. Прочитайте статью «Химические связи в молекулах веществ». Составьте схему образования молекул известных вам веществ: водорода (Н2), кислорода (02), воды (Н20), хлорида натрия (NaCl) и метана (СН4). Подпишите на схеме названия типов химических связей, участвующих в образовании этих веществ.

В молекуле воды между атомами водорода и кислорода — ковалентная полярная связь. А водородная связь возникает МЕЖДУ МОЛЕКУЛАМИ ВОДЫ (а не В МОЛЕКУЛЕ воды).
Вопрос 12. Используя материалы Википедии (https://ru.wikipedia.org), обобщите собственные представления о строении атома и молекул. Оформите их в виде таблицы.
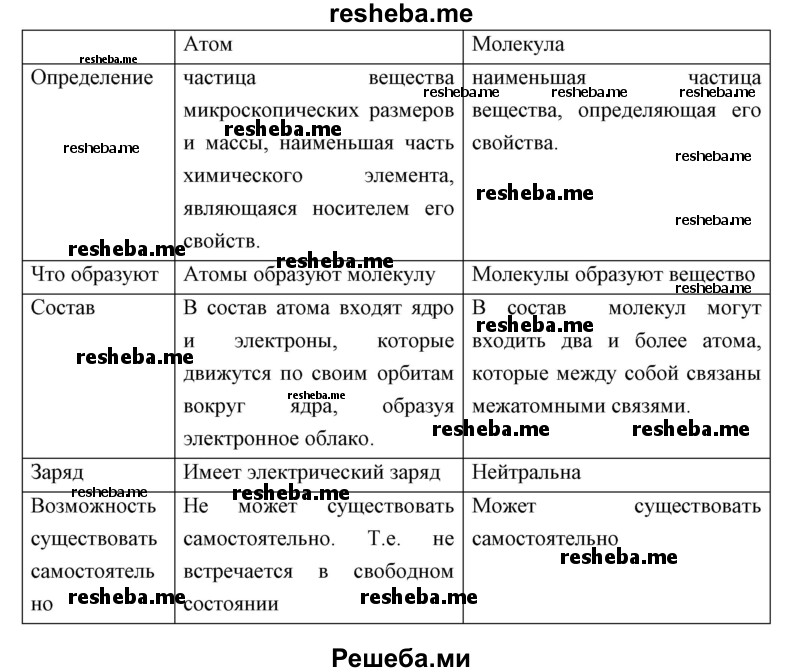
Вопрос 13. Используя доступные информационные источники, найдите и рассмотрите периодическую таблицу химических элементов Д. И. Менделеева. Найдите в ней элементы, относящиеся к микро — и макроэлементам. Атомы нескольких химических элементов обладают строением, сходным со строением атомов углерода. Назовите эти элементы. Могли бы они заменить углерод в структуре органических веществ? Ответ обоснуйте и подкрепите известными вам примерами.
К макроэлементам относятся 12 химических элементов: кислород, углерод, водород и азот, кальций, фосфор, калий, сера, хлор, натрий, магний и железо. Всего в живых организмах найдено более 80 химических элементов, однако содержание большинства из них крайне мало — это микроэлементы (медь, йод, цинк, кобальт, кремний, марганец, литий и др.).
Макроэлементы обозначены красным, а микроэлементы — синим.
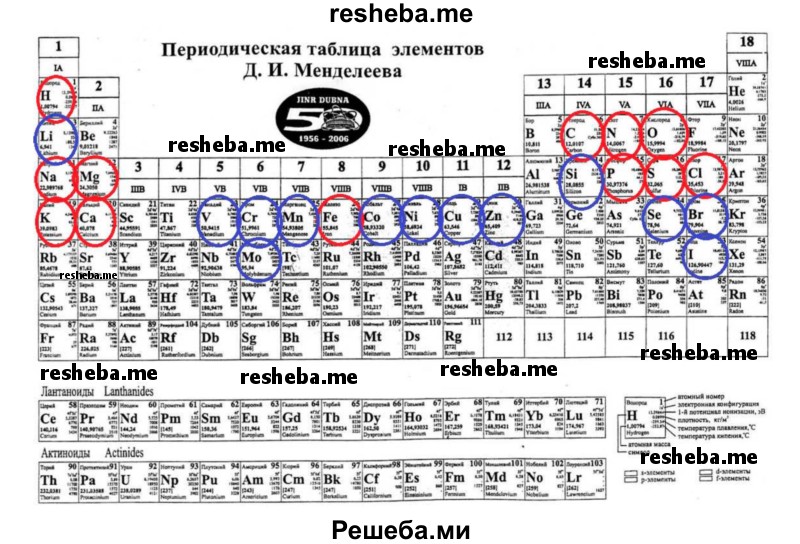
Кремний, бор и азот обладают строением, сходным со строением атомов углерода. Но они не могут заменить углерод в структуре органических веществ, потому что:
1. Заполненный внешний электрический слой.
2. Обладает низкой окислительной способностью.
3. Строение атома элемента углерода включает две оболочки, на которых расположено шесть электронов. Валентность углерода, входящего в состав органических веществ, постоянна и равна IV. Это значит, что на внешнем электронном уровне находится четыре электрона, а на внутреннем — два.
4. Возбуждённый атом углерода имеет четыре неспаренных электрона. Его конфигурацию можно выразить формулой 2s12p3. Это даёт возможность образовывать четыре ковалентные связи с другими элементами.
5. Полимерные молекулы способны образовывать в большей степени углерод, сера, фосфор, селен и теллур, а в меньшей — кремний, германий, бор, мышьяк (As), олово (Sn) и сурьма (Sb). Способность образовывать достаточно прочные гомоцепные полимеры зависит от прочности связей атомов данного элемента друг с другом (у углерода этот показатель самый высокий — 80 ккал/моль, смотрите табл.)
Табл. Энергия некоторых связей в гомоцепных полимерах.
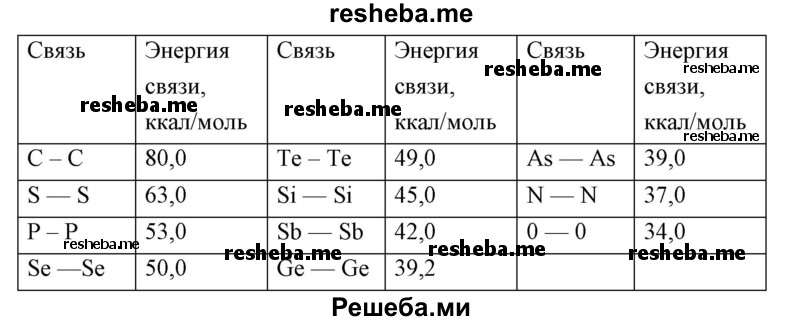
Среди всех элементов периодической системы углерод выделяется своей уникальной способностью образовывать необычайно длинные цепи полимеров.
6. Атомы бора, кремния, фосфора и др., также образуют прочные цепи из атомов этих элементов (в элементарном состоянии). Но уникальность углерода обусловлена в значительной степени тем обстоятельством, что образуемые им углерод — углеродные связи прочны и в тех случаях, когда атомы углерода одновременно связаны с другими элементами. Например, углерод — водородные и углерод — фторные соединения высоко стабильны и в химическом отношении относительно мало реакционноснособны, а соответствующие производные бора, кремния, фосфора и т. д. либо не могут быть получены, либо являются крайне реакционноснособными веществами.
7. Атомы углерода могут связываться по — разному, называясь при этом аллотропами углерода.
Вопрос 14. Основные макроэлементы, в первую очередь углерод, водород и азот, присутствуют в живых организмах в больших количествах, чем в неживой природе. Почему? Что из этого следует?
Потому что все органические соединения получены соединением этих элементов. Это связано в основном с их валентностью, равной соответственно 1, 4 и 3, а также с их способностью образовывать более прочные ковалентные связи, нежели связи, образуемые другими элементами той же валентности. Атомы углерода способны образовывать цепочки и кольца, создавая гигантское разнообразие органических молекул. Вода — вещество с уникальными свойствами, способное растворять огромное разнообразие веществ, а также стабилизировать температуру за счет высокой теплоемкости, теплоты замерзания и теплоты испарения. Азот входит в состав аминокислот. Все эти элементы входят в обменные процессы клеток и являются жизненно необходимыми химическими компонентами живых организмов.
Присутствие в живых организмах этих химических элементов в больших количествах, чем в неживой природе, наталкивает на мысль: химические соединения, содержащие углерод, водород, кислород и азот (наиболее распространенные в живой природе элементы) были отобраны из неживой природы в ходе эволюции благодаря их особой приспособленности для участия в процессах жизнедеятельности.
Вопрос 15. Какую проблему необходимо учитывать учёным в связи с разработкой и внедрением в производство новых искусственно созданных органических веществ? Обсудите это с учителем и одноклассниками.
Здесь можно выделить не одну, а несколько проблем.
1. Уменьшение количества отходов с целью уменьшения вредного воздействия на окружающую природу.
В экологическом отношении коксохимическое производство является одним из наиболее опасных. На всех его стадиях выделяется значительная масса загрязнителей. На долю коксохимического производства приходится более 70% канцерогенов от их общего количества, образующегося в металлургии (бензол, каменноугольная смола и др.).
Добыча, переработка и транспортировка нефти сопряжены с загрязнением окружающей среды (в первую очередь загрязнение Мирового океана).
2. Сохранение невозобновляемых источников сырья.
3. Увеличение эффективности переработки сырья.
Например, при переработке нефти выход наиболее ценных продуктов (бензина) недостаточен и обычно не превышает 15%, что не может покрыть все возрастающий спрос народного хозяйства на этот и другие виды моторного топлива. Увеличения их выхода достигают применением химических процессов переработки, резко увеличивающих выход бензина (до 70% массы сырья).
4. Снижение энергоёмкости производств.
5. И др.
Химические свойства углерода
Углерод способен образовывать несколько аллотропных модификаций. Это алмаз (наиболее инертная аллотропная модификация), графит, фуллерен и карбин.
Древесный уголь и сажа представляют собой аморфный углерод. Углерод в таком состоянии не имеет упорядоченной структуры и фактически состоит из мельчайших фрагментов слоев графита. Аморфный углерод, обработанный горячим водяным паром, называют активированным углем. 1 грамм активированного угля из-за наличия в нем множества пор имеет общую поверхность более трехсот квадратных метров! Благодаря своей способности поглощать различные вещества активированный уголь находит широкое применение как наполнитель фильтров, а также как энтеросорбент при различных видах отравлений.
С химической точки зрения аморфный углерод является наиболее активной его формой, графит проявляет среднюю активность, а алмаз является крайне инертным веществом. По этой причине, рассматриваемые ниже химические свойства углерода следует прежде всего относить к аморфному углероду.
Восстановительные свойства углерода
Как восстановитель углерод реагирует с такими неметаллами как, например, кислород, галогены, сера.
В зависимости от избытка или недостатка кислорода при горении угля возможно образование угарного газа CO или углекислого газа CO2:
При взаимодействии углерода со фтором образуется тетрафторид углерода:
При нагревании углерода с серой образуется сероуглерод CS2:
Углерод способен восстанавливать металлы после алюминия в ряду активности из их оксидов. Например:
Также углерод реагирует и с оксидами активных металлов, однако в этом случае наблюдается, как правило, не восстановление металла, а образование его карбида:
Взаимодействие углерода с оксидами неметаллов
Углерод вступает в реакцию сопропорционирования с углекислым газом CO2:
Одним из наиболее важных с промышленной точки зрения процессов является так называемая паровая конверсия угля. Процесс проводят, пропуская водяной пар через раскаленный уголь. При этом протекает следующая реакция:
При высокой температуре углерод способен восстанавливать даже такое инертное соединение как диоксид кремния. При этом в зависимости от условия возможно образование кремния или карбида кремния (карборунда):
Также углерод как восстановитель реагирует с кислотами окислителями, в частности, концентрированными серной и азотной кислотами:
Окислительные свойства углерода
Химический элемент углерод не отличается высокой электроотрицательностью, поэтому образуемые им простые вещества редко проявляют окислительные свойства по отношению к другим неметаллам.
Примером таких реакций является взаимодействие аморфного углерода с водородом при нагревании в присутствии катализатора:
а также с кремнием при температуре 1200-1300 оС:
Окислительные свойства углерод проявляет по отношению к металлам. Углерод способен реагировать с активными металлами и некоторыми металлами средней активности. Реакции протекают при нагревании:
Карбиды активных металлов гидролизуются водой:
а также растворами кислот-неокислителей:
При этом образуются углеводороды, содержащие углерод в той же степени окисления, что и в исходном карбиде.
Химические свойства кремния
Кремний может существовать, как и углерод в кристаллическом и аморфном состоянии и, также, как и в случае углерода, аморфный кремний существенно более химически активен, чем кристаллический.
Иногда аморфный и кристаллический кремний, называют его аллотропными модификациями, что, строго говоря, не совсем верно. Аморфный кремний представляет собой по сути конгломерат беспорядочно расположенных друг относительно друга мельчайших частиц кристаллического кремния.
Взаимодействие кремния с простыми веществами
неметаллами
При обычных условиях кремний ввиду своей инертности реагирует только со фтором:
С хлором, бромом и йодом кремний реагирует только при нагревании. При этом характерно, что в зависимости от активности галогена, требуется и соответственно различная температура:
Так с хлором реакция протекает при 340-420 оС:
С бромом – 620-700 оС:
С йодом – 750-810 оС:
Все галогениды кремния легко гидролизуются водой:
а также растворами щелочей:
Реакция кремния с кислородом протекает, однако требует очень сильного нагревания (1200-1300оС) ввиду того, что прочная оксидная пленка затрудняет взаимодействие:
При температуре 1200-1500 оС кремний медленно взаимодействует с углеродом в виде графита с образованием карборунда SiC – вещества с атомной кристаллической решеткой подобной алмазу и почти не уступающего ему в прочности:
С водородом кремний не реагирует.
металлами
Ввиду своей низкой электроотрицательности кремний может проявлять окислительные свойства лишь по отношению к металлам. Из металлов кремний реагирует с активными (щелочными и щелочноземельными), а также многими металлами средней активности. В результате такого взаимодействия образуются силициды:
Силициды активных металлов легко гидролизуются водой или разбавленными растворами кислот-неокислителей:
При этом образуется газ силан SiH4 – аналог метана CH4.
Взаимодействие кремния со сложными веществами
С водой кремний не реагирует даже при кипячении, однако аморфный кремний взаимодействует с перегретым водяным паром при температуре около 400-500оС. При этом образуется водород и диоксид кремния:
Из всех кислот кремний (в аморфном состоянии) реагирует только с концентрированной плавиковой кислотой:
Кремний растворяется в концентрированных растворах щелочей. Реакция сопровождается выделением водорода:
