Какое число молекул содержится в 1 м3
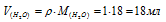
1
Сколько молекул содержится в 1 см3 воды? Какова масса молекулы воды? Каков приблизительный размер молекулы воды?
Ответ и решение
n = 3,33·1022 1/см3; m = 2,99·10-26 кг; a = 3,11·10-10 м.
Масса 1 моля воды составляет 18 г, а его объем V — 18 см3. В 1 моле воды содержится число молекул, равное постоянной Авогадро NА = 6·1023. Число молекул в 1 см3n = NА/V = 3,33·1022. Масса одной молекулы m = 18/NА = 3·10-26 кг. Объем V0 одной молекулы приблизительно равен 1/n см3. Тогда размер молекулы составит
.
2
Хорошо откачанная лампа накаливания объемом 10 см3 имеет трещину, в которую ежесекундно проникает миллион частиц газа. Сколько времени понадобится для наполнения лампы до нормального давления, если скорость проникновения газа остается постоянной? Температура 0 °С.
Ответ и решение
t ≈ 8,5 млн. лет.
Найдем число частиц газа, необходимое для наполнения лампы:
N = VNЛ = 10·2,69·1019 см3·см-3 = 2,69·1020,
где V – объем лампы, NЛ – постоянная Лошмидта.
Время, необходимое для наполнения лампы со скоростью v = 106 с-1, равно:
t = N/v = 2,69·1020/(106·с-1) = 2,69·1014 c ≈ 8,5 млн. лет.
3
За 10 суток полностью испарилось из стакана 100 г воды. Сколько в среднем вылетало молекул с поверхности воды за 1 с?
Ответ и решение
≈ 3,8·1018 молекул в секунду.
Переведем время t испарения воды из суток в секунды:
t = 10 сут. = 8,64·105 с.
Поскольку 1 моль воды имеет массу 18 г, то, используя постоянную Авогадро, можно найти число N молекул в 100 г воды:
N = NА·100/18 = 3,3·1024 шт.
Теперь найдем скорость v испарения воды:
v = N/t ≈ 3,8·1018 c-1.
4
В озеро средней глубиной 10 м и площадью 10 км2 бросили кристаллик поваренной соли NaCl массой 0,01 г. Сколько ионов хлора оказалось бы в наперстке воды объемом 2 см3, зачерпнутом из этого озера, если считать, что соль, растворившись, равномерно распределилась в озере?
Ответ и решение
≈ 2·106 ионов.
1 моль поваренной соли имеет массу 58,5 г, из которых 23 г — масса натрия, а 35,5 г — масса хлора. Чтобы рассчитать массу хлора в брошенном кристаллике хлора, решим систему из двух уравнений:
m(Na) + m(Cl) = 0,01
m(Na)/m(Cl) = 0,65
Из системы получим, m(Cl) = 6·10-3 г.
Теперь можно вычислить число частиц хлора N(Cl):
N(Cl) = NA· 6·10-3/35,5 ≈ 1020 ионов хлора.
Число ионов хлора в наперстке будет меньше полученного числа во столько раз, во сколько раз объем наперстка меньше объема озера. Найдем это число:
N = 1020·2·10-6/108 = 2·106 ионов хлора в наперстке.
5
Кристаллы поваренной соли NaCl кубической системы состоят из чередующихся атомов (ионов) Na и Cl.

Определить наименьшее расстояние между их центрами. Молярная масса поваренной соли ν = 58,5 г/моль, а ее плотность ρ = 2,2 г/см3.
Ответ и решение
r = 2,83·10-8 см.
Найдем сторону a куба, который занимает объем одного моля поваренной соли:
a =  = 3 см.
= 3 см.
Найдем, какое число ионов натрия и хлора приходится на одно ребро куба (общее число ионов натрия и хлора в 1 моле поваренной соли равно удвоенному числу молекул NaCl, т.е. 2NА):
n = 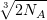 ≈ 108 ионов.
≈ 108 ионов.
Теперь найдем расстояние между ионами:
l = a/n = 2,83·10-8 см.
6
Кубическая кристаллическая решетка железа содержит один атом железа на элементарный куб, повторяя который, можно получить всю решетку кристалла. Определить расстояние между ближайшими атомами железа, если плотность железа ρ = 7,9 г/см3, атомная масса А = 56.
Ответ и решение
2,3·10-8 см.
Найдем сторону a куба, который занимает объем одного моля железа:
a =  = 1,9 см.
= 1,9 см.
Найдем, какое число атомов железа приходится на одно ребро куба (общее число атомов железа в 1 моле равно NА):
n = ≈ 8,4·107 атомов.
≈ 8,4·107 атомов.
Теперь найдем расстояние между атомами железа:
l = a/n = 2,3·10-8 см.
7
На пути молекулярного пучка стоит «зеркальная» стенка. Найти давление, испытываемое этой стенкой, если скорость молекул в пучке v = 103 м/с, концентрация n = 5·1017 1/м3, масса m = 3,32·10-27 кг. Рассмотреть три случая: а) стенка расположена перпендикулярно скорости пучка и неподвижна; б) пучок движется по направлению, составляющему со стенкой угол α = 45°; в) стенка движется навстречу молекулам со скоростью u = 50 м/с.
Ответ
а) pа ≈ 3,3·10-3 Па; б) pб ≈ 2,4·10-3 Па; в) pв ≈ pа.
8
Как изменилось бы давление в сосуде с газом, если бы внезапно исчезли силы притяжения между его молекулами?
Ответ
99
ninushka77 Какое число молекул содержится в 1 м 3 хлора при ну. Хотяб формулу напишите, остальноесам!категория: химия ответить в избранное 58
goruch 02 апреля 2018 Эта задача решается по двум формулам первая: n=V/Vm (Vm=22,4) N=n*Na (Na=6,02*10 в минус 23 степени) удачи пользователи выбрали этот ответ лучшим комментировать в избранное ссылка отблагодарить Знаете другой ответ? Другие вопросы по химии siid717 02 апреля 2018 1 ответ Народ! Помощь! Срочно! У чего ярче выражены неметаллические свойства у Углерода или Кислорода? Почему? david13-90 02 апреля 2018 1 ответ На сгорание алкана израсходовалось 40 л кислорода, при этом выделилось 25,6 л оксида углерода (IV). Установите молекулярную формулуалкана. korsar 02 апреля 2018 1 ответ Получение бутадиена-1,3 из бутена-1. Очень срочно! Ребят помогите! kerm84 02 апреля 2018 1 ответ Ионное уравнение 2 Ag+S2-=Ag2S (осадок) drumnbuss 02 апреля 2018 1 ответ КАК БУДЕТ структурная формула 4-метил mistika 02 апреля 2018 1 ответ РАССЧИТАТЬ МАССУ СОЛИ, КОТОРУЮ НЕОБХОДИМО ВЗЯТЬ ДЛЯ ПРИГОТОВЛЕНИЯ 100 МЛ 0,2 М РАСТВОРА ХЛОРИДА КАЛИЯ. ПОМОГИИТЕПОЖАЛУЙСТАА shtefan444 02 апреля 2018 1 ответ Вычислите массовые доли элементов в веществе H2SO4… Помогиите (Кто сделает, тому дам 17 пкт (Мне на завтра срочнонадоо thickstone 02 апреля 2018 1 ответ Очень нужно даю 32 пункта Равновесие в системе: 2NO+O2 -> tatyana_schukina11 02 апреля 2018 1 ответ Вычислите массу соли, образовавшейся при взаимодействии оксида цинка массой 32,4 г и 20%-го раствора соляной кислоты массой 292 г. | Задайте свой вопрос ПОПУЛЯРНОЕ siid717, 02 апреля 2018 Народ! Помощь! Срочно! У чего ярче выражены неметаллические свойства у Углерода или Кислорода? Почему? david13-90, 02 апреля 2018 На сгорание алкана израсходовалось 40 л кислорода, при этом выделилось 25,6 л оксида углерода (IV) korsar, 02 апреля 2018 Получение бутадиена-1,3 из бутена-1. Очень срочно! Ребят помогите! kerm84, 02 апреля 2018 Ионное уравнение 2 Ag+S2-=Ag2S (осадок) drumnbuss, 02 апреля 2018 КАК БУДЕТ структурная формула 4-метил mistika, 02 апреля 2018 РАССЧИТАТЬ МАССУ СОЛИ, КОТОРУЮ НЕОБХОДИМО ВЗЯТЬ ДЛЯ ПРИГОТОВЛЕНИЯ 100 МЛ 0,2 М РАСТВОРА ХЛОРИДА КАЛИЯ shtefan444, 02 апреля 2018 Вычислите массовые доли элементов в веществе H2SO4… Помогиите (Кто сделает, тому дам 17 пкт (Мне на завтра срочнонадоо thickstone, 02 апреля 2018 Очень нужно даю 32 пункта Равновесие в системе: 2NO+O2 -> tatyana_schukina11, 02 апреля 2018 Вычислите массу соли, образовавшейся при взаимодействии оксида цинка массой 32… 27400 Алгебра 14821 Английский язык 14216 Биология 7369 Другой 720 Экономика 18828 Физика 8304 География 15850 Геометрия 5255 Информатика 11818 История 23332 Химия 15992 Литература 73118 Математика 8152 Обществознание 465 Правоведение 46271 Русский язык |
Химия
8 класс
Химия — это наука о веществах. А как измерять вещество? В каких единицах? Вы можете предложить отсчитывать необходимое число молекул вещества, если оно состоит из них. Однако сделать это чрезвычайно сложно. Некоторые из вас предложат измерять вещество в граммах, килограммах или миллиграммах. Но ведь это единицы измерения массы.
Для измерения вещества была выбрана особая единица, в которой как бы соединились число молекул и масса вещества. Эта единица была названа моль.
Чтобы отмерить 1 моль вещества, нужно взять столько граммов его, какова относительная атомная (Аr) или относительная молекулярная масса (Мr) вещества.
Например, 1 моль воды имеет массу, равную 18 г, так как Мr(Н2O) = 18; 1 моль кислорода имеет массу, равную 32 г, так как Мr(O2) = 32; 1 моль железа имеет массу, равную 56 г, так как Mr(Fe) = 56.
А если нужно отмерить 2 моль воды, то сколько граммов её нужно взять? Верно, 36 г (18 × 2). А можно отмерить 0,5 моль кислорода? Конечно, 0,5 моль O2 имеют массу в два раза меньше массы 1 моль, т. е. 16 г (32 : 2). А сколько молей воды взяли, если, например, отмерили 45 г воды? Очевидно, нужно эту массу разделить на массу 1 моль воды (45 г : 18 г/моль = 2,5 моль), т. е. взяли 2,5 моль.
А как связано с количеством вещества число его молекул? Установлено, что 1 моль любого вещества всегда содержит одинаковое число молекул. Это число равно 6 × 1023. В честь итальянского учёного А. Авогадро это число назвали постоянной Авогадро. Обозначают её NA.
Таким образом, 1 моль воды имеет массу 18 г и содержит 6 × 1023 молекул Н2O. 1 моль кислорода O2 имеет массу 32 г и также содержит 6 × 1023 молекул O2.
Очевидно, что в 2 моль воды и любого вещества содержится 12 × 1023 молекул, а в 0,5 моль — 3 × 1023 молекул.
Значит, чтобы узнать число молекул (N), содержащихся в определённом количестве вещества, можно воспользоваться формулой:

где п — количество вещества, т. е. число молей.
Отсюда верны и следующие равенства:

Теперь дадим определение понятия «моль».
Моль — это такое количество вещества, в котором содержится 6 × 1023 молекул этого вещества.
Однако следует помнить, что в молях измеряют и число других частиц: атомов, ионов, электронов и т. д. Во всех случаях 1 моль содержит 6 × 1023 соответствующих частиц (атомов, ионов, электронов и т. д.).
Массу 1 моль вещества называют его молярной массой и обозначают буквой М.
Как вы теперь знаете, количество вещества измеряют в молях и обозначают буквой n, в некоторых учебниках — греческой буквой v («ню»). Чтобы найти количество вещества, нужно его массу разделить на молярную массу:

Следовательно, верны и обратные формулы:

Молярная масса — это физическая величина, которая равна отношению массы вещества к количеству вещества.
Отсюда можно определить и единицу молярной массы — г/моль. М(Н2O) = 18 г/моль.
Вы знаете, что единицу массы, в 1000 раз большую одного грамма, называют килограммом, а единицу массы, в 1000 раз меньшую одного грамма, — миллиграммом. И количество вещества можно измерять не только в молях, но и в киломолях — кмоль (1 кмоль = 1000 моль), и в миллимолях — ммоль (1 моль = 1000 ммоль). Соответственно вместо молярной массы в некоторых случаях удобнее использовать понятия киломолярная масса (кг/кмоль) и миллимолярная масса (мг/ммоль).
Мы определили, как связаны между собой количество вещества и его масса. Теперь решим задачи с использованием рассмотренных выше понятий.
Задача 1. Сколько молекул содержится в 11 г углекислого газа СO2?
 Задача 2. Найдите массу 15 × 1023 молекул кислорода.
Задача 2. Найдите массу 15 × 1023 молекул кислорода.

Ключевые слова и словосочетания
- Количество вещества.
- Моль, киломоль, миллимоль.
- Молярная, киломолярная и миллимолярная массы.
- Постоянная Авогадро.
Работа с компьютером
- Обратитесь к электронному приложению. Изучите материал урока и выполните предложенные задания.
- Найдите в Интернете электронные адреса, которые могут служить дополнительными источниками, раскрывающими содержание ключевых слов и словосочетаний параграфа. Предложите учителю свою помощь в подготовке нового урока — сделайте сообщение по ключевым словам и словосочетаниям следующего параграфа.
Вопросы и задания
- Сколько молекул содержит: а) 1 кмоль вещества; б) 1 ммоль вещества?
- Найдите массу: а) 0,75 моль азота N2; б) 9 • 1023 молекул глюкозы С6Н12O6; в) 3 кмоль серной кислоты H2SO4.
- Сколько молекул содержат: а) 1,5 моль водорода; б) 7 г водорода; в) 4 кмоль водорода?
- Вставьте пропущенные слова в предложения: «Массу измеряют в миллиграммах, …, килограммах. Количество вещества измеряют в …, …, …».
- Плотность кислорода равна 1,3 г/л. Вычислите количество вещества кислорода, которое содержится в 1 л его. Сколько молекул кислорода содержится в 1 л; в 1 мл; в 1 м3?
Задача 53.
Сопоставить числа молекул, содержащихся в 1г NH3 и в 1г N2. В каком случае и во сколько раз число молекул больше?
Решение:
В одном моле любого вещества содержится 6,02 . 1023 молекул этого вещества.
Рассчитаем содержание количества вещества в 1г NH3 и N2 по формуле:
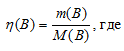
 (B) — количество вещества (В);
(B) — количество вещества (В);
m(B)- масса вещества (В);
M(B) — Молярная масса вещества (В).
М(NH3) = 17г/моль, M(N2) = 28г/моль.
Тогда
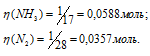
Число молекул NH3 больше числа молекул N2, так как  (NH3) >
(NH3) > (N2) . Теперь рассчитаем, во сколько раз число молекул NH3 больше числа молекул N2:
(N2) . Теперь рассчитаем, во сколько раз число молекул NH3 больше числа молекул N2:
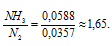
Ответ: в 1,65 раз число молекул NH3 больше числа молекул N2.
Задача 54.
Выразить в граммах массу одной молекулы диоксида серы.
Решение:
Находим молекулярную массу диоксида серы:
M(SO2) = 32 + (16 . 2) = 64г/моль.
Молекулярная масса численно составляет массу одного моля вещества, а значит, вес одного моля численно равен молекулярной массе и составляет 64г. Известно, что в одном моле любого вещества содержится 6,02 . 1023 молекул данного вещества. Исходя из этого, рассчитаем массу в граммах одной молекулы диоксида серы:
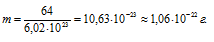
Ответ: масса одной молекулы диоксида серы равна.
Задача 55.
Одинаково ли число молекул в 0,001кг Н2 и в 0,001кг О2? В 1 моле Н2 и в 1 моле 02? В 1л Н2 и в 1л О2 при одинаковых условиях?
Решение:
Молекулярные массы водорода и кислорода равны соответственно 2г/моль и 32г/моль. Отсюда находим количество водорода и кислорода, зная их массы:
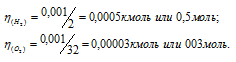
Один моль любого вещества содержит 6,02 .1023 молекул. Следовательно, в 0,001кг водорода и в 0,001кг кислорода содержится разное число молекул:

Так как имеется по одному молю водорода и кислорода, то количество молекул веществ будет одинаково:
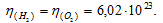
Согласно закону Авогадро в равных объёмах любых газов, взятых при одинаковых условиях, содержится одинаковое число молекул, Один моль любого газа занимает 22,4л, В которых содержится 6,02 . 1023 молекул. Отсюда рассчитаем количество молекул вещества, содержащихся в 1л водорода и в 1л кислорода:
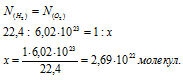
Ответ: а) в 0,001кг водорода и в 0,001кг кислорода содержится разное число молекул; б) в одном моле водорода и в одном моле кислорода содержится одинаковое число молекул: в) в одном литре водорода и в одном литре кислорода содержится одинаковое число молекул.
Задача 56.
Сколько молекул содержится в 1,00 мл водорода при нормальных условиях?
Решение:
Согласно закону Авогадро в равных объёмах любых газов, взятых при одинаковых условиях, содержится одинаковое число молекул, Один моль любого газа занимает 22,4л, В которых содержится 6,02 .1023 молекул. Отсюда рассчитаем количество молекул вещества, содержащихся в 1мл водорода из пропорции:
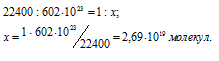
Ответ: 2,69 .1019 молекул.
Задача 57.
Какой объем при нормальных условиях занимают 27 .1021 молекул газа?
Решение:
Согласно закону Авогадро в равных объёмах любых газов, взятых при одинаковых условиях, содержится одинаковое число молекул, Один моль любого газа занимает 22,4л, В которых содержится 6,02 . 1023 молекул. Отсюда находим какой объём при нормальных условиях занимают 27 .1021 молекул газа, составив пропорцию:
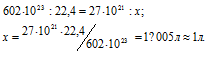
Ответ: V=1л.
Задача 58.
Каково соотношение объемов, занимаемых 1 молем О2 и 1 молем О3 (условия одинаковые)?
Решение:
Согласно закону Авогадро в равных объёмах любых газов, взятых при одинаковых условиях, содержится одинаковое число молекул, Один моль любого газа занимает 22,4л. Следовательно соотношение объёмов, занимаемых одним молем О2 и одним молем О3 иметь вид:
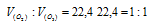
Ответ: 1:1
Задача 59.
Взяты равные массы кислорода, водорода и метана при одинаковых условиях. Найти отношение объемов взятых газов.
Решение:
Согласно закону Авогадро в равных объёмах любых газов, взятых при одинаковых условиях, содержится одинаковое число молекул, Один моль любого газа занимает 22,4л. Мольные массы кислорода, водорода и метана, соответственно равны 32 г/моль; 2г/моль; 16 г/моль.
Так как массы кислорода, водорода и метана одинаковы при одинаковых условиях, то отношение объёмов взятых газов находим из пропорции:
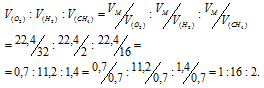
Ответ: 1:16:2.
Задача 60.
На вопрос, какой объем займет 1моль воды при нормальных условиях, получен ответ: 22,4л. Правильный ли это ответ?
Решение:
Согласно закону Авогадро в равных объёмах любых газов, взятых при одинаковых условиях, содержится одинаковое число молекул, Один моль любого газа занимает 22,4л. Так как вода при нормальных условиях находится в жидкой, а не в газообразной фазе, то ответ, что 1моль воды займёт 22,4л не правильный. Учитывая, что молярная масса воды равна 18г/моль, а плотность равна единице, то правильный ответ будет равен:
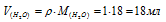
Ответ: 18мл.
Задача 61.
Сколько молекул диоксида углерода находится в 1л воздуха, если объемное содержание СО2 составляет 0,03% (условия нормальные)?
Решение:
При нормальных условиях углекислый газ, содержащийся в 1л воздуха, занимает объём 0,0003л. Зная, что мольный объём любого газа занимает 22,4л, рассчитаем число молей углекислого газа в 0,0003л из пропорции:
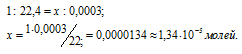
Учитывая, что в одном моле вещества содержится 6,02 . 1023 молекул, находим число молекул в 0,0003л газа:

Ответ: 8,07 .1018 молекул.
