Какие свойства растворов называются коллигативными
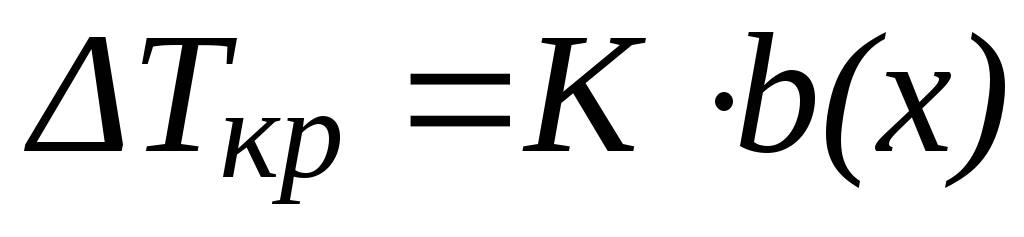
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 7 июля 2017;
проверки требуют 4 правки.
Коллигативные свойства растворов — это свойства растворов, обусловленные только самопроизвольным движением молекул, то есть они определяются не химическим составом, а числом кинетических единиц — молекул в единице объёма или массы[1]. К таким коллигативным свойствам относятся:
- Понижение упругости растворителя над раствором,
- Повышение температуры кипения растворов (в сравнении с чистыми растворителями),
- Понижение температуры замерзания растворов (в сравнении с чистыми растворителями),
- Возникновение осмотического давления,
- Диффузия.
Законы Рауля[править | править код]
Первый закон Рауля[править | править код]
Пар, находящийся в равновесии с жидкостью, называют насыщенным. Давление такого пара над чистым растворителем (p0) называют давлением или упругостью насыщенного пара чистого растворителя.
В 1886 (1887) году Ф. М. Рауль сформулировал закон:
Давление насыщенного пара раствора, содержащего нелетучее растворенное вещество, прямо пропорционально мольной доле растворителя в данном растворе:
p = p0 · χр-ль, где
p — давление пара над раствором, Па;
p0 — давление пара над чистым растворителем;
χр-ль —— мольная доля растворителя.
Для растворов электролитов используют несколько другую форму уравнения, позволяющую добавить в неё изотонический коэффициент:
Δp = i · p0 · χв-ва, где
Δp — собственно изменение давления по сравнению с чистым растворителем;
χв-ва — мольная доля вещества в растворе.
Второй закон Рауля[править | править код]
Также Рауль экспериментально доказал, что
повышение температуры кипения раствора по сравнению с температурой кипения растворителя равно и понижение температуры замерзания раствора по сравнению с аналогичным характеризующей величиной для растворителя прямо пропорциональна моляльности раствора, то есть,
ΔTкип/зам= Kэб/кр · mв-ва, где
Kэб/кр — соответственно эбуллиоскопическая (от лат. ebullire — «кипеть» и др.-греч. σκοπέω — «наблюдаю») и криоскопическая (относится к замерзанию) константы, характерные для данного растворителя;
mв-ва — моляльность вещества в растворе.
Осмотическое давление[править | править код]
Рассмотрим ситуацию, при которой частично проницаемая мембрана (то есть, такая, через которую могут проходить лишь мелкие объекты, например, молекулы растворителя, но не крупные — например, молекулы растворённого вещества) разделяет чистый растворитель и раствор (или два раствора с разными концентрациями). Тогда молекулы растворителя находятся практически в равных физических условиях по обе стороны мембраны, однако в более насыщенном растворе некоего вещества их концентрация, разумеется, меньше, чем в более разбавленном (в котором меньше места в растворе занимают молекулы растворённого вещества). Следовательно, со стороны менее насыщенного раствора через мембрану диффундирует большее число молекул, чем с противоположной стороны. А это значит, что растворитель попросту переходит из менее насыщенного раствора в более насыщенный, разбавляя его (выравнивая концентрации обоих растворов) и создавая давление на мембрану. Процесс этот (он называется осмосом) можно прекратить, оказав определённое давление на более насыщенный раствор (например, при помощи поршня) —— это давление и называется осмотическим давлением.
Растворы с одинаковым осмотическим давлением называются изотоническими.
Определить осмотическое давление раствора можно по формуле, полученной в 1886 году Я. Х. Вант-Гоффом:
π = CMв-ва · R · T, где
CMв-ва — молярная концентрация раствора, выраженная в , а не в , как обычно;
R — универсальная газовая постоянная;
T — термодинамическая температура системы.
См. также[править | править код]
- Осмос
Примечания[править | править код]
- ↑ Д.А.Фридрихсберг. Курс коллоидной химии. — Ленинград «Химия», 1984. — С. 368.
Литература[править | править код]
- Ершов Ю.А. Общая химия.Биофизическая химия.Химия биогенных элементов. — Издание восьмое,стериотипное. — Москва: Высшая школа, 2010. — 559 с.
После изучения этой темы вы должны:
— иметь представления о следующих понятиях и явлениях:
— осмос, осмотическое давление (закон Вант-Гоффа), его роль.
— закон Рауля о давлении паров растворителя над раствором и изменении температур кипения и замерзания растворов (следствия закона Рауля).
Коллигативные свойства – это свойства, которые не зависят от природы частиц растворенного вещества, а зависят только от концентрации частиц в растворе.
Коллигативными свойствами разбавленных растворов являются:
— скорость диффузии
— осмотическое давление (Закон Вант-Гоффа)
— давление насыщенного пара растворителя над раствором (Закон Рауля)
— температура кипения раствора (1следствие из закона Рауля)
— температура кристаллизации раствора (2 следствие из закона Рауля)
Свойства неэлектролитов
Осмосом называется самопроизвольное перемещение молекул растворителя через полупроницаемую мембрану из раствора меньшей концентрации в раствор большей концентрации. В результате протекания осмоса возникает осмотическое давление раствора. Гипертоническим раствором называют тот раствор, у которого осмотическое давление больше. Гипотоническим раствором – раствор с меньшим осмотическим давлением. Изотоничные растворы – это растворы с одинаковой величиной осмотического давления.
Растительная клетка (С >) (внутриклеточный раствор)
Внешняя среда (С <) (межклеточный раствор)
Н2О Н2О
Вант-Гофф, изучая зависимость осмотического давления от внешних факторов установил, что оно не зависит от природы растворенного вещества, а зависит только от числа частиц в растворе и от температуры:
Росм = СмRT, где Росм [кПа], T [K] — абсолютная температура, R = 8,32 кДж/моль — универсальная газовая постоянная, См — молярная концентрация раствора [моль/л].
Осмотическое давление раствора, содержащего несколько веществ, равно сумме осмотических давлений, вызываемых каждым из них.
Давление насыщенного пара растворителя над раствором (Закон Рауля):
Относительное понижение давления насыщенного пара над раствором прямо пропорционально мольной доле растворенного вещества: где — давление насыщенного пара над чистым растворителем; РА-давление насыщенного пара растворителя над раствором; NB — мольная доля растворенного вещества: , где na, nb – число молей растворителя (а) и растворенного вещества (b).
Набольшее практическое значение получили I, II следствие закона Рауля.
I следствие закона Рауля: Повышение температуры кипения раствора прямо пропорционально молярной концентрации растворенного вещества: Dtкип = Kэб.Сm , где Dtкип = t кип р-ра – t кип н2o, 0С ; Kэб – эбулиоскопическая константа растворителя (Kэб н2о ); Сm- моляльная концентрация растворенного вещества, моль/1000г растворителя.
II следствие закона Рауля: Понижение температуры замерзания раствора прямо пропорционально молярной концентрации растворенного вещества: Dtзам = Kкр.Сm , где Dt = t зам.н2о – t зам р-ра, 0С; Kкр — криоскопическая константа растворителя (Ккр н2о =1,86); Сm- моляльная концентрация растворенного вещества, моль/1000г растворителя.
| Росм = См R T Dtкип = Кэб Cm Dtзам = Ккр Cm | ß | Коллигативные свойства для молекулярных растворов |
Примечание: см. приложение 7 – «Криоскопические константы некоторых растворителей», приложение 8 – «Эбулиоскопические константы некоторых растворителей».
Эти уравнения справедливы только для растворов, в которых отсутствует взаимодействие частиц, т.е. для идеальных растворов. В реальных растворах имеют место межмолекулярные взаимодействия между молекулами вещества и растворителя, которые могут приводить либо к процессам диссоциации, либо к процессам ассоциации молекул. Диссоциация молекул вещества в водном растворе характерна для сильных электролитов. В результате диссоциации число частиц увеличивается.
Доля (i) образовавшихся частиц определяется как отношение общего числа частиц к первоначальному числу молекул. Она зависит от степени диссоциации электролита и от числа частиц, на которые распадается молекула:
i = (n -1)a + 1, i – получил название изотонический коэффициент, n – число частиц (ионов), на которые распадается молекула, a – степень диссоциации (в долях).
| Росм = iСМ R Т Dt кип = i Кэб Сm Dtзам = i Ккр Сm | ß | Коллигативные свойства для растворов электролитов |
Примеры расчетов температур кипения, замерзания, осмотического давления растворов различных концентраций.
Пример 1. Вычислить температуру замерзания, кипения раствора этилового спирта с процентной концентрацией (w), равной 40 %.
Решение: Вычислим температуру замерзания раствора исходя из II следствия закона Рауля: Dtзам = Kкр.Сm, однако для решения необходимо перейти от одного вида концентрации к другому:
w [m в-ва, г 100г р-ра] ® Сm[ n молей 1000 г р-ля ]
1. Перейдем от массы вещ-ва (m) к молям (n) через пропорцию:
1 моль С2Н5ОН содержит ——- 46 г
х моль //——//——-//——-//——40 г
или по формуле х(n) = = моль/100р-ра,
где m(с2н5он) = 40г, M(с2н5он) = 46г/моль
2. Перейдем от массы раствора к массе растворителя:
m р-ля = m р-ра — m в-ва = 100 – 40 = 60г р-ля
2. Через пропорцию выразим Сm :
0,87 молей С2Н5ОН содержит в 60 г растворителя
х (Сm) -//——//——//——//——/- 1000 г
х (Сm) = = 14,5 молей/1000г р-ля
4. По формуле Dtзам = Kкр.Сm найдем Dt: Dt = 1,86.14,5 = 26,97 0C
5. Dt = tзам н2о – tзамр-ра Þ tзам р-ра = tзам н2о – Dt = 0 — 26,97 = -26,97 0C — температура замерзания 40 % раствора этилового спирта.
Вычислим температуру кипения раствора исходя из I следствия закона Рауля: Dtкип = Kэб. Сm, Сm = 14,5 моль/1000р-ля (см. выше)
Из формулы найдем Dt: Dt = 0,516 . 14,5 = 7,48 0C
Dt = tкипр-ра – tкип н2о Þ tкип р-ра = tкип н2о + Dtкип = 100 + 7,48 = 107,48 0C- температура кипения 40% раствора этилового спирта.
Пример 2. Вычислить концентрацию физиологического раствора (NaCl) изотоничного с осмотическим давлением крови равное » 800 Кпа. Степень диссоциации NaCl принять за 90%.
Решение: Для растворов электролитов Росм(NaCl ) = i·См·R·T Þ
См = (1)
Условие изотоничности означает, что Росм(NaCl ) = Росм крови = 800 кПа,
i = (n-1)·a + 1= (2 — 1) ·0,9 = 1,9
NaCl Û Na++Cl-, где n = 2, a = 0,9
Подставим найденные значения в формулу (1) См = 0,17 моль/л – концентрация хлорида натрия, которая создает осмотическое давление 800 кПа.
Коллигативные свойства растворов — это свойства растворов, обусловленные только самопроизвольным движением молекул, то есть они определяются не химическим составом, а числом кинетических единиц — молекул в единице объёма или массы[1]. К таким коллигативным свойствам относятся:
- Понижение упругости растворителя над раствором,
- Повышение температуры кипения растворов (в сравнении с чистыми растворителями),
- Понижение температуры замерзания растворов (в сравнении с чистыми растворителями),
- Возникновение осмотического давления,
- Диффузия.
Законы Рауля
Первый закон Рауля
Пар, находящийся в равновесии с жидкостью, называют насыщенным. Давление такого пара над чистым растворителем (p0) называют давлением или упругостью насыщенного пара чистого растворителя.
В 1886 (1887) году Ф. М. Рауль сформулировал закон:
Давление пара раствора, содержащего нелетучее растворенное вещество, прямо пропорционально мольной доле растворителя в данном растворе:
p = p0 · χр-ль, где
p — давление пара над раствором, Па;
p0 — давление пара над чистым растворителем;
χр-ль —— мольная доля растворителя.
Для растворов электролитов используют несколько другую форму уравнения, позволяющую добавить в неё изотонический коэффициент:
Δp = i · p0 · χв-ва, где
Δp — собственно изменение давления по сравнению с чистым растворителем;
χв-ва — мольная доля вещества в растворе.
Второй закон Рауля
Также Рауль экспериментально доказал, что
повышение температуры кипения раствора по сравнению с температурой кипения растворителя равно и понижение температуры замерзания раствора по сравнению с аналогичным характеризующей величиной для растворителя прямо пропорциональна моляльности раствора, то есть,
ΔTкип/зам= Kэб/кр · mв-ва, где
Kэб/кр — соответственно эбуллиоскопическая (от лат. ebullire — «кипеть» и др.-греч. σκοπέω — «наблюдаю») и криоскопическая (относится к замерзанию) константы, характерные для данного растворителя;
mв-ва — моляльность вещества в растворе.
Осмотическое давление
Рассмотрим ситуацию, при которой частично проницаемая мембрана (то есть, такая, через которую могут проходить лишь мелкие объекты, например, молекулы растворителя, но не крупные — например, молекулы растворённого вещества) разделяет чистый растворитель и раствор (или два раствора с разными концентрациями). Тогда молекулы растворителя находятся практически в равных физических условиях по обе стороны мембраны, однако в более насыщенном растворе некоего вещества их концентрация, разумеется, меньше, чем в более разбавленном (в котором меньше места в растворе занимают молекулы растворённого вещества). Следовательно, со стороны менее насыщенного раствора через мембрану диффундирует большее число молекул, чем с противоположной стороны. А это значит, что растворитель попросту переходит из менее насыщенного раствора в более насыщенный, разбавляя его (выравнивая концентрации обоих растворов) и создавая давление на мембрану. Процесс этот (он называется осмосом) можно прекратить, оказав определённое давление на более насыщенный раствор (например, при помощи поршня) —— это давление и называется осмотическим давлением.
Растворы с одинаковым осмотическим давлением называются изотоническими.
Определить осмотическое давление раствора можно по формуле, полученной в 1886 году Я. Х. Вант-Гоффом:
π = CMв-ва · R · T, где
CMв-ва — молярная концентрация раствора, выраженная в , а не в , как обычно;
R — универсальная газовая постоянная;
T — термодинамическая температура системы.
См. также
- Осмос
Примечания
- ↑ Д.А.Фридрихсберг. Курс коллоидной химии. — Ленинград «Химия», 1984. — С. 368.
Литература
- Ершов Ю.А. Общая химия.Биофизическая химия.Химия биогенных элементов. — Издание восьмое,стериотипное. — Москва: Высшая школа, 2010. — 559 с.
БЛОК ИНФОРМАЦИИ
Ранее
уже отмечалось, что растворы, являясь
многокомпо-нентными системами, приобретают
некоторые свойства, которыми не обладают
отдельные компоненты раствора. Для
химии большой интерес представила бы
возможность определения свойств
растворов по известным характеристикам
индивидуальных компонентов. Однако в
настоящее время такая задача не решена
и общая теория растворов не создана.
В то же время
термодинамическая теория растворов
позволяет устанавливать взаимосвязь
между отдельными характеристиками
раствора. Иными словами, можно вычислять
одни параметры раствора, если известны
другие.
Основными
независимыми переменными в теории
растворов являются концентрация,
температура и
давление.
В некоторых случаях число переменных,
необходимых для расчета остальных
параметров раствора, удается свести к
минимуму. Так, определенные свойства
разбавленного раствора нелетучего
неэлектролита можно рассчитать, зная
только концентрацию раствора и при этом
абстрагируясь от химической природы
растворенного вещества.
Свойства
растворов, которые зависят только от
концентрации компонентов, но не
зависят
от их природы, называются коллигативными.
К коллигативным
свойствам растворов относят:
1) понижение
давления насыщенного пара над раствором
по сравнению с растворителем;
2) повышение
температуры кипения и понижение
температуры замерзания (кристаллизации)
растворов по сравнению с раствори-телем;
3) осмотические
явления.
Давление насыщенного пара. Закон Рауля
Пар,
находящийся в динамическом равновесии
со своей жидкостью называется насыщенным.
Насыщенный пар характери-зуется давлением
P
(Па, атм), которое иногда называют
упругостью пара. Давление насыщенного
пара зависит от природы жидкости и от
температуры. С ростом температуры
давление насыщенного пара возрастает
(рис. 1.).

Рис. 1. Зависимость
давления насыщенного пара растворителя
от температуры.
Добавление в
растворитель растворенного вещества
(нелетучего неэлектролита) приводит к
тому, что на протяжении всего температурного
интервала давление насыщенного пара
растворителя над раствором (кривая 2)
ниже давления насыщенного пара над
чистым растворителем (кривая 1). Это
связано с уменьшением количества
свободных молекул растворителя на
поверхности жидкости.
Закон Рауля:
Относительное
понижение давления пара растворителя
над раствором нелетучего неэлектролита
равно мольной доле раство-ренного
вещества:
| (1) |
где
Р – давление
насыщенного пара растворителя над
раствором
(атм; Па;
мм. рт. ст.);
Р – давление
насыщенного пара над чистым растворителем
(атм;
Па; мм. рт. ст.);
n1 – количество
растворенного вещества (моль);
n2 – количество
растворителя (моль).
Температура,
при которой давление пара растворителя
над раствором становится равным давлению
пара над твердой фазой, называется
температурой кристаллизации
раствора (Tкр.).
Температура,
при которой давление пара растворителя
над раствором становится равным
атмосферному давлению, назы-вается
температурой кипения
раствора (Tкип.).
Из
рис. 1 видно, что температура кристаллизации
раствора (Tкр.)
несколько ниже температуры кристаллизации
чистого растворителя (T0
кр.).
Разность температур кристаллизации
растворителя и раствора Tкр.можно
рассчитать по одному из следствий из
закона Рауля:
Понижение
температуры кристаллизации раствора
по сравнению с растворителем прямо
пропорционально моляльной концентрации
раствора:
| (2) |
где
К – криоскопическая
постоянная растворителя (Ккг/моль);
b(х)
– моляльная концентрация раствора
(моль/кг).
Другое
следствие из закона Рауля позволяет
рассчитать повышение температуры
кипения раствора по сравнению с
растворителем Tкип.:
Повышение
температуры кипения раствора по сравнению
с растворителем прямо пропорционально
моляльной концентрации раствора:
| (3) |
где
Е – эбулиоскопическая
постоянная растворителя (Ккг/моль).
Значения
констант К и Е определяются исключительно
природой растворителя.
Значения
криоскопических и эбулиоскопических
констант некоторых растворителей
приведены в таблице 1.
Таблица 1.
Физико-химические характеристики
растворителей.
Растворитель | Температура | Температура | Эбулиоско-пическая | Криоско-пическая |
Вода | 100 | 0,52 | 1,86 | |
Бензол | 80,1 | 5,5 | 2,56 | 5,10 |
Этанол | 78,4 | 114,15 | 1,16 | 1,99 |
Ацетон | 56,2 | 95,35 | 1,50 | 2,40 |
Хлороформ | 61,2 | 63,5 | 4,90 | 3,90 |
Диэтиловый эфир | 34,5 | 116,2 | 2,02 | 1,79 |
Камфора | 204 | 179 | 5,95 | 39,7 |
Следствия
из закона Рауля позволяют также решить
и обратную задачу: зная величину Tкип.
(или Tкр.)
можно рассчитать молярную массу
растворенного вещества M(x):
| (4) |
| (5) |
Соседние файлы в папке часть 3
- #
- #


