Какие свойства проявляет фосфор и почему

А) Характеристика фосфора.
1. Фосфор— элемент пятой группы и третьего периода, Z = 15,
Аr(Р) = 31.
Соответственно, атом фосфора содержит в ядре 15 протонов,
16 нейтронов и 15 электронов. Строение его электронной оболочки
можно отразить с помощью следующей схемы:
![]()
Атомы фосфора проявляют как окислительные свойства (принима-
ют недостающие для завершения внешнего уровня три электрона, получая при этом степень окисления -3, например, в соединениях с менее электроотрицательными элементами— металлами, водородом и т.п.) так и восстановительные свойства (отдают 3 или 5 электронов более электроотрицательным элементам — кислороду, галогенам и т.п., приобретая при этом степени окисления +3 и +5.)
Фосфор менее сильный окислитель, чем азот, но более сильный, чем мышьяк, что связано с ростом радиусов атомов от азота к мышьяку. По этой же причине восстановительные свойства, наоборот, усиливаются.
2. Фосфор — простое вещество, типичный неметалл. Фосфору свойственно явление аллотропии. Например, существуют аллотропные модификации фосфора такие, как белый, красный и черный фосфор, которые обладают разными химическими и физическими свойствами.
3. Неметаллические свойства фосфора выражены слабее, чем у азота, но сильнее, чем у мышьяка (соседние элементы в группе).
4. Неметаллические свойства фосфора выражены сильнее, чем у
кремния, но слабее, чем у серы (соседние элементы в периоде).
5. Высший оксид фосфора имеет формулу Р2O5. Это кислотный оксид.
Он проявляет все типичные свойства кислотных оксидов. Так, например, при взаимодействии его с водой получается фосфорная кислота.
Р2O5 + 3Н2O => 2Н3РO4.
При взаимодействии его с основными оксидами и основаниями он
дает соли.
Р2O5 + 3MgO = Mg3(PO4)2; Р2O5 + 6КОН = 2К3РO4+ 3Н2O.
6. Высший гидроксид фосфора— фосфорная кислота Н3РO4, рас-
твор которой проявляет все типичные свойства кислот: взаимодействие с основаниями и основными оксидами:
Н3РO4 + 3NaOH = Na3PO4 + 3Н2O. 2Н3РO4 + 3СаО = Са,(РO4)2↓ + 3Н2O.
7. Фосфор образует летучее соединение Н3Р — фосфин.
Б) Характеристика калия.
1. Калий имеет порядковый номер 19, Z = 19 и относительную атомную массу Аr(К) = 39. Соответственно заряд ядра его атома +19 (равен числу протонов). Следовательно, число нейтронов в ядре равно 20. Так как атом электронейтрален, то число электронов, содержащихся в атоме калия, тоже равно 19. Элемент калий находится в четвертом периоде периодической системы, значит, все электроны располагаются на четырех энергетических уровнях. Таким образом, строение атома калия записывается так:
![]()
Исходя из строения атома, можно предсказать степень окисления
калия в его соединениях. Так как в химических реакциях атом калия отдает один внешний электрон, проявляя восстановительные свойства, следовательно, он приобретает степень окисления +1.
Восстановительные свойства у калия выражены сильнее, чем у на-
трия, но слабее, чем у рубидия, что связано с ростом радиусов от Na к Rb.
2. Калий— простое вещество, для него характерна металлическая
кристаллическая решетка и металлическая химическая связь, а отсюда — и все типичные для металлов свойства.
3. Металлические свойства у калия выражены сильнее, чем у на-
трия, но слабее, чем у рубидия, т.к. атом калия легче отдает электрон, чем атом натрия, но труднее, чем атом рубидия.
4. Металлические свойства у калия выражены сильнее, чем у кальция, т.к. один электрон атома калия легче оторвать, чем два электрона
атома кальция.
5. Оксид калия К2O является основным оксидом и проявляет все типичные свойства основных оксидов. Взаимодействие с кислотами и кислотными оксидами.
К2O + 2НСl = 2КСl +Н2O; К2O + SO3 = K2SO4.
6. В качестве гидроксида калию соответствует основание (щелочь) КОН, которое проявляет все характерные свойства оснований: взаимодействие с кислотами и кислотными оксидами.
KOH+HNO3 = KNO3+H2O; 2KOH+N2O5 = 2KNO3+H2O.
7. Летучего водородного соединения калий не образует, а образует гидрид калия КН.
Фосфор (греч. phos — свет + phoros — несущий) — химический элемент, принадлежащий к Vа группе и 3 периоду. Простое желтоватое вещество,
легко воспламеняющееся и светящееся.

Основное и возбужденное состояние фосфора
При возбуждении атома фосфора электроны на s-подуровне распариваются и переходят на d-подуровень.

Природные соединения
В природе фосфор встречается в виде следующих соединений:
- 3Ca3(PO4)2*CaCO3*SiO2 — фосфорит
- 3Ca3(PO4)2*Ca(F,Cl,OH)2 — апатит

Получение
В промышленности фосфор получают в ходе сплавления фосфата кальция, песка и угля.
Ca3(PO4)2 + SiO2 + C → (t) CaSiO3 + P + CO
Химические свойства
Химическая активность фосфора значительно выше, чем у азота. Активность также определяется аллотропной модификацией: наиболее активен белый
фосфор, излучающий видимый свет из-за окисления кислородом.
В жидком и газообразном состоянии до 800 °C фосфор состоит из молекул P4. Свыше 800 °C молекулы P4 распадаются до
P2.
- Реакции с неметаллами
- Реакции с металлами
- Реакция с водой
- Реакция с щелочами
- Восстановительные свойства
C неметаллами фосфор часто проявляет себя как восстановитель и окислитель. Легко окисляется кислородом.
4P + 3O2 → 2P2O3 (недостаток кислорода)
4P+ 5O2 → 2P2O5 (избыток кислорода)
Схожим образом происходит взаимодействие фосфора и хлора.
2P + 3Cl2 → 2PCl3 (недостаток хлора)
2P + 5Cl2 → 2PCl5 (избыток хлора)
P + S → P2S3
Реакции с водородом крайне затруднена. Тем не менее, в ходе разложения фосфидов металлов можно получить ядовитый газ — фосфин — боевое
отравляющее вещество.
Ca3P2 + H2O → Ca(OH)2 + PH3↑

2P + 3Ca → Ca3P2 (фосфид кальция)
При взаимодействии с водой фосфор вступает в реакцию диспропорционирования (так называются реакции, в которых одно и то же вещество
является и окислителем, и восстановителем).
P + H2O → (t) PH3 + H3PO4
При добавлении фосфора в растворы щелочей также происходит реакция диспропорционирования.
P + LiOH + H2O → LiH2PO2 + PH3↑ (LiH2PO2 — гипофосфит лития)
При поджигании спичек происходит реакция между фосфором и бертолетовой солью, которая выступает в качестве окислителя.
KClO3 + P → KCl + P2O5

Оксид фосфора V — P2O5
Кислотный оксид, пары которого имеют формулу P4O10. Твердый оксид характеризуется белым цветом.
Получение
P + O2 → P2O5
Химические свойства
- Кислотные свойства
- Дегидратационные свойства
Активно реагирует с водой с образованием фосфорной кислоты. При недостатке воды образует метафосфорную кислоту.
P2O5 + 3H2O = 2H3PO4
P2O5 + H2O = HPO3 (при недостатке воды)
Реагирует с основными оксидами и основаниями, образуя соли фосфорной кислоты. Какая именно получится соль — определяет соотношение основного
оксида/основания и кислотного оксида.
P2O5 + Na2O → Na3PO4
6KOH + P2O5 = 2K3PO4 + 3H2O (фосфат калия, избыток щелочи — соотношение 6:1)
4KOH + P2O5 = 2K2HPO4 + H2O (гидрофосфат калия, незначительный избыток кислотного оксида — соотношение 4:1)
2KOH + P2O5 = 2KH2PO4 + H2O (дигидрофосфат калия, избыток кислотного оксида — соотношение 2:1)

Обладает выраженным водоотнимающим (дегидратационным) свойством: легко извлекает воду из других соединений.
HClO4 + P2O5 → HPO3 + Cl2O7 (HPO3 — метафосфорная кислота)
HNO3 + P2O5 → HPO3 + N2O5
Фосфорные кислоты
Существует несколько кислородсодержащих фосфорных кислот:
- Ортофосфорная кислота — H3PO4 (соли — фосфаты PO43-)
- Метафосфорная кислота — HPO3 (соли — метафосфаты PO3-)
- Фосфористая — H3PO3 (соли — фосфиты PO33-)
- Фосфорноватистая — H3PO2 (соли гипофосфиты — PO23- )
Фосфорноватистая кислота способна вытеснять из солей малоактивные металлы, при этом превращаясь в ортофосфорную кислоту.
CuSO4 + H3PO2 + H2O → Cu + H2SO4 + H3PO4
Ортофосфорная кислота
В твердом виде представляет собой кристаллы белого цвета, хорошо растворимые в воде.
Получение
Фосфорную кислоту получают из фосфатов, воздействуя на них серной кислотой. Также известны способы гидролиза пентахлорида фосфора,
взаимодействия оксида фосфора V с водой.
Ca3PO4 + H2SO4 → CaSO4 + H3PO4
P2O5 + H2O → H3PO4
PCl5 + H2O → H3PO4 + HCl
Фосфорная кислота может образоваться при окислении фосфора сильной кислотой:
P + HNO3 + H2O → H3PO4 + NO

Химические свойства
- Кислотные свойства
- Реакции с солями
- Реакции с металлами
- Дегидратация
За счет кислотных свойств отлично реагирует с основными оксидами, основаниями. При различных соотношениях кислоты и основания получаются различные
соли (фосфаты, гидрофосфаты и дигидрофосфаты).
3K2O + H3PO4 = 2K3PO4 + 3H2O
3KOH + H3PO4 = K3PO4 + 3H2O
2KOH + H3PO4 = K2HPO4 + H2O
KOH + H3PO4 = KH2PO4 + H2O
Реакции идут, если выделяется газ, выпадает осадок или образуется слабый электролит (вода). Например, характерный осадок
желтого цвета — фосфат серебра — образуется в результате реакции с нитратом серебра.
AgNO3 + H3PO4 → Ag3PO4 + HNO3
В реакции с карбонатами образуется нестойкая угольная кислота, которая распадается на воду и углекислый газ.
K2CO3 + H3PO4 → K3PO4 + H2O + CO2
Металлы, стоящие в ряду напряжений до водорода, способны вытеснить водород из фосфорной кислоты.
Mg + H3PO4 → Mg3(PO4)2 + H2↑
При сильном нагревании ортофосфорная кислота теряет воду и переходит в метафосфорную кислоту.
H3PO4 → (t) HPO3 + H2O
Соли фосфорной кислоты
Соли фосфорной кислоты получаются в ходе реакции ортофосфорной кислоты и оснований.
3Ca(OH)2 + 2H3PO4 = Ca3(PO4)2 + 6H2O
Фосфаты являются хорошими удобрениями, которые повышают урожайность. Перечислим наиболее значимые:
- Фосфоритная мука — Ca3(PO4)2
- Простой суперфосфат — смесь Ca(H2PO4)2*H2O и CaSO4
- Двойной суперфосфат — Ca(H2PO4)2*H2O
- Преципитат — CaHPO4*2H2O
- Костная мука — продукт переработки костей домашних животных Ca3(PO4)2
- Аммофос — в основном состоит из моноаммонийфосфата — NH4H2PO4

© Беллевич Юрий Сергеевич 2018-2020
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение
(в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов
без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования,
обратитесь, пожалуйста, к Беллевичу Юрию.
Ключевые слова конспекта: свойства простых веществ, фосфор, строение и физические свойства, химические свойства, производство и применение фосфора.
Фосфор – элемент группы VA. Его важнейшие параметры приведены в таблице.
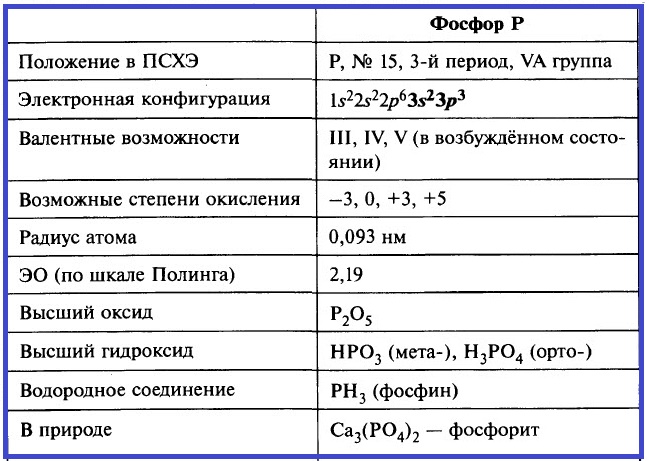
Таблица. Важнейшие параметры элемента фосфор.
На валентном слое атома фосфора, в отличие от азота, есть вакантные 3d-орбитали. В отличие от азота, фосфор может быть пятивалентным. В этом случае атомы фосфора находятся в возбуждённом состоянии:

СТРОЕНИЕ И ФИЗИЧЕСКИЕ СВОЙСТВА ФОСФОРА
Элемент фосфор образует несколько простых веществ, среди которых наиболее известны белый, красный и чёрный фоcфоp.
Белый фосфор состоит из тетраэдрических молекул Р4. В молекуле все связи одинарные ковалентные неполярные. С Р4 связи Р – Р легко разрываются. Этим объясняется высокая химическая активность белого фосфора и его склонность переходить (при хранении или при нагревании) в более стабильные полимерные модификации.
При обычных условиях это твёрдое белое вещество, мягкое как воск (легко режется ножом), летучее при слабом нагревании, легкоплавкое (t°пл = 44 °С), практически нерастворимое в воде (его хранят под слоем воды), хорошо растворимое в неполярных растворителях (например, в сероуглероде CS2). Уже при обычных условиях легко испаряется и в газообразном состоянии окисляется кислородом воздуха, освобождающаяся в результате окисления энергия выделяется в виде света, что и является причиной свечения белого фосфора на воздухе.
Красный фосфор образован полимерными молекулами Рn разной длины, состоящими из пирамидально связанных атомов. Название «красный фoсфoр» используют для описания нескольких различных модификаций фосфора красного цвета.
Красный фocфор – это твёрдое аморфное вещество красного цвета (от тёмно-коричневого до красного и фиолетового), возгоняется при нагревании. При конденсации паров образуется белый фосфop. Красный фoсфoр нерастворим ни в воде, ни в сероуглероде, ни в других растворителях.
Чёрный фосфор представляет собой вещество немолекулярного строения, кристаллическая решётка атомно–слоистая, с характерным для фосфора пирамидальным расположением связей. Чёрный фосфор твёрдый, по внешнему виду похож на графит, проводит электрический ток, имеет высокую t°пл (587 °С).
ХИМИЧЕСКИЕ СВОЙСТВА ФОСФОРА
Фосфор – более активное вещество, чем азот. Фосфору присуща окислительно-восстановительная двойственность. По отношению к металлам фосфор выступает в роли окислителя, образуя фосфиды:
По отношению к большинству неметаллов фосфop выступает в роли восстановителя. При недостатке окислителя обычно образуются соединения фосфора(III), при избытке – соединения фосфора(V), например, РCl3 и РCl5.
Фосфор сгорает на воздухе и в кислороде. Белый фосфор самовоспламеняется в атмосфере кислорода. На воздухе белый фосфор воспламеняется при 50 °С, красный – при температуре выше 250 °С, чёрный – при температуре выше 400 °С. При этом образуются оксиды фосфора. В избытке кислорода образуется оксид фосфора (V):![]()
При нагревании выше 100 °С фосфор бурно взаимодействует с серой с образованием смеси сульфидов (P2S5, P2S3):![]()
Красный и белый фocфор самовозгораются в атмосфере фтора и хлора:![]()
С водородом и азотом фосфор практически не взаимодействует.
Фосфор восстанавливает азотную и серную концентрированные кислоты, хлораты и некоторые другие окислители. Так, например, каждый раз, зажигая спичку, мы проводим реакцию между бертолетовой солью, которая входит в состав спичечной головки, и красным фосфором, нанесённым на спичечный коробок:
ПОЛУЧЕНИЕ И ПРИМЕНЕНИЕ ФОСФОРА
Сырьём для получения фосфора являются фосфориты, основной компонент которых – ортофосфат кальция. Фосфорит измельчают, смешивают с песком и углём и прокаливают в электропечах без доступа воздуха. Происходит восстановление фосфора:![]()
Основная область использования фосфора – производство спичек. Кроме того, фocфор применяется в металлургии для синтеза фосфорорганических соединений, к числу которых относятся очень ядовитые средства для борьбы с вредителями–насекомыми (инсектициды). Фoсфор используется для получения некоторых полупроводников (фосфидов галлия GaP и индия InP). Фоcфoр также используется для получения оксида фосфора (V), который является сильным водоотнимающим реагентом.
Вся информация о Фосфоре в одной таблице

Всё о фосфоре кратко в одной таблице
Конспект урока «Свойства простых веществ: Фосфор».
Следующая тема: «».

Фосфор (лат. Phosphorus) P — химический элемент V группы периодической системы Менделеева атомный номер 15, атомная масса 30,973762(4). Рассмотрим строение атома фосфора. На наружном энергетическом уровне атома фосфора находятся пять электронов. Графически это выглядит так:
1s22s22p63s23p33d

В 1699 г. гамбургский алхимик X.Бранд в поисках «философского камня», якобы способного превратить неблагородные металлы в золото, при выпаривании мочи с углём и песком выделил белое воскообразное вещество, способное светиться.
Название «фосфор» происходит от греч. «phos» — свет и «phoros» — несущий. В России термин «фосфор» введён в 1746 г. М.В. Ломоносовым.
К основным соединениям фосфора относят оксиды, кислоты и их соли (фосфаты, дигидрофосфаты, гидрофосфаты, фосфиды, фосфиты).
Очень много веществ, содержащих фосфор, содержатся в удобрениях. Такие удобрения называют фосфорными.
Фосфор в природе
Фосфор относится к числу распространенных элементов. Общее содержание в земной коре составляет около 0,08%. Вследствие лёгкой окисляемости фосфор в природе встречается только в виде соединений. Главными минералами фосфора являются фосфориты и апатиты, из последних наиболее распространён фторапатит 3Ca3(PO4)2 * CaF2. Фосфориты широко распространены на Урале, в Поволжье, Сибири, Казахстане, Эстонии, Беларуси. Самые большие залежи апатитов находятся на Кольском полуострове.
Фосфор — необходимый элемент живых организмов. Он присутствует в костях, мышцах, в мозговой ткани и нервах. Из фосфора построены молекулы АТФ — аденозинтрифосфорной кислоты (АТФ — собиратель и носитель энергии). В организме взрослого человека содержится в среднем около 4,5 кг фосфора, в основном в соединении с кальцием.
Фосфор содержится также в растениях.
Природный фосфор состоит лишь из одного стабильного изотопа 31Р. В наши дни известно шесть радиоактивных изотопов фосфора.
Физические свойства
Фосфор имеет несколько аллотропных модификаций — белый, красный, чёрный, коричневый, фиолетовый фосфор и др. Первые три из названных наиболее изучены.
Белый фосфор — бесцветное, с желтоватым оттенком кристаллическое вещество, светящееся в темноте. Его плотность 1,83 г/см3. Не растворяется в воде, хорошо растворяется в сероуглероде. Имеет характерный чесночный запах. Температура плавления 44°С, температура самовоспламенения 40°С. Чтобы защитить белый фосфор от окисления, его хранят под водой в темноте (на свету идёт превращение в красный фосфор). На холоде белый фосфор хрупок, при температурах выше 15°С становится мягким и режется ножом.
Молекулы белого фосфора имеют кристаллическую решётку, в узлах которой находятся молекулы Р4, имеющие форму тетраэдра.
Каждый атом фосфора связан тремя ?-связями с другими тремя атомами.
Белый фосфор ядовит и даёт труднозаживающие ожоги.
Красный фосфор -порошкообразное вещество тёмно-красного цвета без запаха, в воде и сероуглероде не растворяется, не светится. Температура воспламенения 260°С, плотность 2,3 г/см3. Красный фосфор представляет собой смесь нескольких аллотропных модификаций, отличающихся цветом (от алого до фиолетового). Свойства красного фосфора зависят от условий его получения. Не ядовит.
Чёрный фосфор по внешнему виду похож на графит, жирный на ощупь, обладает полупроводниковыми свойствами. Плотность 2,7 г/см3.
Красный и чёрный фосфоры имеют атомную кристаллическую решётку.
Химические свойства
Фосфор — неметалл. В соединениях он обычно проявляет степень окисления +5, реже — +3 и -3 (только в фосфидах).
Реакции с белым фосфором идут легче, чем с красным.
I. Взаимодействие с простыми веществами.
1. Взаимодействие с галогенами:
2P + 3Cl2 = 2PCl3 (хлорид фосфора (III)),
PCl3 + Cl2 = PCl5 (хлорид фосфора (V)).
2. Взаимодействие с нематаллами:
2P + 3S = P2S3 (сульфид фосфора (III).
3. Взаимодействие с металлами:
2P + 3Ca = Ca3P2 (фосфид кальция).
4. Взаимодействие с кислородом:
4P + 5O2 = 2P2O5 (оксид фосфора (V), фосфорный ангидрид).
II. Взаимодействие со сложными веществами.
3P + 5HNO3 + 2H2O = 3H3PO4 + 5NO^.
Получение
Фосфор получают из измельченных фосфоритов и апатитов, последние смешиваются с углем и песком и прокаливаются в печах при 1500°С:
2Ca3(PO4)2 + 10C + 6SiO2 6CaSiO3 + P4^ + 10CO^.
Фосфор выделяется в виде паров, которые конденсируются в приёмнике под водой, при этом образуется белый фосфор.
При нагревании до 250-300°С без доступа воздуха белый фосфор превращается в красный.
Чёрный фосфор получается при длительном нагревании белого фосфора при очень большом давлении (200°С и 1200 МПа).
Применение
Красный фосфор применяется при изготовлении спичек (см. рисунок). Он входит в состав смеси, наносимой на боковую поверхность спичечного коробка. Основным компонентом состава головки спички является бертолетова соль KClO3. От трения головки спички о намазку коробка частицы фосфора на воздухе воспламеняются. В результате реакции окисления фосфора выделяется тепло, приводящее к разложению бертолетовой соли.
KClO3 KCl + .

Образующийся кислород способствует воспламенению головки спички.
Фосфор используют в металлургии. Он применяется для получения проводников и входит в состав некоторых металлических материалов, например оловянных бронз.
Также фосфор используют при производстве фосфорной кислоты и ядохимикатов (дихлофос, хлорофос и др.).
Белый фосфор используют для создания дымовых завес, так как при его горении образуется белый дым.
