Какие свойства характеризуют и молекулу и вещество
Химия – наука о веществах, их свойствах, превращениях и явлениях, сопровождающих эти превращения.
Вещества – это то, из чего состоят предметы (физические тела) окружающего мира. Вещества, существующие в природе, постоянно претерпевают различные изменения.
Явления – различные изменения, которые происходят с веществами.
Физические явления – явления, не сопровождающиеся превращениями одних веществ, в другие (обычно изменяется агрегатное состояние веществ или их форма).
Химические явления – явления, в результате которых из данных веществ образуются другие.
Иначе химические явления называют химическими реакциями.
Каждое вещество обладает строго определёнными свойствами.
Свойства веществ – признаки, позволяющие отличить одни вещества от других, или установить сходство между ними.
Физические свойства:
m — масса, V — объём, ρ — плотность.
Масса может быть выражена в граммах, объем в миллилитрах (если это жидкость) или литрах (если это газ).
1 мл = 1 см3, 1 л = 1 дм3, 1000 л = 1 м3
Поэтому плотность измеряют в г/мл, г/см3 (если это жидкость), или в г/л, г/дм3 (если это газ).
Если принять V = 1, то плотность — это масса единичного объёма вещества.
Химические свойства — это те химические реакции, в которые вступает данное вещество.
Так же можно сказать, что химические свойства — это те химические реакции, которые характеризуют группу веществ (класс веществ). Например, мы будем в дальнейшем изучать свойства воды, свойства класса оксидов, свойства класса алканов и т.д.
ООсновы атомно – молекулярного учения
Идея о том, что вещества состоят из мельчайших частиц возникла в Древней Греции в философских учениях Левкиппа и его ученика Демокрита. Эти частицы они назвали атомами (неделимые).
Существование атомов было доказано эмпирическим путём в конце 16 – начале 17 века Джоном Дальтоном и М. В. Ломоносовым. Ими же были заложены основы атомно – молекулярного учения.
В настоящее время, в связи с открытием делимости атома и появлением теории химической связи, основные положения атомно – молекулярного учения существенно изменились. Его суть можно свести к ряду важных положений, которые необходимо запомнить.
Все вещества, существующие в природе, представляют собой совокупность очень большого числа частиц (атомов, молекул или ионов). В зависимости от типа частиц все вещества условно подразделяют на две группы: вещества молекулярного строения и вещества немолекулярного строения (атомного или ионного).
Вещества молекулярного строения – вещества, основной структурной единицей которых является молекула.
Вещества немолекулярного строения – вещества, основными структурными единицами которых являются атомы или ионы.
Частицы, из которых состоит данное вещество, взаимодействуют между собой посредством электромагнитных (кулоновских) сил и находятся в постоянном движении. Движение частиц ограничено силами взаимодействия между ними.Каждое вещество, в зависимости от условий (температуры, давления) может находиться в определённом агрегатном состоянии.
В твёрдом агрегатном состоянии вещества, составляющие его частицы находятся относительно упорядоченно (кристаллическое состояние), их кинетическая энергия (энергия движения) существенно меньше чем потенциальная (энергия покоя). В газообразном состоянии, частицы свободно движутся в предоставленном им объёме и их кинетическая энергия существенно выше чем потенциальная.
В жидкости же потенциальная энергия частиц примерно равна их кинетической энергии. Это связано с тем, что часть частиц жидкости находится относительно упорядоченно в составе так называемых кластеров(англ. cluster— скопление). Другие же частицы свободно перемещаются по объёму жидкости. Чем ниже температура жидкости, тем больше в ней кластеров и наоборот.
Рис. Кластеры воды, где число молекул 20-220
Следует отметить, что существуют еще два дополнительные «состояния». Это жидкокристаллическое состояние и состояние плазмы.
Цитоплазматическая мембрана клетки — типичный пример жидкого кристалла. Молекулы фосфолипидов в биологической мембране относительно упорядоченно распределяются в двух слоях, но при этом могут в пределах слоя свободно перемещаться, а также «перескакивать» из одного слоя в другой.
Жидкие кристаллы имеют широкое применение в технике (напр., ЖК-мониторы компьютеров).
Плазма (от греч. πλάσμα «вылепленное», «оформленное») — ионизованный газ.
Плазма в своём составе содержит свободные электроны, катионы (положительно заряженные ионы) и анионы (отрицательно заряженные ионы).
Так как плазма содержит заряженные частицы, то она проводит электрический ток и на неё можно воздействовать внешним магнитным полем. Различают низкотемпературную и высокотемпературную плазму.
Изучает свойства плазмы наука физика.
Вещество из одного агрегатного состояния может переходить в другие агрегатные состояния при изменении внешних условий — температуры (T) и давления (P). Такие переходы принято называть фазовыми переходами.
Так, при повышении температуры, твердое вещество превращается в жидкость, а жидкость при ещё большей температуре превращается в газ. Дальнейшее повышение температуры переводит газ в плазму. При таких переходах вещество в другие вещества не превращается. Напомним, что такие явления мы называем физическими. Поэтому фазовые переходы — это физические явления.
При понижении температуры происходят обратные фазовые переходы — газ превращается в жидкость, а жидкость переходит в твердое состояние.
Фазовые переходы имеют названия.
Твердое —> Жидкое (плавление, обратный переход — кристаллизация)
Жидкое —> Газообразное (испарение, обратный переход — конденсация)
Газообразное —> Плазма (ионизация, обратный переход — деионизация)
Твердое —> Газообразное (сублимация или возгонка, обратный переход — десублимация)
Вещество – совокупность большого числа частиц, находящаяся в определённом агрегатном состоянии в зависимости от условий (температуры и давления).
Поэтому, например, такая фраза как: «Вода — жидкое вещество», является некорректной. Если мы говорим об агрегатном состоянии вещества, то следует обязательно уточнить условия в которых находится вещество — температуру и давление. Такая фраза как: «При нормальном атмосферном давлении и комнатной температуре, вода — жидкое по агрегатному состоянию вещество», является правильной.
С точки зрения физики, что более точно, вещество — это форма материи, состоящая из частиц, обладающих массой покоя. Существуют частицы, не обладающие массой покоя, например, фотоны. Материя, состоящая из частиц, не обладающих массой покоя называется поле.
Протоны, нейтроны, электроны — это частицы, обладающие массой покоя, следовательно это частицы вещества. Но химия не изучает вещество, состоящее, к примеру, из электронов (электронный газ), или вещество, состоящее из нейтронов (нейтронный газ). Это удел физики.
Химия изучает вещества, состоящие из атомов, молекул или ионов.
Ввиду этого вещество условно можно подразделить на физическое (электронный газ в проводнике, нейтронный газ и т.д.) и химическое (состоящее из атомов, молекул, ионов, свободных радикалов).
Одним из основополагающих понятий современной науки является понятие молекулы. Его введение европейскими учеными в 1860 г. дало толчок к развитию не только химии и физики, но и других естественных наук.
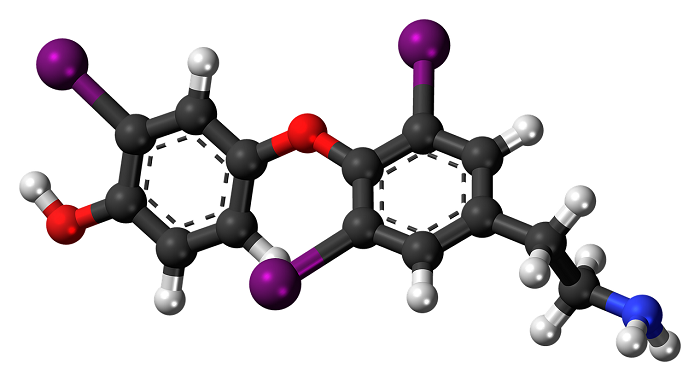
Молекулой, в наиболее общем определении, называется частица, образованная из нескольких (двух или более) атомов, объединенных между собой ковалентными связями. Она не имеет электрического заряда, все электроны в её составе имеют пару.
Молекулы, несущие заряд, называются ионами, неспаренные электроны – радикалами. Качественный и количественный состав их стабилен. Количество ядер атомов, электронов и их взаимное расположение позволяют отличать молекулы разных веществ друг от друга.
Что такое молекула в физике
В физике этим понятием оперируют при изучении свойств разных сред (газы, жидкости) и твердых тел.

Также их свойствами объясняются явления диффузии, теплопроводности и вязкость веществ.
Что такое молекула в химии
Учение о молекулах для химической науки является одним из самых главных. Именно химические исследования дали важнейшие сведения о составе и свойствах этой мельчайшей единицы вещества.
При прохождении химического превращения молекулы обмениваются атомами, распадаются. Поэтому знания о строении и состоянии этих частиц лежат в основе изучения химии веществ и их превращений.
На основании знаний о проходящей химической реакции можно предсказать строение молекул веществ, в ней участвующих. Противоположное заключение тоже будет верным: на основании сведений о строении молекулы вещества реально предсказать его поведение во время химической реакции.
Строение молекулы
Понятие о строении включает геометрическую структуру и распределение электронной плотности.
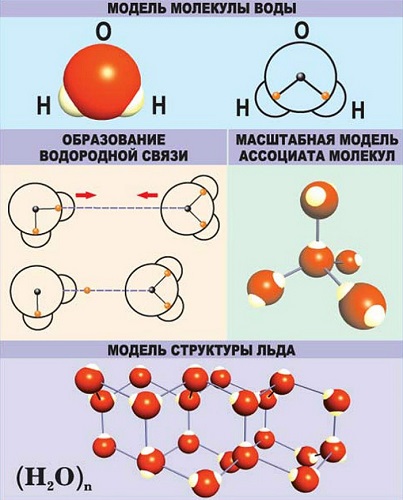
В качестве примера рассмотрим строение наименьшей частицы воды.
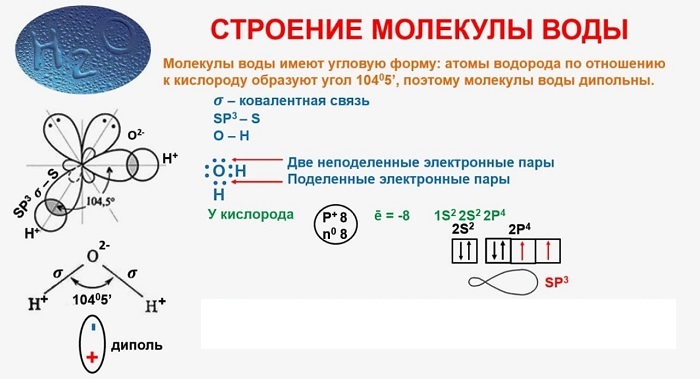
Существует несколько способов взаимодействия атомов. Основным способом являются химические связи, благодаря им поддерживается стабильное существование молекул. Прочие (неосновные) взаимодействия происходят между теми атомами, которые не связаны непосредственно.
Виды химической связи:
Металлическая — ядра атомов металлов, расположенные в узлах кристаллических решёток, объединены общим облаком электронов.
Водородная — основана на способности атома водорода образовывать дополнительную связь при смещении от него электронной плотности.
Ионная — имеет электрическую природу. Сильно поляризована. Возникает при притяжении ионов, несущих противоположный заряд.
Ковалентная — может быть полярной и неполярной. Образуется за счет пары электронов, совместно принадлежащей двум атомам. Отличается наибольшей устойчивостью и энергетической емкостью.
Связи характеризуются следующими показателями:
длина – степень удаления друг от друга ядер атомов, образовавших связь;
энергия – сила, прилагаемая для разрушения связи;
полярность – смещение электронного облака к одному из атомов;
порядок или кратность – количество пар электронов, образовавших связь.
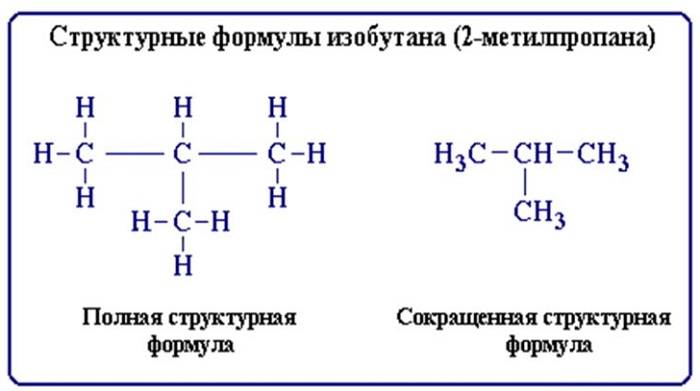
Строение молекул условно отражается структурными формулами. Основные взаимодействия атомов, при составлении таких формул, отображается черточками. В таких формулах связи образуют неразрывную цепь и иллюстрируют валентности образовавших их элементов (атомов).
Структурные формулы также отражают то, как выглядит молекула (линейная, циклическая, наличие радикалов и т. д.).
Строение частицы вещества активно изучается. Для этого используют различные экспериментальные и теоретические методы. К экспериментальным относят рентгеновский структурный анализ, спектроскопия, массспектрометрия и др. К теоретическим — расчётные методы квантовой химии.
Масса (размер) молекулы
В зависимости о количества ядер атомов, входящих в их состав, можно выделить молекулы двухатомные, трехатомные и т. д.

В том случае, если количество атомов велико, молекула носит название макромолекулы.
Путем сложения масс атомов, входящих в состав частицы, можно определить молекулярную массу. В зависимости от её величины, все вещества делят на высоко- и низкомолекулярные.
Свойства молекулы

Современная наука выделяет следующие свойства молекул:
Электрические — этими свойствами определяется то, как ведет себя вещество в электрическом поле. Атомы, входящие в состав молекулы, состоят, в свою очередь, из положительно заряженного ядра и электронов, несущих отрицательный заряд. Эти заряды внутри самой молекулы располагаются неравномерно, в связи с этим возникает так называемый дипольный момент и смещение электронной плотности в сторону одного из атомов.
Оптические — дают характеристику того, как ведет себя вещество в поле световой волны. К оптическим свойствам относят способность поляризовать свет, преломлять его и рассеивать.
Магнитные — объясняются распределением электронов в атомах.
Различают вещества:
диамагнитные — парных электронов нет;
парамагнитные — имеются непарные электроны.
Знания о свойствах и строении молекул являются основополагающими для развития теоретических и прикладных наук и играют важную роль в жизни человека.
Все тела, которые нас окружают, состоят из атомов. Атомы, в свою очередь, собираются в молекулу. Именно благодаря различию в молекулярном строении, можно говорить об отличных друг от друга веществах, опираясь на их свойства и параметры. Молекулы и атомы всегда находятся в состоянии динамики. Двигаясь, они все же не разбегаются в разные стороны, а удерживаются в определенной структуре, чем мы обязаны существованию такого огромного разнообразия веществ во всем окружающем нас мире. Что же это за частички и каковы их свойства?
Общие понятия
Если отталкиваться от теории квантовой механики, то молекула состоит не из атомов, а их ядер и электронов, которые постоянно взаимодействуют между собой.
Для некоторых веществ молекула – это наименьшая частица, имеющая состав и химические свойства самой субстанции. Так, свойства молекул с точки зрения химии определяются ее химическим строением и составом. Но только для веществ с молекулярным строением работает правило: химические свойства веществ и молекул одинаковы. Для некоторых полимеров, например, этилена и полиэтилена, состав не соответствует молекулярному.
Известно, что свойства молекул определяются не только количеством атомов, их типом, но и конфигурацией, порядком соединения. Молекула – это сложная архитектурная постройка, где каждый элемент стоит на своем месте и имеет своих конкретных соседей. Атомная структура может быть более или менее жесткой. Каждый атом совершает колебание относительно своего равновесного положения.

Конфигурация и параметры
Бывает, что некоторые части молекулы совершают вращение по отношению к другим частям. Так, в процессе теплового движения свободная молекула обретает причудливые формы (конфигурации).
В основном свойства молекул определяются связью (ее типом) между атомами и архитектурой самой молекулы (структурой, формой). Таким образом, в первую очередь общая химическая теория рассматривает химические связи и основывается на свойствах атомов.
При сильно выраженной полярности свойства молекул трудно описать двух- или трехконстантными корреляциями, которые отлично подходят для неполярных молекул. Поэтому был введен дополнительный параметр с дипольным моментом. Но такой способ не всегда успешен, так как полярные молекулы имеют индивидуальные характеристики. Также были предложены параметры для учета квантовых эффектов, имеющие важность при низких температурах.
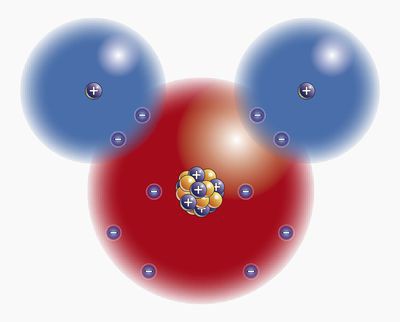
Что мы знаем о молекуле самого распространенного вещества на Земле?
Из всех веществ на нашей планете, самое распространенное – это вода. Она, в прямом смысле, обеспечивает жизнь всему сущему на Земле. Только вирусы могут без нее обойтись, остальные живые структуры в своем составе по большей части имеют воду. Какие свойства молекулы воды, характерные только ей, используются в хозяйственной жизни человека и живой природе Земли?
Ведь это поистине уникальная субстанция! Набором свойств, присущих воде, не может похвастаться больше ни одно вещество.
Вода — это основной растворитель в природе. Все реакции, протекающие в живых организмах, так или иначе происходят в водной среде. То есть вещества вступают в реакции, находясь в растворенном состоянии.
Вода обладает отличной теплоемкостью, но низкой теплопроводностью. Благодаря таким свойствам мы можем использовать ее в качестве транспортировки тепла. Этот принцип входит в механизм охлаждения большого числа организмов. В атомной энергетике свойства молекулы воды послужили поводом для использования этого вещества в качестве теплоносителя. Помимо возможности быть реактивной средой для других веществ, вода сама может вступать в реакции: фотолиз, гидратацию и другие.

Природная чистая вода – это жидкость, не имеющая запаха, цвета и вкуса. Но на толщине слоя, большем чем 2 метра, цвет становится голубоватым.
Вся молекула воды – это диполь (два разноименных полюса). Именно дипольная структура в основном определяет необычные свойства этого вещества. Молекула воды является диамагнетиком.
Еще одним интересным свойством обладает талая вода: ее молекула приобретает строение золотой пропорции, а структура вещества – пропорции золотого сечения. Многие свойства, которыми обладает молекула воды, установлены с помощью анализа поглощения и испускания полосатых спектров в газовой фазе.
Естествознание и молекулярные свойства
Все вещества, кроме химических, имеют физические свойства молекул, входящих в их структуру.
В физической науке понятие молекул используют для объяснения свойств твердых тел, жидкостей и газов. Способность всех веществ к диффузии, их вязкость, теплопроводность и другие свойства определяются подвижностью молекул. Когда французский ученый-физик Жан Перрен изучал броуновское движение, он экспериментально доказал существование молекул. Все живые организмы существуют благодаря тонко сбалансированному внутреннему взаимодействию в структуре. Все химические и физические свойства веществ имеют фундаментальное значение для естествознания. Развитие физики, химии, биологии и молекулярной физики послужило возникновению такой науки, как молекулярная биология, исследующая основные явления в жизни.
Используя статистическую термодинамику, физические свойства молекул, которые определяют методами молекулярной спектроскопии, в физической химии определяют термодинамические свойства веществ, необходимые для расчета химических равновесий и скоростей его установления.

Чем отличаются свойства атомов и молекул между собой?
Прежде всего, атомы не встречаются в свободном состоянии.
У молекул оптические спектры более богаты. Это связано с меньшей симметрией системы и с появлением возможности новых вращений и колебаний ядер. У молекулы суммарная энергия складывается из трех энергий, отличных по порядку величин составляющих:
- электронной оболочки (оптическое или ультрафиолетовое излучение);
- колебания ядер (инфракрасная часть спектра);
- вращения молекулы в целом (радиочастотный диапазон).
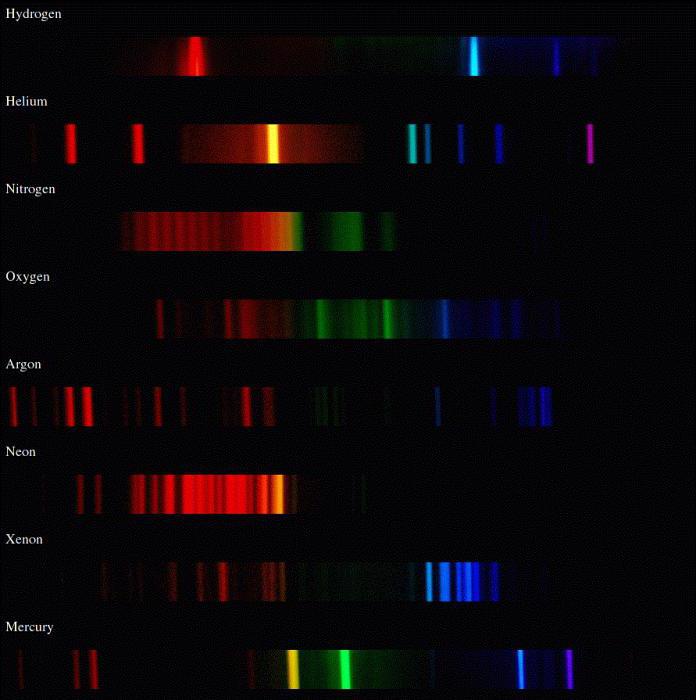
Атомы излучают характерные линейчатые спектры, а молекулы – полосатые, состоящие из множества близко расположенных линий.
Спектральный анализ
Оптические, электрические, магнитные и другие свойства молекулы определяются еще и связью с волновыми функциями. Данные о состояниях молекул и вероятном переходе между ними показывают молекулярные спектры.
Переходы (электронные) в молекулах показывают химические связи и структуру их электронных оболочек. Спектры, имеющие большее количество связей, имеют длинноволновые полосы поглощения, попадающие в видимую область. Если вещество построено из таких молекул, оно имеет характерную окраску. Это все органические красители.
Свойства молекул одной и той же субстанции являются одинаковыми во всех агрегатных состояниях. Это значит, что у одних и тех же веществ свойства молекул жидких, газообразных субстанций не отличаются от свойств твердого. Молекула одного вещества всегда имеет одинаковую структуру, независимо от агрегатного состояния самого вещества.
Электрические характеристики
То, как вещество ведет себя в электрическом поле, определяется электрическими характеристиками молекул: поляризуемостью и постоянным дипольным моментом.
Дипольный момент – это электрическая асимметрия молекулы. У молекул, которые имеют центр симметрии, как H2, нет постоянного дипольного момента. Способность электронной оболочки молекулы перемещаться под воздействием электрического поля, в результате которого в ней образуется наведенный дипольный момент, – это поляризуемость. Чтобы найти значение поляризуемости и дипольного момента, необходимо измерить диэлектрическую проницаемость.
Поведение в переменном электрическом поле световой волны характеризуют оптические свойства вещества, которые определяются поляризуемостью молекулы этой субстанции. Непосредственно с поляризуемостью связаны: рассеяние, преломление, оптическая активность и другие явления молекулярной оптики.
Часто можно услышать вопрос: «От чего, кроме молекул, зависят свойства вещества?» Ответ на него достаточно прост.
Свойства веществ, кроме изометрии и кристаллической структуры, определяются температурой окружающей среды, самой субстанции, давлением, наличием примесей.

Химия молекул
До формирования такой науки, как квантовая механика, природа химических связей в молекулах была нераскрытой тайной. Классическая физика объяснить направленность и насыщаемость валентных связей не могла. После создания базовых теоретических сведений о химической связи (1927 г.) на примере простейшей молекулы Н2, теория и методы расчёта стали постепенно совершенствоваться. К примеру, на основе широкого применения метода молекулярных орбиталей, квантовой химии, стало возможным вычислять межатомные расстояния, энергию молекул и химических связей, распределение электронной плотности и других данных, которые вполне совпадали с экспериментальными.
Вещества с одинаковым составом, но разным химическим строением и разными свойствами, называются структурными изомерами. У них разные структурные формулы, но одинаковые молекулярные.
Известны различные типы структурной изомерии. Различия заключаются в строении углеродного скелета, положении функциональной группы или положении кратной связи. Кроме того, еще существуют пространственные изомеры, у которых свойства молекулы вещества характеризуются одинаковым составом и химическим строением. Поэтому и структурные, и молекулярные формулы у них одинаковые. Отличия заключаются в пространственной форме молекулы. Для изображения разных пространственных изомеров используют специальные формулы.
Есть соединения, которые называются гомологами. Они похожи по строению и свойствам, но отличаются по составу на одну или несколько групп СН2. Все вещества, похожие по строению и свойствам, объединены в гомологические ряды. Изучив свойства одного гомолога, можно рассуждать о любом другом из них. Совокупность гомологов – это гомологический ряд.
При преобразованиях структур вещества химические свойства молекул резко меняются. Примером служат даже простейшие соединения: метан, соединяясь даже с одним атомом кислорода, становится ядовитой жидкостью с названием метанол (метиловый спирт – СН3ОН). Соответственно, его химическая комплементарность и действие на живые организмы становятся другими. Аналогичные, но более сложные изменения, происходят при модификации структур биомолекул.
Химические молекулярные свойства сильно зависят от строения и свойств молекул: от энергетических связей в ней и геометрии самой молекулы. Особенно это работает в биологически активных соединениях. Какая конкурирующая реакция окажется преобладающей, часто определяется только пространственными факторами, зависящими, в свою очередь, от исходных молекул (их конфигурации). Одна молекула, имеющая «неудобную» конфигурацию, вообще не вступит в реакцию, а другая, с таким же химическим составом, но другой геометрией, может среагировать на реакцию мгновенно.
Большое число биологических процессов, наблюдающихся при росте и размножении, связано с геометрическими соотношениями между продуктами реакции и исходными веществами. К сведению: действие немалого количества новых лекарств основывается на аналогичном строении молекул какого-либо соединения, вредного с биологической точки зрения для человеческого организма. Лекарство занимает место вредоносной молекулы и затрудняет ее действие.
С помощью химических формул выражают состав и свойства молекул разных веществ. На основании молекулярной массы, химического анализа устанавливается атомное соотношение и составляется эмпирическая формула.
Геометрия
Определение геометрической структуры молекулы производится с учетом равновесного расположения атомных ядер. От расстояния между ядрами атомов зависит энергия взаимодействия атомов. При очень больших расстояниях эта энергия нулевая. При сближении атомов начинает формироваться химическая связь. Тогда атомы сильно притягиваются друг к другу.
Если наблюдается слабое притяжение, то образование химической связи при этом не обязательно. Если атомы начинают сближаться на более близкие расстояния, между ядрами начинают действовать электростатические силы отталкивания. Препятствием для сильного сближения атомов является несовместимость их внутренних электронных оболочек.
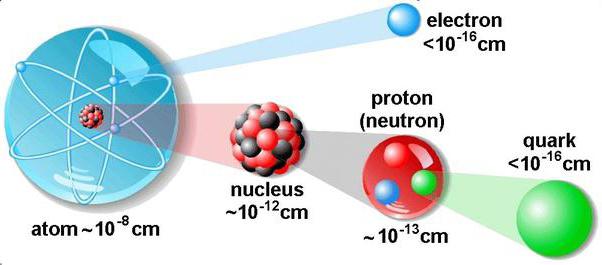
Размеры
Невооруженным глазом увидеть молекулы невозможно. Они так малы, что даже микроскоп с 1000-кратным увеличением нам не поможет их разглядеть. Биологи наблюдают бактерии размером 0,001 мм. Но молекулы в сотни и тысячи раз меньше их.
Сегодня строение молекул некой субстанции определяют дифракционными методами: дифракцией нейтронов, рентгеноструктурным анализом. Также существует колебательная спектроскопия и электронный парамагнитный метод. Выбор метода зависит от типа вещества и его состояния.
Размер молекулы — это условная величина, если учитывать электронную оболочку. Дело в расстояниях электронов от атомных ядер. Чем они больше, тем вероятность найти электроны молекулы меньше. На практике размер молекул можно определить, учитывая равновесное расстояние. Это тот промежуток, на который сами молекулы могут сблизиться при плотной упаковке в молекулярном кристалле и в жидкости.
Большие расстояния располагают молекулы к притяжению, а малые, наоборот, к отталкиванию. Поэтому рентгеноструктурный анализ молекулярных кристаллов помогает найти размеры молекулы. Используя коэффициент диффузии, теплопроводности и вязкости газов, а также плотности вещества в конденсированном состоянии, можно определить порядок величины молекулярных размеров.
