Какие простые и сложные вещества содержатся в воздухе укажите

Простые вещества: молекулы состоят из атомов одного вида (атомов одного элемента).
Пример: H2, O2,Cl2, P4, Na, Cu, Au.
Сложные вещества (или химические соединения): молекулы состоят из атомов разного вида (атомов различных химических элементов).
Пример: H2O, NH3, OF2, H2SO4, MgCl2, K2SO4.
Аллотропия — способность одного химического элемента образовывать несколько простых веществ, различающихся по строению и свойствам.
Пример:
- С — алмаз, графит, карбин, фуллерен.
- O — кислород, озон.
- S — ромбическая, моноклинная, пластическая.
- P — белый, красный, чёрный.
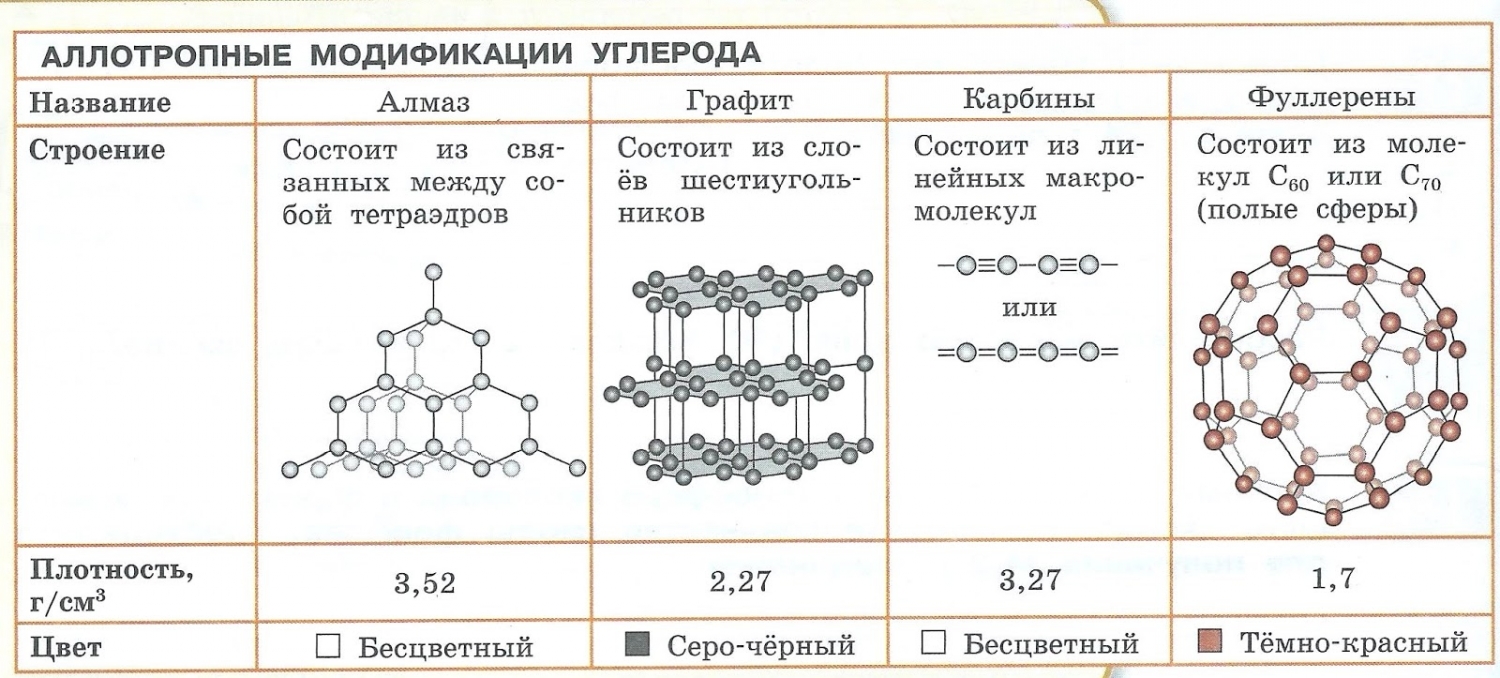
Явление аллотропии вызывается двумя причинами:
- Различным числом атомов в молекуле, например кислород O2 и озон O3.
- Образованием различных кристаллических форм, например алмаз, графит, карбин и фуллерен (смотри рисунок выше).
Основные классы неорганических веществ
Бинарные соединения
Вещества, состоящие из двух химических элементов называются бинарными (от лат. би – два) или двухэлементными.
Названия бинарных соединений образуют из двух слов – названий входящих в их состав химических элементов.
Первое слово обозначает электроотрицательную часть соединения – неметалл, его латинское название с суффиксом –ид стоит всегда в именительном падеже.
Второе слово обозначает электроположительную часть – металл или менее электроотрицательный элемент, его название стоит в родительном падеже, затем указывается степень окисления (только в том случае, если она переменная):
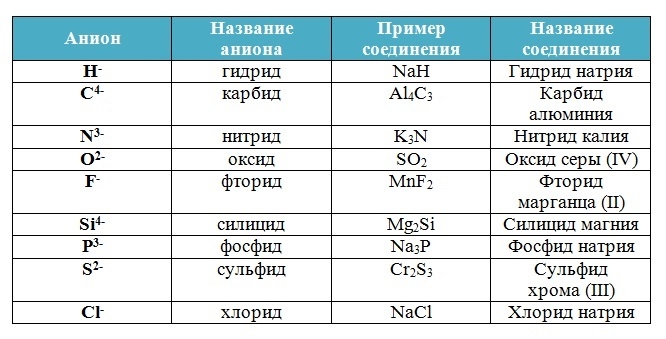
Запомни!
BH3 — боран
B2H6 — диборан
CH4 — метан
SiH4 — силан
NH3 — аммиак
PH3 — фосфин
AsH3 — арсин
Оксиды
Оксиды — сложные вещества, состоящие из двух химических элементов, один из которых кислород в степени окисления -2.
Общая формула оксидов: ЭхОу
Основные оксиды
Основные оксиды — оксиды, которым соответствуют основания.
Основные оксиды образованы металлом со степенью окисления +1, +2.
Пример
Соответствие основных оксидов и оснований
- Na2O — Na2(+1)O(-2) — NaOH
- MgO — Mg(+2)O(-2) — Mg(OH)2
- FeO — Fe(+2)O(-2) — Fe(OH)2
- MnO — Mn(+2)O(-2) — Mn(OH)2
Амфотерные оксиды
Амфотерные оксиды — оксиды, которые в зависимости от условий проявляют либо основные, либо кислотные свойства.
Амфотерные оксиды образованы металлом со степенью окисления +3, +4, а также некоторыми металлами (Zn, Be) со степенью окисления +2.
Пример
Al2(+3)O3(-2), Fe2(+3)O3(-2), Mn(+4)O2(-2), Zn(+2)O(-2), Be(+2)O(-2)
Кислотные оксиды
Кислотные оксиды — оксиды, которым соответствуют кислоты.
Кислотные оксиды образованы неметаллом, а также металлом со степенью окисления +5, +6, +7.
Пример
Соответствие кислотных оксидов и кислот
- SO3 — S(+6)O3(-2) — H2SO4
- N2O5 — N2(+5)O5(-2) — HNO3
- CrO3 — Cr(+6)O3(-2) — H2CrO4
- Mn2O7 — Mn2(+7)O7(-2) — HMnO4
Гидроксиды
Гидроксиды — сложные вещества, состоящие из трех элементов, два из которых водород со степенью окисления +1 и кислород со степенью окисления -2.
Общая формула гидроксидов: ЭхОуНz
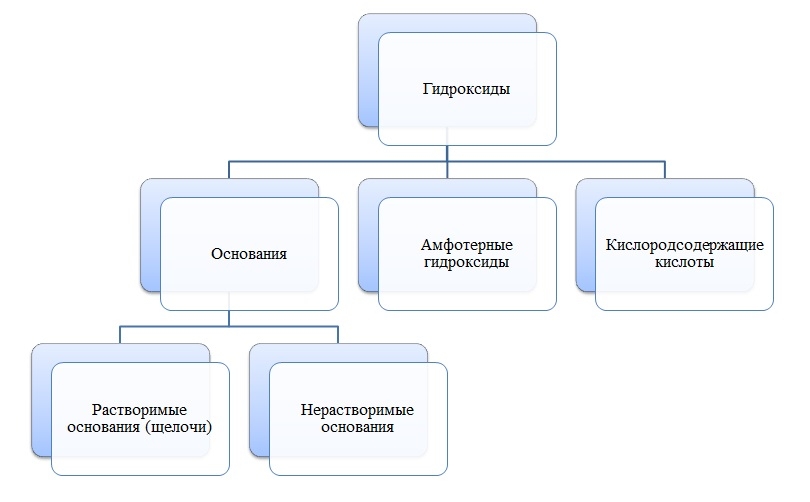
Основания
Основания — сложные вещества, состоящие из ионов металла и одной или нескольких гидроксо-групп (ОН-).
В основаниях металл имеет степень окисления +1, +2 или вместо металла стоит ион аммония NH4+
Пример
NaOH, NH4OH, Ca(OH)2
Амфотерные гидроксиды
Амфотерные гидроксиды — сложные вещества, которые в зависимости от условий проявляют свойства оснований или кислот.
Амфотерные гидроксиды имеют металл со степенью окисления +3, +4, а также некоторые металлы (Zn, Be) со степенью окисления +2.
Пример
Zn(OH)2, Be(OH)2, Al(OH)3, Cr(OH)3
Кислоты
Кислоты — сложные вещества, состоящие из атомов водорода и кислотных остатков.
В состав кислот входит неметалл или металл со степенью окисления +5, +6, +7.
Пример
H2SO4, HNO3, H2Cr2O7, HMnO4
Соли
Соли- соединения, состоящие из катионов металлов (или NH4+) и кислотных остатков.
Общая формула солей: MexAcy
- Me — металл
- Ac — кислотный остаток
Пример
KNO3 — нитрат калия
(NH4)2SO4 — сульфат аммония
Mg(NO3)2 — нитрат магния
Названия кислот и кислотных остатков
| Кислота | Кислотный остаток | ||
| Название | Формула | Название | Формула |
| Соляная (хлороводородная) | HCl | Хлорид | Cl(-) |
| Плавиковая (фтороводородная) | HF | Фторид | F(-) |
| Бромоводородная | HBr | Бромид | Br(-) |
| Иодоводородная | HI | Иодид | I(-) |
| Азотистая | HNO2 | Нитрит | NO2(-) |
| Азотная | HNO3 | Нитрат | NO3(-) |
| Сероводородная | H2S | Сульфид Гидросульфид | S(2-) HS(-) |
| Сернистая | H2SO3 | Сульфит Гидросульфит | SO3(2-) HSO3(-) |
| Серная | H2SO4 | Сульфат Гидросульфат | SO4(2-) HSO4(-) |
| Угольная | H2CO3 | Карбонат Гидрокарбонат | СО3(2-) НСО3(-) |
| Кремниевая | H2SiO3 | Силикат | SiO3(2-) |
| Ортофосфорная | H3PO4 | Ортофосфат Гидроортофосфат Дигидроортофосфат | РО4(3-) НРО4(2-) Н2РО4(-) |
| Муравьиная | НСООН | Формиат | НСОО(-) |
| Уксусная | СН3СООН | Ацетат | СН3СОО(-) |
Полезные ссылки
Источник материала
Классификация неорганических веществ (видео)
Классификация неорганических веществ. Сложные вопросы (видео)
Кислотные оксиды (видео)
Основные оксиды (видео)
Основания (видео)
Характеристика солей (видео)
Дополнительные материалы
Классификация и номенклатура неорганических веществ (видео)
Классификация соединений (видео)
Аллотропные формы углерода (видео)
Об атомах и химических элементах
Другого ничего в природе нет
ни здесь, ни там, в космических глубинах:
все — от песчинок малых до планет —
из элементов состоит единых.
С. П. Щипачев, «Читая Менделеева».
В химии кроме терминов “атом” и “молекула”
часто употребляется понятие “элемент”. Что общего и чем эти понятия
различаются?
Химический элемент – это атомы одного
и того же вида. Так,
например, все атомы водорода – это элемент водород; все атомы кислорода и ртути
– соответственно элементы кислород и ртуть.
В настоящее время известно более 107 видов атомов, то
есть более 107 химических элементов. Нужно различать понятия “химический
элемент”, “атом” и “простое вещество”
Простые и
сложные вещества
По
элементному составу различают простые вещества, состоящие из атомов
одного элемента (H2, O2,Cl2, P4,
Na, Cu, Au), и сложные вещества, состоящие из атомов разных элементов (H2O,NH3,
OF2, H2SO4, MgCl2,K2SO4).
В настоящее
время известно 115 химических элементов, которые образуют около 500простых
веществ.

Самородное золото — простое
вещество.
Способность
одного элемента существовать в виде различных простых веществ, отличающихся по
свойствам, называется аллотропией.Например, элемент кислород O имеет две
аллотропные формы — дикислород O2 и озон O3с различным
числом атомов в молекулах.
Аллотропные
формы элемента углерод C — алмаз и графит — отличаются строение их
кристаллов.Существуют и другие причины аллотропии.
Название | Аллотропные формы |
Углерод С | Графит
|
Алмаз
|
Сложные
вещества часто называют химическими соединениями, например оксид
ртути(II) HgO (получается путем соединения атомов простых веществ — ртути Hg и
кислорода O2), бромид натрия(получается путем соединения атомов
простых веществ — натрия Na и брома Br2).
Итак,
подытожим вышесказанное. Молекулы вещества бывают двух видов:
1. Простые
– молекулы таких веществ состоят из атомов одного вида. В химических
реакциях не могут разлагаться с образованием нескольких более простых веществ.
2. Сложные
– молекулы таких веществ состоят из атомов разного вида. В химических
реакциях могут разлагаться с образованием более простых веществ.
Различие понятий “химический элемент” и
“простое вещество”
Отличить понятия “химический элемент” и “простое
вещество” можно при сравнении свойств простых и сложных веществ. Например,
простое вещество – кислород – бесцветный газ, необходимый для дыхания,
поддерживающий горение. Мельчайшая частица простого вещества кислорода –
молекула, которая состоит из двух атомов. Кислород входит также всостав оксида
углерода (угарный газ) и воды. Однако, в состав воды и оксида углерода входит
химически связанный кислород, который не обладает свойствами простого вещества,
в частности он не может быть использован для дыхания. Рыбы, например, дышат не
химически связанным кислородом, входящим в состав молекулы воды, а свободным,
растворенным в ней. Поэтому, когда речь идет о составе каких – либо химических
соединений, следует понимать, что в эти соединения входят не простые вещества,
а атомы определенного вида, то есть соответствующие элементы.
При разложении сложных веществ, атомы могут выделяться
в свободном состоянии и соединяясь, образовывать простые вещества. Простые
вещества состоят из атомов одного элемента. Различие понятий «химический
элемент» и «простое вещество» подтверждается и тем, что один и тот же элемент
может образовывать несколько простых веществ. Например, атомы элемента
кислорода могут образовать двухатомные молекулы кислорода и трехатомные –
озона. Кислород и озон – совершенно различные простые вещества. Этим
объясняется тот факт, что простых веществ известно гораздо больше, чем
химических элементов.
Пользуясь понятием «химический элемент», можно дать
такое определение простым и сложным веществам:
Простыми называют такие вещества, которые
состоят из атомов одного химического элемента.
Сложными называют такие вещества, которые
состоят из атомов разных химических элементов.
Отличие понятий «смесь» и «химическое
соединение»
Сложные
вещества часто называют химическими соединениями.
Осуществите
переход по ссылке и просмотрите опыт
взаимодействия простых веществ железа и серы.
Попробуйте ответить
на вопросы:
1.Чем отличаются по
составу смеси от химических соединений?
2. Сопоставьте
свойства смесей и химических соединений?
3. Какими
способами можно разделить на составляющие компоненты смеси и химического
соединения?
4. Можно
ли судить по внешним признакам об образовании смеси и химического соединения?
Сравнительная
характеристика смесей и химических
Вопросы для сопоставления смесей с | Сопоставление | |
Смеси | Химические соединения | |
Чем отличаются по составу смеси от | Вещества можно смешивать в любых соотношениях, т.е. | Состав химических соединений постоянный. |
Сопоставьте свойства смесей и | Вещества в составе смесей сохраняют свои свойства | Вещества, образующие соединения, свои свойства не |
Какими способами можно разделить | Вещества можно разделить физическими способами | Химические соединения можно разложить только с |
Можно ли судить по внешним | Механическое смешивание не сопровождается выделением | Об образовании химического соединения можно судить |
Задания для закрепления
I. Поработайте с тренажёрами
Тренажёр №1
Тренажёр №2
Тренажёр №3
Тренажёр №4
Тренажёр №5
II. Решите задание
Из предложенного списка веществ выпишите отдельно простые и сложные вещества:
NaCl, H2SO4, K, S8, CO2, O3, H3PO4, N2, Fe.
Объясните ваш выбор, в каждом из случаев.
III. Ответьте на вопросы
№1
Сколько
простых веществ записано в ряду формул:
H2O, N2, O3, HNO3, P2O5,
S, Fe, CO2, KOH.
№2
К
сложным относятся оба вещества:
А) С (уголь) и S (сера);
Б) CO2 (углекислый газ)и H2O (вода);
В) Fe (железо) и CH4 (метан);
Г) H2SO4 (серная кислота) и H2 (водород).
№3
Выберите
правильное утверждение:
Простые вещества состоят из атомов одного вида.
А) Верно
Б)
Неверно
№4
Для
смесей характерно то, что
А) Они имеют постоянный состав;
Б) Вещества в составе «смеси» не сохраняют свои индивидуальные
свойства;
В) Вещества в «смесях» можно разделить физическими свойствами;
Г) Вещества в «смесях» можно разделить при помощи химической реакции.
№5
Для
«химических соединений» характерно следующее:
А) Переменный состав;
Б) Вещества, в составе «химического соединения»можно разделить
физическими способами;
В) Об образовании химического соединения можно судить по признакам химических
реакций;
Г) Постоянный состав.
№6
В каком
случае идёт речь о железе как о химическом элементе?
А) Железо — это металл, который притягивается магнитом;
Б) Железо входит с состав ржавчины;
В) Для железа характерен металлический блеск;
Г) В состав сульфида железа входит один атом железа.
№7
В каком
случае идёт речь о кислороде как о простом веществе?
А) Кислород — это газ, поддерживает дыхание и горение;
Б) Рыбы дышат кислородом, растворённым в воде;
В) Атом кислород входит в состав молекулы воды;
Г) Кислород входит в состав воздуха.
2.4. Простые
и сложные вещества. Аллотропия.
Химические соединения и смеси
Все
вещества делятся на простые и сложные.
Простые вещества
– это вещества, которые состоят из атомов одного элемента.
Сложные вещества
– это вещества, которые состоят из атомов разных химических элементов.
Сложные
вещества часто называют химическими
соединениями. В химических соединениях свойства простых веществ, из которых
образуются эти соединения, не сохраняются.
Свойства
сложного вещества отличаются от свойств простых
веществ, из которых оно образуется.
Существует также
группа простых веществ, которые называются благородными газами.
Каждый
элемент образует как минимум одно простое вещество. Некоторые элементы могут
образовывать не одно, а два или несколько простых веществ. Это явление
называется аллотропией.
Аллотропия – это
явление образования нескольких простых веществ одним элементом.
Разные
простые вещества, которые образуются одним и тем же химическим элементом,
называются аллотропными видоизменениями (модификациями).
В
природе, как правило, встречаются не чистые вещества, а смеси веществ. Любая смесь состоит из двух или большего числа
веществ, которые называются компонентами
смеси.
Смеси
веществ бывают гомогенными (однородными)
и гетерогенными (неоднородными).
Важнейшие
отличия смесей от химических соединений:
1.
В
смесях свойства отдельных веществ (компонентов) сохраняются.
2.
Состав
смесей не является постоянным.
УПРАЖНЕНИЯ
1.
Укажите, где о кислороде говорится как о
химическом элементе, а где – как о простом веществе:
а) кислород мало
растворим в воде; б) молекулы воды состоят из двух атомов водорода и одного
атома кислорода;
в) в воздухе содержится 20% кислорода (по объему);
г) кислород входит в состав углекислого газа.
Решение:
О
химическом элементе:
б) молекулы воды состоят из двух атомов водорода и одного атома кислорода;
г) кислород входит в состав углекислого газа.
О простом веществе:
а) кислород мало растворим в воде;
в) в воздухе содержится 20% кислорода (по объему).
_______________________________________________________________
2.
Укажите, где о водороде говорится как о
простом веществе, а где – как о химическом элементе:
а) водород
входит в состав большинства органических соединений;
б) водород – самый легкий газ;
в) водородом заполняют воздушные шары;
г) молекула метана содержит четыре атома водорода.
Решение:
О
химическом элементе:
а) водород входит в состав большинства органических соединений;
г) молекула метана содержит четыре атома водорода.
О простом веществе:
б) водород – самый легкий газ;
в) водородом заполняют воздушные шары;
_______________________________________________________________
ЗАДАНИЯ ДЛЯ САМОСТОЯТЕЛЬНОГО РЕШЕНИЯ
1.
Из
предложенного списка веществ выпишите отдельно простые и сложные вещества:
NaCl, H2SO4, K, S8,
CO2, O3, H3PO4, N2, Fe.
2.
Сколько простых
веществ записано в ряду формул:
H2O, N2, O3, HNO3, P2O5,
S, Fe, CO2, KOH.
3.
Какие простые вещества имеют
молекулярное строение (названия и формулы).
4.
Какие простые вещества имеют
атомное строение, приведите примеры.
5.
Почему число простых веществ больше
числа химических элементов.
6.
Сохраняются ли свойства простых
веществ при образовании из них сложного вещества.
7.
Напишите формулы известных вам:
а)простых веществ (5 примеров); б)
сложных веществ (5 примеров).
8.
Чем отливаются смеси от химических
соединений.
9.
Разделите вещества, формулы которых
приведены ниже на простые и сложные:
10.
Элемент фосфор образует три простых вещества,
отличающихся, в частности, цветом: белый, красный и черный фосфор. Чем являются
эти простые вещества по отношению друг к другу.
ВИДЕО ОПЫТ
1. В каком | |
а) кислород, азот, вода | б) хлор, аммиак, углекислый газ |
в) водород, бром, углерод | г) алмаз, оксид кремния (IV), медь |
2. Аллотропные видоизменения кислорода – озон и | |
а) все ответы верны | б) физическими свойствами |
в) химическими свойствами | г) количественным составом молекул |
3. В каких выражениях речь идет о простом веществе | |
а) кислород входит в состав воды | б) кислород плохо растворяется в воде |
в) в оксиде меди (II) массовая доля кислорода составляет 20 % | г) все ответы верны |
4. Какие утверждения справедливы для понятия «простое | |
а) форма существования химического | б) все ответы верны |
в) состоит из атомов одного вида | г) простых веществ больше, чем |
5. Найдите вариант ответа, где | |
а) H2O | б) CO2 |
в)O2 | г) FeO |
6. К простым веществам относится | |
а) | б)хлор |
в) | г) серная кислота и аммиак |
7. В перечне азотная кислота, калий, | |
а) | б) двум |
в)трем | г) |
8. К сложным веществам относятся: | |
а) O2 | б)H3PO4 |
в) Ra | г) |
9. Аллотропные модификации углерода: | |
а) алмаз | б) графит |
в) феллерен | г) все ответы верны |
10. Благородные газы: | |
а) гелий | б) неон |
в) аргон | г) все ответы верны |
Ответы:
1 | б |
2 | а |
3 | б |
4 | б |
5 | в |
6 | б |
7 | в |
8 | б |
9 | г |
10 | г |



