Какие продукты выделяются на аноде а какие на катоде
| Дано: а)CuCl2, б) NaОН. Анод инертный | Решение а) CuCl2 = Cu2+ + 2Cl-. Схему электролиза составляем в соответствии с табл. 11.1 и 11.2: K(-) A(+) инертный Cu2+ + 2ē = Cu 2Cl- –2ē = Cl2 H2O H2O |
| 1. Схема электролиза – ? 2. Продукты электролиза – ? |
На катоде выделяется Cu, на аноде – Cl2.
б) NaОН = Na+ + ОН-.
K(-) A(+) инертный
Na+ 4ОН – 4ē = О2 + 2H2О
2H2O + 2ē = H2 + 2OH-
На катоде выделяется Н2, на аноде – О2.
2. Составить схемы электролиза и написать уравнения электродных процессов водного раствора сульфата никеля (II) , если: а) анод инертный; б) анод никелевый. Какие продукты выделяются на катоде и аноде?
| Дано: NiSO4 а) анод инертный б) анод никелевый | Решение а) анод – инертный NiSO4 = Ni2+ + . Схему электролиза составляем в соответствии с табл. 11.1. и 11.2: |
| 1. Схема электролиза – ? 2. Продукты электролиза – ? |
K(-) A(+) инертный
Ni2+ + 2ē = Ni
2H2O + 2ē = H2 + 2OH- 2H2O – 4ē = О2 + 4H+.
На катоде выделяется Ni и H2 , на аноде выделяется О2.
б) анод – никелевый:
NiSO4 = Ni2+ +
K(-) A(+) (Ni)
Ni2+ + 2ē = Ni , Н2О
2H2O + 2ē = H2 + 2OH- Ni – 2ē = Ni2+.
На катоде выделяется Ni и H2, на аноде растворяется Ni.
3. При электролизе растворов а) нитрата кальция, б) нитрата серебра на аноде выделяется 560 мл газа (н.у.). Составить схему электролиза и написать уравнения электродных процессов. Определить, какое вещество и в каком количестве выделилось на катоде. Анод инертный.
В соответствии со схемой электролиза
nэк (О2)(анод) = nэк (Н2)(катод) или ,
откуда
= = = 1120 см3,
= 11200 см3/моль.
= 5600 см3/моль.
На катоде выделилось 1120 см3 водорода.
Ответ: 1120 см3 водорода.
б) AgNO3 = Ag+ + .
Схема электролиза:
K(-) A(+) инертный
Ag+ + ē = Ag
H2O 2H2O – 4ē = О2 + 4H+
На катоде выделяется Ag, на аноде выделяется О2.
По закону эквивалентов: nэк(О2)(анод) = nэк(Ag)(катод) или
,
Откуда = = 10,8 г.
где .
На катоде выделилось 10,8 г серебра.
Ответ: 10,8 г серебра.
УРОВЕНЬ С
Составить схему электролиза и написать уравнения электродных процессов водного раствора сульфата калия (анод инертный). Определить, какие вещества и в каком количестве выделяются на катоде и аноде, если проводить электролиз в течение четырех часов при силе тока 2 А. Температура 298 К, давление 99 кПа.
= = 3,34 л,
где = 11,2 л/моль.
F = 96500 Кл/моль, если τ – c,
F = 26,8 А∙ч/моль, если τ – ч.
= = 1,67 л,
где = 5,6 л/моль, т.е. = 2 .
Объем водорода при заданных условиях
,
откуда
= = 3,73 л.
Объем кислорода при заданных условиях
= 1/2 = 1,87 л.
Ответ: 3,73 л водорода, 1,87 л кислорода.
2. Металлическую деталь, площадь поверхности которой равна 100 см2, необходимо покрыть слоем электролитически осажденной меди из раствора хлорида меди (II). Составить схему электролиза и написать уравнения электродных процессов, если анод медный. Сколько времени должно длиться осаждение при силе тока 8 А и выходе по току 98 %, если толщина покрытия 0,15 мм? Плотность меди 8,9 г/см3.
| Дано: Электролит: CuCl2S = 100 см2h = 0,15 мм I = 8 A BT = 98 % ρCu = 8,9 г/см3 | Решение CuCl2 = Cu2+ + 2Cl- . Схема электролиза: K(-) A(+) (Cu) Cu2+ + 2ē = Cu Cl- H2O H2O Cu – 2ē = Cu2+ На катоде выделяется Cu, на аноде растворяется Cu. |
| Анод медный Схема электролиза – ? Время электролиза τ – ? |
ВТ= .
По закону Фарадея с учетом выхода по току (ВТ) масса меди, фактически выделившейся на катоде:
mCu(факт) = .
Масса меди, необходимая для получения медного покрытия:
mCu(факт) = S ∙ h ∙ ρ, г,
где S – см2, h – см, ρ – г/см3.
S ∙ h ∙ ρCu = ,
откуда
τ = 1,43 часа,
где Mэк(Cu) = = 32 г/моль.
F = 26,8 А∙ч/моль,
10-1 – коэффициент пересчета миллиметров в сантиметры.
Ответ: 1,43 часа.
3. Определить молярную концентрацию эквивалента раствора нитрата серебра, если для выделения всего серебра из 75 см3 этого раствора потребовалось пропустить ток силой 4А в течение
25 минут. Составить схему электролиза и написать уравнения электродных процессов. Анод инертный. Выход по току серебра 100 %.
Молярная концентрация эквивалента раствора AgNO3:
= .
По закону эквивалентов
nэк(AgNO3) = nэк(Ag), nэк(Ag) = ,
где mAg – масса серебра, выделившегося при электролизе с учетом 100 % выхода по току:
mAg = ,
откуда = ,
тогда nэк(AgNO3) = nэк(Ag) = .
Молярная концентрация эквивалента раствора AgNO3
= = 0,83 моль/л,
где τ – c, F = 96500 Кл/моль, Vр-ра – л;
60 – коэффициент пересчета минут в секунды.
10-3 – коэффициент пересчета сантиметров кубических в литры
Ответ: = 0,83 моль/л.
| Дано: а) CuCl2, б) NaОН. Анод инертный | Решение а) CuCl2 = Cu2+ + 2Cl-. Схему электролиза составляем в соответствии с табл. 11.1 и 11.2: K(-) A(+) инертный Cu2+ + 2ē = Cu 2Cl- – 2ē = Cl2 H2O H2O |
| 1. Схема электролиза – ? 2. Продукты электролиза – ? |
На катоде выделяется Cu, на аноде – Cl2.
б) NaОН = Na+ + ОН-.
K(-) A(+) инертный
Na+ 4ОН – 4ē = О2 + 2H2О
2H2O + 2ē = H2 + 2OH-
На катоде выделяется Н2, на аноде – О2.
2. Составить схемы электролиза и написать уравнения электродных процессов водного раствора сульфата никеля (II) , если: а) анод инертный; б) анод никелевый. Какие продукты выделяются на катоде и аноде?
| Дано: NiSO4 а) анод инертный б) анод никелевый | Решение а) анод – инертный NiSO4 = Ni2+ + . Схему электролиза составляем в соответствии с табл. 11.1. и 11.2: |
| 1. Схема электролиза – ? 2. Продукты электролиза – ? |
K(-) A(+) инертный
Ni2+ + 2ē = Ni
2H2O + 2ē = H2 + 2OH- 2H2O – 4ē = О2 + 4H+.
На катоде выделяется Ni и H2 , на аноде выделяется О2.
б) анод – никелевый:
NiSO4 = Ni2+ +
K(-) A(+) (Ni)
Ni2+ + 2ē = Ni , Н2О
2H2O + 2ē = H2 + 2OH- Ni – 2ē = Ni2+.
На катоде выделяется Ni и H2, на аноде растворяется Ni.
3. При электролизе растворов а) нитрата кальция, б) нитрата серебра на аноде выделяется 560 мл газа (н.у.). Составить схему электролиза и написать уравнения электродных процессов. Определить, какое вещество и в каком количестве выделилось на катоде. Анод инертный.
В соответствии со схемой электролиза
nэк (О2)(анод) = nэк (Н2)(катод) или ,
Откуда
= = = 1120 см3,
= 11200 см3/моль.
= 5600 см3/моль.
На катоде выделилось 1120 см3 водорода.
Ответ: 1120 см3 водорода.
б) AgNO3 = Ag+ + .
Схема электролиза:
K(-) A(+) инертный
Ag+ + ē = Ag
H2O 2H2O – 4ē = О2 + 4H+
На катоде выделяется Ag, на аноде выделяется О2.
По закону эквивалентов: nэк(О2)(анод) = nэк(Ag)(катод) или
,
Откуда = = 10,8 г.
где .
На катоде выделилось 10,8 г серебра.
Ответ: 10,8 г серебра.
СПОСОБЫ ВЫРАЖЕНИЯ СОСТАВА РАСТВОРОВ
УРОВЕНЬ А
Записать выражение массовой доли растворенного вещества. Указать единицу измерения.
Ответ:
, %.
Записать выражение молярной доли растворенного вещества.
Ответ:
.
Записать выражение молярной концентрации вещества. Указать единицу измерения.
Ответ:
св = , моль/л.
Записать выражение молярной концентрации эквивалентов вещества. Указать единицу измерения.
Ответ:
сэк(в) = , моль/л.
Записать выражение моляльности вещества в растворе. Указать единицу измерения.
сm(в) = , моль/кг.
Записать выражение титра раствора вещества. Указать единицу измерения.
Ответ:
Tв = , г/см3.
ЭНЕРГЕТИКА ХИМИЧЕСКИХ РЕАКЦИЙ
УРОВЕНЬ А
1. Указать, какие из приведенных реакций являются эндотермическими:
а) Mn(к) + 1/2O2(г) = MnO(к);
б) 1/2N2(г) + 3/2H2(г) = NH3(г);
в) 1/2N2(г) + 1/2O2(г) = NO(г).
Решение
Так как данные реакции являются реакциями образования 1 моль сложного вещества из простых веществ, то изменение энтальпии приведенных процессов есть стандартная энтальпия образования этих веществ. Для определения теплового эффекта (изменения энтальпии) реакции из таблицы выписываем значения стандартных энтальпий образования: MnO(к)), NH3(г), NO(г):
ΔfHо (298 К, MnO(к)) = –384,93 кДж/моль;
ΔfHо(298 К, NH3(г)) = –46,2 кДж/моль;
ΔfHо = (298 К, NO(г)) = 90,3 кДж/моль.
Реакции а, б имеют отрицательные значения изменения энтальпии, а реакция в – положительное значение изменения энтальпии. Эндотермическими являются те реакции, изменения энтальпии которых имеют положительные значения.
Ответ: в).
2. Без использования табличных данных определить, для каких из перечисленных реакций изменение энтропии имеет положительное значение:
а) CO(г) + H2(г) = C(к) + H2O(г);
б) 2Cu(NO3)2(к) = 2CuO(к) + 4NO2(г) + O2(г);
в) 2PbS(к) + 3O2(г) = 2PbO(к) + 2SO2(г).
Решение
Так как наибольшее значение стандартной энтропии имеют вещества, находящиеся в газообразном состоянии, то энтропия увеличивается, если в ходе реакции возрастает число газовых моль (реакция б)). При протекании реакций а и в наблюдается уменьшение числа газовых моль системы. Следовательно, изменение энтропии данных реакций имеет отриательное значение.
Ответ: б).
Написать формулу для расчета стандартной энтальпии растворения вещества. Указать единицы измерения.
Ответ:
ΔраствН°(298К) = = , кДж/моль.
СКОРОСТЬ ХИМИЧЕСКИХ РЕАКЦИЙ
И ХИМИЧЕСКОЕ РАВНОВЕСИЕ
УРОВЕНЬ А
1.Написать формулу связи Кр с термодинамическими функциями.
Ответ: ∆rGº(298 K) = ∆rHº(298 K) – T∆rSº(298 K) = –2,3 RT lg Kp .
2. Написать формулу зависимости скорости реакции от температуры и Еакт.
Ответ: .
Электролиз (греч. elektron — янтарь + lysis — разложение) — химическая реакция, происходящая при прохождении постоянного тока через
электролит. Это разложение веществ на их составные части под действием электрического тока.
Процесс электролиза заключается в перемещении катионов (положительно заряженных ионов) к катоду (заряжен отрицательно), и отрицательно
заряженных ионов (анионов) к аноду (заряжен положительно).
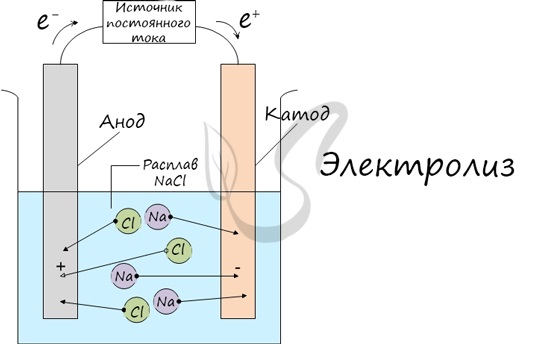
Итак, анионы и катионы устремляются соответственно к аноду и катоду. Здесь и происходит химическая реакция. Чтобы успешно решать задания
по этой теме и писать реакции, необходимо разделять процессы на катоде и аноде. Именно так и будет построена эта статья.
Катод
К катоду притягиваются катионы — положительно заряженные ионы: Na+, K+, Cu2+, Fe3+,
Ag+ и т.д.
Чтобы установить, какая реакция идет на катоде, прежде всего, нужно определиться с активностью металла: его положением в электрохимическом
ряду напряжений металлов.
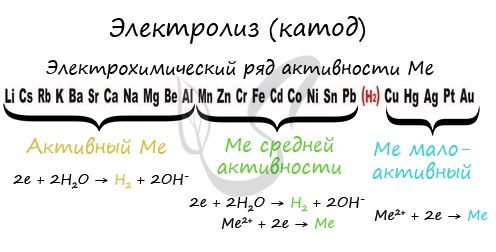
Если на катоде появился активный металл (Li, Na, K) то вместо него восстанавливаются молекулы воды, из которых выделяется водород. Если металл средней
активности (Cr, Fe, Cd) — на катоде выделяется и водород, и сам металл. Малоактивные металлы выделяются на катоде в чистом виде (Cu, Ag).
Замечу, что границей между металлами активными и средней активности в ряду напряжений считается алюминий. При электролизе на катоде металлы
до алюминия (включительно!) не восстанавливаются, вместо них восстанавливаются молекулы воды — выделяется водород.
В случае, если на катод поступают ионы водорода — H+ (например при электролизе кислот HCl, H2SO4) восстанавливается
водород из молекул кислоты: 2H+ — 2e = H2
Анод
К аноду притягиваются анионы — отрицательно заряженные ионы: SO42-, PO43-, Cl-, Br-,
I-, F-, S2-, CH3COO-.

При электролизе кислородсодержащих анионов: SO42-, PO43- — на аноде окисляются не анионы, а молекулы
воды, из которых выделяется кислород.
Бескислородные анионы окисляются и выделяют соответствующие галогены. Сульфид-ион при оксилении окислении серу. Исключением является фтор — если он
попадает анод, то разряжается молекула воды и выделяется кислород. Фтор — самый электроотрицательный элемент, поэтому и является исключением.
Анионы органических кислот окисляются особым образом: радикал, примыкающий к карбоксильной группе, удваивается, а сама карбоксильная группа (COO)
превращается в углекислый газ — CO2.
Примеры решения
В процессе тренировки вам могут попадаться металлы, которые пропущены в ряду активности. На этапе обучения вы можете пользоваться расширенным рядом
активности металлов.
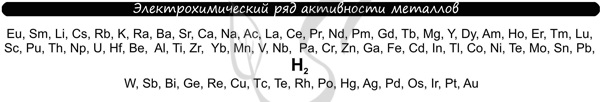
Теперь вы точно будете знать, что выделяется на катоде 😉
Итак, потренируемся. Выясним, что образуется на катоде и аноде при электролизе растворов AgCl, Cu(NO3)2, AlBr3,
NaF, FeI2, CH3COOLi.

Иногда в заданиях требуется записать реакцию электролиза. Сообщаю: если вы понимаете, что образуется на катоде, а что на аноде,
то написать реакцию не составляет никакого труда. Возьмем, например, электролиз NaCl и запишем реакцию:
NaCl + H2O → H2 + Cl2 + NaOH
Натрий — активный металл, поэтому на катоде выделяется водород. Анион не содержит кислорода, выделяется галоген — хлор. Мы пишем уравнение, так
что не можем заставить натрий испариться бесследно 🙂 Натрий вступает в реакцию с водой, образуется NaOH.
Запишем реакцию электролиза для CuSO4:
CuSO4 + H2O → Cu + O2 + H2SO4
Медь относится к малоактивным металлам, поэтому сама в чистом виде выделяется на катоде. Анион кислородсодержащий, поэтому в реакции выделяется
кислород. Сульфат-ион никуда не исчезает, он соединяется с водородом воды и превращается в серую кислоту.
Электролиз расплавов
Все, что мы обсуждали до этого момента, касалось электролиза растворов, где растворителем является вода.
Перед промышленной химией стоит важная задача — получить металлы (вещества) в чистом виде. Малоактивные металлы (Ag, Cu) можно легко получать
методом электролиза растворов.
Но как быть с активными металлами: Na, K, Li? Ведь при электролизе их растворов они не выделяются на катоде в чистом виде, вместо них восстанавливаются
молекулы воды и выделяется водород. Тут нам как раз пригодятся расплавы, которые не содержат воды.

В безводных расплавах реакции записываются еще проще: вещества распадаются на составные части:
AlCl3 → Al + Cl2
LiBr → Li + Br2
© Беллевич Юрий Сергеевич 2018-2020
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение
(в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов
без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования,
обратитесь, пожалуйста, к Беллевичу Юрию.
Определение
Электролиз – это физико-химический окислительно-восстановительный процесс, протекающий в растворах или расплавах электролитов под действием электрического тока, заключающийся в выделении на электродах составных частей растворённых веществ или других веществ — продуктов вторичных реакций на электродах.
процесс на катоде K(-): катион принимает электроны и восстанавливается
процесс на аноде A(+): анион отдает электроны и окисляется
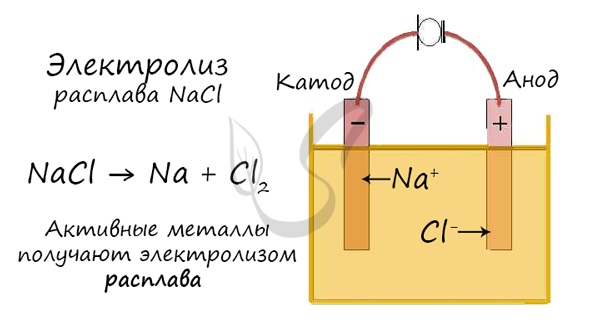
Рассмотрим процессы, протекающие при электролизе, на примере хлорида натрия. При сильном нагревании твердый хлорид натрия плавится. Полученный расплав содержит подвижные ионы натрия и хлора, освободившиеся из кристаллической решетки, и поэтому проводит электрический ток. Если в расплав опустить угольные электроды, присоединенные к источнику тока, ионы приобретают направленное движение: катионы $mathrm{Na^+}$ движутся к отрицательно заряженному электроду – катоду, анионы $mathrm{Cl^–}$ – к положительно заряженному электроду – аноду.
На катоде ионы $mathrm{Na^+}$ получают электроны и восстанавливаются до металла:
$ Na^+ + e^- rightarrow Na$ (восстановление),
а на аноде ионы $mathrm{Cl^–}$ отдают электроны и окисляются до свободного хлора:
$2Cl^– – 2e^- rightarrow Cl_2$ (окисление).
Таким образом, в результате процесса электролиза расплав хлорида натрия разлагается на простые вещества:
$K^-: hspace{0.5cm} 2Na^+ + 2e^- rightarrow 2Na$
$A^+: hspace{0.5cm} 2Cl^- — 2e^- rightarrow Cl_2$
Суммарное уравнение электролиза: $2Na^+ + 2Cl^- xrightarrow[]{textrm{эл.ток}} 2Na + Cl_2$
Электролиз отличается от обычных окислительно-восстановительных реакций. При электролизе полуреакции разделены в пространстве: восстановление происходит только на катоде, а окисление – на противоположном электроде — аноде.
Окислительное и восстановительное действие электрического тока намного сильнее действия обычных химических веществ. Только с помощью тока ученым удалось получить наиболее активные простые вещества – натрий, калий и фтор. Пионером в использовании электрического тока в химии был английский ученый Гемфри Дэви. Подвергая электролизу расплавы различных соединений, он открыл восемь неизвестных до него химических элементов.
Электролиз растворов электролитов
В водных растворах процессы электролиза осложняются присутствием воды, которая проявляет двойственную природу: она может проявлять свойства и окислителя, и восстановителя. На катоде вода может принимать электроны, и тогда атомы водорода в ней будут восстанавливаются до газообразного водорода:
$K^-: hspace{0.5cm} 2H_2O + 2e^- rightarrow H_2uparrow + 2OH^–$.
На аноде вода может отдавать электроны, при этом атомы кислорода будут окисляться до газообразного кислорода:
$A^+: hspace{0.5cm} 2H_2O – 4e^- rightarrow O_2 + 4H^+$.
Другими словами, при электролизе растворов электролитов (чаще всего солей) на катоде и аноде протекают конкурирующие процессы: катионы металла $Me^{+n}$ конкурируют с катионами водорода $H^+$, а анионы кислотных остатков $An^{n-}$ конкурируют с анионами гидроксильных групп $(OH)^-$. Рассмотрим подробнее процессы, протекающие на электродах.
ЗАКОНОМЕРНОСТИ ПРОЦЕССОВ НА КАТОДЕ
На отрицательно заряженном электроде — катоде, происходит восстановление катионов, которое не зависит от материала катода, из которого он сделан, но зависит от активности металла, т.е. от положения металла в электрохимическом ряду напряжения (ЭХР). (Сравниваем окислительную способность, то есть способность принимать электроны, ионов металлов и иона водорода)

| Li K Ca Na Mg Al | Mn Zn Fe Ni Sn Pb | Cu Hg Ag Pt Au |
|---|---|---|
$Me^+n bar{e} ne$ $2H_2O + 2bar{e} =H_2 + 2OH^-$ | $Me^{+n} + n bar{e} = Me^0$ $2 H_2O + 2bar{e} = H_2 + 2OH^-$ | $Me^{+n} + n bar{e} = Me^0$ |
На катоде всегда восстанавливаются молекулы воды | На катоде могут восстанавливаться и ионы металла, и воды в зависимости от плотности тока, Т и концентрации соли | На катоде всегда восстанавливаются ионы металлов |
Если соль образована активным металлом, стоящим в ряду напряжения до марганца, на катоде не восстанавливаются катионы металла, а происходит восстановление воды с выделением газообразного водорода.
Если металл, образующий соль средней активности (после алюминия, но до водорода), то на катоде возможны два конкурирующих процесса: и восстановление воды, и восстановление катионов металла. Преобладание того или иного процесса зависит от плотности тока, температуры и концентрации соли.
Легче всего принимаю электроны неактивные металлы (стоящие в ЭХР после Н), поэтому они легко восстанавливаются на катоде до простого вещества — металла.
Закономерности процессов на аноде
Процесс на положительно заряженном электроде — аноде зависит от материала анода и от природы аниона. При электролизе растворов электролитов на аноде происходит окисление анионов. Образующийся продукт зависит от восстановительной активности аниона кислотного остатка.
Ряд восстановительной активности анионов (уменьшается). По способности окисляться анионы располагаются в следующем порядке:
$J^- hspace{6pt} > hspace{6pt} Br^- hspace{6pt} > hspace{6pt} S^{2-} hspace{6pt} > hspace{6pt} Cl^- hspace{6pt} > hspace{6pt} OH^- hspace{6pt} > hspace{6pt} SO_4^{2-} hspace{6pt} > hspace{6pt} NO_3^- hspace{6pt} > hspace{6pt} F^-$
Анод может быть растворимым и нерастворимым (инертным).
Запомни!
1. Растворимый анод при электролизе, как правило, растворяется с образованием катионов металла анода.
2. На нерастворимом аноде, если кислотный остаток соли бескислородный (кроме фторидов!), происходит окисление аниона до простого вещества — неметалла.
3. Если в состав соли входит остаток кислородсодержащей кислоты, то на аноде происходит окисление воды и выделяется кислород.
| Анод | Кислотный остаток | |||
|---|---|---|---|---|
бескислородный $Cl^-, Br^-, I^-, S^{2-} $ | кислородсодержащий $NO_3^-, SO_4^{2-}, PO_4^{3-}, F^-$ | |||
на аноде окисляются ионы кислотного остатка | на аноде окисляются молекулы воды | |||
| нерастворимый | Окисление аниона (кроме фторидов): $Ac^{ m-} — mbar{e} = Ac^0$ | В щелочной среде: $4OH^- – 4bar{e} rightarrow 2H_2O + O_2$ В кислой, нейтральной среде: $2H_2O – 4bar{e} rightarrow 4H^+ + O_2$ | ||
| растворимый | Окисление металла анода: $Me^0- nbar{e}= Me^{+n}$ анод раствор | |||
Рассмотрим процесс электролиза растворов электролитов на конкретных примерах.
Пример 1
Электролиз раствора соли активного металла и бескислородной кислоты
$NaCl leftrightarrow Na^+ + Cl^−$
Рассмотрим полуреакции окисления и восстановления. Натрий – активный металл, он стоит в ряду напряжений левее водорода, поэтому на катоде восстанавливается вода и выделяется водород. Хлорид-ион не содержит атомов кислорода, поэтому на аноде он окисляется и выделяется хлор:
K»катод»(-): $2H_2O + 2bar{e} = H_2 uparrow+ 2OH^−hspace{0.2cm} | 1$
A»анод»(+): $2Cl^- − 1bar{e} cdot 2 = Cl_2 uparrow hspace{1.1cm} |1$
При сложении уравнений полуреакций получаем сокращенное ионное уравнение электролиза:
$mathrm{2Cl^– + 2H_2O rightarrow H_2 + Cl_2 + 2 OH^–}$.
Если добавить в левую и правую часть по два иона $mathrm{Na^+}$, которые в самом электролизе не участвуют, получим молекулярное уравнение электролиза раствора хлорида натрия:
$Sigma: hspace{0.5cm} 2NaCl (p-p) + 2H_2O xrightarrow[]{textrm{эл.ток}} H_2 uparrow + Cl_2 uparrow+2NaOH$
Мы видим, что при электролизе раствора такого широко доступного и дешевого вещества, как хлорид натрия, получилось сразу три ценных продукта: водород, хлор и щелочь. Именно поэтому электролиз широко используется в разных отраслях промышленности. С его помощью получают химически чистые металлы и удаляют растворимые примеси из воды.
Пример 2
Электролиз раствора соли активного металла и кислородсодержащей кислоты
$Na_2SO_4 (p-p)leftrightarrow 2Na^++SO_4^{2−}$
K(-): $2H_2O + 2bar{e} = H_2 uparrow+ 2OH^−hspace{0.3cm} | 2$
A(+): $2H_2O — 4bar{e} = O_2 uparrow+ 4H^+hspace{0.5cm} | 1$
Если первое уравнение умножить на 2 и сложить со вторым уравнением, получим:
$2cdot2H_2O + 2H_2O= 2H_2 + O_2 + 4H^+ + 2cdot 2OH^–$
$6H_2O= 2H_2 + O_2 + 4H^+ + 4OH^–$.
Ионы водорода и гидроксид-ионы реагируют друг с другом:
$mathrm{4H^+ + 4OH^– = 4H_2O}$
После сокращения молекул воды в левой и правой частях получаем полное уравнение электролиза:
$Sigma: hspace{0.5cm} 2H_2O xrightarrow[]{textrm{эл.ток}} 2H_2 uparrow + O_2 uparrow$
Пример 3
Электролиз раствора гидроксида активного металла
$NaOH (p-p) leftrightarrow Na^+ + OH^−$
K(-): $2H_2O + 2bar{e} = H_2 uparrow + 2OH^−$
A(+): $2H_2O — 4bar{e} = O_2 uparrow + 4H^+$
$Sigma: hspace{0.5cm} 2H_2O xrightarrow[]{textrm{эл.ток}} 2H_2 uparrow + O_2 uparrow$
Пример 4
Электролиз раствора соли среднеактивного металла и бескислородной кислоты
$ZnCl_2 leftrightarrow Zn^{2+} + 2Cl^−$
K»катод»(-): $Zn^{2+} + 2bar{e} = Zn^0$
$2H_2O + 2bar{e} = H_2 uparrow + 2OH^−$
A»анод»(+): $2Cl^- − 1bar{e} cdot 2 = Cl_2 uparrow$
$Sigma: hspace{0.5cm} 2ZnCl_2(p-p) + 2H_2O xrightarrow[]{textrm{эл.ток}} Zn +H_2uparrow + Zn(OH)_2downarrow + 2Cl_2 uparrow$
Обратите внимание, что при электролизе водных растворов солей среднеактивных металлов на катоде одновременно выделяется и металл и водород.
Иногда, в рамках решения ЕГЭ, требуется упрощенная запись этого процесса. В таком случае следует записать только выделение водорода на катоде (основной процесс):
$Sigma: hspace{0.5cm} ZnCl_2(p-p) + 2H_2O xrightarrow[]{textrm{эл.ток}} H_2uparrow + + Zn(OH)_2downarrow + Cl_2 uparrow$
Пример 5
Электролиз раствора соли среднеактивного металла и кислородсодержащей кислоты
$ZnSO_4 (p-p) leftrightarrow Zn^{2+} +SO_4^{2−}$
K(-): $Zn^{2+} + 2bar{e} = Zn^0$
$2H_2O + 2bar{e} = H_2 uparrow + 2OH^−$
A(+): $2H_2O — 4bar{e} = O_2 uparrow + 4H^+$
$Sigma: hspace{0.5cm} 2ZnSO_4 (p-p)+ 4H_2O xrightarrow[]{textrm{эл.ток}} Zn + +H_2uparrow + Zn(OH)_2downarrow + 2H_2SO_4 + O_2 uparrow$
Иногда, в рамках решения ЕГЭ, требуется упрощенная запись этого процесса. В таком случае следует записать только выделение водорода на катоде (основной процесс):
$Sigma: hspace{0.5cm} 2ZnSO_4 (p-p)+ 2H_2O xrightarrow[]{textrm{эл.ток}} 2Zn + 2H_2SO_4 + O_2 uparrow$
Пример 6
Электролиз гидроксида менее активного металла :
$Fe(OH)_3xrightarrow[]{textrm{эл.ток}} ne$
невозможно (нерастворим)
