Какие продукты получаются при окислении метилового спирта

Гидроксисоединения – это органические вещества, молекулы которых содержат, помимо углеводородной цепи, одну или несколько гидроксильных групп ОН.
Гидроксисоединения делят на спирты и фенолы.
Строение, изомерия и гомологический ряд спиртов
Химические свойства спиртов
Способы получения спиртов

Если гидроксогруппа ОН соединена с бензольным кольцом, то вещество относится к фенолам.
Общая формула предельных нециклических спиртов: CnH2n+2Om, где m ≤ n.
Спирты – органические вещества, молекулы которых содержат, помимо углеводородной цепи, одну или несколько гидроксильных групп ОН.
Химические реакции гидроксисоединений идут с разрывом одной из связей: либо С–ОН с отщеплением группы ОН, либо связи О–Н с отщеплением водорода. Это реакции замещения, либо реакции отщепления (элиминирования).
Свойства спиртов определяются строением связей С–О–Н. Связи С–О и О–Н — ковалентные полярные. При этом на атоме водорода образуется частичный положительный заряд δ+, на атоме углерода также частичный положительный заряд δ+, а на атоме кислорода — частичный отрицательный заряд δ–.
Такие связи разрываются по ионному механизму. Разрыв связи О–Н с отрывом иона Н+ соответствует кислотным свойствам гидроксисоединения. Разрыв связи С–О соответствует основным свойствам и реакциям нуклеофильного замещения.
С разрывом связи О–Н идут реакции окисления, а с разрывом связи С–О — реакции восстановления.
- слабые кислотные свойства, замещение водорода на металл;
- замещение группы ОН
- отрыв воды (элиминирование) – дегидратация
- окисление
- образование сложных эфиров — этерификация
1. Кислотные свойства
Спирты – неэлектролиты, в водном растворе не диссоциируют на ионы; кислотные свойства у них выражены слабее, чем у воды.
1.1. Взаимодействие с раствором щелочей
При взаимодействии спиртов с растворами щелочей реакция практически не идет, т. к. образующиеся алкоголяты почти полностью гидролизуются водой.
![]()
Равновесие в этой реакции так сильно сдвинуто влево, что прямая реакция не идет. Поэтому спирты не взаимодействуют с растворами щелочей.
Многоатомные спирты также не реагируют с растворами щелочей.
1.2. Взаимодействие с металлами (щелочными и щелочноземельными)
Спирты взаимодействуют с активными металлами (щелочными и щелочноземельными). При этом образуются алкоголяты. При взаимодействии с металлами спирты ведут себя, как кислоты.
![]()
Например, этанол взаимодействует с калием с образованием этилата калия и водорода.
![]()
Видеоопыт взаимодействия спиртов (метанола, этанола и бутанола) с натрием можно посмотреть здесь.
Алкоголяты под действием воды полностью гидролизуются с выделением спирта и гидроксида металла.
Например, этилат калия разлагается водой:
CH3OH > первичные спирты > вторичные спирты > третичные спирты
Многоатомные спирты также реагируют с активными металлами:

Видеоопыт взаимодействия глицерина с натрием можно посмотреть здесь.
1.3. Взаимодействие с гидроксидом меди (II)
Многоатомные спирты взаимодействуют с раствором гидроксида меди (II) в присутствии щелочи, образуя комплексные соли (качественная реакция на многоатомные спирты).
Например, при взаимодействии этиленгликоля со свежеосажденным гидроксидом меди (II) образуется ярко-синий раствор гликолята меди:
Видеоопыт взаимодействия этиленгликоля с гидроксидом меди (II) можно посмотреть здесь.
2. Реакции замещения группы ОН
2.1. Взаимодействие с галогеноводородами
При взаимодействии спиртов с галогеноводородами группа ОН замещается на галоген и образуется галогеналкан.
Например, этанол реагирует с бромоводородом.

Видеоопыт взаимодействия этилового спирта с бромоводородом можно посмотреть здесь.
третичные > вторичные > первичные > CH3OH.
Многоатомные спирты также, как и одноатомные спирты, реагируют с галогеноводородами.
Например, этиленгликоль реагирует с бромоводородом:

2.2. Взаимодействие с аммиаком
Гидроксогруппу спиртов можно заместить на аминогруппу при нагревании спирта с аммиаком на катализаторе.
Например, при взаимодействии этанола с аммиаком образуется этиламин.
![]()
2.3. Этерификация (образование сложных эфиров)
Одноатомные и многоатомные спирты вступают в реакции с карбоновыми кислотами, образуя сложные эфиры.

Например, этанол реагирует с уксусной кислотой с образованием этилацетата (этилового эфира уксусной кислоты):

Многоатомные спирты вступают в реакции этерификации с органическими и неорганическими кислотами.
Например, этиленгликоль реагирует с уксусной кислотой с образованием ацетата этиленгликоля:

2.4. Взаимодействие с кислотами-гидроксидами
Спирты взаимодействуют и с неорганическими кислотами, например, азотной или серной.
Например, при взаимодействии этанола с азотной кислотой образуется сложный эфир этилнитрат:
Например, глицерин под действием азотной кислоты образует тринитрат глицерина (тринитроглицерин):
3. Реакции замещения группы ОН
В присутствии концентрированной серной кислоты от спиртов отщепляется вода. Процесс дегидратации протекает по двум возможным направлениям: внутримолекулярная дегидратация и межмолекулярная дегидратация.
3.1. Внутримолекулярная дегидратация
При высокой температуре (больше 140оС) происходит внутримолекулярная дегидратация и образуется соответствующий алкен.
Например, из этанола под действием концентрированной серной кислоты при температуре выше 140 градусов образуется этилен:
В качестве катализатора этой реакции также используют оксид алюминия.
Отщепление воды от несимметричных спиртов проходит в соответствии с правилом Зайцева: водород отщепляется от менее гидрогенизированного атома углерода.
Например, в присутствии концентрированной серной кислоты при нагревании выше 140оС из бутанола-2 в основном образуется бутен-2:
3.2. Межмолекулярная дегидратация
При низкой температуре (меньше 140оС) происходит межмолекулярная дегидратация по механизму нуклеофильного замещения: ОН-группа в одной молекуле спирта замещается на группу OR другой молекулы. Продуктом реакции является простой эфир.
Например, при дегидратации этанола при температуре до 140оС образуется диэтиловый эфир:
![]()
4. Окисление спиртов
Реакции окисления в органической химии сопровождаются увеличением числа атомов кислорода (или числа связей с атомами кислорода) в молекуле и/или уменьшением числа атомов водорода (или числа связей с атомами водорода).
В зависимости от интенсивности и условий окисление можно условно разделить на каталитическое, мягкое и жесткое.
Первичный спирт → альдегид → карбоновая кислота
Метанол → формальдегид → углекислый газ
Вторичные спирты окисляются в кетоны: вторичные спирты → кетоны
Типичные окислители — оксид меди (II), перманганат калия KMnO4, K2Cr2O7, кислород в присутствии катализатора.
Легкость окисления спиртов уменьшается в ряду:
метанол < первичные спирты < вторичные спирты < третичные спирты
Продукты окисления многоатомных спиртов зависят от их строения. При окислении оксидом меди многоатомные спирты образуют карбонильные соединения.
4.1. Окисление оксидом меди (II)
Cпирты можно окислить оксидом меди (II) при нагревании. При этом медь восстанавливается до простого вещества. Первичные спирты окисляются до альдегидов, вторичные до кетонов, а метанол окисляется до метаналя.
Например, этанол окисляется оксидом меди до уксусного альдегида

Видеоопыт окисления этанола оксидом меди (II) можно посмотреть здесь.
Например, пропанол-2 окисляется оксидом меди (II) при нагревании до ацетона

Третичные спирты окисляются только в жестких условиях.
4.2. Окисление кислородом в присутствии катализатора
Cпирты можно окислить кислородом в присутствии катализатора (медь, оксид хрома (III) и др.). Первичные спирты окисляются до альдегидов, вторичные до кетонов, а метанол окисляется до метаналя.
Например, при окислении пропанола-1 образуется пропаналь

Видеоопыт каталитического окисления этанола кислородом можно посмотреть здесь.
Например, пропанол-2 окисляется кислородом при нагревании в присутствии меди до ацетона
Третичные спирты окисляются только в жестких условиях.
4.3. Жесткое окисление
При жестком окислении под действием перманганатов или соединений хрома (VI) первичные спирты окисляются до карбоновых кислот, вторичные спирты окисляются до кетонов, метанол окисляется до углекислого газа.
При нагревании первичного спирта с перманганатом или дихроматом калия в кислой среде может образоваться также альдегид, если его сразу удаляют из реакционной смеси.
Третичные спирты окисляются только в жестких условиях (в кислой среде при высокой температуре) под действием сильных окислителей: перманганатов или дихроматов. При этом происходит разрыв углеродной цепи и могут образоваться углекислый газ, карбоновая кислота или кетон, в зависимости от строения спирта.
| Спирт/ Окислитель | KMnO4, кислая среда | KMnO4, H2O, t |
| Метанол СН3-ОН | CO2 | K2CO3 |
| Первичный спирт R-СН2-ОН | R-COOH/ R-CHO | R-COOK/ R-CHO |
| Вторичный спирт R1-СНОН-R2 | R1-СО-R2 | R1-СО-R2 |
Например, при взаимодействии метанола с перманганатом калия в серной кислоте образуется углекислый газ
![]()
Например, при взаимодействии этанола с перманганатом калия в серной кислоте образуется уксусная кислота

Например, при взаимодействии изопропанола с перманганатом калия в серной кислоте образуется ацетон

4.4. Горение спиртов
Образуются углекислый газ и вода и выделяется большое количество теплоты.
CnH2n+1ОН + (3n+1)/2O2 → nCO2 + (n+1)H2O + Q
Например, уравнение сгорания метанола:
2CH3OH + 3O2 = 2CO2 + 4H2O
5. Дегидрирование спиртов
При нагревании спиртов в присутствии медного катализатора протекает реакция дегидрирования. При дегидрировании метанола и первичных спиртов образуются альдегиды, при дегидрировании вторичных спиртов образуются кетоны.
Например, при дегидрировании этанола образуется этаналь

Например, при дегидрировании этиленгликоля образуется диальдегид (глиоксаль)

Получение йодоформа основано на химическом или электрохимическом окислении растворов иода в ацетоне или метиловом спирте. Окисление гипохлоритом можно описать следующим уравнением реакции [c.296]
Метиловый спирт Окисление в функции Формальдегид, Н2О анальных группах СеОа (1—10%) — МоОз газовая фаза. Выход —93% [75] [c.324]
Было, однако, замечено, что перевод карбоксильной группы в сложноэфирную снимает дезактивирующее действие карбоксильной группы. На этой основе разработан четырехстадийный процесс получения диметилтерефталата, состоящий в окислении -ксилола в п-толуиловую кислоту, этерификации последней метиловым спиртом, окислении эфира /г-толуиловой кислоты в моноэфир терефта- [c.484]
Для подсчета количества граммов метилового спирта, окисленного бихроматом калия, нужно полученную величину разделить на 6 (перевод нормальности бихромата в молярность) и умножить на 32 (молекулярную массу метанола). [c.193]
При отсутствии других окисляющихся веществ можно пользоваться методами, основанными на окислении метилового спирта раствором хромовой кислоты с последующим иодометрическим определением ее избытка. Метод пригоден и в присутствии формальдегида [34]. Об определении метилового спирта окислением перманганатом в щелочной среде см. [35]. [c.64]
Хроматографические методы обнаружения алифатических спиртов приведены при описании количественных методов (стр. 975). Там же описано обнаружение метилового спирта окислением его до формальдегида (стр. 977). [c.942]
Методы получения уксусной кислоты разнообразны. Ранее она Производилась из сырья растительного происхождения или биохимическим путем (окислением этилового спирта кислородом воздуха в присутствии уксусного грибка ) или из продуктов сухой перегонки древесины. Однако основное количество уксусной кислоты получают синтетическим путем. Основными методами являются окисление уксусного альдегида, синтез из ацетона через кетен, синтез из Окиси углерода и метилового спирта, окисление предельных углеводородов (бутана и выше). Часть уксусной кислоты регенерируют в Процессе производства ацетилцеллюлозы. Наибольшее распространение среди методов синтеза уксусной кислоты получил процесс [c.293]
| Рис. 55. Схема произвойств метилового спирта окислением метана. | 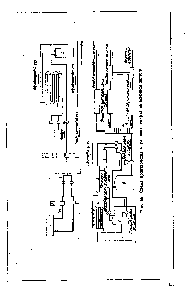 |
Омыление диметилтерефталата с образованием метилового спирта, окисление последнего до формальдегида, определяемого колориметрически по реакции с хромотроповой кислотой. [c.92]
Омыление метилацетатя до метилового спирта, окисление последнего и колориметрическое определение формальдегида по реакции с хромотроповой кислотой. [c.102]
Один из первых способов производства формальдегида и метилового спирта окислением метана бьил разработан Glo k oM В этом процессе метан и кислород пропускают над нагретой смесью металлической меди и пемзы или асбеста получающиеся продукты конденсируют. Можно также применять смесь газа, получающегося при коксове.нии угля, или светильного газа, с воздухом. [c.932]
Для подсчета количества граммов метилового спирта, окисленного хромпиком, нужно полученную величину разделить на 6 (перевод нормальности бихромата в молярность) и умножить на 32 (молекулярный вес метанола). Такое количество граммов метанола содержится в -2 г ксходногораствора. Переводя на 100 с.и , получим [c.200]
Исследовано растение южной Европы. L. van Itallie и А. J. Steenhauer [337] получили при перегонке с водяным паром плодов растения из Лейденского ботанического сада эфирное масло с сильным анисовым запахом и сладким вкусом. Выход — 0,167%. Масло застывает при температуре около +18° и имеет п 1,5592. При окислении хромовой кислотой дает анисовую кислоту с т. пл. 175°. Кислота также идентифицирована микрохимическим способом через серебряные, кальциевые, бариевые и стронциевые соли. Установлено, что масло в большей своей части состоит из анетола. В дестиллационной воде найдены ацетон (иодоформенная реакция) и метиловый спирт (окислением с перманганатом калия и серной кислотой в формальдегид). Содержание анетола выше в масле из семян и меньше в масле из травы. [c.316]
Препаративная органическая химия (1959) — [
c.666
]
Препаративная органическая химия (1959) — [
c.666
]
Общая химическая технология органических веществ (1966) — [
c.232
]
Общая химическая технология органических веществ (1955) — [
c.203
]
Органическая химия 1971 (1971) — [
c.137
]
Органическая химия 1974 (1974) — [
c.114
]
Органическая химия (1956) — [
c.226
]
Органическая химия Издание 6 (1972) — [
c.113
,
c.114
]
Препаративная органическая химия Издание 2 (1964) — [
c.681
]
Гидролитическое расщепление оксифлавонов и флавонолов протекает по приведенной схеме, если реакция проводится без доступа кислорода. Если же гидролиз происходит в обычных условиях, то наступают осложнения вследствие чувствительности указанных соединений к окислению кислородом воздуха, причем в этом случае удается выделить лишь более стойкие продукты распада [22[]. Удобнее проводить гидролиз метиловых эфиров оксифлавонов и флавонолов (XXVIII), так как при этом образуются продукты не столь глубокого распада [222]. Лучшие результаты получаются при применении 20%-ного раствора едкого кали в 50%-ном этиловом спирте [223], однако применилась и более концентрированная щелочь (до 50%). [c.198]
В шестой пятилетке более чем вдвое увеличивается производство минеральных удобрений до 19,6 млн. т в 1960 г. Значительно расширяется ассортимент удобрений, особенно концентрированных. Будут выпускаться новые, более эффективные средства борьбы с вредителями и болезнями сельскохозяйственных растений. Их применение в сельском хозяйстве отличается исключительно высоким экономическим эффектом стоимость сбереженной продукции в 5—40 раз превышает стоимость затраченных г инсектофунгисидов. В последнее время синтезированы новые сверхсильные инсектисиды. Их создание опирается на работы в области фосфороргани-ческих соединений А. Е. Арбузова и других советских ученых. Орга-низуется широкое производство гербисидов — средств химической про-4- полки, значительно сокращающих затраты труда по сравнению с обычными механическими способами борьбы с сорняками. Увеличивается во много раз производство этилового спирта из этилена его себестоимость в 5 раз ниже, чем спирта из пищевого сырья, а производительность труда при его получении выше более чем в 50 раз. Из парафиновых углеводородов нефти прямым окислением кислородом воздуха получают высшие спирты, что позволяет заменить пищевые жиры в производстве моющих веществ. Народнохозяйственное значение синтетических моющих средств видно из таких, например, данных для производства мыла в 1955 году было затрачено растительных масел, собранных с площади в 1,5 миллиона гектаров. К тому же новые моющие вещества обладают более высоким качеством и могут применяться в жесткой и морской воде и при низкой температуре воды. В течение шестой пятилетки пищевые продукты, идущие на технические цели, полностью заменяются синтетическими. Получены новые синтетические волокна, которые значительно превосходят по своим свойствам капрон. Производство синтетических материалов для волокон возрастает за пятилетие почти в шесть раз, капитальные вложения в эту отрасль производства составят 11 миллиардов рублей. [c.17]
Оригинальный способ окисления одноатомных алифатических спиртов в соответственные кислоты заключается в нагревании спирта с едким натром или едким кали в автоклаве примерно до 250—270 » Так, например, при нагревании этилового, амилового или церилового спиртов с едким кали происходит отщепление водорода и образование калиевой соли соответственной кислоты. Точно таким же способом можно получить изомасляную кислоту . При нагревании п-бутилового спирта с едким натром в автоклаве до 275° выделение водорода заканчивается примерно через 3 часа, причем образуется с хорощим выходом п-масляная кислота, наряду с небольшим количеством а-зтил-капроновой кислоты. Если же п-бутиловый спирт нагревать с 10% металлического натрия до 275°, продукт реакции содержит приблизительно равные весовые количества 2-этилгексило-вого спирта и п-масляной кислоты, наряду с небольшим количеством а-этилкапроновой кислоты. При применении большего количества натрия выход кислоты увеличивается за счет выхода спирта [c.126]



