Какие продукты будут находиться а растворе

Определение
Электролиз – это физико-химический окислительно-восстановительный процесс, протекающий в растворах или расплавах электролитов под действием электрического тока, заключающийся в выделении на электродах составных частей растворённых веществ или других веществ — продуктов вторичных реакций на электродах.
процесс на катоде K(-): катион принимает электроны и восстанавливается
процесс на аноде A(+): анион отдает электроны и окисляется
Рассмотрим процессы, протекающие при электролизе, на примере хлорида натрия. При сильном нагревании твердый хлорид натрия плавится. Полученный расплав содержит подвижные ионы натрия и хлора, освободившиеся из кристаллической решетки, и поэтому проводит электрический ток. Если в расплав опустить угольные электроды, присоединенные к источнику тока, ионы приобретают направленное движение: катионы $mathrm{Na^+}$ движутся к отрицательно заряженному электроду – катоду, анионы $mathrm{Cl^–}$ – к положительно заряженному электроду – аноду.
На катоде ионы $mathrm{Na^+}$ получают электроны и восстанавливаются до металла:
$ Na^+ + e^- rightarrow Na$ (восстановление),
а на аноде ионы $mathrm{Cl^–}$ отдают электроны и окисляются до свободного хлора:
$2Cl^– – 2e^- rightarrow Cl_2$ (окисление).
Таким образом, в результате процесса электролиза расплав хлорида натрия разлагается на простые вещества:
$K^-: hspace{0.5cm} 2Na^+ + 2e^- rightarrow 2Na$
$A^+: hspace{0.5cm} 2Cl^- — 2e^- rightarrow Cl_2$
Суммарное уравнение электролиза: $2Na^+ + 2Cl^- xrightarrow[]{textrm{эл.ток}} 2Na + Cl_2$
Электролиз отличается от обычных окислительно-восстановительных реакций. При электролизе полуреакции разделены в пространстве: восстановление происходит только на катоде, а окисление – на противоположном электроде — аноде.
Окислительное и восстановительное действие электрического тока намного сильнее действия обычных химических веществ. Только с помощью тока ученым удалось получить наиболее активные простые вещества – натрий, калий и фтор. Пионером в использовании электрического тока в химии был английский ученый Гемфри Дэви. Подвергая электролизу расплавы различных соединений, он открыл восемь неизвестных до него химических элементов.
Электролиз растворов электролитов
В водных растворах процессы электролиза осложняются присутствием воды, которая проявляет двойственную природу: она может проявлять свойства и окислителя, и восстановителя. На катоде вода может принимать электроны, и тогда атомы водорода в ней будут восстанавливаются до газообразного водорода:
$K^-: hspace{0.5cm} 2H_2O + 2e^- rightarrow H_2uparrow + 2OH^–$.
На аноде вода может отдавать электроны, при этом атомы кислорода будут окисляться до газообразного кислорода:
$A^+: hspace{0.5cm} 2H_2O – 4e^- rightarrow O_2 + 4H^+$.
Другими словами, при электролизе растворов электролитов (чаще всего солей) на катоде и аноде протекают конкурирующие процессы: катионы металла $Me^{+n}$ конкурируют с катионами водорода $H^+$, а анионы кислотных остатков $An^{n-}$ конкурируют с анионами гидроксильных групп $(OH)^-$. Рассмотрим подробнее процессы, протекающие на электродах.
ЗАКОНОМЕРНОСТИ ПРОЦЕССОВ НА КАТОДЕ
На отрицательно заряженном электроде — катоде, происходит восстановление катионов, которое не зависит от материала катода, из которого он сделан, но зависит от активности металла, т.е. от положения металла в электрохимическом ряду напряжения (ЭХР). (Сравниваем окислительную способность, то есть способность принимать электроны, ионов металлов и иона водорода)

| Li K Ca Na Mg Al | Mn Zn Fe Ni Sn Pb | Cu Hg Ag Pt Au |
|---|---|---|
$Me^+n bar{e} ne$ $2H_2O + 2bar{e} =H_2 + 2OH^-$ | $Me^{+n} + n bar{e} = Me^0$ $2 H_2O + 2bar{e} = H_2 + 2OH^-$ | $Me^{+n} + n bar{e} = Me^0$ |
На катоде всегда восстанавливаются молекулы воды | На катоде могут восстанавливаться и ионы металла, и воды в зависимости от плотности тока, Т и концентрации соли | На катоде всегда восстанавливаются ионы металлов |
Если соль образована активным металлом, стоящим в ряду напряжения до марганца, на катоде не восстанавливаются катионы металла, а происходит восстановление воды с выделением газообразного водорода.
Если металл, образующий соль средней активности (после алюминия, но до водорода), то на катоде возможны два конкурирующих процесса: и восстановление воды, и восстановление катионов металла. Преобладание того или иного процесса зависит от плотности тока, температуры и концентрации соли.
Легче всего принимаю электроны неактивные металлы (стоящие в ЭХР после Н), поэтому они легко восстанавливаются на катоде до простого вещества — металла.
Закономерности процессов на аноде
Процесс на положительно заряженном электроде — аноде зависит от материала анода и от природы аниона. При электролизе растворов электролитов на аноде происходит окисление анионов. Образующийся продукт зависит от восстановительной активности аниона кислотного остатка.
Ряд восстановительной активности анионов (уменьшается). По способности окисляться анионы располагаются в следующем порядке:
$J^- hspace{6pt} > hspace{6pt} Br^- hspace{6pt} > hspace{6pt} S^{2-} hspace{6pt} > hspace{6pt} Cl^- hspace{6pt} > hspace{6pt} OH^- hspace{6pt} > hspace{6pt} SO_4^{2-} hspace{6pt} > hspace{6pt} NO_3^- hspace{6pt} > hspace{6pt} F^-$
Анод может быть растворимым и нерастворимым (инертным).
Запомни!
1. Растворимый анод при электролизе, как правило, растворяется с образованием катионов металла анода.
2. На нерастворимом аноде, если кислотный остаток соли бескислородный (кроме фторидов!), происходит окисление аниона до простого вещества — неметалла.
3. Если в состав соли входит остаток кислородсодержащей кислоты, то на аноде происходит окисление воды и выделяется кислород.
| Анод | Кислотный остаток | |||
|---|---|---|---|---|
бескислородный $Cl^-, Br^-, I^-, S^{2-} $ | кислородсодержащий $NO_3^-, SO_4^{2-}, PO_4^{3-}, F^-$ | |||
на аноде окисляются ионы кислотного остатка | на аноде окисляются молекулы воды | |||
| нерастворимый | Окисление аниона (кроме фторидов): $Ac^{ m-} — mbar{e} = Ac^0$ | В щелочной среде: $4OH^- – 4bar{e} rightarrow 2H_2O + O_2$ В кислой, нейтральной среде: $2H_2O – 4bar{e} rightarrow 4H^+ + O_2$ | ||
| растворимый | Окисление металла анода: $Me^0- nbar{e}= Me^{+n}$ анод раствор | |||
Рассмотрим процесс электролиза растворов электролитов на конкретных примерах.
Пример 1
Электролиз раствора соли активного металла и бескислородной кислоты
$NaCl leftrightarrow Na^+ + Cl^−$
Рассмотрим полуреакции окисления и восстановления. Натрий – активный металл, он стоит в ряду напряжений левее водорода, поэтому на катоде восстанавливается вода и выделяется водород. Хлорид-ион не содержит атомов кислорода, поэтому на аноде он окисляется и выделяется хлор:
K»катод»(-): $2H_2O + 2bar{e} = H_2 uparrow+ 2OH^−hspace{0.2cm} | 1$
A»анод»(+): $2Cl^- − 1bar{e} cdot 2 = Cl_2 uparrow hspace{1.1cm} |1$
При сложении уравнений полуреакций получаем сокращенное ионное уравнение электролиза:
$mathrm{2Cl^– + 2H_2O rightarrow H_2 + Cl_2 + 2 OH^–}$.
Если добавить в левую и правую часть по два иона $mathrm{Na^+}$, которые в самом электролизе не участвуют, получим молекулярное уравнение электролиза раствора хлорида натрия:
$Sigma: hspace{0.5cm} 2NaCl (p-p) + 2H_2O xrightarrow[]{textrm{эл.ток}} H_2 uparrow + Cl_2 uparrow+2NaOH$
Мы видим, что при электролизе раствора такого широко доступного и дешевого вещества, как хлорид натрия, получилось сразу три ценных продукта: водород, хлор и щелочь. Именно поэтому электролиз широко используется в разных отраслях промышленности. С его помощью получают химически чистые металлы и удаляют растворимые примеси из воды.
Пример 2
Электролиз раствора соли активного металла и кислородсодержащей кислоты
$Na_2SO_4 (p-p)leftrightarrow 2Na^++SO_4^{2−}$
K(-): $2H_2O + 2bar{e} = H_2 uparrow+ 2OH^−hspace{0.3cm} | 2$
A(+): $2H_2O — 4bar{e} = O_2 uparrow+ 4H^+hspace{0.5cm} | 1$
Если первое уравнение умножить на 2 и сложить со вторым уравнением, получим:
$2cdot2H_2O + 2H_2O= 2H_2 + O_2 + 4H^+ + 2cdot 2OH^–$
$6H_2O= 2H_2 + O_2 + 4H^+ + 4OH^–$.
Ионы водорода и гидроксид-ионы реагируют друг с другом:
$mathrm{4H^+ + 4OH^– = 4H_2O}$
После сокращения молекул воды в левой и правой частях получаем полное уравнение электролиза:
$Sigma: hspace{0.5cm} 2H_2O xrightarrow[]{textrm{эл.ток}} 2H_2 uparrow + O_2 uparrow$
Пример 3
Электролиз раствора гидроксида активного металла
$NaOH (p-p) leftrightarrow Na^+ + OH^−$
K(-): $2H_2O + 2bar{e} = H_2 uparrow + 2OH^−$
A(+): $2H_2O — 4bar{e} = O_2 uparrow + 4H^+$
$Sigma: hspace{0.5cm} 2H_2O xrightarrow[]{textrm{эл.ток}} 2H_2 uparrow + O_2 uparrow$
Пример 4
Электролиз раствора соли среднеактивного металла и бескислородной кислоты
$ZnCl_2 leftrightarrow Zn^{2+} + 2Cl^−$
K»катод»(-): $Zn^{2+} + 2bar{e} = Zn^0$
$2H_2O + 2bar{e} = H_2 uparrow + 2OH^−$
A»анод»(+): $2Cl^- − 1bar{e} cdot 2 = Cl_2 uparrow$
$Sigma: hspace{0.5cm} 2ZnCl_2(p-p) + 2H_2O xrightarrow[]{textrm{эл.ток}} Zn +H_2uparrow + Zn(OH)_2downarrow + 2Cl_2 uparrow$
Обратите внимание, что при электролизе водных растворов солей среднеактивных металлов на катоде одновременно выделяется и металл и водород.
Иногда, в рамках решения ЕГЭ, требуется упрощенная запись этого процесса. В таком случае следует записать только выделение водорода на катоде (основной процесс):
$Sigma: hspace{0.5cm} ZnCl_2(p-p) + 2H_2O xrightarrow[]{textrm{эл.ток}} H_2uparrow + + Zn(OH)_2downarrow + Cl_2 uparrow$
Пример 5
Электролиз раствора соли среднеактивного металла и кислородсодержащей кислоты
$ZnSO_4 (p-p) leftrightarrow Zn^{2+} +SO_4^{2−}$
K(-): $Zn^{2+} + 2bar{e} = Zn^0$
$2H_2O + 2bar{e} = H_2 uparrow + 2OH^−$
A(+): $2H_2O — 4bar{e} = O_2 uparrow + 4H^+$
$Sigma: hspace{0.5cm} 2ZnSO_4 (p-p)+ 4H_2O xrightarrow[]{textrm{эл.ток}} Zn + +H_2uparrow + Zn(OH)_2downarrow + 2H_2SO_4 + O_2 uparrow$
Иногда, в рамках решения ЕГЭ, требуется упрощенная запись этого процесса. В таком случае следует записать только выделение водорода на катоде (основной процесс):
$Sigma: hspace{0.5cm} 2ZnSO_4 (p-p)+ 2H_2O xrightarrow[]{textrm{эл.ток}} 2Zn + 2H_2SO_4 + O_2 uparrow$
Пример 6
Электролиз гидроксида менее активного металла :
$Fe(OH)_3xrightarrow[]{textrm{эл.ток}} ne$
невозможно (нерастворим)
Полный курс химии вы можете найти на моем сайте CHEMEGE.RU. Чтобы получать актуальные материалы и новости ЕГЭ по химии, вступайте в мою группу в ВКонтакте или на Facebook. Если вы хотите подготовиться к ЕГЭ по химии на высокие баллы, приглашаю на занятия (индивидуальные, в мини-группах, очно и онлайн) или на онлайн-курс «40 шагов к 100 баллам на ЕГЭ по химии«.
Тел. для записи на занятия +79778345628, e-mail: ste-vn@ya.ru, профиль Вконтакте.
Друзья! Вот и состоялся долгожданный экзамен по химии 2020 года, к которому вы столько готовились. А кто-то еще будет сдавать химию 24 июля или в резервные дни. Прошедший экзамен заставил о многом задуматься. Мы видели много грустных лиц, слез и волнений. Я не буду сейчас давать оценки составителям и участникам экзамена, а просто выложу некоторые условия и решения задач 34 на так называемую «атомистику». Некоторые из этих заданий вызвали сложности у участников экзамена.
Остановимся на задаче на атомистику с запутанным материальным балансом:
1. Смесь оксида кальция и карбоната кальция с массовой долей кальция 62,5% растворили в 300 г раствора соляной кислоты. Масса раствора стала 361,6 г. Выделившийся газ пропустили через 80 г 10%-ного раствора гидроксида натрия. Вычислите массовую долю соли в конечном растворе.
Пусть n(CaO) = х моль, n(CaCO3) = y моль, тогда:
количество вещества атомов кальция в оксида n1(Ca) = х моль, в карбонате: n₂(Са) = у моль,
общее количество вещества атомов кальция: n(Са) = (x + y) моль.
Масса атомов кальция: m(Ca) = n(Са)·M(Ca) = 40(x + y) г.
Масса оксида кальция: m(CaО) = n(СаО)·M(CaО) = 56x г.
Масса карбоната кальция: m(CaCO3) = n(CaCO3)·M(CaCO3) = 100у г.
Масса смеси: mсм = m(CaО) + m(CaCO3) = (56х + 100у) г
Получаем выражение:
40(x + y)/(56х + 100у) = 0,625
Преобразуя приведённое выше равенство, получаем х = 4,5у.
Далее протекают реакции:
CaO + 2HCl = CaCl₂ + H2O
CaCO3 + 2HCl = CaCl + CO₂ + H₂O
Количество образовавшегося углекислого газа n(CO₂) = y моль, масса m(CO₂ ) = 44y г.
Запишем уравнение материального баланса для конечного раствора:
mр-ра = m(CaO) + m(CaCO3) + mр-ра(HCl) — m(CO₂)
361,6 = 56х + 100у + 300 — 44у
или
61,6 = 56х + 56у
Получаем систему:
х + у = 1,1
х = 4,5у
5,5у = 1,1
у = 0,2 моль, х = 0,9 моль.
Количество углекислого газа: n(CO₂) = 0,2 моль, масса m(CO₂) = 44·0,2 = 8,8 г.
При взаимодействии углекислого газа с гидроксидом натрия возможно образование средней или кислой соли:
2NaOH + CO₂ = Na₂CO3 + H₂O (1)
NaOH + CO₂ = NaHCO3 (2)
Какие продукты образуются, определяется соотношением количества вещества реагентов.
Масса щелочи: m(NaOH) = mр-ра(NaOH) · ω(NaOH) = 80 · 0,1 = 8 г
Количество вещества: n(NaOH) = m(NaOH) / M(NaOH) = 8/40 = 0,2 моль
Соотношение количества вещества реагентов n(NaOH):n(CO₂) = 0,2:0,2 = 1:1
Следовательно, протекает только вторая реакция с образованием кислой соли — гидрокарбоната натрия.
n(NaHCO3) = n(CO₂) = 0,2 моль
m(NaHCO3) = n(NaHCO3)·M(NaHCO3) = 0,2·84 = 16,8 г
Масса конечного раствора гидрокарбоната:
mр-ра = m(CO₂) + mр-ра(NaOH) = 8,8 + 80 = 88,8 г
Массовая доля гидрокарбоната натрия в конечном растворе:
ω(NaHCO3) = m(NaHCO3)/mр-ра = 16,8/88,8 = 0,1892 или 18,92%
Ответ: ω(NaHCO3) = 18,92%
Как видите, задача вполне решаемая, хотя в условиях экзамена решить ее верно «с нуля» очень сложно и не все с этим могут справиться.
Холодный раствор серной кислоты реагирует с пероксидом бария без ОВР:
H2SO4 + BaO2 = BaSO4 + H2O2
При этом в растворе присутствует пероксид водорода, а сульфат бария выпадает в осадок.
Пусть n(H2O2) = х моль, n(H2O) = y моль, тогда:
количество вещества атомов водорода в пероксиде n1(H) = 2х моль, в воде: n2(Н) = 2у моль,
количество вещества атомов кислорода в пероксиде n1(О) = 2х моль, в воде: n2(О) = у моль,
общее количество вещества атомов водорода: n(Н) = (2x + 2y) моль,
общее количество вещества атомов кислорода: n(О) = (2x + y) моль.
Получаем соотношение:
(2x + 2y)/(2x + y) = 9/5
Упрощаем его:
у = 8х
При добавлении каталитического количества оксида марганца (IV) пероксид водорода разлагается:
2H2O2 = 2H2O + O2
Пусть весь пероксид водорода разложился, тогда изменение массы раствора равно массе выделившегося газа, то есть массе кислорода:
m(O2) = 6,4 г
n(O2) = m(O2)/M(O2) = 6,4 / 32 = 0,2 моль
Отсюда
n(H2O2) = 2·n(O2) = 2·0,2 = 0,4 моль
х = 0,4 моль
у = 3,2 моль
Отсюда количество вещества серной кислоты с исходном растворе:
n(H2SO4) = n(H2O2) = 0,4 моль
m(H2SO4) = n(H2SO4)·M(H2SO4) = 0,4·98 = 39,2 г
Количество и масса воды не изменялись:
m(H2O) = n(H2O)·M(H2O) = 3,2·18 = 57,6 г
Массовая доля серной кислоты в исходном растворе:
ω(H2SO4) = m(H2SO4)/(m(H2O)+ m(H2SO4)) = 39,2/(39,2 + 57,6) = 0,405 или 40,5%
Ответ: ω(H2SO4) = 40,5%
Рассмотрим еще одну задачу из реального ЕГЭ, которая вызвала сложности:
2. Дан холодный раствор серной кислоты. К нему добавили пероксид бария, при этом вещества прореагировали полностью. В полученном растворе соотношение атомов водорода к кислороду составило 9 к 5. Затем к этому раствору добавили каталитическое количество оксида марганца (IV), в результате масса раствора уменьшилась на 6,4 г. Вычислите массовую долю серной кислоты в исходном растворе.
Другие задачи из реального экзамена по химии:
3. Взяли смесь меди и оксида меди (II) . Массовая доля меди в смеси 96%. Полученную смесь растворили в концентрированной серной кислоте массой 496 г, взятой в избытке. Полученный газ растворили в необходимом количестве раствора гидроксида натрия массой 200 г и массовой долей 10%. Найдите массовую долю соли в растворе после растворения.
4. Смесь из оксида и сульфида алюминия, где массовая доля алюминия 50%, залили 700 г, раствора соляной кислоты, взятой в избытке. Выделившийся газ полностью поглотили 240 г 20% раствора сульфата меди. Вычислите концентрацию соли после того, как залили соляную кислоту.
5. В смеси оксида магния и фосфида магния массовая доля атомов магния равна 54,4%. Они полностью прореагировала с соляной кислотой массой 365 г 34-% раствора. К полученному раствору добавили раствор фторида калия массой 232 грамма 30-% раствора. Найти массовую долю хлорида калия в конечном растворе.
6. Смесь оксида и пероксида натрия, в которой соотношение атомов натрия к атомам кислорода равно 3:2, нагрели с избытком углекислого газа. Полученное вещество растворили в воде. В результате образовалось 600 г раствора. К полученному раствору добавили 229,6 г раствора хлорида железа(III).Найдите массовую долю оксида натрия в исходной смеси, если масса конечного раствора 795 г и массовая доля карбоната натрия в этом растворе 4%.
7. Смесь карбида алюминия и карбида кальция, в которой массовая доля углерода равна 30%, полностью растворили в 547.5 г соляной кислоте. При этом кислота прореагировала без остатка. К образовавшемуся раствору добавили 1260г 8% раствора гидрокарбоната натрия. Найдите массовую долю кислоты в растворе, в котором растворили исходную смесь.
8. В смесь железной окалины и оксида железа(III) добавили 500 г раствора конц. азотной кислоты, причём соотношение атомов железа к атомам кислорода в смеси равно 7:10. Чтобы полностью поглотить выделившийся газ использовали 20 г раствора NaOH с массовой долей 20%. Найдите массу соли, образовавшейся при добавлении кислоты в смесь.
9. Дана смесь оксида и пероксида бария, в которой число атомов бария относится к числу атомов кислорода как 5:9. Добавили 490 г 20% холодной серной кислоты при этом смесь прореагировала полностью и раствор стал нейтральным. Определить массовую долю воды в полученном растворе.
10. Смесь из оксида лития и нитрида лития с массовой долей атомов лития 56%, смешали с 265 г раствора соляной кислоты с массовой долей 20%. (все вещества полностью прореагировали). После к образовавшемуся раствору добавили 410г 20%- ного фосфата натрия. Найдите массовую долю образовавшегося хлорида натрия.
11. Взяли смесь оксида кальция и карбоната кальция. Массовая доля кальция в смеси 50%. Смесь растворили в 300 г раствора избытка соляной кислоты. Выделившийся газ полностью прореагировал с раствором гидроксида натрия массой 200г и массовой долей 8%. Вычислите массовую долю образовавшейся соли.
12-Окт-2012 | комментариев 59 | Лолита Окольнова
Тема электролиза довольна большая, формул в ней много и, как мне кажется, больше ее изучают на уроках физики… Я хочу рассмотреть ту часть, которая касается химии, и при этом только формат ЕГЭ — электролиз водных растворов солей.
Электролиз водных растворов солей
Для начала давайте представим себе систему, в которой происходит электролиз.
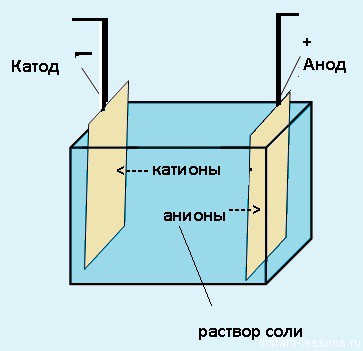
Электролиз — физико-химический процесс, состоящий в выделении на электродах составных частей растворённых веществ или других веществ, который возникает при прохождении электрического тока через раствор либо расплав электролита.
Электроды — это такие пластинки или стержни, опущенные в раствор, они подключены к источнику тока.
- Анод — положительно заряженный электрод
- Катод — отрицательно заряженный электрод
Мы будем рассматривать случай инертных электродов — т.е. они не будут вступать ни в какие химические реакции.
При пропускании электрического тока, вещество раствора будет претерпевать химические изменения, т.е. буду образовываться новые химические вещества. Они будут притягиваться к электродам следующим образом:
- Неметаллы и их производны, анионы — к аноду
- Металлы и их производный, катионы — к катоду
Теперь рассмотрим электролиз водных растворов различных солей
Для этого нам понадобится ряд активности металлов электрохимический ряд напряжений:
![]()
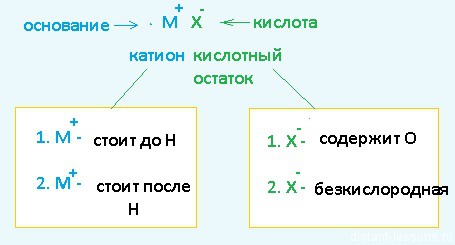
Разберем сначала катионы:
- Если металл стоит до Н, то вместо него электролизу подвергается вода:
2H2O + 2е = H2 + 2OH– Образовавшийся водород H2 идет к катоду - Если металл стоит после Н, то он сам восстанавливается:
Cu2+ + 2е = Cu0 Медь осаждается на катоде - Катионы металлов, стоящие в ряду напряжений после алюминия до водорода, могут восстанавливаться вместе с молекулами воды:
2Н2О + 2е = Н2 + 2ОН—Zn2+ + 2e = Zn0

Теперь анионы-кислотные остатки:
- Кислородсодержащие кислотные остатки — вместо них электролизу подвергается вода:
2H2O — 4e = O2 + 4H+ Образовавшийся O2 выделяется на аноде - Бескислородные кислотные остатки — окисляются до простого вещества:
Cl− — 1e = Cl20 Хлор выделяется на аноде - Исключение: F− — вместо него будет выделяться кислород.
Примеры:
1.1. Катион стоит в ряду до Н, кислотный остаток содержит кислород О:
K2SO4↔2K++SO42−
K(-): 2H2O + 2e = H2 + 2OH−
A(+): 2H2O — 4e = O2 + 4H+
2H2O (электролиз) → 2H2 + O2
1.2. Катион стоит в ряду до Н, кислотный остаток беcкислородный:
LiCl ↔ Li+ + Cl−
катод (-): 2H2O + 2e = H2 + 2OH−
анод (+): Cl− — 1e = Cl0; Cl0+Cl0=Cl2
2LiCl + 2H2O(электролиз) → H2 + Cl2 +2LiOH
2.1. Катион стоит в ряду после Н, кислотный остаток содержит кислород О:
СuSO4 ↔ Cu2++SO42−
K(-): Cu2+ + 2e = Cu0
A(+): 2H2O — 4e = O2 + 4Н+
2CuSO4 + 2H2O(электролиз) → 2Cu + 2H2SO4 + O2
2.2. Катион стоит в ряду после Н, кислотный остаток беcкислородный:
катод (-): Cu2+ + 2e = Cu0
анод (+): 2Cl− — 2e = 2Cl0
CuCl2 (электролиз) →Cu + Cl2

Электролиз водных растворов солей отличается от электролиза расплавов.
Отличие — в наличии растворителя. При электролизе водных растворов солей кроме ионов самого вещества в процессе участвуют ионы растворителя. При электролизе расплавов — только ионы самого вещества.
- ЕГЭ это вопрос Части B № 3
Тест «Электролиз»
1. Щелочь образуется при электролизе водного раствора:
хлорида калия
хлорида меди
хлорида цинка
хлорида алюминия
2. При электролизе водного раствора сульфата натрия на катоде и аноде выделяются, соответственно:
натрий и кислород
водород и кислород
водород и оксид серы
натрий и оксид серы
3. Металл выделяется при электролизе водного раствора:
ацетата калия
хлорида цинка
нитрата серебра
гидроксида магния
4. Лакмус становится красным при электролизе раствора:
нитрата серебра
хлорида серебра
нитрата натрия
сульфата натрия
5. При электролизе раствора KF на катоде и аноде выделятся, соответственно:
калий и фтор
калий и кислород
водород и фтор
водород и кислород
6. На катоде — восстановление воды, на аноде — окисление кислотного остатка при электролизе раствора:
Na2S
Na2SO3
NaF
NaNO3
7. Этан можно получить электролизом:
водного раствора метанола
водного раствора ацетата натрия
водного раствора этилата натрия
водного раствора бутанола
8. При электролизе водного раствора KF на аноде выделяется:
фтор
фтороводород
кислород
калий
9. При электролизе 400 г 20 %-ого раствора NaCl на катоде выделилось 11,2 л (н.у.) газа. Степень разложения NaCl:
25%
73%
24%
50%
10. Уравнение анодного процесса электролиза раствора AgNO3 соответствует реакции:
2NO3(-) -2e → 2NO2 + O2
2H2O + 2e → H2 + 2OH(-)
2H2O – 4e → O2 + 4H(+)
2NO3(-) -2e → 2NO + 2O2
Категории:
|
Обсуждение: «Электролиз водных растворов солей»
(Правила комментирования)
