Какие особенности воды обеспечивают ей свойство растворителя

Вода как растворитель играет предельно важную роль далеко не только в плане нашего быта. Исследователи давно говорят, что данное волшебное соединение является основой для образования жизни вообще. И именно поэтому его наличие выступает обязательным условием для существования чего-то более сложного, нежели неживая природа.
Растворимость тех или иных химических элементов напрямую связана с существованием воды, так как она чаще всего выступает той средой, которая преобразует все вокруг себя и создает новые формы органической и неорганической материи.
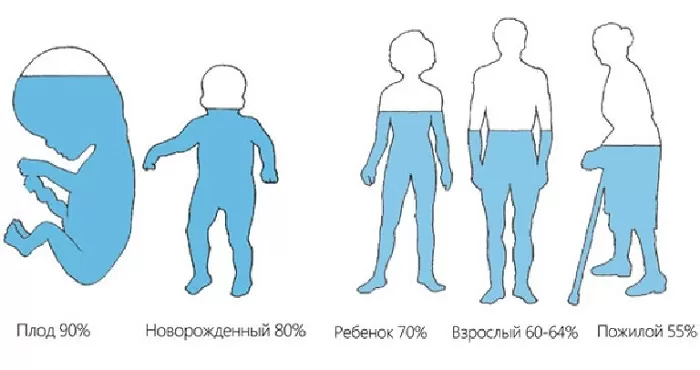
Человек примерно на 70% состоит из воды (имеется ввиду кровь, межклеточная жидкость, плазма крови и прочие вещества), у большинства других существ этот показатель колеблется от 50 до 95%. Очевидно, что свойства данного соединения оказывают решающую роль на происходящие вокруг нас и внутри нас процессы синтеза, регенерации и многие другие.
Это универсальный растворитель, который буквально формирует окружающий мир, постоянно преображает и обновляет его!
Свойства воды как растворителя
Вода – сложное вещество, отличающееся многими уникальными характеристиками, которые нельзя встретить больше нигде.
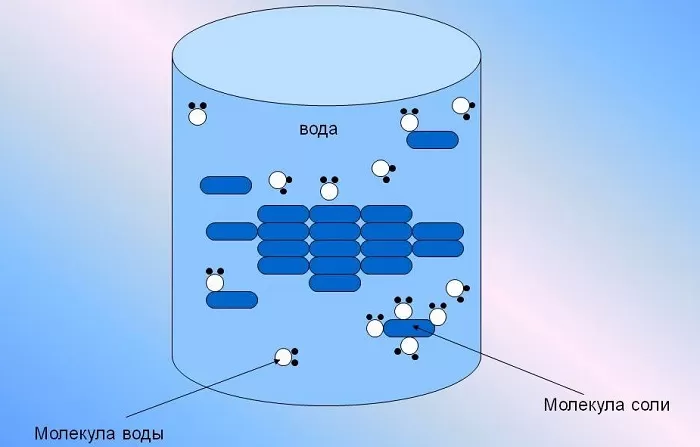
Она способна растворить большую часть существующих в природе комплексных соединений, содержащих в своей структуре молекулы как с положительными, так и отрицательными ионами одновременно.
При проведении так называемых кинетических исследований все растворы также изготавливаются на основе H2O.
Яркий пример особенности воды – при схожести по своей структуре с метаном CH4, она имеет температуру кипения выше на целых 250С!
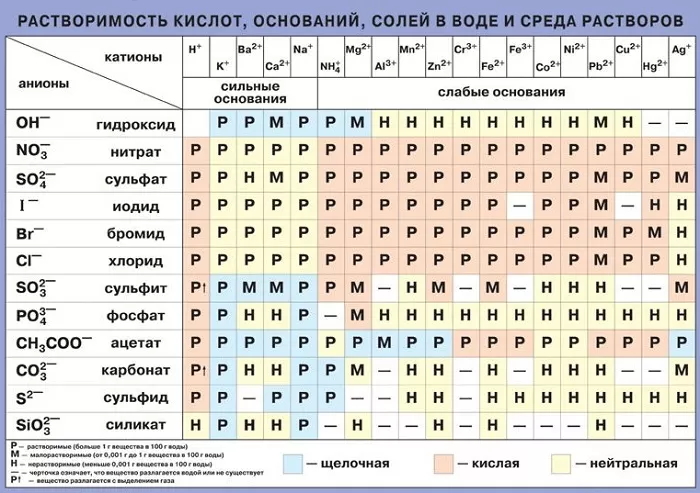
Важную роль играет также ее способность выступать одновременно либо донором, либо акцептором частиц водорода, благодаря чему проходят многие химические процессы. Химия говорит нам еще и о том, что вода выступает идеальным растворителем для диссоциирующих соединений.
Интересно отметить, что по причине высокого уровня диэлектрической проницаемости, вода отлично экранирует электрические поля ионов друг от друга. Благодаря этому притяжение противоположно заряженных частиц в воде снижается примерно в 80 раз.
Какие вещества растворяются в воде
Даже если школьник ходит только в 3 класс, он наверняка может привести примеры материалов, которые боятся контакта с водой, или, другими словами, растворяются в ней и теряют свои свойства.

Вот перечень только некоторых веществ такого типа:
К хорошо растворимым относятся: соль, сахар, сода, хлориды, щелочные металлы и нитраты, а также бромиды. Воздух также претерпевает изменения при контакте с жидкой средой. Крахмал полностью растворим, спирт тоже.
К средней степени взаимодействия относятся: бертолетова соль, метан, гипс, кислород, азот, другие химические элементы, например, сульфаты, некоторые газообразные вещества.
Есть и такие материалы, которые являются нерастворимыми: сульфид меди, стекло, золото, керосин, серебро, растительный жир и многие другие. Правда, при некоторых условиях даже они не способны устоять от такого мощного воздействия.
В организме человека есть целая группа витаминов (С, В1, 2, 3(РР), В12 и другие), которые способны оказывать свое положительное воздействие на здоровье только в контакте с H2O. Это касается также и фолиевой кислоты, биотина и т. д.
Что не растворяется в воде
Существуют такие химические образования, которые не воспринимают воздействия воды в качестве растворителя совсем.

Хороший пример: углерод С, который находится в простом карандаше, многие металлы и сплавы, типа алюминия, а также золото, серебро, медь.
Такая ситуация складывается благодаря тому, что между молекулами и атомами нерастворимых веществ действуют сильные связи, которые водород разрушить не в состоянии. Полярное состояние молекулы также способствует большей прочности материала, который состоит из таких частиц.
Многие вещи, которые мы видим вокруг себя в быту, также являются нерастворимыми. Очень популярный пример – пластик.

В мировом океане плавает огромное пятно из пластикового мусора, которое ежегодно растет, и количество пластмассы там совершенно не желает уменьшаться естественным путем. Его не могут никак переработать, что очень плохо для всей экосистемы.
Именно поэтому экологи бьют тревогу и в ЕС уже сейчас планируется отказ от целлофановых пакетов, пластиковых стаканчиков и трубочек и тому подобные меры.
Значение воды как растворителя
Как уже упоминалось в начале статьи, рассматриваемые свойства воды являются ключевыми для всей живой и неживой природы нашей планеты.

Если бы она не обладала этими характеристиками, то большинство химических процессов на Земле, в живых организмах, в органической природе бы просто остановилось. Картинка такого мира была бы очень неутешительна – темная пустыня без признаков жизни.
Роль воды настолько огромна, что именно ее определение в далеких планетах и галактиках является для астрономов основным занятием в надежде когда-то отыскать там если не разумное существование, то хотя бы зачатки жизни.
Вода (H2O) — важнейшее неорганическое вещество клетки. В клетке в количественном отношении вода занимает первое место среди других химических соединений. Вода выполняет различные функции: сохранение объёма, упругости клетки, участие во всех химических реакциях. Все биохимические реакции происходят в водных растворах. Чем выше интенсивность обмена веществ в той или иной клетке, тем больше в ней содержится воды.
Обрати внимание!
Вода в клетке находится в двух формах: свободной и связанной.
Свободная вода находится в межклеточных пространствах, сосудах, вакуолях, полостях органов. Она служит для переноса веществ из окружающей среды в клетку и наоборот.
Связанная вода входит в состав некоторых клеточных структур, находясь между молекулами белка, мембранами, волокнами, и соединена с некоторыми белками.
Вода обладает рядом свойств, имеющих исключительное значение для живых организмов.
Структура молекулы воды
Уникальные свойства воды определяются структурой её молекулы.
Между отдельными молекулами воды образуются водородные связи, определяющие физические и химические свойства воды.
Характерное расположение электронов в молекуле воды придаёт ей электрическую асимметрию. Более электроотрицательный атом кислорода притягивает электроны атомов водорода сильнее, в результате молекула воды является диполем (обладает полярностью). Каждый из двух атомов водорода обладает частично положительным зарядом, а атом кислорода несёт частично отрицательный заряд.
Частично отрицательный заряд атома кислорода одной молекулы воды притягивается частично положительными атомами водорода других молекул. Таким образом, каждая молекула воды стремится связаться водородной связью с четырьмя соседними молекулами воды.
Свойства воды
Так как молекулы воды полярны, то вода обладает свойством растворять полярные молекулы других веществ.
Вещества, растворимые в воде, называются гидрофильными (соли, сахара, простые спирты, аминокислоты, неорганические кислоты). Когда вещество переходит в раствор, его молекулы или ионы могут двигаться более свободно и, следовательно, реакционная способность вещества возрастает.
Вещества, нерастворимые в воде, называются гидрофобными (жиры, нуклеиновые кислоты, некоторые белки). Такие вещества могут образовывать с водой поверхности раздела, на которых протекают многие химические реакции. Следовательно, тот факт, что вода не растворяет некоторые вещества, для живых организмов также очень важен.
Вода обладает высокой удельной теплоёмкостью, т. е. способностью поглощать тепловую энергию при минимальном повышении собственной температуры. Чтобы разорвать многочисленные водородные связи, имеющиеся между молекулами воды, требуется поглотить большое количество энергии. Это свойство воды обеспечивает поддержание теплового баланса в организме. Большая теплоёмкость воды защищает ткани организма от быстрого и сильного повышения температуры.
Для испарения воды необходима довольно большая энергия. Использование значительного количества энергии на разрыв водородных связей при испарении способствует его охлаждению. Это свойство воды предохраняет организм от перегрева.
Пример:
примерами этого могут являться транспирация у растений и потоотделение у животных.
Вода обладает также высокой теплопроводностью, обеспечивая равномерное распределение тепла по всему организму.
Обрати внимание!
Высокая удельная теплоёмкость и высокая теплопроводность делает воду идеальной жидкостью для поддержания теплового равновесия клетки и организма.
Вода практически не сжимается, создавая тургорное давление, определяя объём и упругость клеток и тканей.
Пример:
гидростатический скелет поддерживает форму у круглых червей, медуз и других организмов.
Благодаря силам сцепления молекул на поверхности воды создаётся плёнка, обладающая такой характеристикой, как поверхностное натяжение.
Пример:
благодаря силе поверхностного натяжения происходит капиллярный кровоток, восходящий и нисходящий токи растворов в растениях.
К числу важных в физиологическом отношении свойств воды относится её способность растворять газы (O2, CO2 и др.).
Вода является также источником кислорода и водорода, выделяемых при фотолизе в световую фазу фотосинтеза.
Биологические функции воды
- Вода обеспечивает передвижение веществ в клетке и организме, поглощение веществ и выведение продуктов метаболизма. В природе вода переносит продукты жизнедеятельности в почву и к водоёмам.
- Вода — активный участник реакций обмена веществ.
- Вода участвует в образовании смазывающих жидкостей и слизей, секретов и соков в организме (эти жидкости находятся в суставах позвоночных животных, в плевральной полости, в околосердечной сумке).
- Вода входит в состав слизей, которые облегчают передвижение веществ по кишечнику, создают влажную среду на слизистых оболочках дыхательных путей. Водную основу имеют и секреты, выделяемые некоторыми железами и органами: слюна, слёзы, желчь, сперма и т. д.
Источники:
Каменский А. А., Криксунов Е. А., Пасечник В. В. Биология. 9 класс // ДРОФА.
Каменский А. А., Криксунов Е. А., Пасечник В. В. Биология. Общая биология (базовый уровень) 10–11 класс // ДРОФА.
Лернер Г. И. Биология: Полный справочник для подготовки к ЕГЭ: АСТ, Астрель.
https://infourok.ru/prezentaciya_po_biologii_na_temu_mineralnye_veschestva_i_voda-409343.htm
https://otvet.mail.ru/question/182353364
https://www.studfiles.ru/html/2706/741/html_fBK8q_mH0r.UWHS/htmlconvd-PYhDG9_html_1c3325a2.png
Вода — неорганическое вещество, молекулы которого состоят из двух атомов водорода и одного атома кислорода. Количество воды неодинакова в разных организмах. Больше всего воды содержит тело медуз (95-98%), водоросли (более 80%), меньше всего ее у насекомых (40-50%), слоевища лишайников (5-7%). В теле млекопитающих в среднем 75% воды, в том числе у человека — 60-65% массы тела. Количество воды неодинакова и в различных тканях и органах одного и того же организма. Например, у человека содержание воды в тканях и органах таков: кровь (83,0%), почки (82,7%), сердце (79,2%), легкие (79,0%), мышцы (75 6%), мозг (74,8%), кожа (72,0%), скелет (22,0%), жировая ткань (10,0%).
Большая часть воды (70% объема) находится в клетках тела в свободном и связанном виде, меньшая часть (30% объема) — перемещается во внеклеточном пространстве организма и находится в свободном состоянии. Связанная вода (4 5%) бывает осмотически связанной (вода в связях с ионами и низкомолекулярными соединениями), коллоидно связанной (вода в связях как с внутренними, так и с расположенными на поверхности химическими группами высокомолекулярных соединений) и структурно свя связанной (вода в замкнутом пространстве высокомолекулярных биополимеров сложной структуры). Свободная вода (95-96%) является универсальным растворителем.
Значение воды . Количественно вода занимает первое место среди химических соединений любой которой клетки. Наличие воды является обязательным условием жизнедеятельности организмов. Какие же функции выполняет в биосистемах эта самая распространенная на Земле вещество?
• Вода — универсальный растворитель для ионных и многих ковалентных соединений, обеспечивает протекание химических реакций, транспорт веществ в клетку и из клетки.
• Вода — реагент, при участии которого в клетках происходят реакции гидролиза и гидратации, окислительно-восстановительные и кислотно-основные реакции.
• Вода — теплорегулятор, поддерживает оптимальный тепловой режим организмов и обеспечивает равномерное распределение тепла в живых системах.
• Вода — осморегулятора, что обеспечивает форму клеток, транспорт неорганических веществ.
• Вода — опора, обеспечивает упругий состояние клеток (тургор), выступает амортизатором от механических воздействий на организм, выполняет функцию гидроскелет у многих животных.
• Вода — средство транспорта, осуществляет связь в клетках, между клетками, тканями, органами и обеспечивает гомеостаз и функционирование организма как единого целого.
• Вода — среда обитания для водных организмов, в нем осуществляются пассивное движение, внешнее оплодотворение, распространение семян, гамет и личиночных стадий наземных организмов.
• Вода — конформатор, имеет большое значение в организации пространственной структуры (конформации) биополимеров.
Свойства воды. Роль воды в биосистемах определяется ее физико-химическими свойствами.
■ Для чистой воды характерны прозрачность, отсутствие вкуса, цвета, запаха. Природная вода всегда содержит различные примеси: растворенные вещества в виде ионов, нерастворенные вещества — в виде суспензии. Вода — единственное вещество на Земле, которая одновременно и в большом количестве встречается в жидком, твердом и газообразном состояниях.
■ Плотность воды при температуре 4 ° С является максимальной и составляет 1 г / см3. С понижением температуры плотность уменьшается, поэтому лед плавает на поверхности воды.
■ Вода имеет аномально высокие удельную теплоемкость (4,17 Дж / ГК), теплоту испарения (при температуре 100 ° С — 2253 Дж / г), теплоту таяния (при температуре 0 ° С — 333,98 Дж / г).
■ Воде свойственный исключительно большое поверхностное натяжение за счет мощных сил сцепления (когезии), связанных с образованием водородных связей между молекулами.
■ Для воды характерное свойство прилипания (адгезии), которая проявляется в случае поднятия ее против гравитационных сил.
■ Воде в жидком состоянии свойственна текучись, нестискуванисть, чем обусловлены явления осмоса и тургора.
■ Вода обладает амфотерными свойствами, то есть проявляет свойства как кислоты так и основы и участвует в кислотно-основных реакциях.
■ Вода способна выступать и как восстановитель, и как окислитель, осуществляя биологически важные окислительно-восстановительные реакции обмена веществ.
■ Молекулы воды полярны, благодаря чему участвуют в реакциях гидратации, обеспечивая растворения многих химических соединений.
■ Вода участвует в биологически важных реакциях разложения — реакциях гидролиза.
■ Молекулы воды способны диссоциировать на ионы: Н2О = Н + + ОН.
Особенности строения молекул воды. Уникальные свойства воды определяются структурой ее молекул.
В молекуле воды каждый атом водорода содержится у атома кислорода ковалентной связью, энергия которого почти 110 ккал / моль. Благодаря этому вода является очень стойкой химическим соединением. Водяной пар начинает разлагаться на О, и Н, при температуре, выше 1000 ° С.
В молекуле воды две пары электронов из четырех образованные ковалентной связью и смещены к одной из сторон молекулы с формированием двух положительно заряженных полюсов. А две другие пары остаются неразделенными и смещены относительно ядра атома кислорода к противоположной стороне, где образуют два отрицательно заряженные полюса.
Итак, молекулы воды являются полярными.
Благодаря полярности соседние молекулы воды могут взаимодействовать между собой и с молекулами полярных веществ с образованием водородных связей, обуславливающих уникальные физические свойства и биологические функции воды. Энергия этой связи, по сравнению с энергией ковалентной связи, невелика. Она составляет всего 4,5 ккал / моль, и благодаря тепловому движению эти связи между молекулами воды постоянно возникают и разрываются. Водородные связи — это связи между двумя ковалентно связанными атомами с большим значением электроотрицательности ( О, N , F ) посредством атома водорода Н. Обычно водородная связь обозначают тремя точками и этим отмечают , что он намного слабее ; чем ковалентная связь ( примерно в 15-20 раз ).
Водородные связи играют определяющую роль в образовании специфической квази и кристаллической структуры воды. Согласно современным представлениям, основой строения воды является кристаллическая решетка с размытой тепловым движением частью молекул свободной воды. Для воды в твердом состоянии характерные молекулярные кристаллические решетки, поскольку кристаллы строятся из молекул, связанных друг с другом водородными связями. Именно наличием элементов кристаллической решетки, а также дипольнистю молекул воды и обусловлено очень большое значение относительной диэлектрической проницаемости воды.
Молекулы жидкой воды способны к полимеризации или ассоциации с образованием ассоциатов (Н2О) n. Образование плотных ассоциатов происходит +4 С, чем и объясняется большое плотность воды при этой температуре. При нагревании водородные связи разрушаются и ассоциаты начинают расщепляться, поскольку энергия теплового движения становится больше от энергии этих связей. Разрыва связей требует много энергии, откуда и высокие температура кипения и удельная теплоемкость воды. Это имеет существенное значение для организмов во время колебаний температуры среды обитания.
Рентгеноструктурный анализ воды установлено, что и в жидкой воде остаются фрагменты структуры льда. При температуре 20 ° С около 70% молекул находится в воде в виде агрегатов, содержащих в среднем по 57 молекул в каждом. Такие агрегаты называют кластерами. Молекулы воды, входящих в состав кластера, скованные и метаболически инертные. Активная роль в реакциях обмена веществ принадлежит только свободным молекулам воды. Если кластеров много, то это приводит к иммобилизации воды, то есть к исключению свободной воды, ограничения ферментативных процессов и к снижению функциональной активности клетки.
БИОЛОГИЯ + При диссоциации определенных электролитов, в том числе и воды, образуются ионы Н + и ОН — , от концентрации которых зависит кислотность или основность растворов и, соответственно, структурные особенности и активность многих биомолекул и жизненных процессов. Эту концентрацию измеряют с использованием водородного показателя — рН . pH — отрицательный десятинный логарифм концентрации

Образование водородной связи

молекула воды
ионов Н + . В чистой воде эта концентрация составляет 1-10 -7 моль / л ( -log 10 -7 = 7 ) . Поэтому нейтральной реакции воды соответствует pH 7, кислой-pH <7 и основной -pH> 7. Протяженность шкалы pH — от 0 до 14. Значение pH в клетках слабощелочная. Изменение его на одну-две единицы губительна для клетки. Постоянство pH в клетках поддерживается за счет буферных систем, которые содержат смесь электролитов. Они состоят из слабой кислоты ( донора Н +) и сопряженной с ней основы ( акцептора Н +) , которые в соответствии связывают ионы H + и боны ОН — , благодаря чему реакция pH внутри клетки почти не меняется.
Гидрофильные и гидрофобные соединения. В молекул воды две пары совместных электронов смещены к кислорода, поэтому электрический заряд внутри молекул распределен неравномерно: протоны Н + обусловливают положительный заряд на одном полюсе, а пары электронов кислорода — отрицательный заряд на противоположном полюсе. Эти заряды равны по величине и расположены на определенном расстоянии друг от друга. Итак, молекула воды — это постоянный диполь, который может взаимодействовать с носителями положительных и отрицательных зарядов. Наличием полюсов в молекулах воды объясняется способность воды к химическим реакциям гидратации.
Благодаря своей полярности молекулы воды могут присоединяться к молекулам или ионов растворимых в воде веществ с образованием гидратов (соединений воды с растворенным веществом). Эти реакции являются экзотермическими и, в отличие от реакций гидролиза, гидратация не сопровождается образованием водородных или гидроксильных ионов.
При взаимодействии молекул воды с молекулами полярных веществ притяжения молекул воды к розчинюванои вещества превышать энергию притяжения между молекулами воды. Поэтому молекулы или ионы таких соединений встраиваются в общую систему водородных связей воды. Гидрофильные вещества — это полярные вещества, которые способны хорошо растворяться в воде. Это растворимые кристаллические соли, моносахариды, определенные аминокислоты, нулеинови кислоты и др.
В случае взаимодействия молекул воды с молекулами неполярных веществ энергия притяжения молекул воды в них будет меньше, чем энергия водородных связей. Неполярные молекулы пытаются изолироваться от молекул воды, они группируются между собой и вытесняются из водного раствора. Гидрофобные вещества — это неполярные вещества, которые не растворяются в воде. Это нерастворимые минеральные соли, липиды, полисахариды, определенные белки и др. Некоторые органические молекулы имеют двойные свойства: на одних их участках сосредоточены полярные группы, на других — неполярные. Таковы многие белки, фосфолипиды. их называют амфифильных веществами.

Распределение молекул воды вокруг аниона и катиона
Где Карбон, там разнообразие органических веществ, где Карбон, там самые разнообразные по молекулярной архитектурой конструкции.
Энциклопедия юного химика
