Какие химические свойства характерны для сахарозы

Примером наиболее распространенных в природе дисахаридов (олигосахаридом) является сахароза (свекловичный или тростниковый сахар).
Биологическая роль сахарозы
Наибольшее значение в питании человека имеет сахароза, которая в значительном количестве поступает в организм с пищей. Подобно глюкозе и фруктозе сахароза после расщепления ее в кишечнике быстро всасывается из желудочно-кишечного тракта в кровь и легко используется как источник энергии.
Важнейший пищевой источник сахарозы — сахар.
Строение сахарозы
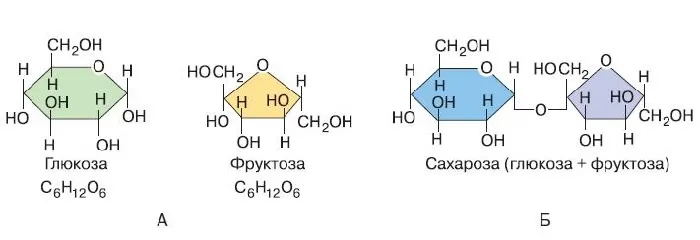
Молекулярная формула сахарозы С12Н22О11.
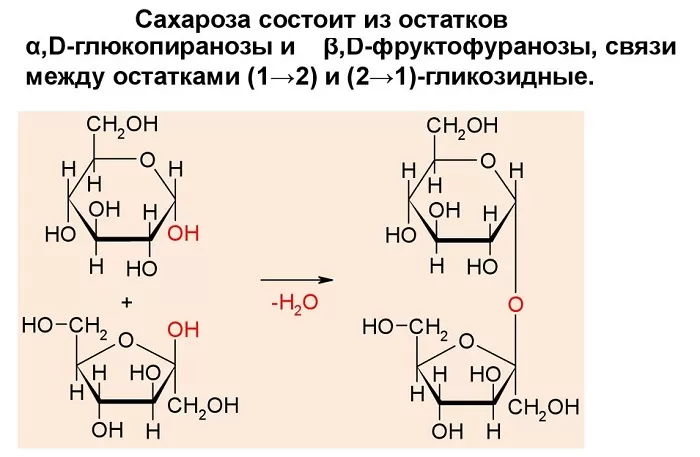
Сахароза имеет более сложное строение, чем глюкоза. Молекула сахарозы состоит из остатков молекул глюкозы и фруктозы в их циклической форме. Они соединены друг с другом за счет взаимодействия полуацетальных гидроксилов (1→2) -гликозидной связью, то есть свободный полуацетальный (гликозидный) гидроксил отсутствует:
Сахароза. Строение
Физические свойства сахарозы и нахождение в природе
Сахароза (обыкновенный сахар) – белое кристаллическое вещество, более сладкое, чем глюкоза, хорошо растворимое в воде.
Температура плавления сахарозы 160°C. При застывании расплавленной сахарозы образуется аморфная прозрачная масса – карамель.
Сахароза является весьма распространённым в природе дисахаридом, она встречается во многих фруктах, плодах и ягодах. Особенно много ее содержится в сахарной свёкле (16-21%) и сахарном тростнике (до 20%), которые и используются для промышленного производства пищевого сахара.
Содержание сахарозы в сахаре 99,5%. Сахар часто называют «носителем пустых калорий», так как сахар – это чистый углевод и не содержит других питательных веществ, таких, как, например, витамины, минеральные соли.
Химические свойства
Для сахарозы характерны реакции по гидроксильным группам.
1. Качественная реакция с гидроксидом меди (II)
Наличие гидроксильных групп в молекуле сахарозы легко подтверждается реакцией с гидроксидами металлов.
Видеоопыт «Доказательство наличия гидроксильных групп в сахарозе»
Если раствор сахарозы прилить к гидроксиду меди (II), образуется ярко-синий раствор сахарата меди (качественная реакция многоатомных спиртов):
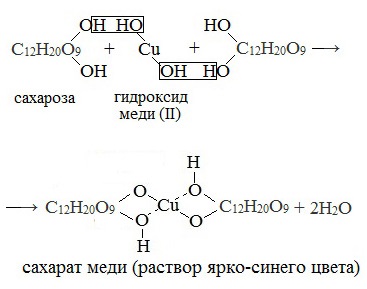
2. Реакция окисления
Восстанавливающие дисахариды
Дисахариды, в молекулах которых сохраняется полуацетальный (гликозидный) гидроксил (мальтоза, лактозы), в растворах частично превращаются из циклических форм в открытые альдегидные формы и вступают в реакции, характерные для альдегидов: реагируют с аммиачным раствором оксида серебра и восстанавливают гидроксид меди (II) до оксида меди (I). Такие дисахариды называются восстанавливающими (восстанавливают Cu (OH)2 и Ag2O).
Реакция «серебряного зеркала»![]()
Реакция с гидроксидом меди (II)![]()
Невосстанавливающий дисахарид
Дисахариды, в молекулах которых нет полуацетального (гликозидного) гидроксила (сахароза) и которые не могут переходить в открытые карбонильные формы, называются невосстанавливающими (не восстанавливают Cu (OH)2 и Ag2O).
Сахароза, в отличие от глюкозы, не является альдегидом. Сахароза, находясь в растворе, не вступает в реакцию «серебряного зеркала» и при нагревании с гидроксидом меди (II) не образует красного оксида меди (I), так как не способна превращаться в открытую форму, содержащую альдегидную группу.
Видеоопыт «Отсутствие восстанавливающей способности сахарозы»
3. Реакция гидролиза
Для дисахаридов характерна реакция гидролиза (в кислой среде или под действием ферментов), в результате которой образуются моносахариды.
Сахароза способна подвергаться гидролизу (при нагревании в присутствии ионов водорода). При этом из одной молекулы сахарозы образуется молекула глюкозы и молекула фруктозы:
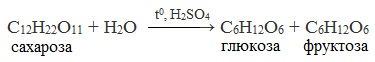
Видеоопыт «Кислотный гидролиз сахарозы»
Мальтоза и лактоза при гидролизе расщепляются на составляющие их моносахариды за счёт разрыва связей между ними (гликозидных связей):

Таким образом, реакция гидролиза дисахаридов является обратной процессу их образования из моносахаридов.
В живых организмах гидролиз дисахаридов происходит при участии ферментов.
Получение сахарозы
Сахарную свеклу или сахарный тростник превращают в тонкую стружку и помещают в диффузоры (огромные котлы), в которых горячая вода вымывает сахарозу (сахар).
Вместе с сахарозой в водный раствор переходят и другие компоненты (различные органические кислоты, белки, красящие вещества и др.). чтобы отделить эти продукты от сахарозы, раствор обрабатывают известковым молоком (гидроксидом кальция). В результате этого образуются малорастворимые соли, которые выпадают в осадок. Сахароза образует с гидроксидом кальция растворимый сахарат кальция С12Н22О11·CaO·2Н2О.
Для разложения сахарата кальция и нейтрализации избытка гидроксида кальция через раствор пропускают оксид углерода ( IV).
Выпавший в осадок карбонат кальция отфильтровывают, а раствор упаривают в вакуумных аппаратах. По мере образования кристалликов сахара отделяют с помощью центрифуги. Оставшийся раствор – меласса – содержит до 50% сахарозы. Его используют для производства лимонной кислоты.
Выделенную сахарозу очищают и обесцвечивают. Для этого ее растворяют в воде и полученный раствор фильтруют через активированный уголь. Затем раствор снова упаривают и кристаллизуют.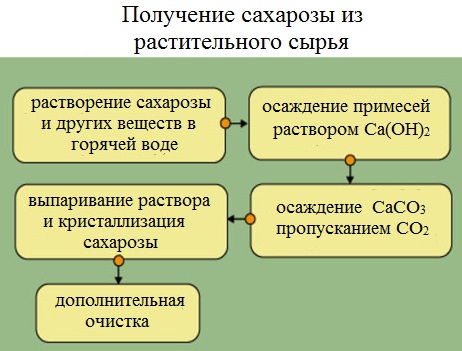
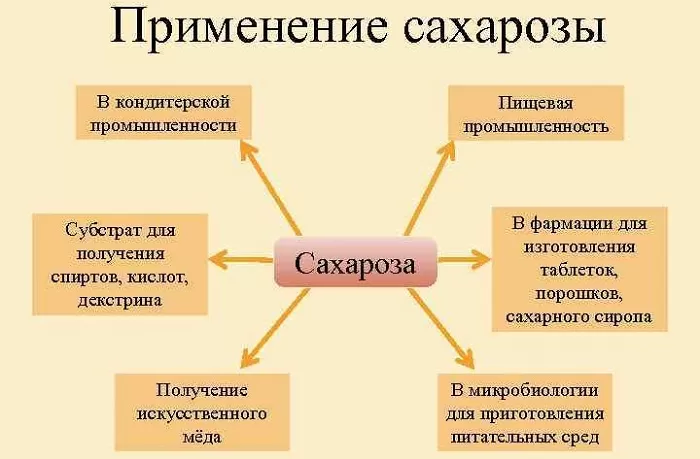
Применение сахарозы
Сахароза в основном используется как самостоятельный продукт питания (сахар), а также при изготовлении кондитерских изделий, алкогольных напитков, соусов. Ее используют в высоких концентрациях в качестве консерванта. Путем гидролиза из нее получают искусственный мёд.
Сахароза находит применение в химической промышленности. С помощью ферментации из нее получают этанол, бутанол, глицерин, левулиновую и лимонную кислоты, декстран.
В медицине сахарозу используют при изготовлении порошков, микстур, сиропов, в том числе для новорожденных детей (для придания сладкого вкуса или консервации).
Углеводы
Олигосахариды. Дисахариды
Сахароза — органическое вещество с кристаллической решеткой. Другое название — сахар. Это дисахарид, образованный остатками двух моносахаридов — фруктозы и глюкозы.
Узнаем больше о сахарозе, ее строении, формуле, физических и химических свойствах и о том, какую пользу играет она для живых организмов.
Формула и строение сахарозы
Структурная формула — C12H22O11, хотя она происходит от соединения двух простых сахаров, таких как глюкоза и фруктоза.
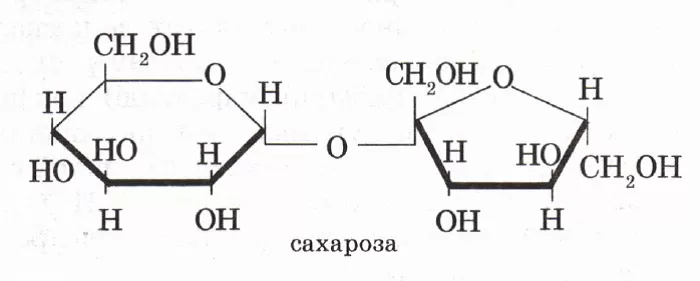
Два кольца этих сахаров объединены отдельным атомом кислорода, соединенным с двумя атомами углерода в цепочке. Другое расширение атома в молекуле также присутствует, главным образом, в комбинациях кислорода и водорода.
Связь между моносахаридами имеет O-глюкозидный тип. Кроме того, эта связь является дикарбонильной.
Физические свойства
По своим физическим свойствам она обладает сладким вкусом, может кристаллизоваться и растворима в воде.
Когда сахароза достигает желудка, она подвергается кислотному гидролизу и разлагается на части: на глюкозу и фруктозу. Остальная часть сахарозы переходит в тонкий кишечник, где ферментная сахароза преобразует ее в глюкозу и фруктозу.
Подчеркиваются ее специфические свойства в качестве питательного вещества для организма человека: она легко усваивается и не выделяет токсичных веществ. Это означает, что сахароза обладает как свойствами глюкозы, так и свойствами фруктозы, что означает, что она является источником энергии для организма.

Существует множество противоречий по поводу вреда, наносимого потреблением сахарозы, и несколько теорий по этому поводу. Основные дебаты сосредоточены на развитии кариеса, диабета, ожирения, атеросклероза и других патологий.
Интересно, что сахароза является триболюминесцентной, производящей свет механическим действием.
Благодаря низкой температуре плавления 1860С она очень быстро становится жидкой, очень легко прилипает к контейнеру, в котором она находится, может запросто обжечь кожу, если не соблюдать меры безопасности. Температура кипения раствора равна 101,40С.
Основные свойства описаны в таблице:
Физические свойства сахарозы | |
Молярная масса | 342,3 г/моль |
Температура плавления | 1860С |
Растворимость | 211,5 г / 100 мл |
Плотность | 1,587 г/см3 |
Химические свойства
В молекуле сахарозы есть гидроксильные группы. Рассмотрим основные уравнения химических реакций сахарозы.
Реакция гидролиза
Сахароза способна подвергаться гидролизу, во время которого она распадается на моносахариды (глюкозу и фруктозу):
C12H22O11
+ H2O → C6H12O6
+ C6H12O6.
Реакции окисления
Дисахариды, которые сохраняют полуацетальный гидроксил, называются восстанавливающими. Дисахариды без полуацетального гидроксила называются невосстанавлиающими. Сахароза не является альдегидом.
Пример каталитического окисления сахарозы кислородом воздуха:
C12H22O11
+ 12 O2 → 12 CO2 + 11 H2O.
Качественная реакция с гидроксидом меди
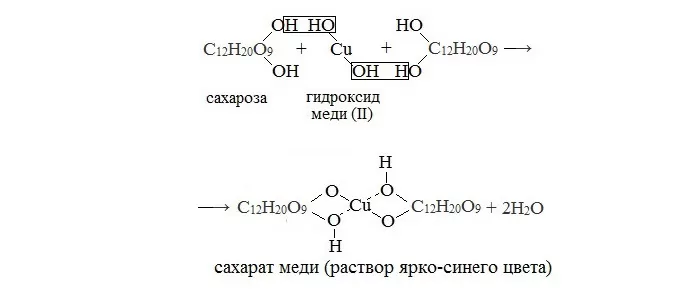
Как провести лабораторный опыт:
лабораторное оборудование: пробирка, горелка;
реагенты: водный раствор сахарозы, гидроксид меди (II);
действия: залейте раствор сахарозы в пробирку, добавьте гидроксид меди (II), разогрейте пробирку над горелкой:
C12H22O11
+ 2 Cu (OH)2 → ярко-синее окрашивание;
Замечания: синий осадок не изменил цвет, несмотря на подачу энергии в виде тепла;
Вывод: сахароза не обладает восстановительными свойствами.
Нахождение сахарозы в природе
Она обычно извлекается из сахарного тростника, свеклы или кукурузы.

Сахарный тростник
Другими коммерческими (незначительными) источниками являются сладкий сорго и кленовый сироп.
Получение сахарозы
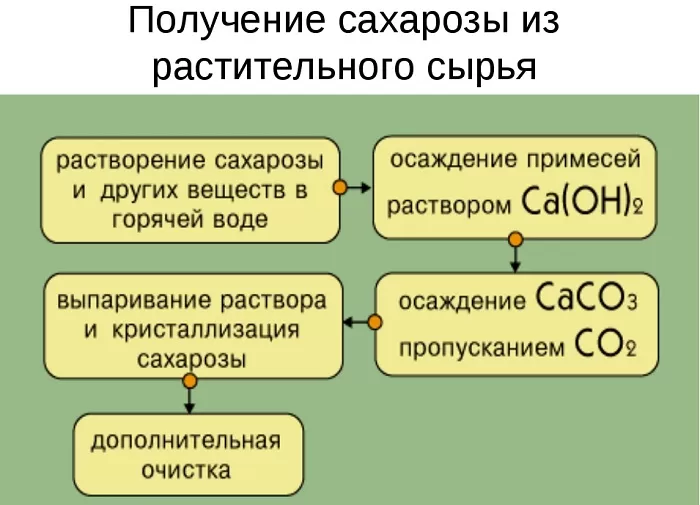
Сахароза извлекается из сырья, в котором она содержится, а затем очищается и кристаллизуется.
Применение и биологическая роль сахарозы
Широкое применение сахарозы обусловлено ее способностью к подслащению и свойствами функциональной консистенции. По этой причине она важна для структуры некоторых продуктов питания, особенно кондитерских изделий.
Также является вспомогательным компонентом в сохранении пищи, будучи добавкой, широко используемой в приготовлении так называемой нездоровой пищи.
В проросших семенах растений жиры и белки, находящиеся на хранении, превращаются в сахарозу для транспортировки в процессе развития растений.
Главная функция сахарозы в организме человека — она помогает вырабатывать энергию, необходимую для функционирования различных органов.
Строение дисахаридов
Определение
Дисахариды – это сахароподобные сложные углеводы, молекулы которых при гидролизе распадаются на две молекулы моносахаридов. Молекулярная формула дисахаридов $C_{12}H_{22}O_{11}$.
Дисахариды содержатся в продуктах природного происхождения:

в виде сахарозы (свекловичный сахар) в большом количестве, до 28%, – в сахарной свёкле и сахарном тростнике;
в форме лактозы (молочный сахар) – в молоке;
в виде трегалозы (грибной сахар) – в грибах, в дрожжах, высших растениях;
в виде мальтозы (солодовый сахар) образуется при частичном гидролизе крахмала и др.



По своему строению дисахариды могут быть отнесены к гликозидам — соединениям, молекулы которых состоят из двух частей: углеводного остатка и другого органического фрагмента (агликона), соединенных через гетероатом (соответственно различают О-, N-, S-гликозиды).
Таким образом, к особенностям строения дисахаридов нужно отнеси:
тип гликозидной связи, соединяющей остатки моносахаридов ($alpha$- или $beta$-),
наличие (отсутствие) полуацетального гидроксила.
Последнее позволяет отнести определенный дисахарид к классу восстанавливающих или невосстанавливающих сахаров. Для восстанавливающих дисахаридов характерна возможность образования открытой формы, и, следовательно, наличие восстановительных свойств.
В зависимости от того, какой гидроксил второго моносахарида участвует в образовании связи с первым моносахаридом, различают дисахариды двух типов: восстанавливающие (редуцирующие) и невосстанавливающие.
У восстанавливающих дисахаридов связь между моносахаридными остатками образована за счёт полуацетального гидроксила одной молекулы и спиртового гидроксила (чаще всего при четвёртом атоме углерода) второй молекулы.
Вспомнить: полуацетали — соединения, отвечающие структуре: $R-CH(OH)-OR’$, где R и R’ — алкильные радикалы.
Важнейшие представители восстанавливающих моносахаридов: мальтоза, лактоза. В растворе они находятся в таутомерных формах: циклической (полуацетальной) и гидроксикарбонильной (альдегидной).
Молекула мальтозы (солодовый сахар) и лактозы (молочный сахар) состоят из двух молекул $alpha$-D-глюкозы:


У невосстанавливающих дисахаридов связь между моносахаридами образована с участием обоих полуацетальных гидроксилов.
Поэтому невосстанавливающие дисахариды не могут переходить в другие таутомерные формы. Важнейшими их представителями являются сахароза (свекловичный сахар) и трегалоза (грибной сахар).


В сахарозе остаток $alpha$-D-глюкозы связан с остатком $beta$-D-фруктозы 1-2-гликозидной связью, а в природной трегалозе два остатка D-глюкозы связаны α-1,1-гликозидной связью.
Номенклатура дисахаридов
Строгая номенклатура олигосахаридов весьма громоздка. В названиях линейных олигосахаридов часто применяется последовательное перечисление моносахаридных остатков с указанием типа связи между ними. Чаще применяются тривиальные названия, принятые во всем мире.
Различия химических свойств дисахаридов
Восстанавливающие дисахариды
Представители ряда восстанавливающих дисахаридов обладают восстановительными свойствами, то есть, аналогично образующим их моносахаридам, могут вступать в реакции «серебряного зеркала» с реактивом Толленса и «медного зеркала» с реактивом Фелинга.
Невосстанавливающие дисахариды
Так как у невосстанавливающих дисахаридов связь между моносахаридами осуществляется за счёт обоих полуацетальных гидроксилов, они не могут таутомерно переходить в оксикарбонильную форму, следовательно, не обладают восстановительными свойствами и не могут давать реакции на альдегидную группу (не вступают в реакцию «серебряного зеркала», и не реагируют с раствором Фелинга).
Общие химические свойства дисахаридов
Оба ряда дисахаридов проявляют свойства многоатомных спиртов, а именно образуют растворимые сахараты с гидроксидом меди, и, как все сложные углеводы, гидролизуются в присутствии минеральных кислот или под действием ферментов (природных катализаторов биохимических процессов). Общее уравнение гидролиза можно записать следующим образом:
$C_{12}H_{22}O_{11} + H_2O xrightarrow{H^+} C_6H_{12}O_6 +C_6H_{12}O_6$
При нагревании растворов сахарозы в кислой среде или под действием фермента $beta$-фруктофуранозидазы она гидролизуется, образуя смесь равных количеств глюкозы и фруктозы, которая называется инвертным сахаром. Схема гидролиза приведена на рисунке:
Производство сахарозы
Свекловичный сахар (сахарозу) стали производить в промышленных масштабах из сахарной свеклы еще в начале XIX века в России и в Германии. Трудность производства заключается в многостадийной очистке получаемой сахарозы от примесей других органических веществ, главным образом, карбоновых кислот, присутствующих в соке свеклы. Горячий раствор, образующийся при замачивании стружки свеклы, подвергают обработке «известковым молоком» — суспензией гидроксида кальция в воде. Большинство образующихся нерастворимых солей выпадает в осадок, а сахароза образует растворимый в воде сахарат кальция, который затем отделяют от осадка. Данные химические процессы можно выразить следующими уравнениями:
$2R-COOH +Ca(OH)_2 longrightarrow (R-COO)_2Ca downarrow + 2H_2O$
$C_{12}H_{22}O_{11} +Ca(OH)_2 longrightarrow C_{12}H_{20}O_{11}Ca +2H_2O$
Для получения сахарозы из сахарата кальция через раствор пропускают углекислый газ. Сахарат кальция разлагается на сахарозу и нерастворимый карбонат кальция:
$C_{12}H_{20}O_{11}Ca + CO_2 + H_2O longrightarrow C_{12}H_{22}O_{11} + CaCO_3 downarrow$
После этого полученный раствор отфильтровывают и упаривают в вакуумных аппаратах, а выделяющиеся кристаллы сахара отделяют и высушивают. Получаемый сахар имеет желтый оттенок и называется «сахар-сырец».


Чтобы полностью его очистить, сахар снова растворяют и нагревают с активированным углем, который сорбирует все посторонние вещества. Финальной стадией, позволяющей получить кристаллы сахара одного размера, является перекристаллизация упаренного раствора с использованием затравки — суспензии измельченной сахарозы в изопропиловом спирте. Каждая маленькая частица становится центром кристаллизации, на котором вырастают кристаллы сахара строго заданного одинакового размера. Полученный сахар носит название «сахар-рафинад».
7.18. Углеводы
Углеводы – органические соединения, содержащие карбонильные и гидроксильные группировки атомов, имеющие общую формулу Cn(H2O)m, (где n и m>3).
Углеводы можно разделить на три группы:
1) Моносахариды – углеводы, способные гидролизоваться с образованием более простых углеводов. К данной группе относятся гексозы (глюкоза и фруктоза), а также пентоза (рибоза).
2) Олигосахариды – продукты конденсации нескольких моносахаридов (например, сахароза).
3) Полисахариды – полимерные соединения, содержащие большое число молекул моносахаридов.
Глюкоза C6H12O6 (альдегидоспирт).
Глюкоза может существовать в линейной и циклической формах:
Химические свойства
1) Реакции альдегидной группы:
а) реакция «серебряного зеркала»:
CH2OH–(CHOH)4–CH=O + 2[Ag(NH3)2]OH →
→ CH2OH–(CHOH)4–COONH4 + 2Ag↓ +3NH3 + H2O;
б) реакция с гидроксидом меди (II):
t
CH2OH–(CHOH)4–CH=O + 2Cu(OH)2 →
→ CH2OH–(CHOH)4–COOH + Cu2O↓ + 2H2O,
в) восстановление:
[H]
CH2OH–(CHOH)4–CH=O →
→ CH2OH–(CHOH)4–CH2OH.
2) Реакции гидроксильной группы:
а) взаимодействие с гидроксидом меди (II):
ярко синий раствор
б) брожение – расщепление глюкозы под действием ферментов:
C6H12O6 → 2C2H5OH + 2CO2 – спиртовое брожение,
C6H12O6 → 2CH3CH(OH)COOH – молочнокислое брожение.
Фруктоза C6H12O6(кетоноспирт).
Химические свойства
Фруктоза вступает во все реакции, характерные для многоатомных спиртов, однако реакции карбонильной (альдегидной) группы, в отличие от глюкозы, для нее не характерны.
Рибоза C5H10O5– пентоза (альдегидоспирт)
Химические свойства аналогичны глюкозе.
Сахароза C12H22O11 – дисахарид.
Сахароза образована остатками a-глюкозы и b-фруктозы:
Химические свойства
1) Гидролиз
C12H22O11 + H2O → C6H12O6 + C6H12O6.
сахароза глюкоза фруктоза
2) Взаимодействие с гидроксидом кальция с образованием сахарата кальция.
3) Сахароза не реагирует с аммиачным раствором оксида серебра, поэтому ее называют невосстанавливающим дисахаридом.
Мальтоза С12H22O11 – дисахарид, образованный двумя остатками a-глюкозы.
Химические свойства аналогичны глюкозе, поэтому ее называют восстанавливающим дисахаридом.
Крахмал (С6H10O5)n – природный полимер, молекулы которого состоят из линейных и разветвленных цепей, содержащих остатки a-глюкозы.
Химические свойства
1) Гидролиз
H+, t
(C6H10O5)n + nH2O → nC6H12O6
глюкоза
2) Крахмал дает интенсивно синее окрашивание с йодом за счет образования внутрикомплексного соединения.
3) Крахмал не вступает в реакцию «серебряного зеркала».
Целлюлоза (С6H10O5)n – природный полимер, молекулы которого состоят из линейных цепей, содержащих остатки b-глюкозы.
Химические свойства
1) Гидролиз:
H+, t
(C6H10O5)n + nH2O → nC6H12O6.
глюкоза
2) Образование сложных эфиров с азотной и уксусной кислотами:
(C6H7O2(OH)3)n + 3nCH3COOH → (C6H7O2(OCOCH3)3)n + nH2O.
