Какие физические свойства вольфрама лежат в основе его применения

Вольфрам (W) – 74-й элемент периодической системы химических элементов Менделеева. Это уникальный металл, отличающийся хорошими механическими и химическими свойствами, а также высокими эксплуатационными показателями. Благодаря этому компонент применяется во многих промышленных сферах.
Сегодня трудно встретить человека, который не слышал о вольфраме. Он был известен еще в далеком 16 веке. Самое простое изделие, в котором присутствует данный элемент – лампочка накаливания. Здесь вольфрамовая нить играет роль проводника электрического тока, за счет чего она накаливается до появления оптического излучения. На этом и построен принцип работы обыкновенной лампы.
В сегодняшней статье обсудим свойства вольфрама, поговорим об особенностях и применении металлического компонента, а также разберем историю происхождения. Приступим!
История появления
Наименование химического элемента Wolframium произошло от названия минерала вольфрамит. Как говорилось, о нем начали говорить в начале – середине 16 века. Но тогда минерал назывался иначе – spuma lupi, что в переводе с латинского означает «волчья пена». На немецком языке компонент называли Wolf Rahm – «волчья пасть».
Обуславливались данные названия следующим: если в оловянной руде находились вольфрамовые соединения, число исходящего олова существенно уменьшалось. Вольфрам «съедал» олово, из-за чего получил такое название.
Вольфрам химические свойства
Современная наука поместила элемент в группу химически активных металлов. Вольфрам участвует в разных реакциях, формируя сложные и простые соединения. Если его сплавить, он также останется химически связанным. Наряду с этим с окислителями W реагирует быстрее, нежели иные металлические вещества.
Ниже приведен список, где вы найдете главные химические свойства вольфрама:
- встречается из изотопов, массовые количества равняются 183;
- 74 электрона без труда отделяются от атома;
- имеет 6 валентностей при различных соединениях с веществами;
- орбита содержит 2 яруса, из-за чего появляется надежная связь.
Интересный факт! Если запустить реакцию, в которой будут участвовать W и сухой фтор, получится уникальное вещество под названием гексафторидом (WF6). Несмотря на высокую температуру самого вольфрама, WF6 плавится при температуре 2,5 градуса по Цельсию, а кипит уже при комнатных условиях.
Вольфрам физические свойства
В чистом виде металл представляет собой блестящее вещество серебристого оттенка. Сегодня W является одним из самых прочных, тяжелых и тугоплавких металлов. Его минимальная температура плавления составляет 3 410 градусов. Пожалуй, в этом он уступает только углероду, который относится к группе неметаллов. Многие вещества не только плавятся, но и кипят при таком температурном режиме. Если довести температурные условия до 5 550 градусов, элемент начинает плавиться. Он с легкостью поддается ковке, в процессе которой возможно получить тонкую нить.
А вот таблица, характеризующая металл еще больше.
| Масса | 184 г/моль |
| Плотность | 19,25 г/м3 |
| Твердость по шкале Мооса | 7,5 |
| Излом | Зазубренный |
| Магнетизм | Парамагнетик |
Получение
При добыче вольфрама из руд образуется оксид WO3, который впоследствии восстанавливается с помощью водорода при нагреве до металлического порошкообразного вещества. Ввиду высоких температурных условий плавления получить небольшие размеры металла довольно затруднительно. А потому полученный порошок спрессовывают и спекают в атмосфере водорода. Затем через него проходит мощное напряжение, из-за чего W накаливается до 3 000 градусов. Таким образом, вольфрам поддается плавлению.
Сам же элемент достаточно редко встречается в природе. После всех веществ он занимает лишь 57-е место. Находят его, как правило, в подземных водах в виде своего иона или различных соединений.
Вольфрам свойства и применение
Как говорилось, наибольшую популярность вольфрам получил в производстве обычных лампочек накаливания. Впервые ее изобрели в начале 19 века. Помимо примитивных изделий W участвует в изготовлении трубок для рентгеновского оборудования, составляющих вакуумных печек и других устройств, использующихся при высоких температурах.
Интересный факт! Сталь включает в свой состав вольфрамовые соединения. Благодаря этому она может похвастаться прочностью и надежностью. Подобные сплавы хорошо зарекомендовали себя в производстве оборудования для бурения скважин, а также в медицинской отрасли и машиностроении.
Самый износоустойчивый сплав, полученный из вольфрама, называется победит. Его нередко применяют в химической сфере, где изготавливают краски и пигменты.

Вольфрамовый карбид
Примерно половина добываемого вольфрама используется в производстве твердых металлических веществ. Сюда же входит карбид, температура плавления которого достигает почти 3 000 градусов. Данный металл выглядит как химическое соединение, в состав которого входит одинаковое число атомов вольфрама и углерода. Такой сплав обладает особенными показателями. Сам же W делает его настолько прочным и твердым, что по характеристикам он превосходит сталь в несколько раз.
Наиболее распространенной продукцией, которую делают из карбида, являются режущие предметы. Некоторые из них имеют высокие требования к температурной устойчивости, а потому этот сплав оптимален для изготовления. Помимо этого соединение хорошо зарекомендовало себя в производстве:
- частей воздушных судов и легковых авто;
- деталей для космических аппаратов;
- медицинских хирургических приборов;
- украшений (кольца, серьги, колье);
- шариков для ручек премиум-сегмента.
Мединструменты, включающие в себя сплав, используются в области полостной хирургии. Они превосходят в цене приборы из стали, но отличаются более высокими показателями. То же самое относится к ювелирным изделиям: отполированный металл долгие годы сохраняет блестящий и изысканный вид.
Вольфрам имеет одни из самых высоких характеристик. У него уникальные физические и химические параметры, похвастаться которыми сможет далеко не каждый металл. Несмотря на маленькую распространенность, он встречается в быту и производстве. Для укрепления других компонентов из него нередко делают сплавы.
Надеемся, статья была интересной и познавательной. Читайте предыдущие статьи и ждите новых полезных публикаций на нашем сайте!
- Главная
- Справочник
- Свойства вольфрама
Вольфрам (W) – удивительный металл с прекрасными физическими и химическими характеристиками. Его активно применяют практически во всех отраслях промышленности.

Физические свойства вольфрама:
- твердый тугоплавкий и тяжелый металл (вес вольфрама почти в 2 раза больше, чем у свинца);
- масса вольфрама составляет 184 г/моль;
- сплавы W отличаются прочностью, твердостью и высоким сопротивлением к высоким температурам;
- цвет зависит от способа получения (порошок имеет серый, темно-серый или черный цвет, сплавленный W – серый оттенок, напоминающий цвет платины);
- плотность вольфрама при нормальних условиях равна 19, 25 г/м3.
Температура плавления вольфрама составляет 3410 °C — соизмерима с температурой на поверхности Солнца – 6690 °C. Высокая твердость вольфрама позволяет применять его в химической промышленности и металлургии. При этом сопротивление вольфрама зависит только от температуры.
Химические свойства вольфрама:
- в природе состоит из стабильных изотопов (5 штук), массовые числа которых находятся в пределах 180-186;
- отделение 74 электронов атома W происходит легко;
- обладает 6 валентностью, в соединениях может иметь 0, 2, 3, 4 и 5-валентным;
- орбита элемента включает 2 яруса, что позволяет образовать крепкую химическую связь.

Наука относит вольфрам к химически активным элементам. Он может вступать в различные реакции и образовывать как простые, так и сложные соединения. В сплавах W чаще всего остается химически связанным. При этом с окислителями (например, с кислородом) он реагирует быстрее, чем другие металлы рода «тяжеловесов».
В случае нагревания элемента он еще быстрее вступает в реакцию с кислородом. Если в реакции участвуют водные пары, реакция протекает гораздо быстрее. Ученые выяснили: при нагреве элемента до 500 °C получается WO2 — низкий окислитель с высокой устойчивочтью. Он затягивает поверхность металла коричневой пленкой. Если повышать температуру — можно получить еще один окислитель, который называют промежуточным (W4O11). Он имеет синюю окраску, а если продолжить нагрев до температуры в 923°C, она изменится на лимонно-желтую. Этому будет способствовать WO3.
Если с вольфрамом смешивают сухой фтор, то даже при небольшом подогреве можно получить вещество WF6. Его именуют гексафторидом. Оно может плавиться даже при 2,5 градусах, а кипеть при 19,5. Такое же соединение можно получить и при использовании хлора. Однако для этой реакции потребуется высокая температура — около 600 °C.
Также вольфрам легко вступает в реакции с йодом и бромом. С ними он образовывает такие малоустойчивые соединения как дибромид, ментамид, а также дииодид и тетрадид. При высоких температурах вольфрам соединяется с селеном, азотом, серой, а также с кремнием и углеродом.
Одним из интересных соединений считают карбонил. В этой реакции вольфрам реагирует на окись углерода. Именно здесь и проявляется его нулевая валентность. Однако это вещество сложно назвать устойчивым. Поэтому его можно получить только при создании специальных условий. Из карбонила получают плотные и ультратонкие покрытия чистого вольфрама.
Нужно уделить внимание и вольфрамовым соединениям. Некоторые из них поддаются полимеризации, в частности окись вольфрама.

Свойства атома
- Имя, символ, номер — Вольфрам/Wolframium (W), 74
- Атомная масса (молярная масса), г/моль — 183,84 а. е. м.
- Электронная конфигурация — [Xe] 4f14 5d4 6s2
- Радиус атома, пм — 141
Химические свойства
- Ковалентный радиус, пм — 170
- Радиус иона, пм — (+6e) 62 (+4e) 70
- Электроотрицательность, шкала Полинга — 2.3
- Электродный потенциал, В — W < W3+ 0,11
- W < W6+ 0,68
- Степени окисления — 6, 5, 4, 3, 2, 0
- Энергия ионизации, кДж/моль(1-й ионизац. потенциал, эВ) — 769,7 (7,98)
Термодинамические свойства простого вещества
- Плотность, кг/м3 (при н. у., г/см3) — 19300 (19,3)
- Температура плавления, °C, K — 3422, 3695
- Температура кипения, °C, K — 5555, 5828
- Теплота плавления, кДж/кг, кДж/моль — 191, 35
- Теплота испарения, кДж/кг, кДж/моль — 4482, 824
- Теплоемкость, кДж/(кг·°С) — 0,134
- Молярная теплоемкость, Дж/(K·моль) — 24,27
- Молярный объем, см3/моль — 9,53

Кристаллическая решетка простого вещества
- Структура решетки — кубическая объемноцентрированая
- Параметры решетки, A — 3,160
- Температура Дебая, K — 310,00
Прочие характеристики
- Теплопроводность, K, Вт/(м·К) — 300, 173
- Удельное электросопротивление при 20°С, ом·мм2/м — 5,03
- Коэффициент теплопроводности при 20°С, кал/ (см·сек·град) — 0,4
- Коэффициент линейного расширения, 1/град — 43·10-6
- Временное сопротивление при растяжении, кг/мм2 — 35
Глава 2. Металлы
Из курса химии 9 класса вы уже имеете представление о природе химической связи, существующей в кристаллах металлов, — металлической связи. Напомним, что в узлах металлических кристаллических решёток располагаются атомы и положительные ионы металлов, связанные посредством обобществлённых внешних электронов, принадлежащих всему кристаллу. Эти электроны компенсируют силы электростатического отталкивания между положительными ионами и тем самым связывают их, обеспечивая устойчивость металлической решётки.
Металлическая связь обусловливает все важнейшие физические свойства металлов: пластичность, электро- и теплопроводность, металлический блеск и другие свойства, характерные для этого класса простых веществ.
Пластичность — это свойство вещества изменять форму под внешним воздействием и сохранять принятую форму после прекращения этого воздействия.
Способность расплющиваться от удара или вытягиваться в проволоку под действием силы составляет важнейшее механическое свойство металлов. Оно лежит в основе такой уважаемой большинством народов мира профессии, как профессия кузнеца. Недаром покровителем кузнечного дела у разных народов был бог огня: у греков — Гефест, у римлян — Вулкан, у славян — Сварог.
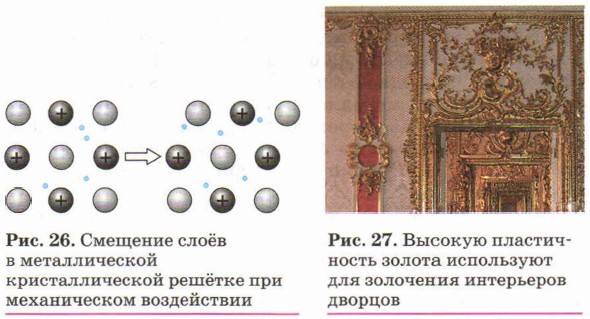
Пластичность металлов обусловлена способностью одних слоёв атом-ионов в кристаллах под внешним воздействием легко смещаться (как бы скользить) по отношению к другим слоям без разрыва связей между ними (рис. 26). Наиболее пластичны золото, серебро и медь. Например, из золота можно изготовить «золотую фольгу» толщиной 0,003 мм, которую используют для золочения изделий (рис. 27).
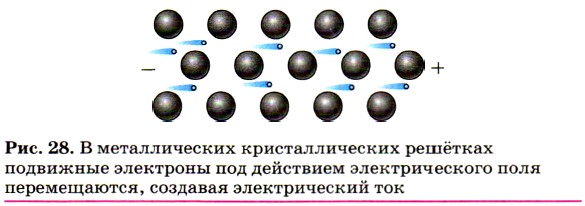
Высокая электропроводность большинства металлов обусловлена присутствием в их кристаллических решётках подвижных электронов, которые направленно перемещаются под действием электрического поля (рис. 28).
При нагревании колебательные движения ионов в кристалле усиливаются, что затрудняет направленное движение электронов и ведёт к снижению электрической проводимости. При охлаждении электропроводность металлов увеличивается и вблизи абсолютного нуля переходит в сверхпроводимость. Наибольшую электропроводность имеют серебро и медь, наименьшую — марганец, свинец, ртуть и вольфрам.
Такое свойство, как теплопроводность металлов, также связано с высокой подвижностью свободных электронов: сталкиваясь с колеблющимися в узлах решётки ионами, электроны обмениваются с ними энергией. С повышением температуры колебания ионов при посредстве электронов передаются другим ионам, и температура всего металлического предмета быстро выравнивается.
Для гладкой поверхности металлов характерен металлический блеск — результат отражения световых лучей. В порошкообразном состоянии большинство металлов теряет блеск, приобретая чёрную или серую окраску, и только алюминий и магний сохраняют блеск в порошке. Из алюминия, серебра и палладия, обладающих наиболее высокой отражательной способностью, изготовляют зеркала, в том числе и применяемые в прожекторах.
Для большинства металлов характерен белый или серый цвет. Золото и медь окрашены соответственно в жёлтый и жёлто-красный цвет.
Из других физических свойств металлов наибольший практический интерес представляют твёрдость, плотность и температура плавления.
Для большинства металлов характерен белый или серый цвет. Золото и медь окрашены соответственно в жёлтый и жёлто-красный цвет.
Из других физических свойств металлов наибольший практический интерес представляют твёрдость, плотность и температура плавления.
Для всех металлов (кроме ртути) при обычных условиях характерно твёрдое агрегатное состояние. Однако твёрдость их различна. Наиболее твёрдые — металлы побочной подгруппы VI группы (VIB группы) Периодической системы Д. И. Менделеева. Так, хром по твёрдости приближается к алмазу. Самые мягкие — металлы главной подгруппы I группы (IA группы) Периодической системы Д. И. Менделеева — щелочные металлы. Например, натрий и калий легко режутся ножом.

По плотности металлы делят на лёгкие (плотность меньше 5 г/см3) и тяжёлые (плотность больше 5 г/см3). К лёгким относят щелочные, щёлочноземельные металлы и алюминий. Из переходных металлов сюда включают скандий, иттрий и титан. Эти металлы, благодаря лёгкости и тугоплавкости, всё шире применяют в различных областях техники.
Самый лёгкий металл — это литий (р = 0,53 г/см3). Самый тяжёлый — осмий (р = 22,6 г/см3).
Лёгкие металлы обычно легкоплавки, галлий может плавиться уже на ладони руки, а тяжёлые металлы — тугоплавки. Наибольшей температурой плавления, которая равна 3380 °С, обладает вольфрам. Это свойство вольфрама используют для изготовления ламп накаливания (рис. 29, 2). Кроме него в конструкцию лампы входят ещё семь металлов.
В Российской Федерации в настоящее время, как и ранее в Евросоюзе и США, на государственном уровне принято решение о замене привычных ламп накаливания на более экономичные и долговечные современные лампы, например галогенные, люминесцентные и светодиодные. Галогенная лампа (рис. 29, 2) — это та же лампа накаливания с вольфрамовой нитью, заполненная инертными газами с добавкой паров галогенов (брома или иода).

Люминесцентные (рис. 29, 3) — это хорошо знакомые вам лампы дневного света, имеющие один существенный недостаток — они содержат ртуть, а потому нуждаются в соблюдении особых правил утилизации на специальных пунктах приёма. Светодиодные лампы (рис. 29, 4) — самые экономичные и самые долговечные (срок работы до 100 тыс. ч), но пока и самые дорогие из ламп.
В технике, как вы уже знаете, металлы делят на чёрные (железо и его сплавы) и цветные (все остальные, более подробно о них будет рассказано в следующем параграфе) (рис. 30). Золото, серебро, платину и некоторые другие металлы относят к драгоценным металлам (рис. 31). 1


1. Обратитесь к электронному приложению. Изучите материал урока и выполните предложенные задания.
2. Найдите в Интернете электронные адреса, которые могут служить дополнительными источниками, раскрывающими содержание ключевых слов и словосочетаний параграфа. Предложите учителю свою помощь в подготовке нового урока — сделайте сообщение по ключевым словам и слово-сочетаниям следующего параграфа.

1. Назовите самый легкоплавкий металл.
2. Какие физические свойства металлов используют в технике?
3. Фотоэффект, т. е. свойство металлов испускать электроны под действием лучей света, характерен для щелочных металлов, например для цезия. Почему? Где это свойство находит применение?
4. Какие физические свойства вольфрама лежат в основе его применения в лампах накаливания?
5. Какие свойства металлов лежат в основе образных литературных выражений: «серебряный иней», «золотая заря», «свинцовые тучи»?
- Физические свойства металлов. Ответы
Химия
9 класс
Из курса химии 8 класса вы уже имеете представление о природе химической связи, существующей в кристаллах металлов, — металлической связи. Напомним, что в узлах металлических кристаллических решёток располагаются атомы и положительные ионы металлов, связанные посредством обобществлённых внешних электронов, принадлежащих всему кристаллу. Эти электроны компенсируют силы электростатического отталкивания между положительными ионами и тем самым связывают их, обеспечивая устойчивость металлической решётки.
Металлическая связь обусловливает все важнейшие физические свойства металлов: пластичность, электро- и теплопроводность, металлический блеск и другие свойства, характерные для этого класса простых веществ.
Пластичность — это свойство вещества изменять форму под внешним воздействием и сохранять принятую форму после прекращения этого воздействия.
Способность расплющиваться от удара или вытягиваться в проволоку под действием силы составляет важнейшее механическое свойство металлов. Оно лежит в основе такой уважаемой большинством народов мира профессии, как профессия кузнеца. Недаром покровителем кузнечного дела у разных народов был бог огня: у греков — Гефест, у римлян — Вулкан, у славян — Сварог.
Пластичность металлов обусловлена способностью одних слоёв атом-ионов в кристаллах под внешним воздействием легко смещаться (как бы скользить) по отношению к другим слоям без разрыва связей между ними (рис. 26).

Рис. 26.
Смещение слоёв в металлической кристаллической решётке при механическом воздействии
Наиболее пластичны золото, серебро и медь. Например, из золота можно изготовить «золотую фольгу» толщиной 0,003 мм, которую используют для золочения изделий (рис. 27).

Рис. 27.
Высокую пластичность золота используют для золочения интерьеров дворцов
Высокая электропроводность большинства металлов обусловлена присутствием в их кристаллических решётках подвижных электронов, которые направленно перемещаются под действием электрического поля (рис. 28).

Рис. 28.
В металлических кристаллических решётках подвижные электроны под действием электрического поля перемещаются, создавая электрический ток
При нагревании колебательные движения ионов в кристалле усиливаются, что затрудняет направленное движение электронов и ведёт к снижению электрической проводимости. При охлаждении электропроводность металлов увеличивается и вблизи абсолютного нуля переходит в сверхпроводимость. Наибольшую электропроводность имеют серебро и медь, наименьшую — марганец, свинец, ртуть и вольфрам.
Такое свойство, как теплопроводность металлов, также связано с высокой подвижностью свободных электронов: сталкиваясь с колеблющимися в узлах решётки ионами, электроны обмениваются с ними энергией. С повышением температуры колебания ионов при посредстве электронов передаются другим ионам, и температура всего металлического предмета быстро выравнивается.
Для гладкой поверхности металлов характерен металлический блеск — результат отражения световых лучей. В порошкообразном состоянии большинство металлов теряет блеск, приобретая чёрную или серую окраску, и только алюминий и магний сохраняют блеск в порошке. Из алюминия, серебра и палладия, обладающих наиболее высокой отражательной способностью, изготовляют зеркала, в том числе и применяемые в прожекторах.
Для большинства металлов характерен белый или серый цвет. Золото и медь окрашены соответственно в жёлтый и жёлто-красный цвет.
Из других физических свойств металлов наибольший практический интерес представляют твёрдость, плотность и температура плавления.
Для всех металлов (кроме ртути) при обычных условиях характерно твёрдое агрегатное состояние. Однако твёрдость их различна. Наиболее твёрдые — металлы побочной подгруппы VI группы (VIB группы) Периодической системы Д. И. Менделеева. Так, хром по твёрдости приближается к алмазу. Самые мягкие — металлы главной подгруппы I группы (IA группы) Периодической системы Д. И. Менделеева — щелочные металлы. Например, натрий и калий легко режутся ножом.
По плотности металлы делят на лёгкие (плотность меньше 5 г/см3) и тяжёлые (плотность больше 5 г/см3). К лёгким относят щелочные, щёлочноземельные металлы и алюминий. Из переходных металлов сюда включают скандий, иттрий и титан. Эти металлы, благодаря лёгкости и тугоплавкости, всё шире применяют в различных областях техники.
Самый лёгкий металл — это литий (р = 0,53 г/см3). Самый тяжёлый — осмий (р = 22,6 г/см3).
Лёгкие металлы обычно легкоплавки, галлий может плавиться уже на ладони руки, а тяжёлые металлы — тугоплавки. Наибольшей температурой плавления, которая равна 3380 °С, обладает вольфрам. Это свойство вольфрама используют для изготовления ламп накаливания (рис. 29, 1). Кроме него в конструкцию лампы входят ещё семь металлов.

Рис. 29.
Лампы, при изготовлении которых используют различные металлы: 1 — лампа накаливания; 2 — галогенная лампа; 3 — люминесцентная лампа; 4 — светодиодная лампа
В Российской Федерации в настоящее время, как и ранее в Евросоюзе и США, на государственном уровне принято решение о замене привычных ламп накаливания на более экономичные и долговечные современные лампы, например галогенные, люминесцентные и светодиодные. Галогенная лампа (рис. 29, 2) — это та же лампа накаливания с вольфрамовой нитью, заполненная инертными газами с добавкой паров галогенов (брома или иода). Люминесцентные (рис. 29, 3) — это хорошо знакомые вам лампы дневного света, имеющие один существенный недостаток — они содержат ртуть, а потому нуждаются в соблюдении особых правил утилизации на специальных пунктах приёма. Светодиодные лампы (рис. 29, 4) — самые экономичные и самые долговечные (срок работы до 100 тыс. ч), но пока и самые дорогие из ламп.

Рис. 30.
Металлы условно делят на две группы: чёрные (а — чугун; б — сталь); цветные (в — медь; г — алюминий)
В технике, как вы уже знаете, металлы делят на чёрные (железо и его сплавы) и цветные (все остальные, более подробно о них будет рассказано в следующем параграфе) (рис. 30). Золото, серебро, платину и некоторые другие металлы относят к драгоценным металлам (рис. 31).

Рис. 31.
Драгоценные металлы: золото (1, 2); платина (3); серебро (4, 5);
Новые слова и понятия
- Пластичность.
- Электропроводность и теплопроводность.
- Металлический блеск.
- Твёрдость металлов.
- Плотность металлов.
- Лёгкие и тяжёлые металлы.
- Чёрные и цветные металлы.
- Драгоценные металлы.
Задания для самостоятельной работы
- Назовите самый легкоплавкий металл.
- Какие физические свойства металлов используют в технике.
- Фотоэффект, т. е. свойство металлов испускать электроны под действием лучей света, характерен для щелочных металлов, например для цезия. Почему? Где это свойство находит применение?
- Какие физические свойства вольфрама лежат в основе его применения в лампах накаливания?
- Какие свойства металлов лежат в основе образных литературных выражений: «серебряный иней», «золотая заря», «свинцовые тучи»?
