Какая масса фосфорной кислоты содержится в растворе с объемом 3 л

Похожие вопросы:

Химия, 12.05.2019 15:12
1. при выпаривании 300 г 5%-ного раствора сахара получили раствор массой 240 г. какова процентная концентрация полученного раствора? 2. какие массы йода и спирта необходимы для приготовления 300 г раствора с массовой долей йода 5%? 3. какая масса хлорида меди (ii) cucl2 содержится в растворе объемом 15 л, если его молярная концентрация 0,3 моль/л? 4.какую массу фосфорной кислоты надо взять для приготовления раствора объемом 500 мл, если молярная концентрация н3ро4 равна 0,02 моль/л? вариант 1. приготовить 250 мл раствора хлорида калия, молярная концентрация которого 0,2 моль/л. вариант 2. приготовить 200 мл раствора карбоната натрия, молярная концентрация которого 0,5 моль/л. вариант 3. приготовить 300 мл раствора хлорида натрия, молярная концентрация которого 0,1 моль/л. 1. приготовьте 10 г водного раствора карбоната натрия с массовой долей соли 10%.
Ответов: 3

Химия, 22.05.2019 15:10
Рассчитайте какая масса азотной кислоты содержится в растворе массой 200г, если при взаимодействии с карбонатом бария количеством вещества 0,5 моль выделяется co2 объемом 11,2 л (при н. у). какова массовая доля кислоты в растворе?
Ответов: 2

Химия, 23.05.2019 07:50
В300 мл. раствора содержится 6г. фосфорной кислоты. какова молярная концентрация эквивалента фосфорной кислоты.
Ответов: 2

Химия, 25.05.2019 22:40
Решить . ! 1.смешали 200г раствора уксусной кислоты с массовой долей 5% и 300г раствора с массовой долей 10%. определить массовую долю уксусной кислоты в получившемся растворе. 2.в растворе объемом 200мл содержится н3ро4 массой 19,6г. рассчитать молярную концентрацию и молярную концентрацию эквивалента раствора кислоты, если молярная масса=98г/моль. 3.к 100мл 96% раствора h2so4 с плотностью 1,84г/мл добавили 100мл h2o(плотность=1г/мл). какова массовая доля полученного раствора?
Ответов: 3

Химия, 09.06.2019 10:00
1.составить уравнение гидролиза соли mnf2 по первой ступени. 2.какова массовая доля раствора хлорида кальция, в 3 литре которого содержится 4,2 моль cacl2,если плотность этого раствора 1,12г/моль расставить коэффициэнты в схеме реакции ,написать в ионном полном и сокращенном виде: nibr2+na3po4= ni3(po4)2=nabr 3.в растворе массой 250г содержится 25 г сахарозы. какова массовая доля растворенного вещества в этом растворе? 4 в растворе объемом 300 мл содержится 50 г азотной кислоты какова молярная концентрация азотной кислоты? (решите, ! )
Ответов: 2

Химия, 11.06.2019 14:30
Какая масса сульфатной кислоты содержится в растворе объемом 30 мл с массовой долей кислоты 2%, если плотность раствора установит 1,08 гмл
Ответов: 1

Химия, 19.06.2019 08:30
1)в растворе объёмом 150 мл содержится хлорид бария массой 17,5 г. какова массовая доля хлорида бария в растворе, если плотность раствора составляет 1,1 г/см3? 2)какие массы нитрата калия и воды необходимо взять для приготовления 2 л раствора (плотность раствора равна 1,3 г/см3) с массовой долей kn03 равной 0,05? 3)молярность раствора едкого калия кон равна 3,8 моль/л, его плотность 1,17 г/мл. вычислить массовую долю (%) кон в этом растворе. объём раствора 0,5 л. 4)вычислить молярную концентрацию раствора серной кислоты, если массовая доля h2s04 в этом растворе 12%. плотность раствора 1,08 г/мл при 20°с. масса раствора 500 грамм. 5)вычислить массу хлорида натрия nacl, содержащегося в растворе объемом 200 мл, если его молярная концентрация 2 моль/л.
Ответов: 2

Химия, 01.07.2019 20:20
Массовая доля элемента фосфора в растворе фосфорной кислоты в воде равна 5%. найдите массовую долю фосфорной кислоты в растворе. какая масса фосфорной кислоты будет содержаться в 500г раствора? чему равна массовая доля элемента кислорода в растворе?
Ответов: 3

Химия, 03.07.2019 04:10
Какая масса cucl2 содержится в растворе объёмом 15 литров если его молярная концентрация 0,3 моль/л. решить ! (подробно) за ранее !
Ответов: 2

Химия, 09.08.2019 17:40
Какая масса карбоната натрия содержится в растворе объемом 250 мл, для которого молярная концентрация эквивалента составляет 0,2 моль/л
Ответов: 3

Химия, 02.09.2019 11:30
Какая масса фосфорной кислоты находится в 230 г её раствора, если массовая доля кислоты в этом растворе равняется 0.2
Ответов: 1

Химия, 22.09.2019 14:50
Какая масса растворённого вещества и какая масса воды содержится в 400г, 10% раствора фосфорной кислоты?
Ответов: 2
У тебя есть свой ответ?
Какая масса фосфорной кислоты содержится в растворе объемом равным 0,3 л если его молярная концентра…
Отправлено
Вопросы по другим предметам:

Математика, 24.06.2019 21:20

Математика, 24.06.2019 21:20

Алгебра, 24.06.2019 21:20

Математика, 24.06.2019 21:20

Математика, 24.06.2019 21:20

Русский язык, 24.06.2019 21:20

Математика, 24.06.2019 21:20

Биология, 24.06.2019 21:20

Литература, 24.06.2019 21:20

Английский язык, 24.06.2019 21:20
Асия, 3 задание
Посмотрим в стандартную табличку тепловых значений:
CuO + 2HCl = CuCl2 + H2O + 63,6 кДж
Далее составим пропорцию:
80 г. (CuO) — 63,6 кДж
100 г. (CuO) — x кДж => x = 79,5 кДж.
Ответ: Q(CuO) на 100 г. = 79,5 кДж.
Асия, похожая задача.
Сколько мл 50%-ной серной кислоты (р = 1,4 г/см3) необходимо взять для приготовления 500 мл 0,5н.
раствора?
1/найдем массу серной кислоты в 500 мл 0,5 н раствора:
m(H2SO4)=0,5мольэкв/л*0,5л*49г/мольэкв=12,25г
2. Масса кислоты связана с объемом, плотностью и концентрацией исходного раствора соотношением:
m(H2SO4)=VPW, где V- объем раствора мл, Р- плотность раствора, г/см3, w- массовая доля кислоты (в данном случае =0,5)
отсюда V=m(H2SO4)/pW=12,25/(1,4*0,5)=17,5 см3
Асия, 5 номер похожая задача.
На сколько градусов понизится температура замерзания С6Н6, если в 100 г его расстворить 4 г нафталина С10Н8?Криоскопическая константа бензола равна 2,57
Криоскопическая константа бензола К = 5,07 !!!
^t = K*Cm .
М (С10Н8) = 128 г/моль n = 4/128 = 0.031 моль
Cm = 0.031*1000/100 = 0.31 моль/кг — моляльная концентрация раствора .
^t = 5.07*0.31 = 1.572 град
Какой объем 0,1 н. раствора серной кислоты необходимо отмерить для приготовления 100 мл 0,02 н. раствора?
Решение. Т.к. количество молей эквивалентов H2SO4 в исходном и приготовленном растворах одинаково, то, в соответствии с законом эквивалентов (7), объем исходного раствора фото
Какой объем 12%-ного раствора H2SO4 потребуется для приготовления 1 л 0,1н. раствора этой кислоты.
Плотность водного раствора NaCl = 1095,0 г/л. Определить массовую долю соли в растворе, рассчитать молярную долю NaCl, молярную концентрацию, молярную концентрацию эквивалента соли, моляльную концентрацию и массовую концентрацию раствора.
Решение. Для определения массовой доли соли в растворе используем данные табл.3 Приложения. Т.к. заданное значение плотности раствора NaCl в табл.3 отсутствует, применяем метод интерполяции. Для этого используем ближайшие меньшее и большее значения плотностей и соответствующие им массовые доли раствора данной соли. Считая, что в указанных пределах зависимость между плотностью и массовой долей раствора линейная, рассчитаем массовую долю растворенного вещества в растворе по пропорции (индекс б означает «большее», м — «меньшее»)
Определить процентную концентрацию КОН в растворе, если КОН массой 40 г растворен в воде массой 160 г.
Масса раствора составит m = m(KOH) + m(H2O) = 40 + 160 = 200 г.
ω = 100m(вещество) / m(раствор) = 100*40 / 200 = 20%.
При 0 °С предельная растворимость AgNO3 составляет 22 г. Вычислить процентное содержание AgNO3 в растворе, насыщенном при 0 оС.
Растворимость в данном случае обозначает массу вещества на 100 г. растворителя (вода)
Масса раствора составит 22 + 100 = 122 г.
ω = 100m(вещество) / m(раствор) = 100*22/122 = 18,03%.
. Смешали 300 г 20%-го раствора, и 500 г 40%-го раствора NaCI. Чему равна процентная концентрация полученного раствор?
В 300 г 20%-го раствора содержится (применим обратную формулу) m(вещество) = ω*m(раствор)/100 = 20*300/100 = 60 г. соли.
В 500 г 40%-го раствора содержится m(вещество) = ω*m(раствор)/100 = 40*500/100 = 200 г. соли.
Суммарно соли будет m(вещество) = 60 + 200 = 260 г.
Масса полученного раствора составит, очевидно, m(раствор) = 300 + 500 = 800 г.
Итак,
ω = 100m(вещество) / m(раствор) = 100*260/800 = 32,5%.
Определить процентную концентрацию хлорида натрия в растворе, полученном при растворении соли массой 20 г в воде массой 300 г.
ω = 100m(вещество) / m(раствор) = 100*20/(20 + 300) = 6,25%.
Сколько граммов гидроксида натрия содержится в растворе массой 250 граммов с концентрацией 20%?
m(вещество) = ω*m(раствор)/100 = 20*250/100 = 50 г.
13.1.6 К 300 мл гидроксида калия с концентрацией 20% (плотность 1,2 г/мл) прибавили КОН массой 40 граммов. Определить процентную концентрацию КОН в новом растворе.
Плотность определяется по формуле: ρ = m/V
Отсюда, масса раствора связана с плотностью соотношением: m = ρV
Определим массу 300 мл гидроксида калия с концентрацией 20% с плотностью 1,2 г/мл.
m(раствор) = ρV = 1,2*300 = 360 г.
m(вещество) = ω*m(раствор)/100 = 20*360/100 = 72 г.
После прибавления КОН массой 40 граммов масса вещества станет равной 72 + 40 = 112 г.
Масса раствора станет равной 360 + 40 = 400 г.
ω = 100m(вещество) / m(раствор) = 100*112/400 = 28%.
К 200 мл раствора серной кислоты (пл. 1,066) с концентрацией 10% прилили 1 л воды (пл. 1). Определить процентную концентрацию серной кислоты в новом растворе.
Решение аналогично предыдущему примеру.
Масса раствора кислоты составит 200*1,066 = 213,2 г. с содержанием кислоты 213,2*10/100 = 21,32 г.
Масса раствора составит 213,2 + 1000 = 1213,2 г. (1 л. воды весит 1000 г.)
ω = 100m(вещество) / m(раствор) = 100*21,32/1213,2 = 1,76%.
При упаривании раствора хлорида натрия массой 500 граммов с концентрацией раствора 1% получили новый раствор массой 100 граммов. Какова процентная концентрация полученного раствора?
Поясним, что при упаривании из раствора испаряется вода, количество соли при этом остается неизменным. Поэтому ее концентрация возрастает.
Определим массу соли.
m(вещество) = ω*m(раствор)/100 = 1*500/100 = 5 г.
Масса упаренного раствора задана, 100 г.
ω = 100m(вещество) / m(раствор) = 100*5/100 = 5 %.
Сколько соли надо растворить в воде массой 2 кг, чтобы получить раствор с концентрацией 20%?
Пусть количество соли = х.
Тогда масса раствора составит 2000+х граммов.
Подставим в уравнение ω = 100m(вещество) / m(раствор) наши данные.
20 = 100х/(2000 + х)
х = 500 г.
Сколько воды надо прибавить к раствору массой 3 кг с концентрацией соли 20% для получения 15% раствора?
Пусть масса воды = х.
В растворе содержится 3000*20/100 = 600 г соли.
Масса раствора составит 3000+х граммов.
Подставим в уравнение ω = 100m(вещество) / m(раствор) наши данные.
15 = 100*600/(3000 + х)
х = 1000 г.
Какой объем воды (плотность 1) потребуется для растворения сахара массой 8 граммов, если в приготовленном растворе концентрация должна быть 1%?
Если 1% весит 8 г., то весь раствор весит (пропорция из арифметики для 5 класса):
1% — 8
100% — х
х = 800 г.
Воды в нем будет 800 — 8 = 792 г. При плотности, равной 1, это соответствует объему 792 мл.
Какое количество 10% р-ра соли надо добавить к 200 г. 40% р-ра, чтобы получить 25% раствор?
Чтобы лишний раз не возиться с множителем 100, выразим концентрацию не через процент, а в долях.
10% = 0,1, 40% = 0,4, 25% = 0,25.
Пусть масса искомого раствора = х, тогда масса соли в нем будет 0,1х.
Масса соли во втором растворе составит 200*0,4 = 80 г.
Наконец, масса полученного раствора будет равна х+200. Очевидно, что масса соли в нем будет 0,25(х + 200)
Так же очевидно, что масса соли в третьем растворе равна сумме масс солей в двух исходных.
Тогда,
0,1х + 80 = 0,25(х + 200)
х = 200 г.
Задачи подобного плана на поиск массы добавляемого раствора или определение соотношения смешиваемых растворов решаются по общему уравнению:
ω1m1 + ω2m2 = ω3(m1 + m2)
Сколько граммов 80% и 20%-ной фосфорной кислоты следует взять для приготовления 3000 г 50%-ного раствора?
Пусть х — масса 80%-го раствора, тогда кислоты в нем содержится 0,8х.
Пусть у — масса 20%-го раствора, тогда кислоты в нем содержится 0,2у.
Приготовлено 3000 г раствора, в котором кислоты 3000*0,5 = 1500 г.
Можем составить систему уравнений:
0,8х + 0,2у = 1500
х + у = 3000
Решение системы приводит к ответам:
х = 1500
у = 1500
То есть, надо смешать по 1500 граммов.
Внимание! Для выражения одних концентраций через другие (перерасчета из одних концентраций в другие),
Плотность раствора серной кислоты с концентрацией 1,4 моль/л составляет 1,085 гр/см3. Определите массовую долю H2SO4 в этом растворе.
Возьмем литр раствора.
Масса растворенной кислоты составит
m = C*V*Mr = 1,4*1*98 = 137,2 г.
Масса раствора составит m(p-p) = ρ*V = 1,085*1000 = 1085 г.
ω = 100m/m(p-p) = 100*137,2/1085 = 12,6%.
Задача 421.
Сколько миллилитров 96%-ного (по массе) раствора H2SO4 (р = 1,84 г/мл) нужно взять для приготовления 1л 0,25 н. раствора?
Решение:
Определим молярную массу эквивалента H2SO4 из соотношения:

где
MЭ(В) — молярная масса эквивалента соли, г/моль; М(В) — молярная масса соли; n — коэффициент при атоме металла; A — валентность металла.
Отсюда

Рассчитаем массу H2SO4 в 1л 0,25н раствора по формуле:

где
m(B) — масса вещества; mЭ(В) — молярная масса эквивалента вещества, г; СЭ(В) — эквива-лентная концентрация или нормальность; V — объём раствора.
Отсюда

Теперь рассчитаем массу раствора, если известны массовая доля H2SO4 (96%) и масса H2SO4 (12,25г) по формуле:

где — массовая доля растворённого вещества; m(в-ва) — масса растворённого вещества; m(р-ра) — масса раствора.
— массовая доля растворённого вещества; m(в-ва) — масса растворённого вещества; m(р-ра) — масса раствора.
Тогда

Определим объём раствора H2SO4, необходимого для приготовления 1л 0,25н раствора по формуле: m = pV, где p — плотность раствора, V — объём раствора.
Тогда

Ответ: 6,93 мл.
Задача 422.
Сколько миллилитров 0,5М раствора H2SO4 можно приготовить из 15 мл 2,5М раствора?
Решение:
Для нахождения массы серной кислоты, содержащейся в 15мл 2,5М раствора, можно определить по формуле:

где
С(В) – молярная концентрация вещества (В), m(B) – масса растворённого вещества (В), М(В) – молярная масса вещества (В), V – объём раствора.
Тогда

По этому же уравнению рассчитаем объём раствора, который можно приготовить из 3,675г H2SO4:

Ответ: 75мл.
Задача 423.
Какой объем 0,1М раствора H3PO4 можно приготовить из 75 мл 0,75н. раствора?
Решение:
Для решения задачи используем формулы:

где
СЭ(В) – молярная концентрация эквивалента вещества (В);
С(В) — молярная концентрация вещества (В);
МЭ(В) – молярная масса эквивалента вещества (В);
M(B) — молярная масса вещества (В);
m(B) – масса растворённого вещества (В);
V(мл) – объём раствора.
Определим молярную массу эквивалента H3PO4 из соотношения:
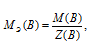
МЭ(В) — молярная масса эквивалента кислоты, г/моль; М(В) — молярная масса кислоты; Z(В) — эквивалентное число; Z(кислоты) равно числу ионов H+ в H3PO4 → 3.
Отсюда

Рассчитаем массу ортофосфорной кислоты:

Определим объём раствора H3PO4, необходимого для приготовления раствора:

Ответ: 185,7мл.
Задача 424.
Какой объем 6,0М раствора НСI нужно взять для приготовления 25 мл 2,5М раствора НСI?
Решение:
Для нахождения массы соляной кислоты, содержащейся в 25 мл 2,5М раствора, а также объёма 6,0М раствора можно использовать формулу:

С(В) — молярная концентрация вещества (В);
M(B) — молярная масса вещества (В);
m(B) – масса растворённого вещества (В);
V(мл) – объём раствора.
Тогда

Ответ: 10,42мл.
Задача 425.
Плотность 40%-ного (по массе) раствора HNO3 равна 1,25г/мл. Рассчитать молярность и моляльность этого раствора.
Решение:
Молярная(объёмно-молярная) концентрация показывает число молей растворённого вещества, содержащихся в 1 литре раствора.
Массу HNO3, содержащуюся в 1 литре раствора, рассчитаем по формуле:

где — массовая доля растворённого вещества; m(в-ва) — масса растворённого вещества; m(р-ра) — масса раствора.
— массовая доля растворённого вещества; m(в-ва) — масса растворённого вещества; m(р-ра) — масса раствора.
Тогда

Молярную концентрацию раствора (CM) получим делением числа граммов HNO3 в 1л раствора на молярную массу HCl (36,5г/моль):

Моляльная концентрация (или моляльность) показывает число молей растворённого вещества, содержащихся в 1000г растворителя.
Находим, сколько граммов HNO3 приходится на 1000г воды, составив пропорцию:

Теперь рассчитаем моляльность раствора:

Ответ: 7,94 моль/л; 10б=,58 моль/л.
Задача 426.
Вычислить массовую долю гидроксида натрия в 9,28н. растворе NaOН (р = 1,310г/мл).
Решение:
Найдём массу NaOН, содержащуюся в 1000 мл раствора из пропорции:

Масса 1 литра раствора NaOН (р = 1,310г/мл) равна 1310г (1000 . 1,310 = 1310).
Массовую долю гидроксида натрия вычислим по формуле:

где — массовая доля растворённого вещества; m(в-ва) — масса растворённого вещества; m(р-ра) — масса раствора.
— массовая доля растворённого вещества; m(в-ва) — масса растворённого вещества; m(р-ра) — масса раствора.
Тогда

Ответ: 28,34%.
Задача 421.
Сколько миллилитров 96%-ного (по массе) раствора H2SO4 (р = 1,84 г/мл) нужно взять для приготовления 1л 0,25 н. раствора?
Решение:
Определим молярную массу эквивалента H2SO4 из соотношения:

где
MЭ(В) — молярная масса эквивалента соли, г/моль; М(В) — молярная масса соли; n — коэффициент при атоме металла; A — валентность металла.
Отсюда

Рассчитаем массу H2SO4 в 1л 0,25н раствора по формуле:

где
m(B) — масса вещества; mЭ(В) — молярная масса эквивалента вещества, г; СЭ(В) — эквива-лентная концентрация или нормальность; V — объём раствора.
Отсюда

Теперь рассчитаем массу раствора, если известны массовая доля H2SO4 (96%) и масса H2SO4 (12,25г) по формуле:

где — массовая доля растворённого вещества; m(в-ва) — масса растворённого вещества; m(р-ра) — масса раствора.
— массовая доля растворённого вещества; m(в-ва) — масса растворённого вещества; m(р-ра) — масса раствора.
Тогда

Определим объём раствора H2SO4, необходимого для приготовления 1л 0,25н раствора по формуле: m = pV, где p — плотность раствора, V — объём раствора.
Тогда

Ответ: 6,93 мл.
Задача 422.
Сколько миллилитров 0,5М раствора H2SO4 можно приготовить из 15 мл 2,5М раствора?
Решение:
Для нахождения массы серной кислоты, содержащейся в 15мл 2,5М раствора, можно определить по формуле:

где
С(В) – молярная концентрация вещества (В), m(B) – масса растворённого вещества (В), М(В) – молярная масса вещества (В), V – объём раствора.
Тогда

По этому же уравнению рассчитаем объём раствора, который можно приготовить из 3,675г H2SO4:

Ответ: 75мл.
Задача 423.
Какой объем 0,1М раствора H3PO4 можно приготовить из 75 мл 0,75н. раствора?
Решение:
Для решения задачи используем формулы:

где
СЭ(В) – молярная концентрация эквивалента вещества (В);
С(В) — молярная концентрация вещества (В);
МЭ(В) – молярная масса эквивалента вещества (В);
M(B) — молярная масса вещества (В);
m(B) – масса растворённого вещества (В);
V(мл) – объём раствора.
Определим молярную массу эквивалента H3PO4 из соотношения:
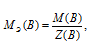
МЭ(В) — молярная масса эквивалента кислоты, г/моль; М(В) — молярная масса кислоты; Z(В) — эквивалентное число; Z(кислоты) равно числу ионов H+ в H3PO4 → 3.
Отсюда

Рассчитаем массу ортофосфорной кислоты:

Определим объём раствора H3PO4, необходимого для приготовления раствора:

Ответ: 185,7мл.
Задача 424.
Какой объем 6,0М раствора НСI нужно взять для приготовления 25 мл 2,5М раствора НСI?
Решение:
Для нахождения массы соляной кислоты, содержащейся в 25 мл 2,5М раствора, а также объёма 6,0М раствора можно использовать формулу:

С(В) — молярная концентрация вещества (В);
M(B) — молярная масса вещества (В);
m(B) – масса растворённого вещества (В);
V(мл) – объём раствора.
Тогда

Ответ: 10,42мл.
Задача 425.
Плотность 40%-ного (по массе) раствора HNO3 равна 1,25г/мл. Рассчитать молярность и моляльность этого раствора.
Решение:
Молярная(объёмно-молярная) концентрация показывает число молей растворённого вещества, содержащихся в 1 литре раствора.
Массу HNO3, содержащуюся в 1 литре раствора, рассчитаем по формуле:

где — массовая доля растворённого вещества; m(в-ва) — масса растворённого вещества; m(р-ра) — масса раствора.
— массовая доля растворённого вещества; m(в-ва) — масса растворённого вещества; m(р-ра) — масса раствора.
Тогда

Молярную концентрацию раствора (CM) получим делением числа граммов HNO3 в 1л раствора на молярную массу HCl (36,5г/моль):

Моляльная концентрация (или моляльность) показывает число молей растворённого вещества, содержащихся в 1000г растворителя.
Находим, сколько граммов HNO3 приходится на 1000г воды, составив пропорцию:

Теперь рассчитаем моляльность раствора:

Ответ: 7,94 моль/л; 10б=,58 моль/л.
Задача 426.
Вычислить массовую долю гидроксида натрия в 9,28н. растворе NaOН (р = 1,310г/мл).
Решение:
Найдём массу NaOН, содержащуюся в 1000 мл раствора из пропорции:

Масса 1 литра раствора NaOН (р = 1,310г/мл) равна 1310г (1000 . 1,310 = 1310).
Массовую долю гидроксида натрия вычислим по формуле:

где — массовая доля растворённого вещества; m(в-ва) — масса растворённого вещества; m(р-ра) — масса раствора.
— массовая доля растворённого вещества; m(в-ва) — масса растворённого вещества; m(р-ра) — масса раствора.
Тогда

Ответ: 28,34%.
