Какая функциональная группа придает аминокислоте кислые щелочные свойства

- Главная
- Вопросы & Ответы
- Вопрос 3854151
 Гость:
Гость:
8 Января в 16:53
12
1
Лучший ответ:


Гость:
б.Кислые — карбоксильной группы , щелочные аминогруппа
8 Января в 16:56
Ваш ответ (не менее 20 символов):
Ваше имя (не менее 2 символов):

Лучшее из галереи:































Другие вопросы:
 Гость:
Гость:
Рассчитайте объем, который занимает (при н.у.) порция газа, если в этой порции содержитсясодержится 6,187·10^22 молекул этого газа.
8 Января в 16:53
Смотреть ответ
7
1
 Гость:
Гость:
Пенсия бабушки составляет 1500 рублей. Какой будет пенсия после повышения на 20%? Задача должна быть в два действия) И еще, кто может, решите плиз- Зарплата работника в этом месяце увеличилась на 10% и составила 7700 рублей. Какова была зарплата в прошлом месяце?задача в три действия) . 1. Сколько…
8 Января в 16:52
Смотреть ответ
13
1
 Гость:
Гость:
(952-x)-137=255 Помогите пожалуйста решить уравнение
8 Января в 16:52
Смотреть ответ
12
1
 Гость:
Гость:
Фонетический разбор слова-встречаются
8 Января в 16:51
Смотреть ответ
8
1
 Гость:
Гость:
Какие страны лидируют по объёму экономики
8 Января в 16:51
Смотреть ответ
15
1
Среди
азотсодержащих органических веществ имеются соединения с двойственной функцией.
Особенно важными из них являются аминокислоты.
В клетках и тканях живых организмов
встречается около 300 различных аминокислот, но только 20 (α-аминокислоты) из них служат звеньями (мономерами), из которых построены пептиды и
белки всех организмов (поэтому их называют белковыми аминокислотами).
Последовательность расположения этих аминокислот в белках закодирована в
последовательности нуклеотидов соответствующих генов. Остальные аминокислоты
встречаются как в виде свободных молекул, так и в связанном виде. Многие из
аминокислот встречаются лишь в определенных организмах, а есть и такие, которые
обнаруживаются только в одном из великого множества описанных организмов.
Большинство микроорганизмов и растения синтезируют необходимые им аминокислоты;
животные и человек не способны к образованию так называемых незаменимых
аминокислот, получаемых с пищей. Аминокислоты участвуют в обмене белков и
углеводов, в образовании важных для организмов соединений (например, пуриновых
и пиримидиновых оснований, являющихся неотъемлемой частью нуклеиновых кислот),
входят в состав гормонов, витаминов, алкалоидов, пигментов, токсинов,
антибиотиков и т. д.; некоторые аминокислоты служат посредниками при передаче
нервных импульсов.
Аминокислоты — органические амфотерные соединения, в состав
которых входят карбоксильные группы – СООН и аминогруппы -NH2.
Аминокислоты можно рассматривать как
карбоновые кислоты, в молекулах которых атом водорода в радикале замещен
аминогруппой.
КЛАССИФИКАЦИЯ

Аминокислоты классифицируют по структурным признакам.
1.
В
зависимости от взаимного расположения амино- и карбоксильной групп аминокислоты
подразделяют на α-, β-, γ-, δ-, ε- и
т. д.
2.
В
зависимости от количества функциональных групп различают кислые, нейтральные и
основные.
3.
По
характеру углеводородного радикала различают алифатические (жирные), ароматические,
серосодержащие и гетероциклические
аминокислоты. Приведенные выше аминокислоты относятся к жирному ряду.
Примером
ароматической аминокислоты может служить пара-аминобензойная
кислота:
Примером
гетероциклической аминокислоты может служить триптофан – незаменимая α- аминокислота
НОМЕНКЛАТУРА
По систематической номенклатуре названия
аминокислот образуются из названий соответствующих кислот прибавлением
приставки амино- и указанием места расположения аминогруппы по отношению
к карбоксильной группе. Нумерация углеродной цепи с атома углерода карбоксильной группы.
Например:
Часто используется также другой способ
построения названий аминокислот, согласно которому к тривиальному названию
карбоновой кислоты добавляется приставка амино- с указанием положения
аминогруппы буквой греческого алфавита.
Пример:
Для α-аминокислот R-CH(NH2)COOH

, которые играют исключительно важную
роль в процессах жизнедеятельности животных и растений, применяются тривиальные
названия.
Таблица. Некоторые важнейшие α-аминокислоты
Аминокислота | Сокращённое обозначение | Строение радикала ( R ) |
Глицин | Gly (Гли) | H — |
Аланин | Ala (Ала) | CH3 — |
Валин | Val (Вал) | (CH3)2CH — |
Лейцин | Leu (Лей) | (CH3)2CH – CH2 — |
Серин | Ser (Сер) | OH- CH2 — |
Тирозин | Tyr (Тир) | HO – C6H4 – CH2 — |
Аспарагиновая кислота | Asp (Асп) | HOOC – CH2 — |
Глутаминовая кислота | Glu (Глу) | HOOC – CH2 – CH2 — |
Цистеин | Cys (Цис) | HS – CH2 — |
Аспарагин | Asn (Асн) | O = C – CH2 – │ NH2 |
Лизин | Lys (Лиз) | NH2 – CH2- CH2 – CH2 — |
Фенилаланин | Phen (Фен) | C6H5 – CH2 — |
Если
в молекуле аминокислоты содержится две аминогруппы, то в ее названии
используется приставка диамино-, три группы NH2 – триамино-
и т.д.
Пример:
Наличие
двух или трех карбоксильных групп отражается в названии суффиксом –диовая
или -триовая кислота:
ИЗОМЕРИЯ
1. Изомерия углеродного скелета
2. Изомерия положения функциональных
групп
3. Оптическая изомерия
α-аминокислоты, кроме глицина NН2-CH2-COOH.
ФИЗИЧЕСКИЕ СВОЙСТВА
Аминокислоты представляют собой
кристаллические вещества с высокими (выше 250°С) температурами плавления,
которые мало отличаются у индивидуальных аминокислот и поэтому нехарактерны.
Плавление сопровождается разложением вещества. Аминокислоты хорошо растворимы в
воде и нерастворимы в органических растворителях, чем они похожи на
неорганические соединения. Многие аминокислоты обладают сладким вкусом.
ПОЛУЧЕНИЕ
3. Микробиологический синтез. Известны микроорганизмы, которые
в процессе жизнедеятельности продуцируют α — аминокислоты белков.
ХИМИЧЕСКИЕ СВОЙСТВА
Аминокислоты
амфотерные органические соединения, для них характерны кислотно-основные
свойства.
I.Общие свойства
1. Внутримолекулярная нейтрализация → образуется биполярный цвиттер-ион:
Водные
растворы электропроводны. Эти свойства объясняются тем, что молекулы
аминокислот существуют в виде внутренних солей, которые образуются за счет
переноса протона от карбоксила к аминогруппе:
цвиттер-ион
Водные растворы аминокислот имеют нейтральную, кислую
или щелочную среду в зависимости от количества функциональных групп.
Видео-опыт «Свойства аминоуксусной кислоты»
2. Поликонденсация→ образуются полипептиды (белки):
При взаимодействии двух
α-аминокислот образуется дипептид.
3. Разложение → Амин +
Углекислый газ:
NH2-CH2-COOH → NH2-CH3 + CO2↑
II. Свойства карбоксильной группы
(кислотность)
1. С основаниями → образуются соли:
NH2-CH2-COOH
+ NaOH → NH2-CH2-COONa + H2O
NH2-CH2-COONa — натриевая соль 2-аминоуксусной кислоты
2. Со спиртами → образуются сложные
эфиры – летучие вещества (р.
этерификации): NH2-CH2-COOH
+ CH3OH HCl(газ)→ NH2-CH2-COOCH3
+ H2O
NH2-CH2-COOCH3 — метиловый эфир 2- аминоуксусной кислоты
3. С аммиаком → образуются
амиды:
NH2-CH(R)-COOH + H-NH2 →
NH2-CH(R)-CONH2 + H2O
4. Практическое значение имеет
внутримолекулярное взаимодействие функциональных групп ε-аминокапроновой
кислоты, в результате которого образуется ε-капролактам (полупродукт для
получения капрона):
III. Свойства аминогруппы (основность)
1. С сильными кислотами → соли:
HOOC-CH2-NH2 + HCl → [HOOC-CH2-NH3]Cl
или HOOC-CH2-NH2*HCl
2. С азотистой кислотой (подобно
первичным аминам):
NH2-CH(R)-COOH +
HNO2 → HO-CH(R)-COOH + N2↑+ H2O
гидроксокислота
Измерение
объёма выделившегося азота позволяет определить количество аминокислоты (метод
Ван-Слайка)
IV.Качественная реакция
1. Все аминокислоты окисляются
нингидрином с образованием продуктов сине-фиолетового цвета!
2. С ионами тяжелых металлов α-аминокислоты
образуют внутрикомплексные соли. Комплексы меди (II), имеющие глубокую
синюю окраску, используются для обнаружения α-аминокислот.
Видео-опыт «Образование медной соли аминоуксусной кислоты».
ПРИМЕНЕНИЕ
1) аминокислоты широко
распространены в природе;
2) молекулы аминокислот – это те
кирпичики, из которых построены все растительные и животные белки;
аминокислоты, необходимые для построения белков организма, человек и животные
получают в составе белков пищи;
3) аминокислоты прописываются при
сильном истощении, после тяжелых операций;
4) их используют для питания
больных;
5) аминокислоты необходимы в
качестве лечебного средства при некоторых болезнях (например, глутаминовая
кислота используется при нервных заболеваниях, гистидин – при язве желудка);
6) некоторые аминокислоты
применяются в сельском хозяйстве для подкормки животных, что положительно
влияет на их рост;
7) имеют техническое значение:
аминокапроновая и аминоэнантовая кислоты образуют синтетические волокна –
капрон и энант.
О РОЛИ АМИНОКИСЛОТ
Нахождение в природе и биологическая роль аминокислот
Аминокислоты являются амфотерными соединениями, для них характерны кислотно-основные свойства. Это обусловлено наличием в их молекулах функциональных групп кислотного (-СООН) и основного (-NH2) характера.
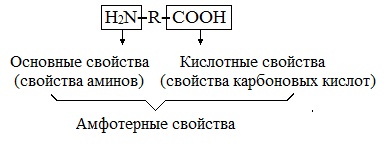
Кислотно-основное равновесие в водных растворах
В водных растворах и твердом состоянии аминокислоты существуют в виде внутренних солей.
Ионизация молекул аминокислот в водных растворах зависит от кислотного или щелочного характера среды:
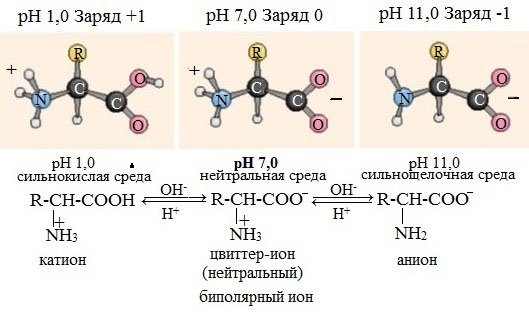
В кислой среде молекулы аминокислот представляю собой катион. В щелочной среде молекулы аминокислот представляют собой анион. В нейтральной среде аминокислоты представляют собой цвиттер-ион или биполярный ион.
Аминокислоты в твердом состоянии всегда существуют в виде биполярного, двухзарядного иона — цвиттер-иона.
Водные растворы аминокислот в кислой и щелочной среде проводят электрический ток.
1. Взаимодействие внутри молекулы – образование внутренних солей (биполярных ионов)
Молекулы аминокислот существуют в виде внутренних солей, которые образуются за счет переноса протона от карбоксила к аминогруппе.
Карбоксильная группа аминокислоты отщепляет ион водорода, который затем присоединяется к аминогруппе той же молекулы по месту неподеленной электронной пары азота. В результате действие функциональных групп нейтрализуется, образуется так называемая внутренняя соль.
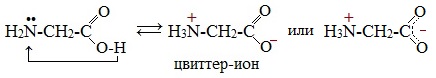
Водные растворы аминокислот в зависимости от количества функциональных групп имеют нейтральную, кислую или щелочную среду.
Аминокислоты с одной карбоксильной группой и одной аминогруппой имеют нейтральную реакцию.
Видеоопыт «Свойства аминоуксусной кислоты»
а) моноаминомонокарбоновые кислоты (нейтральные кислоты)
Внутримолекулярная нейтрализация — образуется биполярный цвиттер-ион.
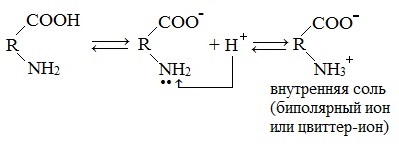
Водные растворы моноаминомонокарбоновых кислот нейтральны (рН≈7).
б) моноаминодикарбоновые кислоты (кислые аминокислоты)
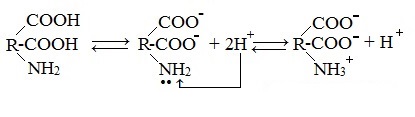
Водные растворы моноаминодикарбоновых кислот имеют рН<7 (кислая среда), так как в результате образования внутренних солей этих кислот в растворе появляется избыток ионов водорода Н+.
в) диаминомонокарбоновые кислоты (основные аминокислоты)
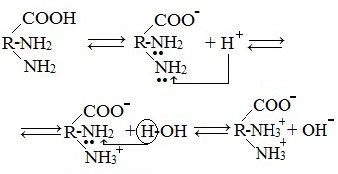
Водные растворы диаминомонокарбоновых кислот имеют рН>7 (щелочная среда), так как в результате образования внутренних солей этих кислот в растворе появляется избыток гидроксид-ионов ОН— .
2. Взаимодействие с основаниями и кислотами
Аминокислоты как амфотерные соединения образуют соли как с кислотами (по группе NH2), так и со щелочами (по группе СООН).
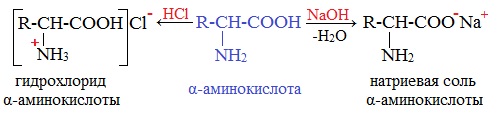
Как кислота (участвует карбоксильная группа)
Как карбоновые кислоты α-аминокислоты образуют функциональные производные: соли, сложные эфиры, амиды.
а) взаимодействие с основаниями
Образуются соли:
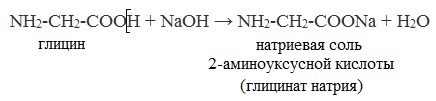
б) взаимодействие со спиртами (р. этерификации)
Аминокислоты могут реагировать со спиртами в присутствии газообразного хлороводорода, превращаясь в сложный эфир. Сложные эфиры аминокислот не имеют биполярной структуры и являются летучими соединениями.
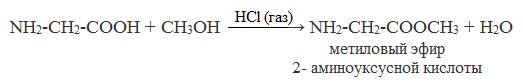
в) взаимодействие с аммиаком
Образуются амиды:
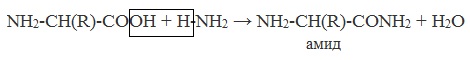
Как основание (участвует аминогруппа)
а) взаимодействие с сильными кислотами
Подобно аминам, аминокислоты реагируют с сильными кислотами с образованием солей аммония:
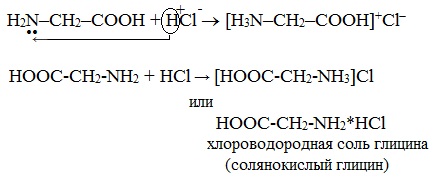
б) взаимодействие с азотистой кислотой (р. дезаминирования)
Подобно первичным аминам, аминокислоты реагируют с азотистой кислотой, при этом аминогруппа превращается в гидроксогруппу, а аминокислота – в гидроксикислоту:
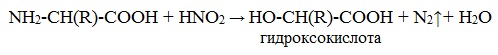
Измерение объёма выделившегося азота позволяет определить количество аминокислоты (метод Ван-Слайка).
3. Внутримолекулярное взаимодействие функциональных групп ε-аминокапроновой кислоты, в результате которого образуется ε-капролактам (полупродукт для получения капрона).
4. Межмолекулярное взаимодействие α-аминокислот – образование пептидов (р. поликонденсации)
При взаимодействии карбоксильной группы одной молекулы аминокислоты и аминогруппы другой молекулы аминокислоты образуются пептиды. При взаимодействии двух α-аминокислот образуется дипептид.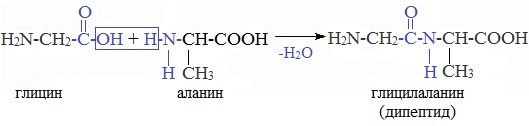
Межмолекулярная реакция с участием трех α-аминокислот приводит к образованию трипептида и т.д.
Важнейшие природные полимеры – белки (протеины) – относятся к полипептидам, т.е представляют собой продукт поликонденсации a-аминокислот.
5. Качественные реакции!
а) нингидриновая реакция
Все аминокислоты окисляются нингидрином с образованием продуктов сине-фиолетового цвета:
Иминокислота пролин дает с нингидрином желтое окрашивание.
б) с ионами тяжелых металлов α-аминокислоты образуют внутрикомплексные соли. Комплексы меди (II), имеющие глубокую синюю окраску, используются для обнаружения α-аминокислот.
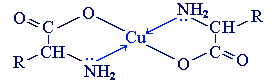
Видеоопыт «Образование медной соли аминоуксусной кислоты»
Аминокислоты

Химический состав клетки Семинар

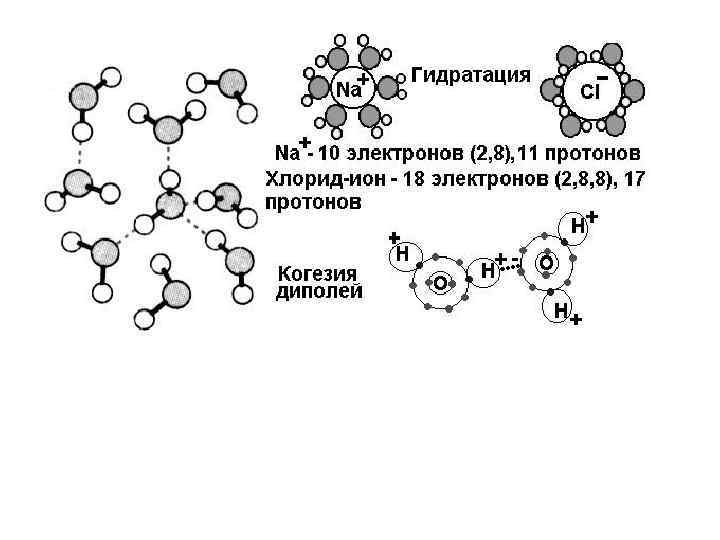
1. Какие элементы называются биогенными? Сколько их? 2. На какие группы делятся макроэлементы? 3. Чем ковалентные связи отличаются от водородных? 4. Почему лед образуется на поверхности воды? 5. Какие вещества называются гидрофобными? Гидрофильными? 6. Какой заряд на атоме кислорода и на атомах водорода в молекуле воды? Почему? 7. Сколько водородных связей может образовывать одна молекула воды? 8. Почему ион натрия имеет положительный заряд? 9. Почему ион хлора имеет отрицательный заряд?

1. К моносахаридам относятся: 1. Крахмал. 5. Свекловичный сахар (сахароза). 2. Гликоген. 6. Мальтоза. 3. Глюкоза. 7. Молочный сахар (лактоза). 4. Дезоксирибоза. 8. Рибоза. 2. К полисахаридам относятся: 1. Крахмал. 5. Рибоза. 2. Гликоген. 6. Мальтоза. 3. Глюкоза. 7. Молочный сахар (лактоза). 4. Дезоксирибоза. 8. Целлюлоза. 3. К дисахаридам относятся: 1. Крахмал. 2. Свекловичный сахар (сахароза). 3. Глюкоза. 4. Дезоксирибоза. 5. Хитин. 6. Мальтоза. 7. Молочный сахар (лактоза). 8. Целлюлоза.
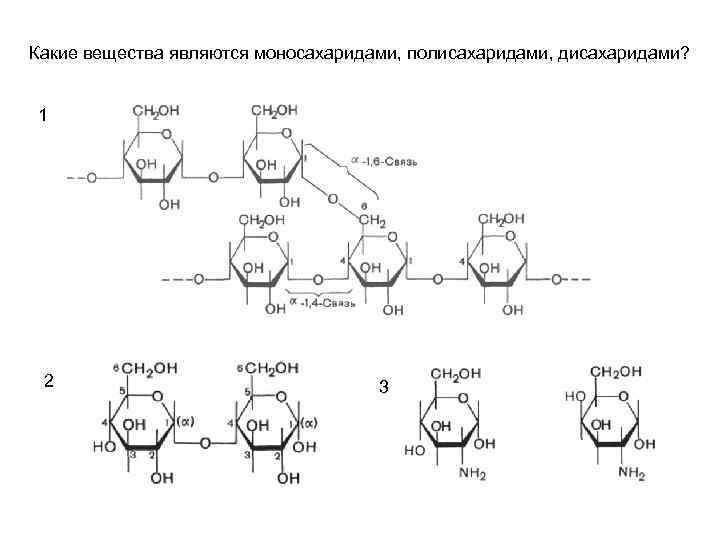
Какие вещества являются моносахаридами, полисахаридами, дисахаридами? 1 2 3
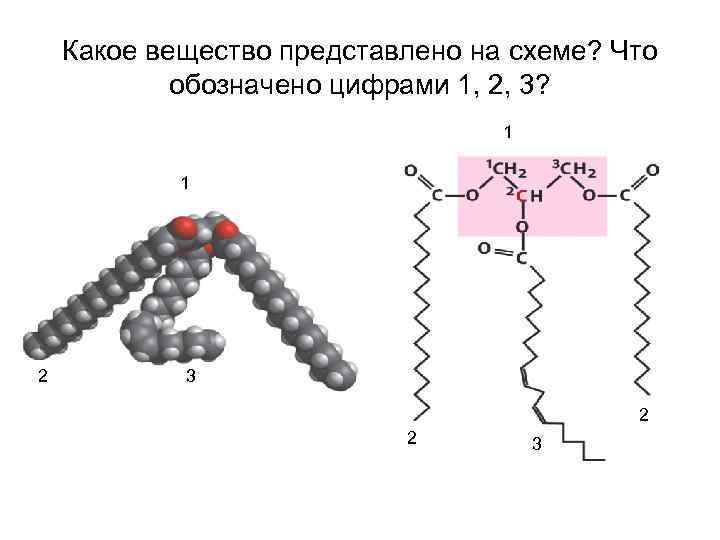
Какое вещество представлено на схеме? Что обозначено цифрами 1, 2, 3? 1 1 2 3 2 2 3

1. При полном сгорании 1 г. вещества выделилось 38, 9 к. Дж энергии. Это вещество относится: 1. К углеводам. 2. К жирам. 3. Или к углеводам, или к липидам. 4. К белкам. 2. Основу клеточных мембран образуют: 1. Жиры. 2. Фосфолипиды. 3. Воска. 4. Липиды. 3. Утверждение: «Фосфолипиды — сложные эфиры глицерина (глицерола) и жирных кислот»: Верно. Ошибочно.

4. Липиды выполняют в организме следующие функции: 1. Структурную. 5. Некоторые являются ферментами. 2. Энергетическую. 6. Источник метаболической воды 3. Теплоизолирующую. 7. Запасающую. 4. Некоторые — гормоны. 8. К ним относятся витамины A, D, E, K. 5. Молекула жира состоит из остатков: 1. Аминокислот. 2. Нуклеотидов. 3. Глицерина. 4. Жирных кислот. 6. Гликопротеины — это комплекс: 1. Белков и углеводов. 2. Нуклеотидов и белков. 3. Глицерина и жирных кислот. 4. Углеводов и липидов.
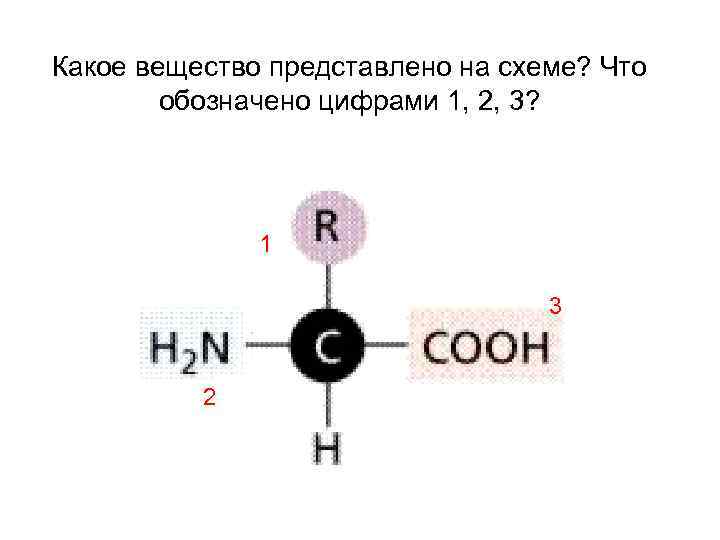
Какое вещество представлено на схеме? Что обозначено цифрами 1, 2, 3? 1 3 2
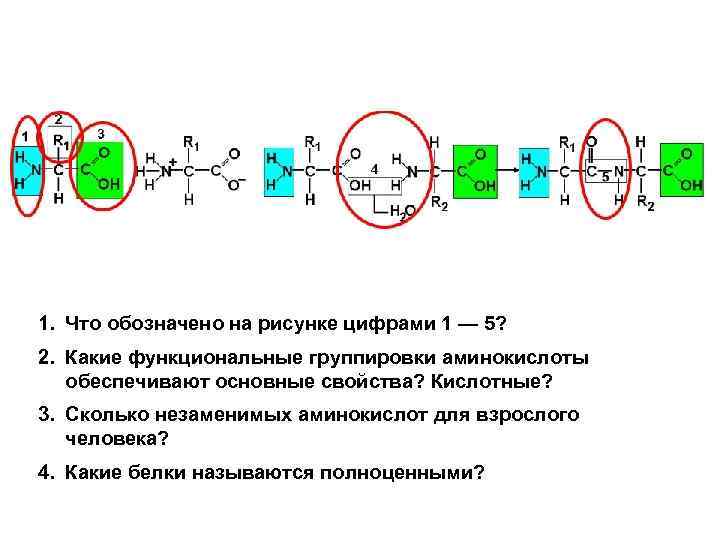
1. Что обозначено на рисунке цифрами 1 — 5? 2. Какие функциональные группировки аминокислоты обеспечивают основные свойства? Кислотные? 3. Сколько незаменимых аминокислот для взрослого человека? 4. Какие белки называются полноценными?

1. На первом месте по массе из органических веществ в клетке находятся: 1. Углеводы. 2. Белки. 3. Липиды. 4. Нуклеиновые кислоты. 2. В состав простых белков входят следующие элементы: 1. Углерод. 5. Фосфор. 2. Водород. 6. Азот. 3. Кислород. 7. Железо. 4. Сера. 8. Хлор. 3. Количество различных стандартных аминокислот, встречающихся в белках: 1. 170. 2. 26. 3. 20. 4. 10.

4. Количество незаменимых для человека аминокислот: 1. Таких аминокислот нет. 2. 20. 3. 10. 4. 7. 5. Неполноценные белки — белки: 1. В которых отсутствуют некоторые аминокислоты. 2. В которых отсутствуют некоторые незаменимые аминокислоты. 3. В которых отсутствуют некоторые заменимые аминокислоты. 4. Все известные белки являются полноценными. 6. Придают аминокислотам свойства: 1. Кислые — радикал, щелочные — аминогруппа. 2. Кислые — аминогруппа, щелочные — радикал. 3. Кислые — карбоксильная группа, — щелочные — радикал. 4. Кислые — карбоксильная группа, щелочные — аминогруппа.

7. Пептидная связь образуется в результате: 1. Реакции гидролиза. 2. Реакции гидратации. 3. Реакции конденсации. 4. Все выше перечисленные реакции могут привести к образованию пептидной связи. 8. Пептидная связь образуется: 1. Между карбоксильными группами соседних аминокислот. 2. Между аминогруппами соседних аминокислот. 3. Между аминогруппой одной аминокислоты и радикалом другой. 4. Между аминогруппой одной аминокислоты и карбоксильной группой другой. 9. Вторичную структуру белков стабилизируют: 1. Ковалентные. 2. Водородные. 3. Ионные. 4. Такие связи отсутствуют.

10. Третичную структуру белков стабилизируют: 1. Ковалентные. 2. Водородные. 3. Ионные. 4. Гидрофильно-гидрофобное взаимодействие. 5. Все выше перечисленные виды связей. 11. Верные суждения: 1. Ферменты специфичны, каждый фермент обеспечивает реакции одного типа. 2. Ферменты универсальны и могут катализировать реакции разных типов. 3. Каталитическая активность ферментов не зависит от р. Н и температуры. 4. Каталитическая активность ферментов напрямую зависит от р. Н и температуры. 12. Верное суждение: 1. Все белки являются биологическими катализаторами, ферментами. 2. Ренатурация — утрата трехмерной конфигурации белка без изменения первичной структуры. 3. Витамины являются коферментами многих ферментов.

Какое вещество представлено на рисунке? Что обозначено цифрами 1, 2, 3, 4? 3 4 2 1
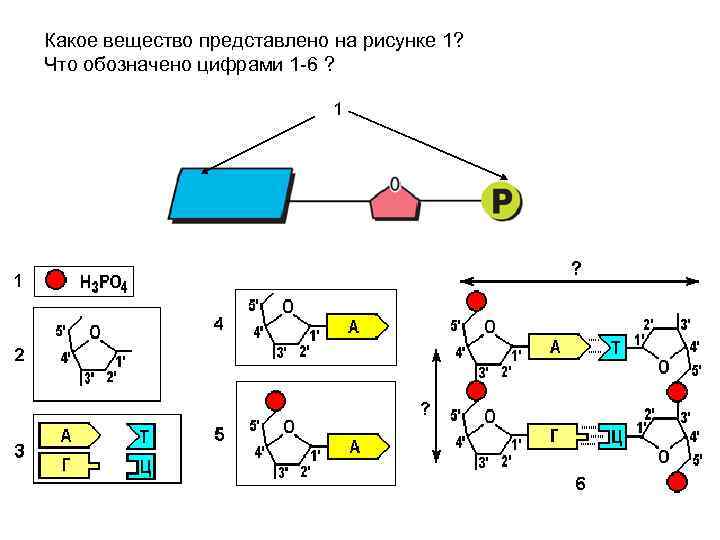
Какое вещество представлено на рисунке 1? Что обозначено цифрами 1 -6 ? 1

1. ДНК в клетках эукариот содержится: 1. В цитоплазме. 5. В пластидах. 2. В ядре. 6. В комплексе Гольджи. 3. В рибосомах. 4. В митохондриях. 2. Размеры молекулы ДНК у человека: 1. Ширина 20 мкм, длина до 8 см. 2. Ширина 2 мкм, длина до 8 см. 3. Ширина 20 нм, длина до 8 см. 4. Ширина 2 нм, длина до 8 см. 3. В состав молекулы ДНК входят пуриновые основания: 1. Аденин. 2. Гуанин. 3. Тимин. 4. Цитозин.

4. Фрагмент ДНК содержит 30000 нуклеотидов. Для удвоения фрагмента потребуется свободных нуклеотидов: 1. 60000. 2. 45000. 3. 30000. 4. 15000. 5. Нуклеотиды ДНК соединены в одну цепь: 1. Через остаток фосфорной кислоты одного нуклеотида и 3′ атом дезоксирибозы другого. 2. Через остаток фосфорной кислоты одного нуклеотида и азотистое основание другого. 3. Через остатки фосфорной кислоты соседних нуклеотидов. 4. Через дезоксирибозы соседних нуклеотидов.

