В каком виде йод содержится в водорослях

Запрос «Йод» перенаправляется сюда; см. также другие значения.
О реке в Республике Коми см. Ёд.
| Иод | ||||
|---|---|---|---|---|
| ← Теллур | Ксенон → | ||||
| ||||
| Блестящий тёмно-серый неметалл. В газообразном состоянии — фиолетовый. | ||||
Элементарный иод | ||||
| Название, символ, номер | Иод / Iodum (I), 53 | |||
| Атомная масса (молярная масса) | 126,90447(3)[1] а. е. м. (г/моль) | |||
| Электронная конфигурация | [Kr] 4d10 5s2 5p5 | |||
| Радиус атома | 136 пм | |||
| Ковалентный радиус | 133 пм | |||
| Радиус иона | (+7e) 50 (-1e) 220 пм | |||
| Электроотрицательность | 2,66 (шкала Полинга) | |||
| Электродный потенциал | +0,535 В | |||
| Степени окисления | +7, +5, +3, +1, 0, −1 | |||
| Энергия ионизации (первый электрон) | 1008,3 (10,45) кДж/моль (эВ) | |||
| Плотность (при н. у.) | 4,93 г/см³ | |||
| Температура плавления | 113,5 °C | |||
| Температура кипения | 184,35 °C | |||
| Уд. теплота плавления | 15,52 (I—I) кДж/моль | |||
| Уд. теплота испарения | 41,95 (I—I) кДж/моль | |||
| Молярная теплоёмкость | 54,44[2] Дж/(K·моль) | |||
| Молярный объём | 25,7 см³/моль | |||
| Структура решётки | орторомбическая | |||
| Параметры решётки | a=7,18 b=4,71 c=9,81[3] | |||
| Отношение c/a | — | |||
| Теплопроводность | (300 K) (0,45) Вт/(м·К) | |||
| Номер CAS | 7553-56-2 | |||
Ио́д[4] (тривиальное (общеупотребительное) название — йод[5]; от греч. ἰώδης — «фиалковый (фиолетовый)») — химический элемент с атомным номером 53[6]. Принадлежит к 17-й группе периодической таблицы химических элементов (по устаревшей короткой форме периодической системы принадлежит к главной подгруппе VII группы, или к группе VIIA), находится в пятом периоде таблицы. Атомная масса элемента 126,90447 а. е. м.[1]. Обозначается символом I (от лат. Iodum). Химически активный неметалл, относится к группе галогенов.
Фазовая диаграмма иода: тройная точка 386,65 К (113,5 °С), 12,1 кПа (0,12 атм); критическая точка 819 К (546 °С), 11,7 МПа (115 атм)
Ниже температуры тройной точки на диаграмме фазового равновесия имеется только линия сублимации. Поэтому при относительно медленном (квазистатическом) нагреве в открытой системе, когда подавляющая часть подводимой от нагревателя энергии расходуется на фазовый переход (возгонку), а не на повышение температуры твёрдой фазы, иод не плавясь возгоняется и превращается сразу в пары. Наоборот, при охлаждении иод десублимируется и образует кристаллы минуя жидкое состояние. Для превращения в жидкость твёрдый иод нагревают в закрытом сосуде. При очень быстром (нестатическом) нагреве иод плавится даже в открытом сосуде.
Простое вещество иод при нормальных условиях — кристаллы чёрно-серого цвета с фиолетовым металлическим блеском, легко образует фиолетовые пары, обладающие резким запахом. Элементарный иод высокотоксичен. Молекула простого вещества двухатомна (формула I2).
Название и обозначение[править | править код]
Название элемента предложено Гей-Люссаком и происходит от др.-греч. ἰο-ειδής (букв. «фиалкоподобный»), что связано с цветом пара, который наблюдал французский химик Бернар Куртуа, нагревая маточный рассол золы морских водорослей с концентрированной серной кислотой. В медицине и биологии данный элемент и простое вещество обычно называют йодом, например, «раствор йода», в соответствии со старым вариантом названия, существовавшим в химической номенклатуре до середины XX века.
В современной химической номенклатуре используется наименование иод. Такое же положение существует в некоторых других языках, например, в немецком: общеупотребительное Jod и терминологически корректное Iod. Одновременно с изменением названия элемента в 1950-х годах Международным союзом общей и прикладной химии символ элемента J был заменён на I[7].
История[править | править код]
Иод был открыт в 1811 г. Куртуа. При кипячении серной кислоты с рассолом золы морских водорослей он наблюдал выделение фиолетового пара, при охлаждении превращающегося в тёмные кристаллы с ярким блеском.
Элементная природа иода установлена в 1811—1813 гг. Л. Ж. Гей-Люссаком (а чуть позже и Х. Дэви). Гей-Люссак получил также многие производные (HI, HIO3, I2O5, ICl и др.). Важнейшим природным источником иода служат буровые воды нефтяных и газовых скважин.
Нахождение в природе[править | править код]
Иод — редкий элемент. Его кларк — всего 400 мг/т. Однако он чрезвычайно сильно рассеян в природе и, будучи далеко не самым распространённым элементом, присутствует практически везде. Иод находится в виде иодидов в морской воде (20—30 мг на тонну морской воды). Присутствует в живых организмах, больше всего в водорослях (2,5 г на тонну высушенной морской капусты, ламинарии). Известен в природе также в свободной форме, в качестве минерала, но такие находки единичны, — в термальных источниках Везувия и на острове Вулькано (Италия). Запасы природных иодидов оцениваются в 15 млн тонн, 99 % запасов находятся в Чили и Японии. В настоящее время в этих странах ведётся интенсивная добыча иода, например, чилийская Atacama Minerals производит свыше 720 тонн иода в год. Наиболее известный из минералов иода — лаутарит Ca(IO3)2. Некоторые другие минералы иода — иодобромит Ag(Br, Cl, I), эмболит Ag(Cl, Br), майерсит CuI·4AgI.
Сырьём для промышленного получения иода в России служат нефтяные буровые воды[8], тогда как в зарубежных странах, не обладающих нефтяными месторождениями, используются морские водоросли, а также маточные растворы чилийской (натриевой) селитры, щёлок калийных и селитряных производств, что намного удорожает производство иода из такого сырья[9].
Физические свойства[править | править код]
Жидкий иод на дне химического стакана
Природный иод является моноизотопным элементом, в его состав входит только один изотоп — иод-127 (см. Изотопы иода). Конфигурация внешнего электронного слоя — 5s2p5. В соединениях проявляет степени окисления −1, 0, +1, +3, +5 и +7 (валентности I, III, V и VII).
Радиус нейтрального атома иода 0,136 нм, ионные радиусы I−, I5+ и I7+ равны, соответственно, 0,206; 0,058—0,109; 0,056—0,067 нм. Энергии последовательной ионизации нейтрального атома иода равны, соответственно: 10,45; 19,10; 33 эВ. Сродство к электрону −3,08 эВ. По шкале Полинга электроотрицательность иода равна 2,66, иод принадлежит к числу неметаллов.
Иод при обычных условиях — твёрдое вещество, чёрно-серые или тёмно-фиолетовые кристаллы со слабым металлическим блеском и специфическим запахом.
Пары имеют характерный фиолетовый цвет, так же, как и растворы в неполярных органических растворителях, например, в бензоле — в отличие от бурого раствора в полярном этиловом спирте. Слабо растворяется в воде (0,28 г/л), лучше растворяется в водных растворах иодидов щелочных металлов с образованием трииодидов (например трииодида калия KI3).
При нагревании при атмосферном давлении иод сублимирует (возгоняется), превращаясь в пары фиолетового цвета; при охлаждении при атмосферном давлении пары иода кристаллизуются, минуя жидкое состояние. Этим пользуются на практике для очистки иода от нелетучих примесей.
Жидкий иод можно получить, нагревая его под давлением.
Изотопы[править | править код]
Известны 37 изотопов иода с массовыми числами от 108 до 144. Из них только 127I является стабильным, период полураспада остальных изотопов иода составляет от 103 мкс до 1,57⋅107 лет[10]; отдельные изотопы используются в терапевтических и диагностических целях.
Радиоактивный нуклид 131I распадается с испусканием β-частиц (наиболее вероятные максимальные энергии — 0,248, 0,334 и 0,606 МэВ), а также с излучением γ-квантов с энергиями от 0,08 до 0,723 МэВ[11].
Химические свойства[править | править код]
Иод относится к группе галогенов.
Электронная формула (Электронная конфигурация) иода: 1s22s22p63s23p63d104s24p64d105s25p5.
Образует ряд кислот: иодоводородную (HI), иодноватистую (HIO), иодистую (HIO2), иодноватую (HIO3), иодную (HIO4).
Химически иод довольно активен, хотя и в меньшей степени, чем хлор и бром.
- Довольно известной качественной реакцией на иод является его взаимодействие с крахмалом[12], при котором наблюдается синее окрашивание в результате образования соединения включения. Эту реакцию открыли в 1814 году Жан-Жак Колен (Jean-Jacques Colin) и Анри-Франсуа Готье де Клобри (Henri-François Gaultier de Claubry)[13].
- С металлами иод при лёгком нагревании энергично взаимодействует, образуя иодиды:
- С водородом иод реагирует только при нагревании и не полностью, образуя иодоводород:
⇄
- Иод является окислителем, менее сильным, чем фтор, хлор и бром. Сероводород H2S, Na2S2O3 и другие восстановители восстанавливают его до иона I−:
Последняя реакция также используется в аналитической химии для определения иода.
- При растворении в воде иод частично реагирует с ней (По «Началам Химии» Кузьменко: реакция не идёт даже при нагревании, текст нуждается в проверке)
pKc=15,99
- Реакция образования аддукта нитрида трииода с аммиаком[14]:
Это вещество почти не имеет практического значения и известно лишь своей способностью разлагаться со взрывом от малейшего прикосновения.
- Иодиды щелочных металлов очень склонны в растворах присоединять (растворять) молекулы галогенов с образованием полииодидов (периодидов) — трииодид калия, дихлороиодат(I) калия:
Применение[править | править код]
В медицине[править | править код]
5 % спиртовой раствор иода
5-процентный спиртовой раствор иода используется для дезинфекции кожи вокруг повреждения (рваной, резаной или иной раны), но не для приёма внутрь при дефиците иода в организме. Продукты присоединения иода к крахмалу (т. н. «Синий йод» — Йодинол, Йокс, Бетадин и др.) являются более мягкими антисептиками.
При большом количестве внутримышечных инъекций, на их месте пациенту делается йодная сетка — йодом рисуется сетка на площади, в которую делаются инъекции (например, на ягодицах). Это нужно для того, чтобы быстро рассасывались «шишки», образовавшиеся в местах внутримышечных инъекций.
В рентгенологических и томографических исследованиях широко применяются йодсодержащие контрастные препараты.
Иод-131, как и некоторые радиоактивные изотопы иода (125I, 132I) применяются в медицине для диагностики и лечения заболеваний щитовидной железы[2]. Изотоп широко применяется при лечении диффузно-токсического зоба (болезни Грейвса), некоторых опухолей. Согласно нормам радиационной безопасности НРБ-99/2009, принятым в России, выписка из клиники пациента, лечившегося с использованием иода-131, разрешается при снижении общей активности этого нуклида в теле пациента до уровня 0,4 ГБк[15].
В криминалистике[править | править код]
В криминалистике пары иода применяются для обнаружения отпечатков пальцев на бумажных поверхностях, например, на купюрах.
В технике: рафинирование металлов[править | править код]
Источники света[править | править код]
Иод используется в источниках света:
- галогеновых лампах — в качестве компонента газового наполнителя колбы для осаждения испарившегося вольфрама нити накаливания обратно на неё.
- металлогалогеновых дуговых лампах — в качестве газовой среды разряда используются галогениды ряда металлов, использование различных смесей которых позволяет получать лампы с большим разнообразием спектральных характеристик.
Производство аккумуляторов[править | править код]
Иод используется в качестве компонента положительного электрода (окислителя) в литиево-ионных аккумуляторах для автомобилей.
Лазерный термоядерный синтез[править | править код]
Некоторые иодорганические соединения применяются для производства сверхмощных газовых лазеров на возбуждённых атомах иода (исследования в области лазерного термоядерного синтеза).
Радиоэлектронная промышленность[править | править код]
В последние годы резко повысился спрос на иод со стороны производителей жидкокристаллических дисплеев.
Динамика потребления иода[править | править код]
Мировое потребление иода в 2005 году составило 25,8 тыс. тонн[источник не указан 1263 дня].
Биологическая роль[править | править код]
Иод относится к микроэлементам и присутствует во всех живых организмах. Его содержание в растениях зависит от присутствия его соединений в почве и водах. Некоторые морские водоросли (морская капуста, ламинария, фукус и другие) накапливают до 1 % иода. Богаты иодом водные растения семейства рясковых. Иод входит в скелетный белок губок и скелетопротеинов морских многощетинковых червей.[источник не указан 378 дней]
Иод и щитовидная железа[править | править код]
У животных и человека иод входит в состав так называемых тиреоидных гормонов, вырабатываемых щитовидной железой — тироксина и трииодтиронина, оказывающих многостороннее воздействие на рост, развитие и обмен веществ организма.
В организме человека (масса тела 70 кг) содержится 12—20 мг иода. Суточная потребность человека в иоде определяется возрастом, физиологическим состоянием и массой тела. Для человека среднего возраста нормальной комплекции (нормостеник) суточная доза иода составляет 0,15 мг[16].
Отсутствие или недостаток иода в рационе (что типично для некоторых местностей) приводит к заболеваниям (эндемический зоб, кретинизм, гипотиреоз). В связи с этим к поваренной соли, поступающей в продажу в местностях с естественным геохимическим дефицитом иода, с профилактической целью добавляют иодид калия, иодид натрия или иодат калия (иодированная соль).
Недостаток иода приводит к заболеваниям щитовидной железы (например, к базедовой болезни, кретинизму).
Также при небольшом недостатке иода отмечается усталость, головная боль, подавленное настроение, природная лень, нервозность и раздражительность; слабеет память и интеллект. Со временем появляется аритмия, повышается артериальное давление, падает уровень гемоглобина в крови.
Избыток йода в пище обычно легко переносится организмом, однако в отдельных случаях в людях с повышенной чувствительностью этот избыток может также привести к расстройствам щитовидной железы[17].
Токсичность[править | править код]
Иод в виде свободного вещества токсичен. Смертельная доза (LD50) — 3 г. Вызывает поражение почек и сердечно-сосудистой системы. При вдыхании паров иода появляется головная боль, кашель, насморк, может быть отёк лёгких. При попадании на слизистую оболочку глаз появляется слезотечение, боль в глазах и покраснение. При попадании внутрь появляется общая слабость, головная боль, повышение температуры, рвота, понос, бурый налёт на языке, боли в сердце и учащение пульса. Через день появляется кровь в моче. Через 2 дня появляются почечная недостаточность и миокардит. Без лечения наступает летальный исход[18].
ПДК иода в воде 0,125 мг/дм³, в воздухе 1 мг/м³. Иод относится ко II классу опасности согласно ГОСТ 12.1.007-76[19].
Радиоактивный иод-131 (радиойод), являющийся бета- и гамма-излучателем, особенно опасен для организма человека, так как радиоактивные изотопы биохимически не отличаются от стабильных. Поэтому почти весь радиоактивный иод, как и обычный, концентрируется в щитовидной железе, что приводит к её облучению и дисфункции. Основным источником загрязнения атмосферы радиоактивным иодом являются атомные станции и фармакологическое производство[20]. В то же время это свойство радиоиода позволяет использовать его для борьбы с опухолями щитовидной железы и диагностики её заболеваний (см. выше).
См. также[править | править код]
- Тиреоидит
- Иодная яма
Примечания[править | править код]
- ↑ 1 2 Michael E. Wieser, Norman Holden, Tyler B. Coplen, John K. Böhlke, Michael Berglund, Willi A. Brand, Paul De Bièvre, Manfred Gröning, Robert D. Loss, Juris Meija, Takafumi Hirata, Thomas Prohaska, Ronny Schoenberg, Glenda O’Connor, Thomas Walczyk, Shige Yoneda, Xiang‑Kun Zhu. Atomic weights of the elements 2011 (IUPAC Technical Report) (англ.) // Pure and Applied Chemistry. — 2013. — Vol. 85, no. 5. — P. 1047—1078. — doi:10.1351/PAC-REP-13-03-02.
- ↑ 1 2 Ксензенко В. И., Стасиневич Д. С. Иод // Химическая энциклопедия: в 5 т. / И. Л. Кнунянц (гл. ред.). — М.: Советская энциклопедия, 1990. — Т. 2: Даффа—Меди. — С. 251—252. — 671 с. — 100 000 экз. — ISBN 5-85270-035-5.
- ↑ WebElements Periodic Table of the Elements | Iodine | crystal structures
- ↑ Такое написание термина зафиксировано в [www.xumuk.ru/encyklopedia/2/2957.html химической номенклатуре], Иод — статья из Большой советской энциклопедии. и БРЭ.
- ↑ Такое написание зафиксировано в нормативных Архивная копия от 20 октября 2011 на Wayback Machine словарях русского языка — «Орфографическом словаре русского языка» Б. З. Букчиной, И. К. Сазоновой, Л. К. Чельцовой (6-е издание, 2010; ISBN 978-5-462-00736-1) и «Грамматическом словаре русского языка» А. А. Зализняка (6-е издание, 2009; ISBN 978-5-462-00766-8).
- ↑ Таблица Менделеева на сайте ИЮПАК.
- ↑ Леенсон И. А. Иод или йод? // Химия и жизнь — XXI век. — 2008. — № 12. — С. 58—59. — ISSN 1727-5903.
- ↑ Пятьдесят третий элемент. Прилив и отлив
- ↑ https://chls.web-box.ru/novosti/pochemu-roshal-protiv-joda (недоступная ссылка)
- ↑ Audi G., Bersillon O., Blachot J., Wapstra A. H. The NUBASE evaluation of nuclear and decay properties // Nuclear Physics A. — 2003. — Т. 729. — С. 3—128. — doi:10.1016/j.nuclphysa.2003.11.001. — Bibcode: 2003NuPhA.729….3A.
- ↑ WWW Table of Radioactive Isotopes (англ.). — Энергетические уровни 131I. Дата обращения 27 марта 2011. Архивировано 22 августа 2011 года.
- ↑ Качественная реакция на йод Архивная копия от 28 июля 2014 на Wayback Machine — видеоопыт в Единой коллекции цифровых образовательных ресурсов
- ↑ См. стр. 92 следующей статьи: Colin, Gaultier de Claubry. Mémoire sur les combinaisons de l’iode avec les substances végétales et animales (фр.) // Annales de chimie (англ.)русск. : magazine. — 1814. — Vol. 90. — P. 87—100.
- ↑ Silberrad, O. The Constitution of Nitrogen Triiodide (англ.) // Journal of the Chemical Society (англ.)русск.. — Chemical Society, 1905. — Vol. 87. — P. 55—66. — doi:10.1039/CT9058700055.
- ↑ «Нормы радиационной безопасности (НРБ-99/2009). Санитарные правила и нормативы СанПин 2.6.1.2523-09» Архивная копия от 24 марта 2012 на Wayback Machine.
- ↑ Дефицит йода и йоддефицитные заболевания
- ↑ Angela M. Leung and Lewis E. Braverman. Consequences of excess iodine // Nat Rev Endocrinol. 2014 Mar; 10(3): 136—142. (англ.)
- ↑ Вредные химические вещества. Неорганические соединения элементов V-VIII групп / под ред. Владимира Филова. — М.: Химия. — С. 400. — 592 с. — 33 000 экз. — ISBN 5-7245-0264-X.
- ↑ ГОСТ 12.1.007-76
- ↑ В воздухе над Германией обнаружен радиоактивный йод, Germania.one.
Ссылки[править | править код]
- Иод / В. П. Зломанов // Излучение плазмы — Исламский фронт спасения. — М. : Большая российская энциклопедия, 2008. — С. 539. — (Большая российская энциклопедия : [в 35 т.] / гл. ред. Ю. С. Осипов ; 2004—2017, т. 11). — ISBN 978-5-85270-342-2.
- Иод // Большая советская энциклопедия : [в 30 т.] / гл. ред. А. М. Прохоров. — 3-е изд. — М. : Советская энциклопедия, 1969—1978.
- Иод на Webelements
- Иод в Популярной библиотеке химических элементов
- Из истории йода
Некоторые внешние ссылки в этой статье ведут на сайты, занесённые в спам-лист. Эти сайты могут нарушать авторские права, быть признаны неавторитетными источниками или по другим причинам быть запрещены в Википедии. Редакторам следует заменить такие ссылки ссылками на соответствующие правилам сайты или библиографическими ссылками на печатные источники либо удалить их (возможно, вместе с подтверждаемым ими содержимым). Список проблемных доменов |
Использование бурых водорослей Келп способствует профилактике заболеваний, вызванных дефицитом йода, патологий щитовидной железы и сердечно-сосудистой системы, нормализует обмен веществ, поддерживает умственное и физическое развитие, укрепляет иммунную систему, способствует выводению из организма токсинов.

Келп – объединяющее название различных видов бурых водорослей – макрофитов. Бурые водоросли –многоклеточные представители морской биоты. Они, как правило крепятся к камням и скалам на морской глубине 10-150 м. Самые крупные представители бурых водорослей достигают 150-300 м в длину. В водах морей и океанов бурые водоросли формируют подобие зарослей, что создает уникальную окружающую среду обитания для морских организмов.
Келп. Бурые водоросли
Распространены бурые водоросли практически повсеместно – их можно встретить и в тропических водах, и в полярных. Бурые водоросли имеют тенденцию к фотосинтезу и содержат хлорофилл.
Подписывайтесь на наш аккаунт в INSTAGRAM!
Издавна бурые водоросли считаются полезным продуктом питания и применяются в диетологии, так как являются низкокалорийными и богатыми минералами, витаминами, белками, клетчаткой. Эти водоросли нашли использование в косметологии, фармацевтической и биотехнологической промышленностях. Наиболее известны из них семейства Фукусовые и Ламинариевые.

Бурые водоросли: состав
На биохимический состав бурых водорослей оказывает влияние целый ряд факторов, например, их вид и ареал обитания. Химический состав всех без исключения бурых водорослей чрезвычайно богат. Это десятки макро- и микроэлементов (натрий, кальций, магний, железо, марганец, кремний, фосфор, сера, цинк, селен, медь, молибден и т.д.), витамины (A, C, D, E, K и витамины комплекса В). Но бурые водоросли славятся именно как «чемпион» по содержанию органического йода.
В состав бурых водорослей входят вещества с биологической активностью:
- полисахариды
- производные хлорофилла
- полиненасыщенные жирные кислоты Омега-3
- фенольные соединения
- растительные стерины
- ферменты
- неактивные гормональные вещества
- Бурые водоросли также известны как источник пищевых волокон.
Бурые водоросли: свойства
Богатый состав этих водорослей предполагает следующее воздействие на организм:
- укрепляют иммунную систему;
- поддерживают эндокринную систему;
- «запускают» обмен веществ, замедляют процесс метаболического синдрома;
- укрепляют нервную систему;
- действуют как профилактика рахита, остеопороза, укрепляют зубы, волосы и ногти;
- стабилизируют пищеварение и самочувствие.
Антиоксиданты в составе этих водорослей нейтрализуют негативное влияние свободных радикалов. А содержащиеся в них селен и цинк – мощные антиоксиданты, борются с возникновением злокачественных новообразований. Селен помогает секреции гормонов для здорового функционирования иммунной системы. Без цинка невозможен здоровый обмен веществ. Цинк принимает участие в синтезе молекул ДНК, в механизмах кроветворения.
Подписывайтесь на Эконет в Pinterest!
Бурые водоросли богаты альгинатами (до 25-30%) – растворимыми пищевыми волокнами. Попадая в ЖКТ, альгинаты разбухают и тем самым раздражают нервные окончания слизистой кишечника. Это активирует перистальтику кишечника, помогает его очищению, уменьшает количество усвояемых жиров. Альгинаты, связывая в кишечнике воду и образуя гелевую массу, затрудняют усвоение глюкозы и расщепление крахмала, а это снижает вероятность возникновения сахарного диабета.
Альгинаты имеют детоксикационные и радиопротекторные качества, связывают и удаляют токсины, холестерин, ионы тяжелых металлов, нивелируют пагубные последствия радиоактивного облучения. Сорбционная активность водорослей позволяет использовать их как продукт, помогающий при аллергических и аутоиммунных недугах.
Фитостерины и полиненасыщенные жирные кислоты Омега-3 в составе бурых водорослей имеют противотромботическое действие, нормализуют липидный обмен, противодействуют возникновению атеросклероза, ишемии.
Этот продукт имеет смысл вводить в детокс-диеты.
Водоросли нормализуют водно-солевой баланс, имеют ощелачивающее и антимутагенное действие.
Высокое содержание полифенолов позволяет водорослям оказывать антирадикальный эффект, связанный с защитой кожного покрова. Питательные вещества в составе водорослей контролируют обменные механизмыы, благоприятствуют оттоку лимфы, убирают отеки. Водоросли присутствуют как ингредиенты в составе косметических препаратов.
Антибактериальные и противогрибковые свойства водорослей обусловлены присутствиемием фенольных соединений, сдерживающих развитие патогенных микроорганизмов. Ключевое ценное качество бурых водорослей – они выступают источником йода.
Функции йода
В течение всей жизни человеку требуется только около 5 г йода. Но трудно переоценить роль йода для здоровья. Ключевая функция йода – это секреция гормонов щитовидки (тиреоидных гормонов) и управление ее гормональными функциями.
Функции гормонов щитовидки:
- Отвечают за процессы роста и развития, «запускают» регенерацию тканей организма; связаны с формированием интеллекта при развитии головного мозга плода, развитием скелета и половой системы;
- Отвечают за производство организмом энергии и тепла, повышают энергообмен на 30-50%;
- Контролируют функции около 100 ферментов;
- Активируют биосинтез белка;
- Активируют обмен углеводов и распад жира, снижают показатель холестерина в крови;
- Активируют синтез витамина А в печени;
- Активируют функции соматотропина (гормона роста), ускоряя рост ребенка;
- Воздействуя на обмен кальция и магния, активируют минерализацию костной ткани, оберегают организм от возникновения остеопороза;
- Укрепляют стрессоустойчивость посредством активации глюкокортикоидов – гормонов, секретируемых корой надпочечников;
- Активируют работу иммунной системы, укрепляяая антибактериальный и противовирусный иммунитет;
Источники йода
Йод имеет свойство поступать в организм через пищу, воздух, воду. Ключевой необходимый объем йода мы получаем с едой.
«чемпионы» по наличию йода в продуктах — бурые водоросли. В них количество йода на сухое вещество насчитывает 0,15-0,20%. Плюс, морские водоросли, имеющие в своем составе богатый перечень минералов и биологически активных веществ.
Значительное количество йода содержится в любых морепродуктах и морской рыбе. Некоторый показатель йода имеется в яйцах, грибах шампиньонах, мясе, молочных продуктах.
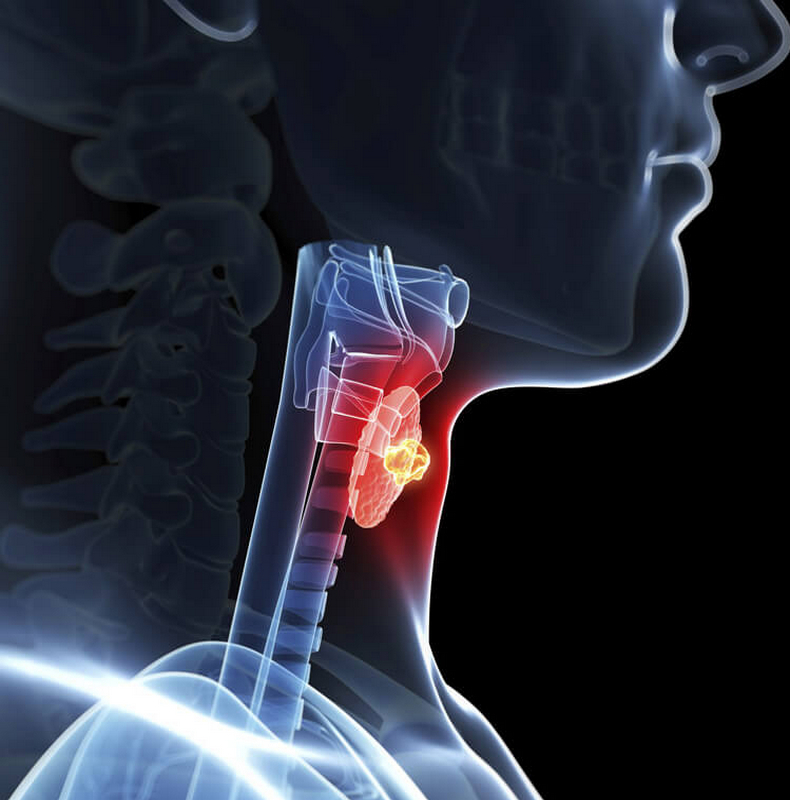
Нехватка йода
Колоссально содержание йода на нашей планете сосредоточено в водах мирового океана. Подсчитано, что это 88 млрд тонн при концентрации 50-60 мкг/л. Если говорить о горных породах, то значительное количество йода имеется в сланцах и вулканическом пепле (32-41 мкг/кг). Хороший показатель йода демонстрируют минеральные воды определенного состава и черноземные грунты.
Статистика ВОЗ свидетельствует, что в условиях нехватки йода существуют примерно 2 млрд людей, среди которых насчитывается 740 млн с болезнями щитовидки, а примерно 50 млн отмечают какую-либо форму умственной отсталости.
Подписывайтесь на наш канал Яндекс Дзен!
Роль микроэлемента йода для здоровья огромна. Его дефицит влечет за собой отклонения физического и умственного развития, провоцирует целый перечень йододефицитных недугов.
Обычная пища и простая питьевая вода не удовлетворят необходимости в йоде, поэтому в борьбе с йододефицитом приходится обращаться к другим источникам (сюда можно отнести йодированную соль и добавки с йодом).
БАД с йодом
Предупредить йододефицит помогают йодсодержащие добавки. Это обычно БАД растительного генезиса с экстрактами бурых водорослей в составе. Результат приема подобных добавок сравним с эффектом от употребления водорослей в салатах или, например, консервах.
Использование Келп
Использование Келп способствует предотвращению большого перечня недугов, вызванннных дефицитом йода, выступает полноценной профилактикой патологий щитовидки и сердечно-сосудистой системы, налаживает обмен веществ, стимулирует умственное и физическое развитие, укрепляет иммунную систему, помогает удалять из организма токсины и радионуклиды.
Предварительно прием Келп имеет смысл обсудить с вашим доктором. Как и любое другое средство, добавки имеют определенные противопоказания.*опубликовано econet.ru.
*Статьи Эконет.ру предназначены только для ознакомительных и образовательных целей и не заменяет профессиональные медицинские консультации, диагностику или лечение. Всегда консультируйтесь со своим врачом по любым вопросам, которые могут у вас возникнуть о состоянии здоровья.
Подписывайтесь на наш youtube канал!
P.S. И помните, всего лишь изменяя свое потребление — мы вместе изменяем мир! © econet
Понравилась статья? Напишите свое мнение в комментариях.
Подпишитесь на наш ФБ:
,
чтобы видеть ЛУЧШИЕ материалы у себя в ленте!
