В каком объеме h2s содержится
Анонимный вопрос · 11 декабря 2017
40,2 K
Чтобы ответить на ваш вопрос необходимо рассчитать молярные массы этих веществ. Это сделать достаточно просто — нужно узнать атомные массы элементов каждого вещества и сложить их. Атомные массы можно посмотреть на Википедии —
https://ru.wikipedia.org/wiki/Список_химических_элементов. Собственно атомная масса серы равно 32, а кислорода равна 16. Дальше производим простые вычисления, с которыми справиться каждый:
Молярная масса SO2 = 32+ 16+16 = 64г/моль
Массовая доля серы = 32/64=0.5
Молярная масса SO3 = 32+ 16+16 + 16= 80г/моль
Массовая доля серы = 32/80=0.4
Как видно, массовая доля серы больше в SO2
Студент-инженер. Люблю козликов, глазированные сырки и «Гражданскую оборону»
Так как в SO2 два атома кислорода, а в SO3 их три, то логично предположить, что в относительном исчислении в молекуле SO2 сера занимает больше «места», а её массовая доля выше.
Сколько литров водорода должно вступить в реакцию с 56 г газа кислорода для образования воды?
Чтобы решить задачу, сначала записываем уравнение реакции:
1) О2 + 2Н2 = 2Н2О
2) Проставляем над веществами, что дано и что требуется найти:
56 г х л
О2 + 2Н2 = 2Н2О
3) Под веществами ставим молекулярную массу кислорода, найденную по таблице Менделеева и молекулярный объем для водорода. Один моль любого газа занимает 22,4 л, в уравнении перед водородом стоит коэффициент 2. что означает 2 моля. Поэтому 22,4 умножаем на 2 и записываем 44,8 л.
56 г х л
О2 + 2Н2 = 2Н2О
32 г 44.8 л
4) Составляем пропорцию:
56 г — х л
32 г — 44.8 л
5) Находим х:
х=44,8*56/32=78,4 (л)
Ответ: 78.4 л водорода должно вступить в реакцию с 56 г кислорода для образования воды.
Рассчитать массовую долю серы в сероводороде?
Живу в своем доме, люблю заниматься садом и животными. Увлекаюсь лингвистикой…
Сперва находим молекулярную массу
Mr (H2S) = 2+32= 342.
Доли элементов:
w (S) % = (n * Ar (S))* 100% / Mr
n – число атомов элемента
w (S) % = (1 * 32)*100 % / 34 = 94%массовая доля серы
Правда ли вулканическая лава при попадании в реку превращает ее в серную кислоту? Если да, то при соединении каких элементов?
Начнем со второго вопроса.
Элементарный состав серной кислоты узнать довольно несложно, достаточно написать в поисковике «серная кислота», если вы уж из школьного куса химии этого не помните. Но окей, ее состав это H2SO4 — водород (2 шт), кислород (4 шт), ну и сама сера.
Вода, как я надеюсь, вы помните, это H2O, так что водород и кислород у нас уже имеется, осталось только найти серу. И, сюрприз, серную кислоту, в том числе получают из воды и оксида серы (IV), он же серный газ, он же SO3.
И да, серный газ содержится в вулканических выхлопах. Но он кипит при температуре в 45 градусов. Лава несколько горячее, так что много его там быть не может. Но в целом да, при контакте лавы с водой, при наличии в лаве оксида серы, может образовываться небольшое количество кислоты. Ключевое слово тут «небольшое».
Но скажу вам даже больше. Оксид серы (IV) содержится в луке. И когда вы его режете, он выделяется. И попадает в глаза. И реагирует с водой, увлажняющей роговицу, и получается, да-да, серная кислота. Самая настоящая. Совсем немного, недостаточно чтобы повредить глаза, но достаточно чтобы вызвать бурю незабываемых ощущений.
Почему Солнце состоит, в основном, из водорода и гелия, а на Земле преобладают железо, кремний и кислород? Ведь они формировались из одного облака вещества.
Для начала стоит отметить что газам образовывать планеты мешает термодинамика с ее закономерностями, потому планеты начинают образовываться из твердых (либо жидких) частичек — изначально зарождаются вообще из пыли, которая слипается. А газу лепить планеты будет мешать как термодинамика ( их температура) так и солнечный ветер , потому и газовые гиганты у нас сравнительно далеко от Солнца, где и температура поменьше и солнечный ветер слабее.
Кроме того, когда-то в атмосфере Земли да и ряда других планет было очень много водорода и гелия, больше чем других газов , но из-за того, что они достаточно легкие, «теплые» планеты постепенно их теряли. Теряли из-за того , что они поднимались в самые внешние слои атмосферы силой Архимеда ( как самые легкие газы), а там либо из-за температурного движения молекулы достигали 3-й космической скорости и покидали планету либо сдувались солнечным ветром. Потому и оставался только тот водород, который связывался в более тяжелые молекулы. В планетах «похолоднее» водорода будет больше.
Так и получилось , что не смотря на то , что в газопылевом облаке, из которого сформировалась Земля, водорода с гелием было очень много, планеты из этих газов в наших краях плохо лепятся.
А почему именно железо , кремний и кислород с углеродом — это уже особенность термоядерных реакций синтеза внутри звезд.
Прочитать ещё 1 ответ
План урока:
Химическая формула
Массовая характеристика вещества
Количество вещества
Закон Авогадро и следствия с закона
Химическая формула
Химия — уникальная наука, которая обладает своим языком и «алфавитом». Каждый химический элемент имеет своё название и собственный «адрес» в периодической системе.
В этом разделе мы будем учиться составлять, читать химические слова, точнее на языке химии – формулы. Периодическая система служит алфавитом, она содержит 126 «букв». Но в ней содержатся только названия и символы элементов, но как они читаются не обозначено. Ниже приведены название и произношение наиболее употребляемых химических элементов.
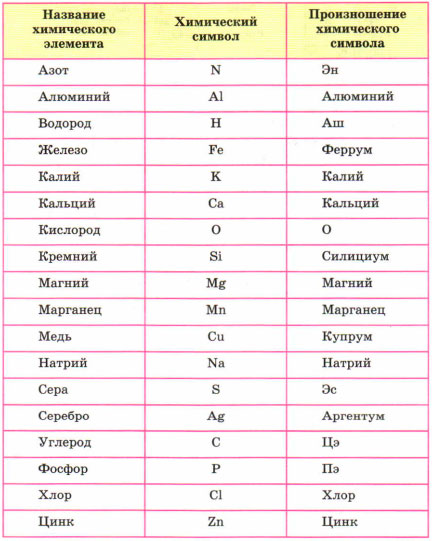
(Источник)
Например, самый лёгкий элемент – водород, но его символ читается как АШ. Кислород читаем – О. Медь – купрум.
Как записать и прочитать с чего состоит соединение, чтобы нас могли понять не только русскоговорящие, но и те, кто говорит на другом языке? Помогут нам в этом символы, а также индексы.
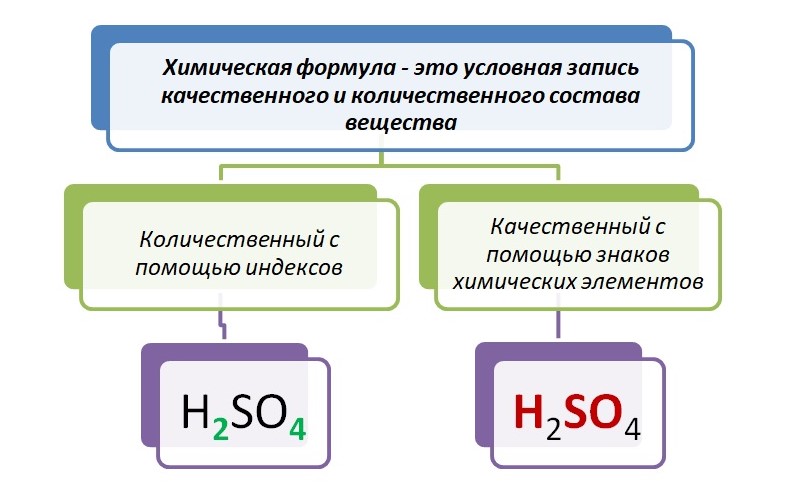
H2SO4 – зелёным цветом выделены индексы – маленькая цифра, которая записывается справа от символа. Он служит показателем количественного состава.
H2SO4 – красным выделены знаки элементов, они указывают качественный состав.
Рассмотрим примеры составления формул, используя условные обозначения на рисунке.
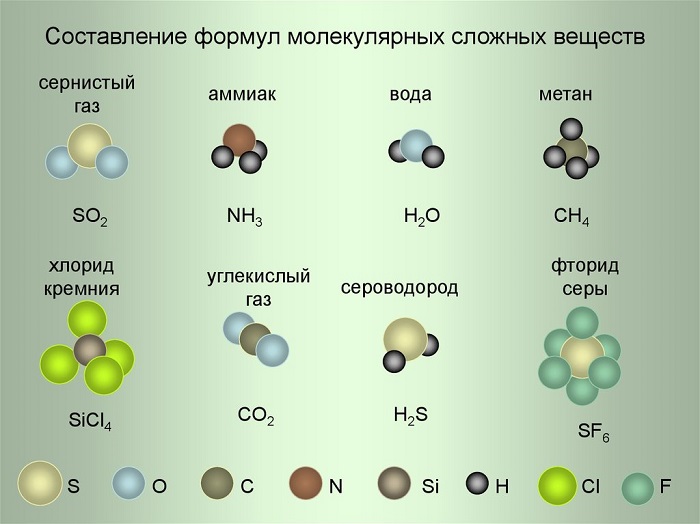 (Источник)
(Источник)
- Сернистый газ. Из условных обозначений видим, что он состоит из одного атома Серы и двух атомов Кислорода – SO2, читается как эс-о-два.
- Аммиак. Один атом Азота и три Водорода – NH3 (эн-аш-три).
- Фторид серы. Один атом Серы и шесть атомов Фтора – SF6 (эс-фтор-шесть).
Коэффициент записывается всегда в начале формулы и никогда не ставится в середину. С его помощью мы узнаём количество молекул, либо свободных атомов. Например, запись 6SiCl4 читаем как: шесть молекул хлорида кремния, 3H2S– 3 молекулы сероводорода.
Массовая характеристика вещества
Относительная атомная масса (ОАМ)
Представим перед собой два кубика одинакового объёма 1 см3, только один сделан из свинца, а второй – из алюминия. ρ(Al) = 2.7 г/см3, ρ(Pb) = 11,3 г/см3. Свинцовый кубик будет 4,2 раза тяжелее алюминиевого. С чем это связано?
Атомы отличаются между собой количеством протонов и электронов. Логично будет предположить, что отличие также будет в размере и массе частиц.
Атом очень мал, что его невозможно увидеть невооружённым глазом. Так, если представить в числах размер Углерода, то его радиус r = 1.5∙10−10м и масса m = 19.94∙10−27кг. Эти параметры достаточно сложно представить. Но если, к примеру, прочертить простым карандашом (стержень карандаша в химии это графит – одна из аллотропных форм Углерода) отрезок длиной 3 см. В данном отрезке будет содержаться около 1 млн. в ширину и 100 млн. атомов Углерода в длину.
Как показывают числовые данные — масса и радиус очень малы, их достаточно трудно увидеть даже в современные оптические микроскопы. Именно по этой причине стали сравнивать атомные массы. На данный момент стандартом сравнения является химический элемент Углерод, а точнее 1/12 часть его массы.
Важно запомнить
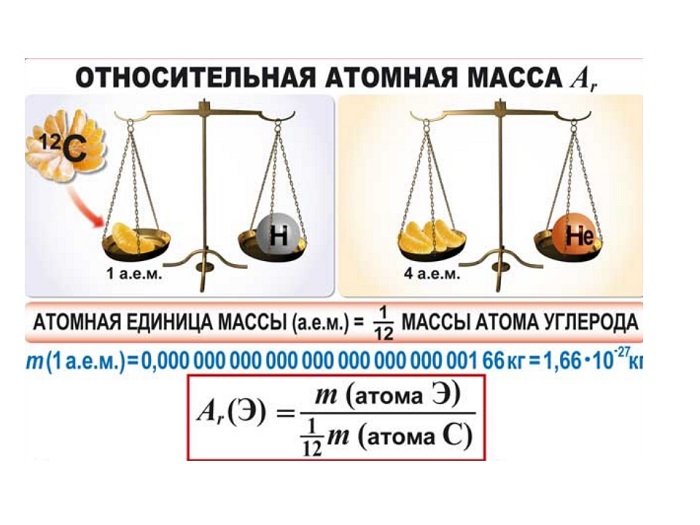 (Источник)
(Источник)
Иными словами, «всё познаётся в сравнении». Эталоном является двенадцатая часть атома Углерода. А ОАМ показывает ВО СКОЛЬКО РАЗ отличается масса элемента от эталона. Иначе можно объяснить: образцом сравнения является корзина, в которой содержится 12 яблок. Вся остальная численность, которая может содержаться в других корзинах (это может быть 10, 15, 5) будет сравниваться во сколько раз больше или меньше.
Закономерно также возникает вопрос, а какую размерность имеет ОАМ: граммы, миллиграммы? Поскольку это число, которое указывает сравнение, то это будет безразмерная величина.
Чему равно Ar элемента подскажет периодическая система. Достаточно часто порядковый номер принимают за Ar. Чтобы избежать путаницы, запомним, что порядковый номер — целое число, а Ar записывается десятичной дробью, которую в химических расчётах общепринято округлять до целых (исключение составляет только Хлор).
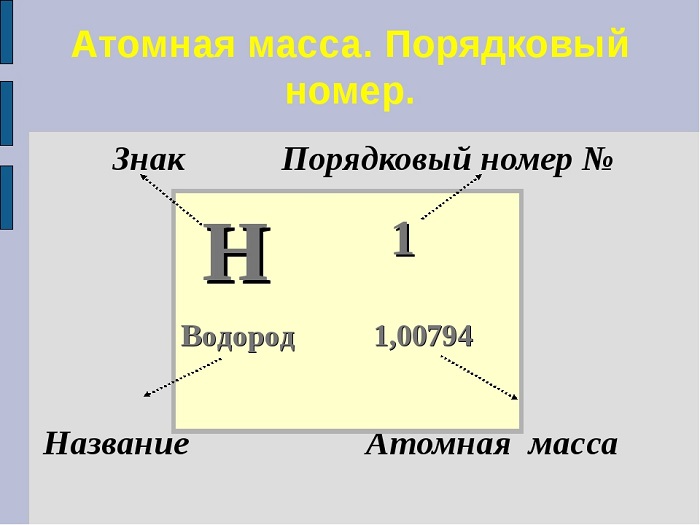 (Источник)
(Источник)
Например: Ar(Mg) = 24,305 ~ 24
Ar(Fe) = 55,847 ~ 56
Ar(Cl) = 35.453 ~ 35,5
Относительная молекулярная масса (ОММ)
Данная величина относится также к количественным характеристикам. Более точное название — относительная формульная масса, потому что строение веществ бывает разным (в зависимости от того, какими частицами оно образовано).
Вычисляют ОММ (Mr) путём сложения Ar каждого элемента, которые входят в состав молекулы с учётом их индексов.
Здесь нам на помощь придут математические знания, а именно правила сложения, умножения и внимательное раскрытие скобок.
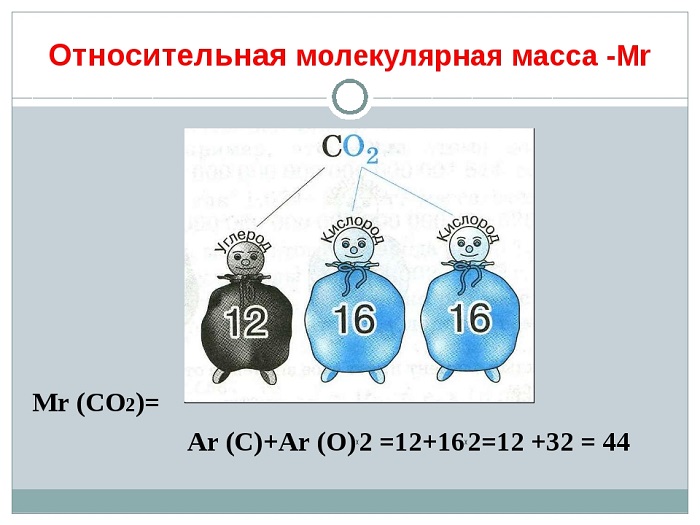 (Источник)
(Источник)
Определим ОММ, например:
Сероводорода
Mr(H2S) = 2∙Ar(H) + Ar(S) = 2 ∙ 1 + 32 = 34
Так как в состав молекулы H2S входит 2 атома водорода, мы это учитываем выражением 2∙Ar(H) и один атом Серы Ar(S). В периодической таблице берём округлённое значение массы Н (1,00797 ~ 1) и S (32,064 ~ 32) и путём сложения вычисляем Mr(H2S).
Глюкозы
Mr (C6H12O6) = 6∙Ar(C) + 12∙Ar(H) + 6∙Ar(O) = 6∙12+12∙1 + 6∙16 = 180
Гашёной извести
Mr (Ca(OH)2) = Ar(Ca) + 2∙Ar(O) + 2∙Ar(H) = 40 + 2 ∙ 16 + 2 ∙ 1 = 74
Эта формула читается как кальций-о-аш-дважды. Что означает индекс два за скобками? Он показывает, что количество атомов H и O равно 2. Это будет равносильно, если раскрыть скобки и написать так: СаО2Н2.
Фосфата кальция
Mr(Ca3(PO4)2) = 3∙Ar(Ca) + 2∙Ar(P) + 8∙Ar(O) = 3 ∙ 40 + 2 ∙31 + 8 ∙ 16 = 310
Кальций-три-пе-о-четыре-дважды. В состав данного вещества входит 3 атома Кальция, два атома Фосфора (индекс 2 относится и к Фосфору и к Кислороду) и 8 атомов Кислорода (2 ∙ 4 = 8). Или, раскрыв скобки Са3Р2О8.
7 молекул угольной кислоты 7 ∙ Н2СО3
Mr (7 ∙ H2CO3) = 7 ∙ (2 ∙ Ar(H) + Ar(C) + 3 ∙ Ar(O)) = 14 ∙ Ar(H) + 7 ∙ Ar(C) + 21 ∙ Ar(O) = 14 ∙ 1 + 7 ∙ 12 + 21 ∙ 16 = 434
Следует обратить внимание, что в химии знак умножение между коэффициентом и формулой не ставится. Более корректная запись 7H2CO3, и действие умножение делается по умолчанию, т. е. раскрываются скобки.
Важно запомнить
Так как ОММ показывает во сколько раз молекула тяжелее 1/12 атома Углерода, то это безразмерная величина.
Не стоит путать с массой молекулы, которая имеет обозначение mM и имеет размерность а.е.м. (атомные единицы массы).
Благодаря химической формуле можно посчитать массовую долю элемента в сложном веществе.
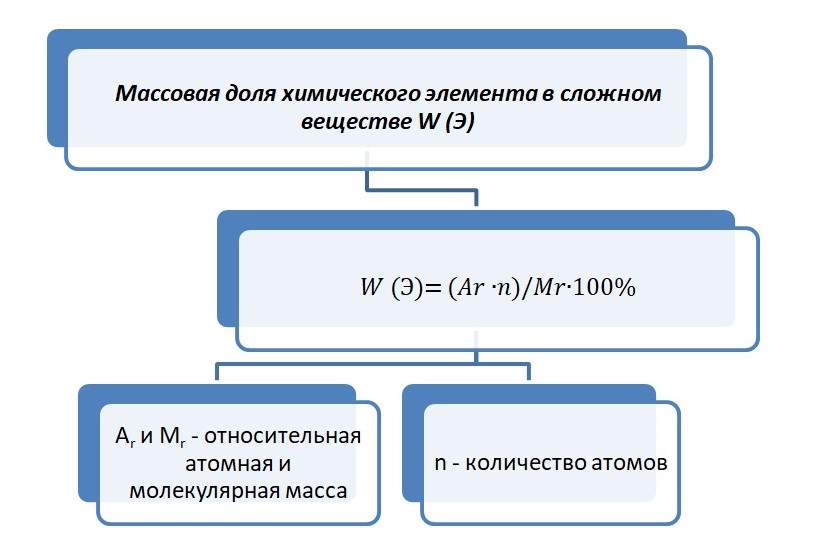
Где n – число атомов элемента.
Сложное вещество можно очень условно сравнить с корзиной, в которой, допустим, находятся ягоды: малины, клубники и арбуз. Возьмём соединение ВаСО3.
Состав:
Mr(BaCO3) = Ar(Ba) + Ar(C) + 3∙Ar(O) = 137 + 12 + 3 ∙ 16 = 197
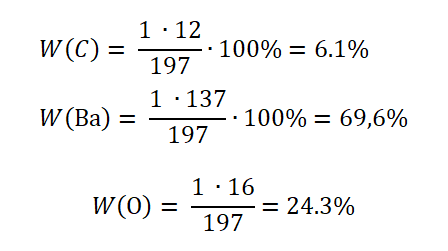
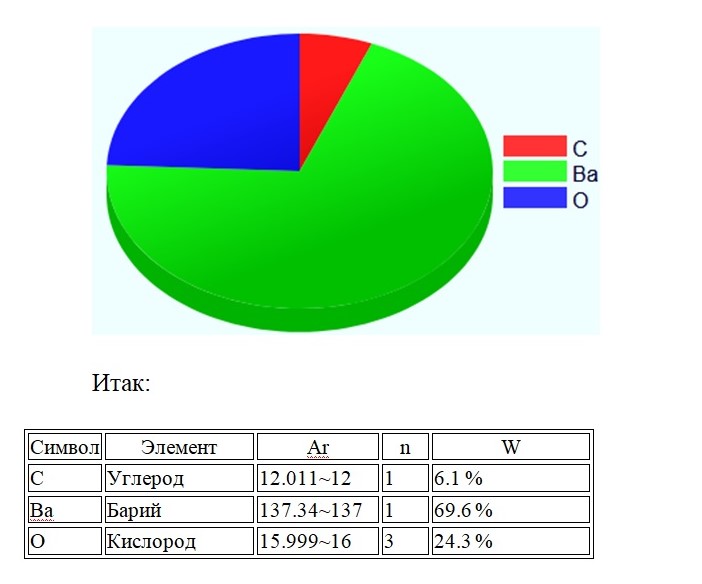
Не трудно догадаться, что арбузом будет атом бария, так как он занимает 69,6 % массы в корзинке фруктов.Проверить правильность решения можно, сложив доли элементов, в сумме должно получиться 100%.
Задача 1. Определите массовую долю Азота в натриевой селитре NaNO3
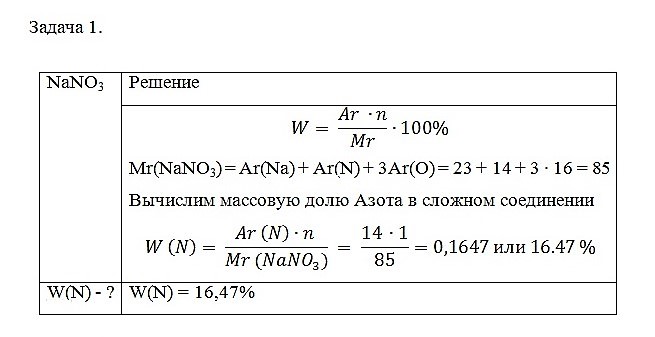
С помощью данных расчётов можно вычислить какая масса Азота, может быть получена из 1 кг натриевой селитры NaNO3.
m(N) = W (N) · m (NaNO3) = 0.1647 · 1 кг = 0,1647 кг или 164,7 г
Селитра применяется как азотное удобрение и с каждым кг растения получают 164,7 г азота.
Бывает так, что опытным путём определены массовые доли элементов и задача стоит в том, что необходимо определить количественный состав соединения. Такие задачи являются обратными идалее их.
Задача 2. Опытным путём установлено, что соединение состоит на 95,2% с Кальция и Водорода. Какова формула вещества?

Количество вещества
Как говорил Д. И. Менделеева «Наука начинается, когда начинают измерять». Но как можно измерить вещество? В порциях, штуках?
 (Источник)
(Источник)
Порцию считаем в граммах, в штуках количество. Например, в магазине вы не покупаете 1000 штук зёрен риса или пшена, а просите взвесить определённый вес (1 кг, 10 кг) или берёте с полки уже расфасованный. Либо необходимо взять молочные продукты, мы берём пакеты объёмом 0,5 л или 1 л. Одинаковая по весу порция содержит примерно одинаковое количество зёрен. Этот принцип применяется и в химии. Порция атомов или молекул называется количеством вещества.
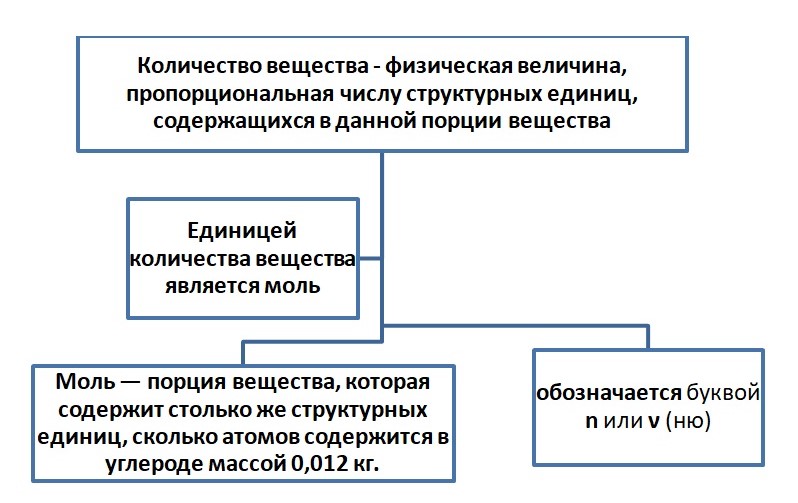
Размерность «моль» не сокращается, т. е. в отличие от литров (л), миллилитров (мл), сантиметров (см) на письме и при чтении указываем 4 моль, 5 сантиметров (5 см).
Если учесть, что атом Углерода имеет вес, (1.994 ∙ 10−23г), то не составит труда узнать, сколько атомов будет содержаться в порции 12 г.
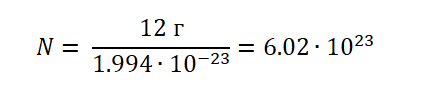
Можно сделать вывод, что 1 моль любого вещества (воды, углекислого газа, поваренной соли, серной кислоты и т. д) будет содержать 6,02∙1023 структурных единиц.
Это число является одним из важнейших не только в химии, но и в физике – оно носит название постоянная Авогадро (NA).
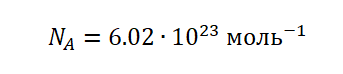
С этого следует, что NA показывает, сколько частиц содержится в 1 моль вещества, в этом и состоит её физический смысл.
Но что делать, если, к примеру, вещество дано в количестве 2 моль, 10 моль или 0.5 моль. Приведём сравнение с математикой, в одной корзине содержится 5 яблок, сколько яблок содержится в трёх таких корзинах. Ответ будет 15 яблок, полученный путём умножения 5 ∙ 3 = 15. Аналогично и с количеством молекул. Чтобы найти эту величину, используем формулу:
N = n * NA
Где N – количество структурных единиц.
Важно: не путать эти две величины, оба эти параметра показывают количество, но:
N — количество структурных единиц,
n — количество вещества (моль)
Рассмотрим подробно данные выводы.
Задача 3. Какое количество вещества составляют 2.709 ∙ 1024 молекул хлора? 
Так, в корзине может содержаться 5 яблок, 10 груш и 8 слив, и наша задача посчитать: «Сколько содержится фруктов?» А сколько будет содержаться в 8 таких корзинах яблок? Эти примеры нам знакомы ещё с первого класса. Молекула может состоять из нескольких атомов, и иногда необходимо точно знать, сколько их штук.
Задача 4. Вычислите сколько атомов Кислорода содержатся в 5 моль глюкозы (C6H12O6)

Молярная масса
Помните вопрос с первого класса: «Что тяжелее 1 кг золота и 1 кг пуха?». Ответ был: одинаковый вес, ведь и золото, и пух весят по 1 кг. Но если спросить, что тяжелее 1 моль метана или 1 моль фруктозы? Чтобы дать ответ на данный вопрос, введём следующее понятие.
Масса 1 моля любого вещества называется молярной массой (размерность г/моль, обозначение М). Не стоит путать с Mr, хоть они численно равны, но отличаются в следующем. Молярная имеет размерность (г/моль).
Связь количества вещества и массы выражается в следующем виде:
m = n * M
Возьмём для примера метан, фруктозу и хлороводород количеством вещества 1 моль.
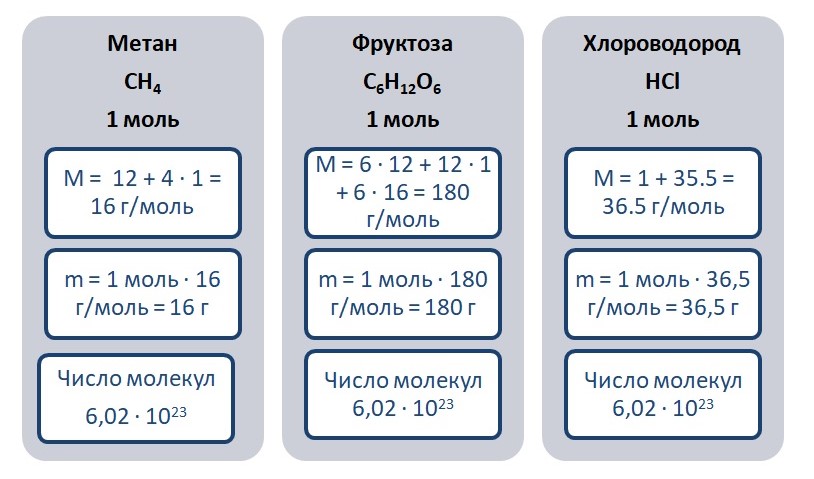
С расчётов делаем вывод, что масса 1 моль фруктозы тяжелее, в её состав входит большее количество атомов.
Задача 5. Какое количество вещества содержится в 61.5 г сернистой кислоты (H2SO3)?
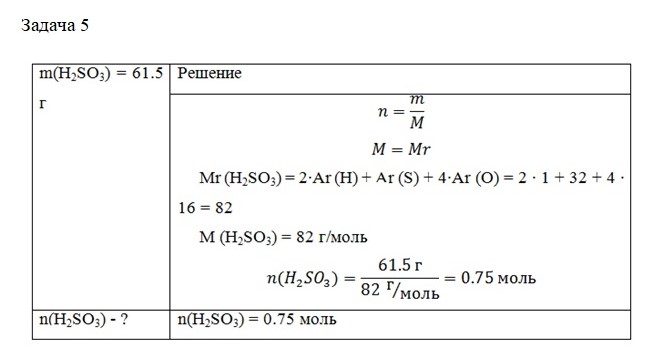
Молярный объём газов
Вещества в газообразном состоянии, в отличие от жидких и твёрдых веществ, при одинаковых условиях (одинаковые давление и температура) будут занимать одинаковый объём.
Допустим, что имеем газ количеством вещества 1 моль. Как известно 1 моль любого соединения содержит 6,02 ∙ 1023 структурных единиц.
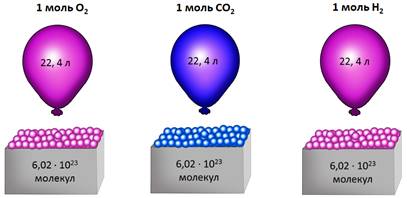
(Источник)
Опытным путём установлено, что 1 моль любого газа при н. у. занимает объём равный 22,4 л/моль.
Связь количества вещества и объёма выражается в следующем виде:
V = n * Vm
Задача 6. Какой объём (н. у.) будет занимать 0,25 моль ацетилена (С2Н2)?

Как можно увидеть, количество вещества связывает три величины:

Приравняв между собой три выражения, а именно:
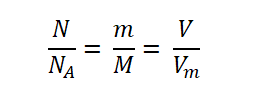
Получаем следующую взаимосвязь
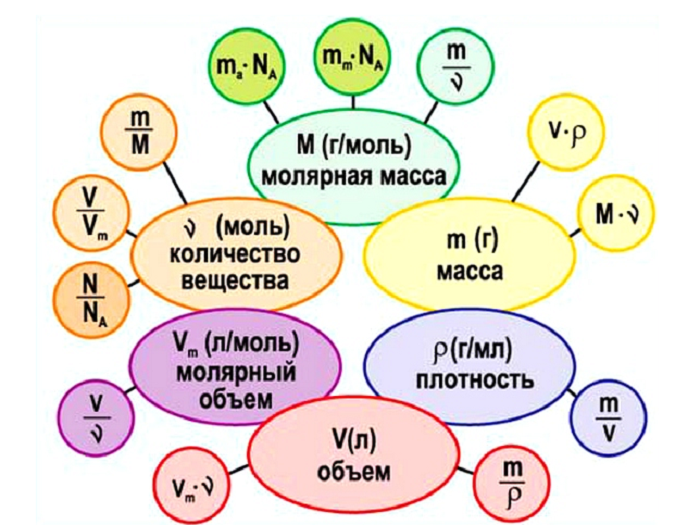
(Источник)
Задача 7. Какую массу составляют 18.06 ∙1023 молекул аммиака (NH3)?

Задача 8. Какой объём (н. у.) будет занимать 51 г сероводорода (H2S)?

Закон Авогадро и его следствия
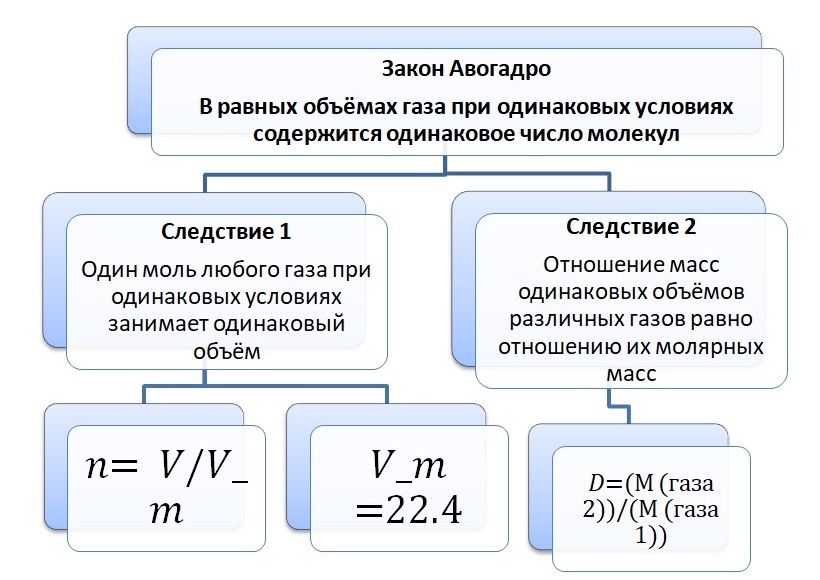
Величина D – это относительная плотность газов. Зная Mr, легко вычислить относительную плотность газов. Приведём пример с шариками. Если один шарик наполнить гелием, а второй углекислым газом. Как вы думаете, какой полетит высоко в небо, а какой упадёт на пол? С детства вы знаете, что гелиевые шарики взлетают в небо, но почему так происходит? Это связано с относительной молекулярной массой.
Mr(He) = 4
Mr(CO2) = 12 + 2 ∙ 16 = 44
Воздух это смесь газов, его Mr = 29
Гелий легче воздуха, поэтому шарик, наполненный этим газом, взлетает высоко в небо. Шарик с углекислым газом остаётся лежать на земле, так как углекислый газ тяжелее воздуха.
Задача 9. Вычислите относительную плотность кислорода по воздуху
Относительная плотность кислорода по воздуху равна
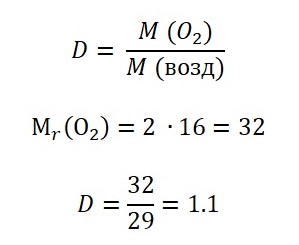
Только ленивый не говорит о том, что в этом году на ЕГЭ по химии будут задачи, в которых надо будет находить число атомов или их соотношение, использовать формулу расчёта количества вещества через постоянную Авогадро и т.п. Но никто точно не знает, в каком виде это будет представлено в задаче 34, поэтому предлагаю вам выборку разных задач, где будет необходимо использовать умение находить число (количество) атомов.
На самом деле, понятия «атомистика» не существует, но в интернете стали так говорить, поэтому и я не буду исключением.
Задачи на «атомистику» — это задачи на соотношения частиц (атомов, молекул, ионов и т.д.) в гомогенных и гетерогенных системах (растворах, твердых и газообразных смесях). Это могут быть массовые соотношения (например, массовая доля элемента в смеси), мольные соотношения (например, соотношение числа атомов водорода и кислорода или мольная доля), объемные соотношения (объемная доля и др.).
Задачи разделены по уровню сложности: от простых до сложных. А также предлагаю вам порешать задачи на удобрения, в которых без «атомистики» не обойтись. Как показывает моя практика, если вы умеете решать задачи на удобрения, то вы полностью понимаете тему «атомистика».
И, конечно же, после каждой задачи вы найдёте подробные видео-объяснения, а ответы в конце страницы.
- Простые задачи
- Задачи средней сложности
- Сложные задачи
- Задачи на удобрения
Простые задачи
Укажите число атомов водорода в одной формульной единице гидросульфита аммония NH4HSO3.
Рассчитайте химическое количество азота в порции простого вещества, содержащей 6,02∙1025 молекул.
Имеется сосуд, в котором содержится 8,428∙1022 молекул некоторого газа. Укажите объём сосуда (в литрах).
Рассчитайте химическое количество (моль) поваренной соли, в которой содержится такое же химическое количество натрия, как и в карбонате натрия химическим количеством 4 моль.
В каком объёме (л) бурого газа содержится столько же атомов, сколько и в аргоне объёмом 2 л (объёмы измерены при одинаковых условиях)?
Рассчитайте количество (моль) CO2, в котором содержится столько же атомов углерода, сколько их содержится в СО массой 1,4 г.
Рассчитайте количество (моль) атомов водорода в аммиаке, объёмом (н.у.) 32,48 л.
Укажите объём (л) порции метана СН4 (н.у.), в которой содержится 0,1 моль атомов углерода.
Рассчитайте объём оксида азота (IV) (л, н.у.), в котором содержится столько же атомов азота и кислорода в сумме, как и общее число атомов в азотной кислоте массой 56,7 г.
Рассчитайте массу (г) порции азотной кислоты, содержащей столько же атомов водорода, сколько в аммиаке объёмом 3,36 л (н.у.).
Укажите число атомов водорода в образце дигидата ацетата цинка ((CH3COO)2Zn∙2H2O) массой 131,4 г.
Вычислите число атомов в образце фтора (н.у.) объёмом 30,24 дм3.
Укажите количество (моль) оксида серы (VI), содержащего столько же атомов кислорода, как и в оксиде серы (IV) массой 76,8 г.
Вычислите число атомов азота в порции гидросульфата аммония массой 16,1.
Рассчитайте массу (г) соли Na2S, содержащей столько же атомов серы, сколько их содержится в сероводороде массой 48,96 г.
Укажите число моль воды в 1 моль кристаллогидрата сульфата натрия с Mr равной 322.
Каков объём кислорода (л, н.у.), содержащего столько же атомов кислорода, сколько их содержится в алебастре массой 87 г?
Рассчитайте количество (моль) ионов в навеске селенида калия массой 39,25.
В порции газа массой 26,4 г содержится 3,612∙1023 молекул. Укажите относительную плотность этого газа по водороду.
Вычислите количество (моль) всех анионов, содержащихся в Ca3(PO4)2 массой 372 г.
Какое число электронов содержится в образце массой 6,4 г, состоящем из нуклида меди-64?
Задачи средней сложности
Образец сплава железа-56 с медью-63 содержит электроны и нейтроны химическим количеством 2,77 моль и 3,21 моль соответственно. Рассчитайте массовую долю (%) меди в сплаве.
Какую массу (г) гидросульфата аммония надо добавить к гидросульфиту натрия массой 15,6 г для получения смеси, содержащей равное число атомов водорода и кислорода?
Какую массу (г) сульфата натрия следует добавить к сульфиду натрия массой 3,9 г, чтобы в полученной смеси массовая доля натрия стала равной 51,9%?
В порции кристаллогидрата сульфата железа (II) содержится 1,204∙1024 атомов железа и 1,3244∙1025 атомов кислорода. Укажите число атомов водорода в данной порции кристаллогидрата.
В смеси оксида железа (II) и оксида железа (III) на 4 атома железа приходится 5 атомов кислорода. Вычислите массовую долю (%) оксида железа (II) в такой смеси.
Газовая смесь содержит 6,02∙1022 молекул и имеет массу 2,3 г. Укажите относительную плотность этой газовой смеси по кислороду.
Для получения бронзы массой 567 г (массовая доля меди 79,01%) использовали минералы медный блеск Cu2S и касситерит SnO2. Укажите общую массу (г) израсходованных минералов, если считать, что минералы не содержали примесей.
Образец минерала браунита массой 100 состоит из вещества, формула которого 3Mn2O3∙MnCO3, и примесей, которые не содержат в своём составе металлы. Массовая доля этих примесей 1,5%. Вычислите массу (г) марганца в исходном образце минерала.
Одна таблетка биологически активных добавок (БАВ) к пище содержит медь массой 2 мг, где медь находится в форме ацетата меди (II). Укажите массу (г) ацетата меди (II), который поступает в организм за неделю при ежедневном приёме 1 таблетки БАВ.
Алюминиевая руда (боксит) состоит из оксида алюминия и других веществ, не содержащих алюминий. Массовая доля алюминия в боксите составляет 21,6%. Вычислите массу (г) оксида алюминия в образце боксита массой 100 г.
Сложные задачи
Для анализа смеси массой 3,125 г, состоящей из хлорида калия и бромида калия, её растворили в воде и к полученному раствору добавили раствор нитрата серебра (I) массой 42,5 г с массовой долей соли 20%. В результате чего образовался осадок массой 5,195 г. Рассчитайте массовую долю (%) ионов калия в исходной смеси.
Твёрдое вещество массой 116 г, состоящее из атомов железа и кислорода, восстановили избытком углерода при нагревании. После полного завершения реакции получили смесь оксидов углерода общим объёмом 33,6 л с массовой долей кислорода 64%. Рассчитайте массу (г) железа в исходном веществе.
Сера, содержащаяся в неизвестном веществе массой 51,2 г, была полностью переведена в соль сульфит натрия массой 100,8 г. Укажите массовую долю (%) серы в неизвестном веществе
Массовая доля трёхвалентного металла в смеси, состоящей из его оксида и гидроксида, составляет 45%. Химические количества веществ равны между собой. Укажите молярную массу (г/моль) металла.
Укажите число электронов, переходящих к окислителю от восстановителя при полном разложении нитрата хрома и нитрита аммония общим химическим количеством 0,2 моль.
Кусочек цинка погрузили в концентрированный раствор гидроксида натрия. В результате образовалась соль массой 1074 г. Рассчитайте химическое количество электронов, которые атомы цинка отдали атомам водорода в результате описанного взаимодействия.
При взаимодействии цинка с избытком концентрированного раствора гидроксида калия от атомов цинка к атомам водорода перешло 4 моль электронов. Укажите массу (г) образовавшейся при этом соли.
Имеется твёрдый образец массой 291,195 г, содержащий только элементы Cu и O. Этот образец полностью восстановили углеродом, в результате чего получили смесь СО и СО2 объёмом 40,32 л (н.у.) с массовой долей кислорода 65,82%. Рассчитайте массу восстановленной меди.
Некоторый металл массой 11,8 г прокалили на воздухе, в результате чего образовалась смесь оксидов массой 16,067 г. Затем эти оксиды растворили в соляной кислоте. Через образовавшийся раствор пропустили газообразный хлор массой 2,345 г, который полностью поглотился. Затем раствор выпарили и получили единственный кристаллогидрат, представляющий собой гексагидрат хлорида металла в степени окисления +3. Рассчитайте массу кристаллогидрата.
В карбоновую трубку поместили порошок металла Х массой 15,36 г и пропустили по трубке ток очищенного хлора при нагревании до 700С и повышенном давлении. Через некоторое время металл полностью прореагировал, а в конце трубки накопились коричневые кристаллы вещества Y массой 26,72 г. Длительное нагревание Y в токе водорода приводит к образованию X и газа Z, который при растворении в воде даёт сильную неорганическую кислоту. Вещество Y состоит из пятиатомных молекул, содержащих один атом металла. Укажите химический символ металла X.
