В каких продуктах есть каталаза

 Все живые организмы используют кислород для метаболизма, а пищевые питательные вещества для получения энергии для выживания. Поэтому кислород является жизненно важным компонентом. С помощью кислорода происходят химические реакции, которые способствуют метаболизму белков, жиров и углеводов для производства энергии.
Все живые организмы используют кислород для метаболизма, а пищевые питательные вещества для получения энергии для выживания. Поэтому кислород является жизненно важным компонентом. С помощью кислорода происходят химические реакции, которые способствуют метаболизму белков, жиров и углеводов для производства энергии.
Однако помимо достоинств, у кислорода есть и недостатки. Кислород отличается высокой реакционностью атомов, которые при окислении способны стать частью потенциально опасных молекул, обычно называемых свободными радикалами.
Свободные радикалы атакуют здоровые клетки организма. Это может привести к их повреждению и, как следствие, тяжелым заболеваниям. Клетки, поврежденные свободными радикалами, являются одной из причин старения, а также таких заболеваний, как рак, болезни сердца, снижение функциональности мозга, снижения иммунитета и т.д.
В целом, свободные радикалы являются причиной как минимум 50-ти болезней.
Что такое антиоксиданты?
Антиоксиданты представляют собой химические вещества, которые взаимодействуют со свободными радикалами и нейтрализуют их, тем самым предотвращая нанесение ущерба организму.

Некоторые антиоксиданты производятся внутри организма, для того, чтобы бороться со свободными радикалами. Такие антиоксиданты называются эндогенными. Тем не менее, этого мало, и организму нужны также и антиоксиданты извне, т.е. экзогенные источники антиоксидантов. Как правило, эту
Примерами пищевых антиоксидантов могут служить бета-каротин, ликопин, витамины А, С и Е. Минеральный элемент селен также часто считают антиоксидантом, но это скорее всего связано с содержанием в нем селен-содержащих белков, а не с самим селеном.часть антиоксидантов человек получает из пищи. Фрукты, овощи и злаки являются источниками антиоксидантов. Также существуют некоторые пищевые добавки с антиоксидантами.
Диета с низким содержанием жиров может привести к снижению поглощения бета-каротина и витамина Е, а также других жирорастворимых питательных веществ. Фрукты и овощи — это основные «поставщики» витамина С, а в цельнозерновых продуктах и высококачественных растительных маслах очень много витамина Е.
Многие вещества растительного происхождения, известные как фитонутриенты, также обладают антиоксидантными свойствами. Фенольные соединения (флавоноиды) борются со свободными радикалами. В основном эти вещества содержатся в зеленом чае, который славится своими антиоксидантными свойствами.
 Эндогенные антиоксиданты вырабатываются с помощью определенных механизмов в человеческом теле, чтобы оно могло защитить себя от поражения свободными радикалами. Это такие ферменты, как глутатионпероксидаза, каталаза и супероксиддисмутаза. Но для выработки этих ферментов требуются микроэлементы – селен, железо, медь, цинк и марганец. Недостаточное потребление этих минералов может привести к низкой выработке антиоксидантных ферментов.
Эндогенные антиоксиданты вырабатываются с помощью определенных механизмов в человеческом теле, чтобы оно могло защитить себя от поражения свободными радикалами. Это такие ферменты, как глутатионпероксидаза, каталаза и супероксиддисмутаза. Но для выработки этих ферментов требуются микроэлементы – селен, железо, медь, цинк и марганец. Недостаточное потребление этих минералов может привести к низкой выработке антиоксидантных ферментов.
В каких продуктах содержатся антиоксиданты?
Как вы уже поняли, для достаточного получения антиоксидантов извне достаточно пройтись по магазинам или заглянуть на овощной рынок.
Тремя активными витаминами-антиоксидантами являются С, E и бета-каротин. Вы найдете их в ярко-окрашенных овощах и фруктах, особенно тех, которые окрашены в фиолетовый, синий, красный, оранжевый и желтый цвета.
 Больше всего бета-каротина и производных от него каротиноидов можно найти в абрикосах, свекле, моркови, кукурузе, дыне, манго, репе и брокколи. Еще эти витамины есть в персиках и нектаринах, грейпфруте, мандаринах, тыкве и арбузе.
Больше всего бета-каротина и производных от него каротиноидов можно найти в абрикосах, свекле, моркови, кукурузе, дыне, манго, репе и брокколи. Еще эти витамины есть в персиках и нектаринах, грейпфруте, мандаринах, тыкве и арбузе.
Витамин С прежде всего содержится во всех видах ягод, капусте брокколи, брюссельской капусте, цветной капусте, дыне, грейпфруте, а также в цитрусовых, киви, и петрушке.
Витамин Е также есть в брокколи и моркови, в семенах горчицы, в репе, манго, тыкве, орехах, шпинате и семечках.
Эти продукты тоже богаты антиоксидантами: чернослив, яблоки, изюм, все ягоды, сливы, красный виноград, лук, баклажан, фасоль.
Другие антиоксиданты, которые могут помочь сохранить здоровье, включают в себя:
Цинк: содержится в устрицах, красном мясе, птице, бобовых, орехах, морепродуктах, цельных зернах, витаминизированных кашах и молочных продуктах.
Селен: в бразильских орехах, тунце, говядине, мясе птицы, цельнозерновом хлебе и других зерновых продуктах.
Совет по обработке продуктов: чтобы получить наибольшую пользу от антиоксидантов, содержащихся в этих продуктах, ешьте эти продукты свежими или слегка сваренными на пару.
В те сезоны, когда на прилавках небольшой выбор овощей и фруктов, и витаминов в них мало, эксперты советуют принимать поливитамины, которые тоже содержат минералы. Если вы не уверены, что питаетесь правильно и ваша диета не содержит достаточное количество антиоксидантов, посоветуйтесь с врачом или диетологом для подбора специального рациона.
Каталаза – фермент, обнаруженный почти во всех живых организмах. Основная его функция – катализировать реакцию разложения перекиси водорода до безвредных для организма веществ. Каталаза имеет большое значение для жизнедеятельности клеток, так как защищает их от разрушения активными формами кислорода.
Общие сведения
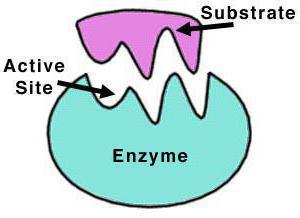
Фермент каталаза относится к оксидоредуктазам – обширному классу ферментов, которые катализируют перенос электронов от молекулы-восстановителя (донора) к молекуле-окислителю (акцептору).
Оптимальный pH для работы каталазы в человеческом организме около 7, однако, скорость реакции существенно не изменяется при значениях показателя водорода от 6,8 до 7,5. Оптимальное значение рН для других каталаз колеблется от 4 до 11, в зависимости от вида организма. Оптимальная температура также различается, для человека это около 37о С.
Каталаза — один из самых быстрых ферментов. Всего одна его молекула способна превращать миллионы молекул перекиси водорода в воду и кислород за секунду. С точки зрения энзимологии это значит, что для фермента каталазы характерно большое число оборотов.
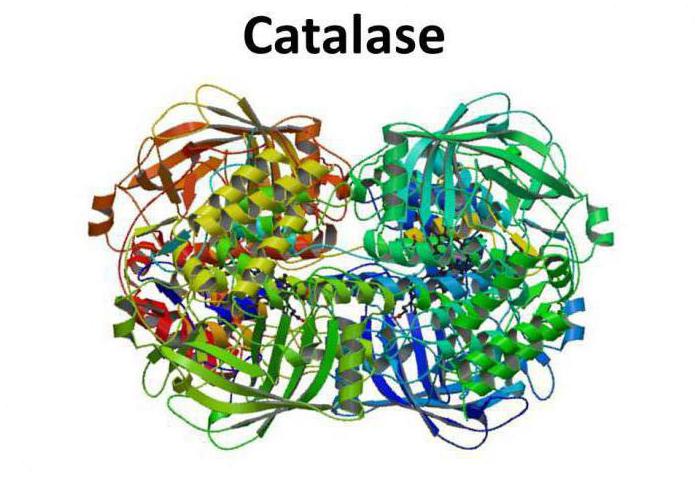
Структура фермента
Каталаза представляет собой тетрамер из четырех полипептидных цепей, каждая из которых имеет длину более 500 аминокислот. Фермент имеет в составе четыре группы порфирового гема, благодаря которым и вступает в реакцию с активными формами кислорода. Окисленный гем представляет собой простетическую группу каталазы.
История открытия
Каталаза не была известна ученым до 1818 года, пока Луи Жак Тенар, химик обнаруживший в живых клетках перекись водорода, не предположил, что ее разрушение связано с действием ранее неизвестного биологического вещества.

В 1900 году немецкий химик Оскар Лев первым ввел термина «каталаза» для обозначения таинственного вещества, разлагающего перекиси. Он же сумел ответить на вопрос, где содержится фермент каталаза. В результате многочисленных экспериментов Оскар Лев выявил, что данный фермент характерен почти для всех животных и растительных организмов. В живой клетке, как и многие другие ферменты, каталаза содержится в пероксисомах.
В 1937 году впервые удалось кристаллизоваться каталазу из говяжьей печени. В 1938 году была определена молекулярная масса фермента – 250 кДа. В 1981 году ученые получили изображение трехмерной структуры бычьей каталазы.
Катализ перекиси водорода
Несмотря на то, что пероксид водорода – продукт многих нормальных метаболических процессов, для организма он не является безвредным.
Чтобы предотвратить разрушение клеток и тканей, перекись водорода должна быть быстро превращена в другое, менее опасное для организма вещество. Именно с этой задачей и справляется фермент каталаза — он разлагает молекулу перекиси до двух молекул воды и молекулы кислорода.
Реакция разложения пероксида водорода в живых тканях:
2 H2O2 → 2 H2O + O2
Молекулярный механизм расщепления перекиси водорода ферментом каталазой пока точно не изучен. Предполагается, что реакция проходит в два этапа — на первом этапе железо в составе простетической группы каталазы связывается с атомом кислорода перекиси, при этом выделяется одна молекула воды. На втором этапе окисленный гем взаимодействует с другой молекулой перекиси водорода, в результате чего образуется еще одна молекула воды и одна молекула кислорода.
Благодаря такому действию фермента каталазы на пероксид водорода, наличие этого активного вещества в образцах ткани легко определить. Для этого достаточно добавить к исследуемому образцу небольшое количество перекиси водорода и наблюдать за реакцией. О наличии фермента говорит формирование пузырьков кислорода. Эта реакция хороша тем, что не требует никакого специального оборудования или инструментов — ее можно наблюдать невооруженным глазом.

Стоит заметить, что ион любого тяжелого металла может выступать как неконкурентный ингибитор каталазы. Кроме того, всем известный цианид ведет себя как конкурентный ингибитор каталазы, если в тканях много перекиси водорода. Арсенаты играют роль активаторов.
Применение
Разлагающее действие фермента каталазы на пероксид водорода нашло применение в пищевой промышленности – с помощью этого фермента из молока удаляетсяН2О2 до приготовления сыра. Еще одно применение – специальные пищевые упаковки, которые защищают продукты от окисления. Каталаза также применяется в текстильной промышленности для удаления пероксида водорода из тканей.
Она в небольших количествах используется в гигиене контактных линз. Некоторые дезинфицирующие средства имеют в составе перекись водорода, и каталаза используется для расщепления этого компонента перед повторным использованием линз.
Активность
Активность фермента каталазы зависит от возраста организма. В молодых тканях активность фермента значительно выше, чем в старых. С возрастом и у людей, и у животных активность каталазы постепенно снижается как результат старения органов и тканей.
Согласно недавним исследованием, снижение активности каталазы является одной из возможных причин поседения волос. Перекись водорода постоянно образуется в человеческом организме, однако не приносит вреда — каталаза быстро разлагает ее. Но если уровень этого фермента снижен, очевидно, что не вся перекись водорода катализируется ферментом. Таким образом, она обесцвечивает волосы изнутри, растворяя естественные красители. Это неожиданное открытие сейчас проверяется исследователями, и, возможно, сыграет роль в разработке препаратов, приостанавливающих поседение волос.
Что такое каталаза, полезные свойства каталазы, противопоказания каталазы
Переключатель меню
- По теме:
- Отзывы в блогах
- Новое в блогах
- Комментарии

О том, как инвалид 2 группы ипотеку

Телёнок по двору скачет, Он неуклюж и смешон, Солнце улыбку не прячет, Льётся со всех сторон… …………………………………….

Рано утром встанет зорька, Краски бросит на луга, Разольётся по пригоркам, Заискрятся облака…

Каталаза представляет собой антиоксидантный фермент, который, подобно супероксиддисмутазе (SOD) и глутатионпероксидазе, образуется естественным образом внутри организма. Это помогает организму превращать перекись водорода в воду и кислород, тем самым предотвращая образование пузырьков углекислого газа в крови. Каталаза также использует перекись водорода для разрушения потенциально вредных токсинов в организме, включая спирт, фенол и формальдегид.
Нам нужен кислород, чтобы жить, но когда наши тела используют кислород, они производят свободные радикалы, которые повреждают клеточные мембраны, белки и ДНК. Свободные радикалы представляют собой химически неустойчивые атомы или молекулы, которые заставляют другие атомы и молекулы в организме также становиться неустойчивыми, процесс, который вызывает обширный ущерб клеткам и ткани, и может привести к депрессии иммунной системы, инфекции, сердечно-сосудистых заболеваний, заболеваний суставов , и умственного упадка. Свободные радикалы также считаются ключевым компонентом процесса старения.
Польза каталазы для организма
Каталаза работает в тесном контакте с супероксиддисмутазой для предотвращения повреждения свободных радикалов организмом. SOD превращает опасный супероксидный радикал в пероксид водорода, который каталаза превращается в безвредную воду и кислород. Каталазы являются одними из наиболее эффективных ферментов, обнаруженных в клетках; каждая молекула каталазы может превращать миллионы молекул пероксида водорода каждую секунду.
Перекись водорода представляет собой природный, но разрушающий отходы всех кислородзависимых организмов. Он вырабатывается в организме человека, когда жирные кислоты превращаются в энергию, и когда белые кровяные клетки атакуют и убивают бактерии. Каталаза, которая находится в пероксосоме клетки, не позволяет этому природному перекисью водорода вредить клетке во время этих процессов. Это также помогает предотвратить превращение перекиси водорода в гидроксильные радикалы, потенциально опасные молекулы, которые могут атаковать и даже мутировать ДНК.
Было высказано предположение, что одним из основных причин возникновения возраст клеток является повреждение ДНК, вызванное свободными радикалами и окислителями, такими как перекись водорода, и что повышение уровней естественных свободнорадикальных истребителей организма — SOD, каталазы и глутатионпероксидазы — могли бы как улучшить здоровье человека, так и увеличить продолжительность жизни людей. Доктор Мартин Чалфи и его коллеги из Колумбийского университета обнаружили новые доказательства, подтверждающие эту теорию, когда они недавно обнаружили и изолировали ген у нематод, который использует каталазу для нейтрализации свободных радикалов и защиты клеток от окислительного повреждения. Мутирование этого гена для включения и выключения производства каталазы увеличивало и уменьшало продолжительность жизни нематоды соответственно. Возможно, что старение человека, как и у нематоды, является результатом воздействия свободных радикалов, а не времени.
Каталаза, супероксиддисмутаза, метионинредуктаза и глутатионпероксидаза производятся в организме. Однако, если вы хотите попытаться бороться с последствиями старения или предотвратить серьезную болезнь, вы можете захотеть дополнить эти ферменты.
Устные дополнения доступны для SOD, каталазы и глутатионпероксидазы; однако эти вещества могут перевариваться в кишечнике до того, как они когда-либо достигнут телесных тканей. Предоставление организму дополнительных количеств строительных блоков, необходимых для создания этих природных антиоксидантов, таких как марганец, цинк, медь и селен, может быть более эффективным способом увеличения их присутствия в организме.

Каталаза — это фермент, являющийся катализатором в реакции разложения перекиси водорода, при которой образуются вода и молекулярный кислород: Н2О2 + Н2О2 = О2 + 2Н2О. Биологическое значение Каталазы заключается именно в разложении перекиси водорода, которая образуется в клетках при воздействии ряда флавопротеиновых оксидаз, чем обеспечивается действенная защита клеточных структур от разрушения, которое осуществляет перекись водорода. Если вследствие генетических причин возникает дефицит Каталазы развивается акаталазия. Это наследственная болезнь, клиническими проявлениями которой являются изъязвления слизистой носа и полости рта, а в некоторых случаях явно выраженные выпадение зубов и атрофические изменения альвеолярных перегородок.
Каталаза имеется в тканях растений, животных и человека, даже в в микроорганизмах, хотя у ряда анаэробных микроорганизмов этот фермент полностью отсутствует. В клетках Каталаза содержится в пероксисомах — специальных органеллах.
Каталаза — это гемопротеин, простетической группой (небелковый элемент, связанный с белком) которого является гем, который содержит ион трехвалентного железа. Молекула Каталазы включает четыре идентичные субъединицы и четыре простетические группы, надежно связанные с апофермектом (белковой частью фермента). При диализе они от него не отделяются. Для Каталазы рН колеблется в пределах 6,0—8,0.
Активность Каталазы
Чтобы определить активность Каталазы фиксируют образованный в процессе реакции кислород, что осуществляется манометрическим, либо полярографическим методами. Возможна и регистрация кислорода с помощью измерения текущей концентрации перекиси водорода спектрофотометрическим иетодом или остаточной концентрации йодометрическим, перманганатометрическим либо иными титриметрическими методами.
Активность Катадазы в эритроцитах постоянна при многих болезнях, однако при злокачественной или другой подобной анемии возрастаетй каталазный индекс, который выражается в отношении величины каталазной активности некоторого объема крови к числу эритроцитов в этом объеме. Этот показатель имеющий большое диагностическое значение. В случае злокачественных новообразований определяется снижение активности Каталазы в печени и почках. Существует даже зависимость между размером опухоли, скоростью роста и уровнем снижения активности Каталазы в печени. Для подтверждения этой теории из некоторых опухолей выделялись токсогормоны, это вещества, вызывающие снижение активности Каталазы в печени у экспериментальных животных при введении.
Где содеожиться каталаза?
Каталаза — это фермент класса оксиредуктаз .
Среди всех органов Каталазы более всего находится в печени. Это один из главных ферментов разрушения активных форм кислорода, то есть Каталаза — основной первичный антиоксидант системы защиты, что обусловлено именно той самой реакцией разложения перекиси водорода до воды , разделяя эту функцию с ферментом GSH-PX. Оба этих вещества лишают токсичности активный кислородный радикал, служа катализатором образования перекиси водорода из супероксида. Имеются и различия в субстратной специфичности этих ферментов, поскольку эти два фермента различаются сродством к субстрату.
Низком содержание Н2О2 требует катализатора пероксидазы для органических пероксидов. В свою очередь высокие концентрации Н2О2 требуют в роли катализатора Каталазу. Уровень активности этих ферментов различен не только в разных тканях, но даже и внутри самой клетки. У печени, почек и красных кровяных телец уровень СТ высокий. В гепатоцитах высокий уровень активности заметен в пероксисомах, при этом СТ активен в цитозоле и в микросомах.
Являясь тетрамерным гем-содержащим белком, Каталаза образуется в цитозоле в виде мономеров, которые не содержат гем. Перенесенные в просвет пероксисом мономеры образуют там тетрамеры в присутствии гема. У каталазы нет сигнальной последовательности, отрезаемой после использования, но у нее должнен быть какой-либо сигнал, который направляет ее в пероксисому. По современным научным погятиям, эту роль может играть специфическая последовательность из трех аминокислот, которая расположена у карбоксильного конца многих пероксисомных белков.
