В каких единицах измеряется кислотность пищевых продуктов
Существует два основных метода измерения кислотности: метод титрования и электропроводности. Давайте рассмотрим преимущества того и другого метода, ответим на часто задаваемые вопросы, а затем покажем на примере кислотометров ATAGO, как можно упростить процедуру измерения кислотности.

Сравнение методов определения кислотности.
Метод титрования
Кислотно-основное титрование, или просто “метод титрования”, является традиционным методом при определении концентрации той или иной кислот и прописан во многих стандартах. При титровании необходимо использовать специальное оборудование и материалы: например, бюретки и реагенты. Титрование может осуществляться вручную, либо с помощью автоматических титровальных машин, которые представляют из себя дорогостоящие профессиональные системы.
Суть простая: в кислотный раствор постепенно добавляется раствор щелочи (основания), приводя его к точке нейтрализации (pH=7). Необходимо тщательно контролировать количество щелочного раствора, чтобы не перейти точку нейтрализации. В этом случае весь раствор из кислотного перейдёт в щелочной.
Для определения точки нейтрализации в раствор добавляют 1-2 капли индикатора (фенолфталеина). И когда раствор переходит в щелочной, в фенолфталеине происходит реакция, которая заставляет цвет изменяться. Концентрацию кислоты определяют по количеству щелочного раствора, которое понадобилось для изменения цвета индикатора (достижения точки нейтрализации).
Концентрация кислоты * объём кислотного раствора * коэффициент = концентрация щелочного раствора * объём добавленного щелочного раствора
Концентрация кислоты выражается из приведённого выше выражения. Коэффициенты различаются для разных типов кислот.
В отличие от ручного способа титрования автоматические титраторы используются pH-сенсор, погружённый в раствор. Определить точку нейтрализации (pH=7.0) таким способом довольно сложно, поэтому часто за конечную точку принимают pH=8.2, 8.0, 7.8 или 7.2.
Метод титрования
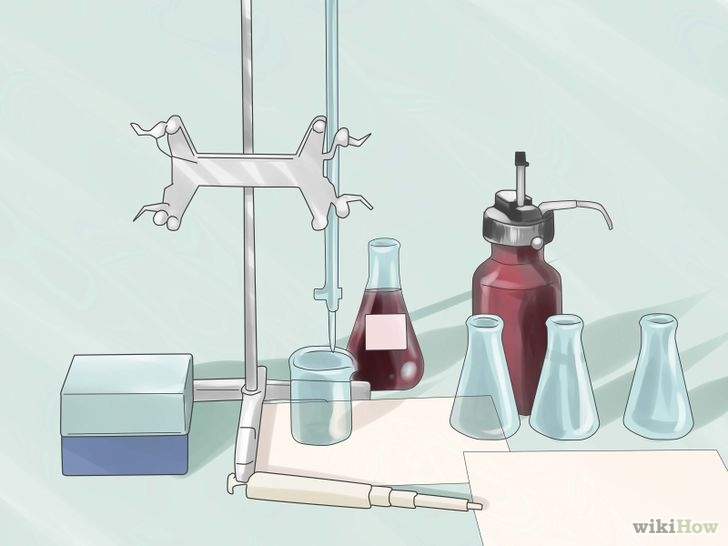
- сложность процедуры измерений и получения результата
- требуется установка и настройка оборудования
- требуются реагенты
- операционные затраты
- невозможность переносить с места на место
Метод электропроводности (измерители кислотности)

Кислотомеры ATAGO измеряют концентрацию кислоты в образце с помощью метод электропроводности. Серия гибридных приборов PAL-BX|ACID представляет собой рефрактометр и кондуктометр в одном корпусе, что позволяет измерить как сухие вещества, так и концентрацию кислоты.
Сахаристость (Brix).
Показатель преломления будет изменяться от концентрации вещества, то есть содержания в нём сухих веществ. Серия PAL-BX|ACID позволяет без особых усилий получать рефрактометрические показания по шкале Brix.
Концентрация кислоты.
Электропроводимость раствора изменяется при изменении концентрации кислоты в нём. Так как с помощью рефрактометра данное изменение определить крайне затруднительно, мы рекомендуем использовать кислотомер-кондуктометр серии PAL-BX|ACID. В пищевых образцах, как правило, присутствует органические кислоты, которые являются очень слабыми электролитами. Вследствие чего необходимо перед измерениями разбавлять образец дистиллированной водой.
Каждая модель из серии кислотомеров оборудована собственной шкалой, нацеленной на измерения отдельных типов фруктов, овощей или других образцов. Пожалуйста, выбирайте модель, наиболее подходящую для ваших образцов.
Кондуктометрический метод
- простота процедуры измерений и получения результата
- не требуется установка и настройка оборудования
- не требуются реагенты
- нет операционных затрат
- возможно переносить с места на место
Кислотометры ATAGO

Кислотомеры-кондуктометры ATAGO выпускаются в двух сериях: PAL-Easy ACID (кислотомер) и PAL-BX/ACID (кислотомер и рефрактометр). Существуб модели со шкалами для различных образцов (например, PAL-BX ACID 101 имеет шкалу с концентрацией кислоты пива).
- F5: Цитрусовые
- 2: Вино и виноград
- 3: Томаты
- 4: Клубника
- 5: Яблоки
- 6: Бананы
- 7: Черника
- 8: Киви
- 9: Ананас
- 181: Уксус
- 101: Пиво
- 121: Сакэ
- 91: Молоко
- 96: Йогурт
Дополнительно каждый прибор может поставляться в комплектации Master kit или Unit. Содержимое данных комплектаций можно посмотреть на картинке ниже.

| Образец / кислотность | На упаковке | Кондуктометр | Титрование |
|---|---|---|---|
| Чистой рисовый уксус A | 4.5 | 4.35 | 4.51 |
| Зерновой уксус B | 4.2 | 4.25 | 4.28 |
| Чистый винный уксус C | 5.0 | 5.68 | 5.11 |
| Чистый уксус из дикого риса C | 4.5 | 4.92 | 4.41 |
| Уксус из дикого риса Кагосимы D | 4.2 | 4.07 | 4.49 |
| Чистый необработанный уксус из коричневого риса E | 4.5 | 4.15 | 4.74 |
| Чёрный уксус Ринкокусан C | 4.2 | 4.51 | 4.05 |
В чём разница между уровнем кислотности и pH?
Уровень кислотности отображает концентрацию кислоты, содержащуюся в растворе, и является индикатором, позволяющим определять кислый вкус. В Японии уровень кислотности выражается в процентах, то есть сколько грамм кислоты содержится в 100 мл раствора. В других странах могут использоваться другие величины: например, граммы кислоты на литр раствора. Для измерения кислотности может также использовать водородный показатель pH, с помощью которого можно определить, является ли раствор кислотным, щелочным или нейтральным. Несмотря на то, что между pH и концентрацией кислоты есть зависимость, их принцип различается. pH отображает концентрацию ионов водорода (H+) в растворе. С помощью pH можно определить примерную концентрацию сильных кислот (например, соляной), а слабых (органических) – очень трудно.
Например, возьмём два апельсина с одинаковым показателем Brix, но разными концентрациями кислоты. Первый будет очень кислым, а второй нормальным. Несмотря на такую разницу во вкусе, pH составляет, соответственно, 3.3 и 3.5.
Что такое пересчёт из общей кислотности?
Многие образцы, включая фрукты, состоят не из одной органической кислоты, а из смеси нескольких. Например, всем понятно, что в уксусе содержится уксусная кислота, но не все знают, что в нём также содержатся и другие кислоты (лимонную, яблочную и другие). А пропорции кислот очень сильно изменяются в зависимости от типа фрукта. Например, в апельсинах преобладающей будет лимонная кислота, в яблоках – яблочная, в томатах – лимонная и яблочная, а в винограде – винная и яблочная. В зависимости от этих пропорций показания концентрации кислоты будут отличаться. Поэтому чтобы не измерять каждую кислоту по отдельности, измеряется общая кислотность, а затем производится пересчёт на ту или иную отдельную кислоту.
Например, при измерении винограда общая кислотность будет содержать винную и яблочную кислоты. После измерения общей кислотности будет произведён пересчёт на винную кислоту. Таким образом измерение общей кислотности позволяет определить содержание отдельной органической кислоты в том или ином фрукте (образце).
Функция офсета.
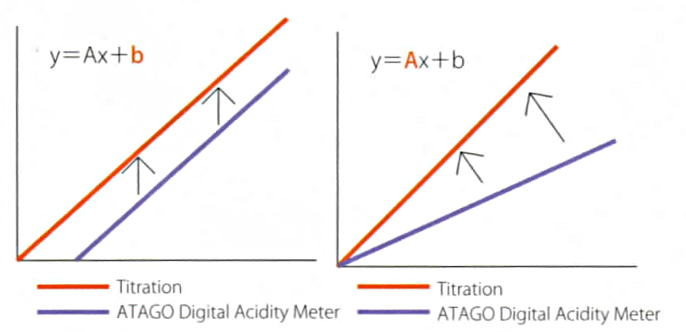
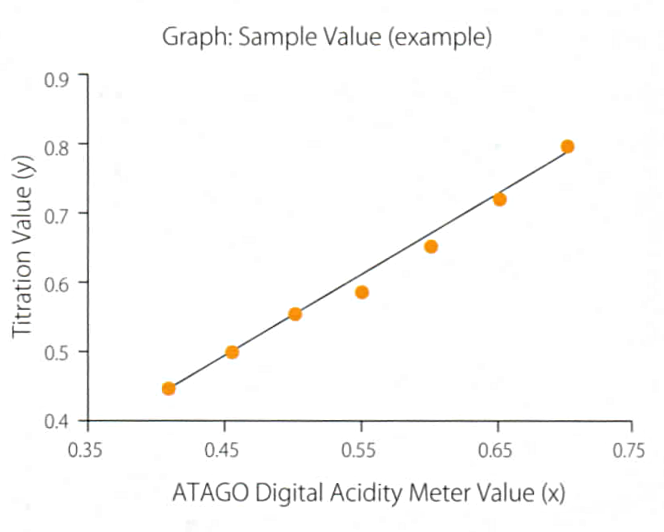
Несмотря на корреляцию между значениями кислотности, полученными методом титрования и электропроводности), из-за различий в подходах конечные показания могут отличаться. Благодаря наличию корреляции, возможно привести значения к таким, чтобы они согласовывались со значениями, полученными методом титрования. В кислотомеры ATAGO серий PAL-Easy ACID и PAL-BX/ACID встроена функция офсета, которая позволяет вводить поправочный коэффициент в полученные значения.
Для функции офсета используется следующая формула:
y=ax+b, где y – конечные показания кислотности, которые будут выводиться на экране, x – изначальные показания кислотности, a – линейный коэффициент, b – добавление или вычитание единичного значения.
Примеры

Кислый вкус пищевого продукта обусловливают ионы водорода, образующиеся в результате электролитической диссоциации содержащихся в нем кислот и кислых солей. Активность ионов водорода (активная кислотность) характеризуется показателем рН (отрицательный логарифм концентрации водородных ионов) Значения рН для некоторых жидких пищевых продуктов представлены в табл. 7.3.
| Практически все пищевые кислоты являются слабыми и в водных растворах диссоциируют незначительно. Кроме того, в пищевой системе могут находиться буферные вещества, в присутствии которых активность ионов водорода будет сохраняться примерно постоянной из-за ее связи с равновесием диссоциации слабых электролитов. Примером такой системы является молоко. В связи с этим, суммарная концентрация в пищевом продукте веществ, имеющих кислотный характер, определяется показателем потенциальной, общей или титруемой (щелочью) кислотности. Для разных продуктов эта величина выражается через различные показатели. Например, в соках определяют общую кислотность в г на 1 л, в молоке — в градусах Тернера и т. д. |
Пищевые кислоты в составе продовольственного сырья и продуктов выполняют различные функции, связанные с качеством пищевых объектов. В составе комплекса вкусоароматических веществ они участвуют в формировании вкуса и аромата, принадлежащих к числу основных показателей качества пищевого продукта. Именно вкус, наряду с запахом и внешним видом, по сей день оказывает более существенное влияние на выбор потребителем того или иного продукта по сравнению с такими показателями, как состав и пищевая ценность. Изменения вкуса и аромата часто оказываются признаками начинающейся порчи пищевого продукта или наличия в его составе посторонних веществ.
Главное вкусовое ощущение, вызываемое присутствием кислот в составе продукта, — кислый вкус, который в общем случае пропорционален концентрации ионов Н+ (с учетом различий в активности веществ, вызывающих одинаковое вкусовое восприятие). Например, пороговая концентрация (мини-мальная концентрация вкусового вещества, воспринимаемая органами чувств), позволяющая ощутить кислый вкус, составляет для лимонной кислоты 0,017%, для уксусной — 0,03%.
В случае органических кислот на восприятие кислого вкуса оказывает влияние и анион молекулы. В зависимости от природы последнего могут возникать комбинированные вкусовые ощущения, например, лимонная кислота имеет кисло-сладкий вкус, а пикриновая — кисло-горький. Изменение вкусовых ощущений происходит и в присутствии солей органических кислот. Так, соли аммония придают продукту соленый вкус. Естественно, что наличие в составе продукта нескольких органических кислот в сочетании с вкусовыми органическими веществами других классов обусловливают формирование оригинальных вкусовых ощущений, часто присущих исключительно одному, конкретному виду пищевых продуктов.
Участие органических кислот в образовании аромата в различных продуктах неодинаково. Доля органических кислот и их лактонов в комплексе ароматообразующих веществ, например земляники, составляет 14%, в помидорах — порядка 11 %, в цитрусовых и пиве — порядка 16%, в хлебе — более 18%, тогда как в формировании аромата кофе на кислоты приходится менее 6%.
В состав ароматообразующего комплекса кисломолочных продуктов входят молочная, лимонная, уксусная, пропионовая и муравьиная кислоты.
Качество пищевого продукта представляет собой интегральную величину, включающую, помимо органолептических свойств (вкуса, цвета, аромата), показатели, характеризующие его коллоидную, химическую и микробиологическую стабильность.
Формирование качества продукта осуществляется на всех этапах технологического процесса его получения. При этом многие технологические показатели, обеспечивающие создание высококачественного продукта, зависят от активной кислотности (рН) пищевой системы.
В общем случае величина рН оказывает влияние на следующие технологические параметры:
— образование компонентов вкуса и аромата, характерных для конкретного вида продукта;
— коллоидную стабильность полидисперсной пищевой системы (например, коллоидное состояние белков молока или комплекса белково-дубильных соединений в пиве);
— термическую стабильность пищевой системы (например, термоустойчивость белковых веществ молочных продуктов, зависящую от состояния равновесия между ионизированным и коллоидно распределенным фосфатом кальция);
— биологическую стойкость (например, пива и соков);
— активность ферментов;
— условия роста полезной микрофлоры и ее влияние на процессы созревания (например, пива или сыров).
Наличие пищевых кислот в продукте может являться следствием преднамеренного введения кислоты в пищевую систему в ходе технологического процесса для регулирования ее рН. В этом случае пищевые кислоты используются в качестве технологических пищевых добавок.
Обобщенно можно выделить три основные цели добавления кислот в пищевую систему:
— придание определенных органолептических свойств (вкуса, цвета, аромата), характерных для конкретного продукта;
— влияние на коллоидные свойства, обусловливающие формирование консистенции, присущей конкретному продукту;
— повышение стабильности, обеспечивающей сохранение качества продукта в течение определенного времени.
Уксусная кислота(ледяная) Е460 является наиболее известной пищевой кислотой и выпускается в виде эссенции, содержащей 70-80% собственно кислоты. В быту используют разбавленную водой уксусную эссенцию, получившую название столовый уксус. Использование уксуса для консервирования пищевых продуктов — один из наиболее старых способов консервирования. В зависимости от сырья, из которого получают уксусную кислоту, различают винный, фруктовый, яблочный, спиртовой уксус и синтетическую уксусную кислоту. Уксусную кислоту получают путем уксуснокислого брожения. Соли и эфиры этой кислоты имеют название ацетаты. В качестве пищевых добавок используются ацетаты калия и натрия (Е461 и Е462).
Наряду с уксусной кислотой и ацетатами, применение находят диацетаты натрия и калия. Эти вещества состоят из уксусной кислоты и ацетатов в молярном соотношении 1:1. Уксусная кислота — бесцветная жидкость, смешивающаяся с водой во всех отношениях. Диацетат натрия — белый кристаллический порошок, растворимый в воде, с сильным запахом уксусной кислоты.
Уксусная кислота не имеет законодательных ограничений; ее действие основано, главным образом, на снижении рН консервируемого продукта, проявляется при содержании выше 0,5% и направлено, главным образом, против бактерий. Основная область использования — овощные консервы и маринованные продукты. Применяется в майонезах, соусах, при мариновании рыбной продукции и овощей, ягод и фруктов. Уксусная кислота широко используется также как вкусовая добавка.
Молочная кислотавыпускается в двух формах, отличающихся концентрацией: 40%-й раствор и концентрат, содержащий не менее 70% кислоты. Получают молочнокислым брожением сахаров. Ее соли и эфиры называются лактатами. В виде пищевой добавки Е270 используется в производстве безалкогольных напитков, карамельных масс, кисломолочных продуктов. Молочная кислота имеет ограничения к применению в продуктах детского питания.
Лимонная кислота — продукт лимоннокислого брожения сахаров. Имеет наиболее мягкий вкус по сравнению с другими пищевыми кислотами и не оказывает раздражающего действия на слизистые оболочки пищеварительного тракта. Соли и эфиры лимонной кислоты — цитраты. Применяется в кондитерской промышленности, при производстве безалкогольных напитков и некоторых видов рыбных консервов (пищевая добавка Е330).
Яблочная кислотаобладает менее кислым вкусом, чем лимонная и винная. Для промышленного использования эту кислоту получают синтетическим путем из малеиновой кислоты, в связи с чем критерии чистоты включают ограничения по содержанию в ней примесей токсичной малеиновой кислоты. Соли и эфиры яблочной кислоты называются малатами. Яблочная кислота обладает химическими свойствами оксикислот. При нагревании до 100°С превращается в ангидрид. Применяется в кондитерском производстве и при получении безалкогольных напитков (пищевая добавка Е296).
Винная кислотаявляется продуктом переработки отходов виноделия (винных дрожжей и винного камня). Не обладает каким-либо существенным раздражающим действием на слизистые оболочки желудочно-кишечного тракта и не подвергается обменным превращениям в организме человека. Основная часть (около 80%) разрушается в кишечнике под действием бактерий. Соли и эфиры винной кислоты называются тартратами. Применяется в кондитерских изделиях и в безалкогольных напитках (пищевая добавка Е334).
Янтарная кислотапредставляет собой побочный продукт производства
адипиновой кислоты. Известен также способ ее выделения из отходов янтаря. Обладает химическими свойствами, характерными для дикарбоновых кислот, образует соли и эфиры, которые получили название сукцинаты. При 235°С янтарная кислота отщепляет воду, превращаясь в янтарный ангидрид. Используется в пищевой промышленности для регулирования рН пищевых систем (пищевая добавка Е363).
Янтарный ангидрид является продуктом высокотемпературной дегидратации янтарной кислоты. Получают также каталитическим гидрированием малеинового ангидрида. Плохо растворим в воде, где очень медленно гидролизуется в янтарную кислоту.
Адипиновая кислотаполучается в промышленности, главным образом, двухстадийным окислением циклогексана. Обладает всеми химическими свойствами, характерными для карбоновых кислот, в частности, образует соли, большинство из которых растворимо в воде. Легко этерифицируется в моно- и диэфиры. Соли и эфиры адипиновой кислоты получили название адипинаты. Является пищевой добавкой (Е355), обеспечивающей кислый вкус продуктов, в частности, безалкогольных напитков.
Фумаровая кислотасодержится во многих растениях и грибах, образуется при брожении углеводов в присутствии Aspergillus fumaricus. Промышленный способ получения основан на изомеризации малеиновой кислоты под действием НС1, содержащей бром. Соли и эфиры называются фумаратами. В пищевой промышленности фумаровую кислоту используют как заменитель лимонной и винной кислот (пищевая добавка Е297). Обладает токсичностью, в связи с чем суточное потребление с продуктами питания лимитировано уровнем 6 мг на 1 кг массы тела.
Глюконо-дельта-лактон — продукт ферментативного аэробного окисления ( ,D-глюкозы. В водных растворах глюконо-дельта-лактон гидро-лизуется в глюконовую кислоту, что сопровождается изменением рН раствора. Используется в качестве регулятора кислотности и разрыхлителя (пищевая добавка Е575) в десертных смесях и продуктах на основе мясных фаршей, например, в сосисках.
Фосфорная кислотаи ее соли — фосфаты (калия, натрия и кальция) широко распространены в пищевом сырье и продуктах его переработки. В высоких концентрациях фосфаты содержатся в молочных, мясных и рыбных продуктах, в некоторых видах злаков и орехов. Фосфаты (пищевые добавки Е339 — 341) вводятся в безалкогольные напитки и кондитерские изделия. Допустимая суточная доза, в пересчете на фосфорную кислоту, соответствует 5-15 мг на 1 кг массы тела (поскольку избыточное количество ее в организме может стать причиной дисбаланса кальция и фосфора).
Кислотность имеет большое значение для оценки качества пищевых продуктов. Повышенная кислотность может характеризовать их несвежесть и недоброкачественность. Поэтому в стандартах на многие пищевые продукты (свежее молоко, сметана, пиво, соки, фруктовые воды и др.) указывают нормы содержания кислот.
Лимонную, виннокаменную, яблочную, молочную и уксусную кислоты в небольших количествах используют в кондитерской, безалкогольной, ликеро-водочной и консервной промышленности для улучшения вкуса продуктов. Уксусную, сорбиновую, молочную и бензойную кислоты добавляют к некоторым продуктам в качестве консерванта.
Некоторые органические кислоты обладают способностью подавлять развитие микроорганизмов за счет концентрации водородных ионов или за счет токсичности недиссоциированных молекул либо анионов. Если токсическое действие минеральных кислот связано главным образом с концентрацией водородных ионов, то токсичность органических кислот не пропорциональна степени их диссоциации и обусловлена в основном действием недиссоциированных молекул или анионов.
Общее количество органических кислот недостаточно характеризует вкусовую кислотность продуктов. Кислый вкус зависит главным образом от степени диссоциации кислот, т. е. от активной кислотности. Чем выше концентрация ионов водорода, тем кислый вкус кислоты будет более сильным. Концентрацию ионов водорода выражают в единицах водородного показателя рН, который является отрицательным логарифмом ионов Н + (рН = log [H +]). Ощущение кислого вкуса увеличивается с понижением значения рН, начиная от 7, которое характеризует нейтральную реакцию.
Растворы различных кислот одинаковой нормальности и, следовательно, с одинаковой титруемой кислотностью могут иметь разную активную кислотность в зависимости от степени -диссоциации кислот.
Контрольные вопросы
1. Охарактеризуйте пищевые кислоты и их значение в питании человека.
2. Приведите примеры содержания пищевых кислот в продуктах питания.
3. Что вы знаете о кислотности пищевых продуктов?
4. Дайте характеристику отдельным представителям пищевых кислот.
Тема 9. «Ферменты»
План
1. Понятие о ферментах.
2. Размер молекул. Селективность. Эффективность.
3. Зависимость от температуры и среды раствора.
4. Классификация ферментов.
5. Использование ферментов в промышленности.
Ферменты, или энзимы, — это органические катализаторы белковой природы, которые ускоряют реакции, необходимые для функционирования живых организмов.
Так как реакции обмена веществ, протекающие в организмах, можно разделить на два типа процессов: синтеза (анаболитические) и распада (катаболитические), то соответственно можно выделить и два типа ферментов.
Сейчас химикам известно более 2000 ферментов. Все они обладают рядом специфических свойств, отличающих их от неорганических катализаторов.
Размер молекул.Понятно, что, будучи по своей природе белками, ферменты должны иметь большие значения молекулярной массы. Действительно. Она может колебаться в пределах от 105 до 107, а это значит, что по своему размеру молекулы ферментов попадают в разряд коллоидных частиц. Это не позволяет отнести их ни к гомогенным, ни к гетерогенным катализаторам. Остаётся отнести их к особому классу катализаторов.
Селективность. Каждый фермент ускоряет только одну какую-либо реакцию или группу однотипных реакций. Эту их особенность называют селективностью (избирательностью) действия. Она позволяет организму быстро и точно выполнить чёткую программу синтеза нужных ему соединений на основе молекул пищевых веществ или продуктов их превращения. Располагая богатым набором ферментов, клетка разлагает молекулы белков, жиров и углеводов до небольших фрагментов-мономеров (аминокислот, глицерина и жирных кислот, моносахаридов соответственно) и из них заново строит белковые и иные молекулы, которые будут точно соответствовать потребностям данного организма.
Эффективность. Большинство ферментов обладает очень большой эффективностью. Скорость некоторых ферментативных реакций может быть в 1015 раз больше скорости реакций, протекающих в их отсутствии. Такая высокая активность ферментов объясняется тем, что их молекулы в процессе «работы» очень быстро восстанавливаются (регенерируют). Типичная молекула фермента может регенерировать миллионы раз за минуту. Ферменты, действуя как катализаторы, снижают энергию активации, которая требуется для того, чтобы могла произойти реакция.
Зависимость от температуры и среды раствора.Многие ферменты обладают наибольшей эффективностью при температуре человеческого тела, т.е. приблизительно при 370С. Человек погибает при более низких и более высоких температурах не столько из-за того, что его убила болезнь, а в первую очередь из-за того, что перестают действовать ферменты, а следовательно, прекращаются обменные процессы, которые и определяют сам процесс жизни.
Ферменты наиболее эффективно действуют на субстрат при строго определённой среде раствора, при определённых значениях рН.
Фермент желудочного сока пепсин наиболее активен при рН 1,5 – 2, каталаза крови – при рН 7 и т.д.
Кислотность или основность среды физиологических жидкостей определяет биологическую активность клеток организма, которая, в свою очередь, определяется «работой» действующих в них ферментов. Каждая из физиологических жидкостей имеет определённое значение рН, и отклонение от нормы может быть причиной тяжёлых заболеваний.
| Среда | Значение рН | Возможные отклонения |
| Кровь Желудочный сок Слёзная жидкость Слюна Спинномозговая жидкость | 7,4 1,7 7,7 6,8 7,6 | 7,25-7,44 0,9-2,0 7,6-7,8 5,6-7,9 7,4-7,8 |
В контакт с субстратом вступает лишь очень небольшая часть молекулы фермента, так называемый активный центр.Он включает обычно от 3 до 15 аминокислотных остатков полипептидной молекулы фермента. Высокая специфичность фермента обусловлена особой формой его активного центра, которая точно соответствует форме молекулы вещества катализируемой реакции.
Многие ферменты для проявления активности нуждаются в веществах небелковой природы – так называемых кофакторах. В роли последних могут выступать ионы металлов (цинка, магния, кальция и др.) или молекулы органических соединений; в последнем случае их называют коферментами. Иногда для действия фермента бывает необходимо присутствие как ионов металла, так и кофермента.
