У какого элемента фосфора или мышьяка свойства неметалла выражены ярче
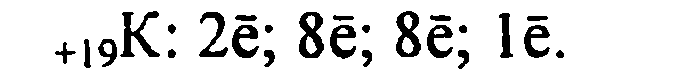
А) Характеристика фосфора.
1. Фосфор— элемент пятой группы и третьего периода, Z = 15,
Аr(Р) = 31.
Соответственно, атом фосфора содержит в ядре 15 протонов,
16 нейтронов и 15 электронов. Строение его электронной оболочки
можно отразить с помощью следующей схемы:
![]()
Атомы фосфора проявляют как окислительные свойства (принима-
ют недостающие для завершения внешнего уровня три электрона, получая при этом степень окисления -3, например, в соединениях с менее электроотрицательными элементами— металлами, водородом и т.п.) так и восстановительные свойства (отдают 3 или 5 электронов более электроотрицательным элементам — кислороду, галогенам и т.п., приобретая при этом степени окисления +3 и +5.)
Фосфор менее сильный окислитель, чем азот, но более сильный, чем мышьяк, что связано с ростом радиусов атомов от азота к мышьяку. По этой же причине восстановительные свойства, наоборот, усиливаются.
2. Фосфор — простое вещество, типичный неметалл. Фосфору свойственно явление аллотропии. Например, существуют аллотропные модификации фосфора такие, как белый, красный и черный фосфор, которые обладают разными химическими и физическими свойствами.
3. Неметаллические свойства фосфора выражены слабее, чем у азота, но сильнее, чем у мышьяка (соседние элементы в группе).
4. Неметаллические свойства фосфора выражены сильнее, чем у
кремния, но слабее, чем у серы (соседние элементы в периоде).
5. Высший оксид фосфора имеет формулу Р2O5. Это кислотный оксид.
Он проявляет все типичные свойства кислотных оксидов. Так, например, при взаимодействии его с водой получается фосфорная кислота.
Р2O5 + 3Н2O => 2Н3РO4.
При взаимодействии его с основными оксидами и основаниями он
дает соли.
Р2O5 + 3MgO = Mg3(PO4)2; Р2O5 + 6КОН = 2К3РO4+ 3Н2O.
6. Высший гидроксид фосфора— фосфорная кислота Н3РO4, рас-
твор которой проявляет все типичные свойства кислот: взаимодействие с основаниями и основными оксидами:
Н3РO4 + 3NaOH = Na3PO4 + 3Н2O. 2Н3РO4 + 3СаО = Са,(РO4)2↓ + 3Н2O.
7. Фосфор образует летучее соединение Н3Р — фосфин.
Б) Характеристика калия.
1. Калий имеет порядковый номер 19, Z = 19 и относительную атомную массу Аr(К) = 39. Соответственно заряд ядра его атома +19 (равен числу протонов). Следовательно, число нейтронов в ядре равно 20. Так как атом электронейтрален, то число электронов, содержащихся в атоме калия, тоже равно 19. Элемент калий находится в четвертом периоде периодической системы, значит, все электроны располагаются на четырех энергетических уровнях. Таким образом, строение атома калия записывается так:
![]()
Исходя из строения атома, можно предсказать степень окисления
калия в его соединениях. Так как в химических реакциях атом калия отдает один внешний электрон, проявляя восстановительные свойства, следовательно, он приобретает степень окисления +1.
Восстановительные свойства у калия выражены сильнее, чем у на-
трия, но слабее, чем у рубидия, что связано с ростом радиусов от Na к Rb.
2. Калий— простое вещество, для него характерна металлическая
кристаллическая решетка и металлическая химическая связь, а отсюда — и все типичные для металлов свойства.
3. Металлические свойства у калия выражены сильнее, чем у на-
трия, но слабее, чем у рубидия, т.к. атом калия легче отдает электрон, чем атом натрия, но труднее, чем атом рубидия.
4. Металлические свойства у калия выражены сильнее, чем у кальция, т.к. один электрон атома калия легче оторвать, чем два электрона
атома кальция.
5. Оксид калия К2O является основным оксидом и проявляет все типичные свойства основных оксидов. Взаимодействие с кислотами и кислотными оксидами.
К2O + 2НСl = 2КСl +Н2O; К2O + SO3 = K2SO4.
6. В качестве гидроксида калию соответствует основание (щелочь) КОН, которое проявляет все характерные свойства оснований: взаимодействие с кислотами и кислотными оксидами.
KOH+HNO3 = KNO3+H2O; 2KOH+N2O5 = 2KNO3+H2O.
7. Летучего водородного соединения калий не образует, а образует гидрид калия КН.
Вариант 1
1. У какого элемента сильнее выражены неметаллические свойства: а) у кислорода или углерода; б) у фосфора или мышьяка? Дайте обоснованный ответ на основании положения элементов в периодической таблице.
а) у кислорода (неметалличность усиливается слева направо по периоду)
б) у фосфора (неметалличность усиливается снизу вверх по группе)
2. Дайте характеристику элемента №11 по плану:
Положение в периодической таблице
Металл или неметалл
Строение атома
Электронная формула
Число электронов на наружном энергетическом уровне, является ли он завершенным
Формула высшего оксида
Образует ли элемент летучее соединение с водородом, если образует, какова его химическая формула
3. Как и почему изменяются свойства химических элементов в периодах? Покажите это на примере элементов 3-го периода.
4. Рассчитайте относительную атомную массу бора, если известно, что доля изотопа 10B составляет 19,6%, а изотопа 11В – 80,4 %. (Ответ: 10,8.)
Вариант 2
1. У какого элемента сильнее выражены металлические свойства:
а) у лития или рубидия; б) у калия или скандия? Дайте обоснованный ответ на основании положения элементов в периодической таблице.
а) у рубидия (металличность усиливается сверху вниз по группе)
б) у калия (металличность усиливается справа налево по периоду)
2. Дайте характеристику элемента №7 по плану:
Положение в периодической таблице
Металл или неметалл
Строение атома
Электронная формула
Число электронов на наружном энергетическом уровне, является ли он завершенным
Формула высшего оксида
Образует ли элемент летучее соединение с водородом, если образует, какова его химическая формула

3. Как изменяются свойства химических элементов в А-группах? Покажите это на примере элементов IIA-группы.
4. Сколько различных видов молекул оксида углерода (IV) можно получить из изотопа углерода 12C и трех изотопов кислорода: 16О, 17О, 18О? Напишите формулы всех оксидов и рассчитайте их молярные массы.
Вариант 3
1. У какого элемента сильнее выражены неметаллические свойства: а) у хлора или йода; б) у серы или кремния? Дайте обоснованный ответ на основании положения элементов в периодической таблице.
а) у хлора (неметалличность усиливается снизу вверх по группе)
б) у серы (неметалличность усиливается слева направо по периоду)
2. Дайте характеристику элемента №12 по плану:
Положение в периодической таблице
Металл или неметалл
Строение атома
Электронная формула
Число электронов на наружном энергетическом уровне, является ли он завершенным
Формула высшего оксида
Образует ли элемент летучее соединение с водородом, если образует, какова его химическая формула
3. Какие общие свойства проявляют элементы одних и тех же групп? Покажите это на примере элементов VIIA-группы.

4. Медь имеет два изотопа: 63Cu и 65Cu. Их доли в природной меди составляют 73 и 27? Соответственно. Рассчитайте среднюю относительную массу меди. (Ответ: 63,5.)
Вариант 4
1. У какого элемента сильнее выражены металлические свойства: а) у бериллия или стронция; б) у натрия или алюминия? Дайте обоснованный ответ на основании положения элементов в периодической таблице.
а) у стронция (металличность усиливается сверху вниз по группе)
б) у натрия (металличность усиливается справа налево по периоду)
2. Дайте характеристику элемента №16 по плану:
Положение в периодической таблице
Металл или неметалл
Строение атома
Электронная формула
Число электронов на наружном энергетическом уровне, является ли он завершенным
Формула высшего оксида
Образует ли элемент летучее соединение с водородом, если образует, какова его химическая формула
3. Что общего и каковы различия в строении малых и больших периодов? Покажите это на примере 3-го и 4-го периодов.
Малые периоды состоят из одного ряда (3-й период), большие и двух рядов (4-й период). Свойства элементов меняются строго от металлов к неметаллам в любом периоде. 4-й период содержит на 10 элементов больше, чем 3-й. Эти элементы являются переходными металлами, у них заполняется d-подоболочка предыдущего энергетического уровня.
4. Оксид элемента имеет состав ЭО3. Массовая доля кислорода в этом оксиде составляет 60%. Какой элемент образуется оксид?
Голосование за лучший ответ
Людмила Лукьянова
Мастер
(1101)
11 лет назад
Азот имеет более выраженные неметаллические свойства (по сравнению с мышьяком) , т. к. радиус атома азота меньше, а количество электронов на внешнем слое у данных атомов одинаковое. Азот сильнее удерживает внешние (валентные) электроны.
глеб редько
Знаток
(423)
1 год назад
У какого элемента сильнее выражены свойства неметалла:
у мышьяка или азотаУ какого элемента сильнее выражены свойства неметалла:
у мышьяка или азотаУ какого элемента сильнее выражены свойства неметалла:
у мышьяка или азотаУ какого элемента сильнее выражены свойства неметалла:
у мышьяка или азотаУ какого элемента сильнее выражены свойства неметалла:
у мышьяка или азотаУ какого элемента сильнее выражены свойства неметалла:
у мышьяка или азотаУ какого элемента сильнее выражены свойства неметалла:
у мышьяка или азотаУ какого элемента сильнее выражены свойства неметалла:
у мышьяка или азотаУ какого элемента сильнее выражены свойства неметалла:
у мышьяка или азотаУ какого элемента сильнее выражены свойства неметалла:
у мышьяка или азотаУ какого элемента сильнее выражены свойства неметалла:
у мышьяка или азотаУ какого элемента сильнее выражены свойства неметалла:
у мышьяка или азотаУ какого элемента сильнее выражены свойства неметалла:
у мышьяка или азотаУ какого элемента сильнее выражены свойства неметалла:
у мышьяка или азотаУ какого элемента сильнее выражены свойства неметалла:
у мышьяка или азотаУ какого элемента сильнее выражены свойства неметалла:
у мышьяка или азотаУ какого элемента сильнее выражены свойства неметалла:
у мышьяка или азотаУ какого элемента сильнее выражены свойства неметалла:
у мышьяка или азотаУ какого элемента сильнее выражены свойства неметалла:
у мышьяка или азотаУ какого элемента сильнее выражены свойства неметалла:
у мышьяка или азотаУ какого элемента сильнее выражены свойства неметалла:
у мышьяка или азотаУ какого элемента сильнее выражены свойства неметалла:
у мышьяка или азотаУ какого элемента сильнее выражены свойства неметалла:
у мышьяка или азотаУ какого элемента сильнее выражены свойства неметалла:
у мышьяка или азотаУ какого элемента сильнее выражены свойства неметалла:
у мышьяка или азотаУ какого элемента сильнее выражены свойства неметалла:
у мышьяка или азотаУ какого элемента сильнее выражены свойства неметалла:
у мышьяка или азотаУ какого элемента сильнее выражены свойства неметалла:
у мышьяка или азотаУ какого элемента сильнее выражены свойства неметалла:
у мышьяка или азотаУ какого элемента сильнее выражены свойства неметалла:
у мышьяка или азотаУ какого элемента сильнее выражены свойства неметалла:
у мышьяка или азотаУ какого элемента сильнее выражены свойства неметалла:
у мышьяка или азотаУ какого элемента сильнее выражены свойства неметалла:
у мышьяка или азотаУ какого элемента сильнее выражены свойства неметалла:
у мышьяка или азотаУ какого элемента сильнее выражены свойства неметалла:
у мышьяка или азотаУ какого элемента сильнее выражены свойства неметалла:
у мышьяка или азотаУ какого элемента сильнее выражены свойства неметалла:
у мышьяка или азотаУ какого элемента сильнее выражены свойства неметалла:
у мышьяка или азотаУ какого элемента сильнее выражены свойства неметалла:
у мышьяка или азотаУ какого элемента сильнее выражены свойства неметалла:
у мышьяка или азотаУ какого элемента сильнее выражены свойства неметалла:
у мышьяка или азотаУ какого элемента сильнее выражены свойства неметалла:
у мышьяка или азотаУ какого элемента сильнее выражены свойства неметалла:
у мышьяка или азотаУ какого элемента сильнее выражены свойства неметалла:
у мышьяка или азотаУ какого элемента сильнее выражены свойства неметалла:
у мышьяка или азотаУ какого элемента сильнее выражены свойства неметалла:
у мышьяка или азотаУ какого элемента сильнее выражены свойства неметалла:
у мышьяка или азотаУ какого элемента сильнее выражены свойства неметалла:
у мышьяка или азотаУ какого элемента сильнее выражены свойства неметалла:
у мышьяка или азотаУ какого элемента сильнее выражены свойства неметалла:
у мышьяка или азотаУ какого элемента сильнее выражены свойства неметалла:
у мышьяка или азотаУ какого элемента сильнее
Описание презентации по отдельным слайдам:
1 слайд

Описание слайда:
Н Е М Е Т А Л Л Ы
2 слайд

Описание слайда:
Удивить готов он нас — Он и уголь, и алмаз, Он в карандашах сидит, Потому что он — графит. Грамотный народ поймет То, что это … В чем горят дрова и газ, Фосфор, водород, алмаз? Дышит чем любой из нас Каждый миг и каждый час? Без чего мертва природа? Правильно, без … В воздухе он главный газ, Окружает всюду нас. Угасает жизнь растений Без него, без удобрений. В наших клеточках живет Важный элемент … КИСЛОРОДА АЗОТ УГЛЕРОД
3 слайд

Описание слайда:
НЕМЕТАЛЛЫ — это химические элементы, для атомов которых характерна способность принимать электроны до завершения внешнего уровня. В главной подгруппе: число электронов на внешнем слое не изменяется радиус атома увеличивается электроотрицательность уменьшается окислительные свойства уменьшаются -НЕМЕТАЛЛИЧЕСКИЕ свойства УМЕНЬШАЮТСЯ В периоде: радиусы атомов уменьш. — число электронов на внешнем слое уменьш. — электроотрицательность увеличивается окислительные свойства увеличиваются — НЕМЕТАЛЛИЧЕСКИЕ свойства УВЕЛИЧИВАЮТСЯ
4 слайд

Описание слайда:
Положение неметаллов в периодической системе химических элементов Немета́ллы — химические элементы с типично неметаллическими свойствами, которые занимают правый верхний угол Периодической системы. Расположение их в главных подгруппах соответствующих периодов: . Группа III IV V VI VII VIII 2-й период B C N O F Ne 3-й период Si P S Cl Ar 4-й период As Se Br Kr 5-й период Te I Xe 6-й период At Rn
5 слайд

Описание слайда:
Кроме того, к неметаллам относят также водород и гелий. Характерной особенностью неметаллов является большее (по сравнению с металлами) число электронов на внешнем энергетическом уровне их атомов: O 1ѕ²2ѕ²2p⁴ Cl 1ѕ²2s²2p⁶3s²3p⁵ Это определяет их большую способность к присоединению дополнительных электронов, и проявлению более высокой окислительной активности, чем у металлов.
6 слайд

7 слайд

Описание слайда:
ЗАДАНИЕ: Напишите электронные формулы — серы, фтора, мышьяка, брома S 1s²2s²2p⁶3s²3p⁴ F 1s²2s²2p⁵ As 1s²2s²2p⁶3s²3p⁶4s²4p³ Br 1s²2s²2p⁶3s²3p⁶4s²4p⁵ У какого из элементов ярче выражены неметаллические свойства и почему: а) As — N б) Cl — S а) N – меньше радиус атома (больше значение электроотрицательности) б) Cl — меньше радиус атома, больше валентных электронов ( больше значение ЭО)
8 слайд

Описание слайда:
НАХОЖДЕНИЕ НЕМЕТАЛЛОВ В ПРИРОДЕ В свободном виде могут быть газообразные неметаллические простые вещества — фтор, хлор, кислород, азот, водород, инертные газы, твёрдые — иод, астат, сера, селен, теллур, фосфор, мышьяк, углерод, кремний, бор, при комнатной температуре в жидком состоянии существует бром. Распространёнными являются кислород, кремний, водород; редкими — мышьяк, селен, иод.
9 слайд

10 слайд

Описание слайда:
Чаще неметаллы находятся в химически связанном виде: вода, минералы, горные породы, различные силикаты, фосфаты, сульфиды. силикат натрия сульфид свинца
11 слайд

Описание слайда:
фосфат кальция
12 слайд

Описание слайда:
а т м о с ф е р а к л е т к а
13 слайд

Описание слайда:
земная кора
14 слайд

Описание слайда:
ЗАДАНИЕ: Какого газа ( по объему) больше всего в атмосфере Земли ? А З О Т А Какого элемента-неметалла ( по массе) больше всего в литосфере? К И С Л О Р О Д А Атомов какого элемента-неметалла (по массе) больше всего в живых организмах ? К И С Л О Р О Д А
15 слайд

Описание слайда:
ФИЗИЧЕСКИЕ СВОЙСТВА НЕМЕТАЛЛОВ ПРОСТЫЕ ВЕЩЕСТВА – атомы в молекуле связаны ковалентной неполярной связью. СТРОЕНИЕ: Молекулярное — а) газы — O₂ , Cl₂ , N₂ , H₂ , F₂ , O₃ (летучие) б) твердые — I₂ , P₄ , S₈ в) жидкие — Br₂ Атомное — твердые — C , B , Si , Se , Te ( длинные цепи атомов) — высокие: твердость, температура плавления и кипения ОБЩИЕ ЧЕРТЫ: почти все – диэлектрики, кристаллы непластичны, легко разрушаются
16 слайд

Описание слайда:
С Е Р А КРАСНЫЙ ФОСФОР БЕЛЫЙ ФОСФОР
17 слайд

Описание слайда:
КРЕМНИЙ СЕЛЕН
18 слайд

Описание слайда:
У некоторых неметаллов наблюдается проявление аллотропии: — для газообразного кислорода характерны две аллотропных модификации — кислород (O2) и озон (O3), — для твёрдого углерода множество форм — алмаз, астралены, графен, графан, графит, карбин, фуллерены, стеклоуглерод ФИЗИЧЕСКИЕ СВОЙСТВА НЕМЕТАЛЛОВ АЛМАЗ ГРАФИТ
19 слайд

Описание слайда:
Гость из космоса пришел, в воздухе приют себе нашел. ВОДОРОД 2.В доме выше всех живем, вдвоем тепло и свет даем. ВОДОРОД И ГЕЛИЙ 3.Он безжизненным зовется, но жизнь без него не создается. АЗОТ 4.Красив в кристаллах и парах, на детей наводит страх. ЙОД 5.Из горы кусочек вынули, в деревянный ствол задвинули. ГРАФИТ В КАРАНДАШЕ 6.Гордиться уголек невзрачный негорючим братом, и братом прозрачным. АЛМАЗ, ГРАФИТ
20 слайд

Описание слайда:
10.Какой неметалл является лесом? БОР 11.Какие химические элементы утверждают, что могут другие вещества рождать? ВОДОРОД, КИСЛОРОД, УГЛЕРОД 7.Прокаленный уголек дышать пожарнику помог. АКТИВИРОВАННЫЙ УГОЛЬ 8.Белый воздуха боится, покраснел чтоб сохраниться. БЕЛЫЙ И КРАСНЫЙ ФОСФОР 9.Хоть многие вещества превращает в яд, в химии она достойна всяческих наград. СЕРА
21 слайд

Описание слайда:
ХИМИЧЕСКИЕ СВОЙСТВА НЕМЕТАЛЛОВ Окислительные свойства простых веществ: Реагируют с металлами 2K + S⁰ = K₂S⁻² 3Ca + N₂⁰ = Ca₃N₂⁻³ 2Fe + 3 Cl₂⁰ = 2 FeCl⁻₃ Реагируют с водородом H₂ + S⁰ = H₂S⁻² 3N₂⁰ + H₂ = 2N⁻³H₃ Реагируют с неметаллами с более низким значением электроотрицательности 2P⁰ + 5S⁰ = P₂⁺⁵S₅⁻² S⁰ + 3 F₂⁰ = S⁺⁶F₆⁻ Реагируют с некоторыми сложными веществами C⁻⁴H⁺₄ + 2 O⁰₂ = C⁺⁴O₂⁻² + 2 H₂⁺O⁻² 2 KI⁻ + Cl₂⁰ = 2 KCl⁻ + I₂⁰
22 слайд

Описание слайда:
ЗАДАНИЕ: Напишите уравнения реакций и укажите окислитель: Na + Br₂ → ? Mg + P → ? Na + Si → ? Ответ: 2Na + Br₂⁰ = 2 NaBr⁻ 3Mg + 2P⁰ = Mg₃P₂⁻³ 4Na + Si⁰ = Na₄Si⁻⁴ H₂ + Cl ₂ → ? P + Cl₂ → ? CH₄ + Cl₂ → ? Ответ: H₂ + Cl₂⁰ = 2HCl⁻ 2P + 5Cl₂⁰ = 2PCl₅⁻ CH₄ + Cl₂⁰ = CH₃Cl⁻ + HCl⁻
23 слайд

Описание слайда:
Восстановительные свойства неметаллов ( простых веществ): Со фтором все восстановители 2) С кислородом S⁰ + O₂ = S⁺⁴O₂ Si⁰ + O₂ = Si⁺⁴O₂ 4P⁰ + 5O₂ = 2P₂⁺⁵O₅ 3) Со сложными веществами-окислителями Например — H₂, C 3C⁰ + 2Fe₂O₃ = 3C⁺⁴O₂ + 4Fe H₂⁰ + CuO = H₂⁺O + Cu
24 слайд

Описание слайда:
ЗАДАНИЕ Составьте уравнения реакций и определите восстановитель: Si + F₂→ S + H₂SO₄ → SO₂ + … H₂ + WO₃ → Br₂ + H₂S → S + … Li + N₂ → C + HNO₃ → NO₂ + … + … ОТВЕТ: Si + 2F₂ = SiF₄ 3H₂ + WO₃ = 3H₂O + W 6Li + N₂ = 2Li₃N S + 2H₂SO₄ = 3SO₂ + 2H₂O Br₂ + H₂S = S + 2HBr C + 4HNO₃ = CO₂ + 2H₂O+ 4NO₂
25 слайд

Описание слайда:
ПОЛУЧЕНИЕ НЕМЕТАЛЛОВ в промышленности
26 слайд

Описание слайда:
Молекулярный азот в промышленности получают фракционной перегонкой жидкого воздуха. Этим методом можно получить и «атмосферный азот: В промышленности кремний технической чистоты получают, восстанавливая расплав SiO2 коксом при температуре около 1800 °C в руднотермических печах шахтного типа. Чистота полученного таким образом кремния может достигать 99,9 %
27 слайд

Описание слайда:
Фосфор получают из апатитов или фосфоритов в результате взаимодействия с коксом и кремнезёмом при температуре 1600 °С: Образующиеся пары белого фосфора конденсируются 2Ca₃(PO₄)₂↓+10C+6SiO₂↓=P₄+10CO↑+6CaSiO₃↓ в приёмнике под водой.
28 слайд

Описание слайда:
Хлор в промышленных масштабах получают вместе с гидроксидом натрия и водородом путём электролиза раствора поваренной соли: 2NaCl + 2H2О ±2е- → H2↑ + Cl2↑ + 2NaOH
29 слайд

Описание слайда:
Р Е Б У С Ы Й О Д К Р Е М Н И Й
30 слайд

Описание слайда:
А З О Т У Г Л Е Р О Д
31 слайд

Описание слайда:
1. Неметаллы, расположенные в порядке усиления их неметалличности, — это 1) азот, углерод, бор 3) фтор, кислород, хлор 2) сера, хлор, фтор 4) бор, кремний, водород 2. Неметаллические свойства элементов в ряду углерод- азот- кислород-фтор: 1) не изменяются 2) усиливаются 3) ослабевают 4) изменяются периодически Т Е С Т ОТВЕТ: 1 — 2 2 — 2 3 — 4 4 — 3 3.Завершенный внешний энергетический имеет частица: 1) P⁺³ 2) S⁺⁴ 3) Cl⁺⁵ 4) C⁻⁴ 4. Частице Si⁻⁴ соответствует электронная конфигурация: 1) 1s²2s²2p⁶3s² 2) 1s²2s²2p⁶3s²3p⁴ 3) 1s²2s²2p⁶3s²3p⁶4s²
32 слайд

Описание слайда:
5. Верны ли следующие суждения о неметаллах и их соединениях: А. Низшая степень окисления азота и фосфора равна -5. Б. Высший оксид кремния проявляет кислотные свойства. 1 ) верно только А 3) верно только Б 2) верны оба суждения 4) оба суждения неверны 6. Ковалентная полярная связь образуется в соединении: 1) NaCl 2) NH₃ 3) P₄ 4) BaCl₂ 7. Атомную кристаллическую решетку имеет: 1) I₂ 2) CO₂ 3) KCl 4) Si 8. Молекулярное строение имеет: 1) Кремний 2) Сера 3) Бор 4) Цинк Ответ: 5 — 3 6 — 2 7 — 4 8 — 2
33 слайд

Описание слайда:
9. Схеме превращения P⁻³→ P⁺⁵ соответствует уравнение: 1) 4P + 5O₂ = 2P₂O₅ 2) P₂O₅ + 3H₂O = 2H₃PO₄ 3)2PH₃ + 4O₂ = P₂O₅ + 3H₂O 4) P₂O₅ + 6NaOH = 2Na₃PO₄ + 3H₂O ОТВЕТ: 9 — 3 10. Простое вещество сера взаимодействует с каждым из веществ ряда: 1) HCl, Na, O₂ 2) Mg, O₂, H₂ 3) K, Zn, Na₂SO₄ 4) Al, H₂O, O₂ ОТВЕТ: 10 — 2 11. Расставьте коэффициенты в схеме реакции: P + H₂SO₄ → H₃PO₄+ SO₂ + H₂O ОТВЕТ: 2P⁰ + 5H₂S⁺⁶O₄ → 2H₃P⁺⁵O₄+ 5S⁺⁴O₂ + 2H₂O
Выберите книгу со скидкой:
БОЛЕЕ 58 000 КНИГ И ШИРОКИЙ ВЫБОР КАНЦТОВАРОВ! ИНФОЛАВКА
Инфолавка — книжный магазин для педагогов и родителей от проекта «Инфоурок»

Курс профессиональной переподготовки
Учитель химии

Курс повышения квалификации

Курс профессиональной переподготовки
Учитель биологии и химии
Найдите материал к любому уроку,
указав свой предмет (категорию), класс, учебник и тему:
также Вы можете выбрать тип материала:
Общая информация
К учебнику:
«Химия. Базовый уровень», Габриелян О.?

