При взаимодействии с какими веществами сера проявляет окислительные свойства
Андрей Ж. · 25 декабря 2019
1,6 K
Как реагирует NaCl с серной кислотой?
Подготовила к ЕГЭ по химии 5000 учеников. С любого уровня до 100 в режиме онлайн 🙂 · vk.com/mendo_him
NaCl+H2SO4
Для этой реакции нужны определённые условия, и тогда реакция пойдёт????
????NaCl(тв) + H2SO4(конц) =NaHSO4+HCl⬆, если t<110 °C
????2NaCl(тв) + H2SO4(конц)=2HCl⬆+Na2SO4, если t>110°C
Получается, что нужны твёрдые кристаллики хлорида натрия, обязательно концентрированная серная кислота и нагревание ???? так получают газ хлороводород
Прочитать ещё 2 ответа
Почему медь не вступает в реакцию с серной кислотой?
Подготовила к ЕГЭ по химии 5000 учеников. С любого уровня до 100 в режиме онлайн 🙂 · vk.com/mendo_him
Здесь нужно уточнить, какая серная кислота, разбавленная или концентрированная?????????
☘️Mедь не реагирует с разбавленной серной кислотой
Cu+H2SO4разб≠
Сu очень неактивный металл, стоит в ряду активности после H. А такие металлы с растворами кислот не реагируют(HNO3-исключение ????, эта кислота почти со всеми металлами ладит)
☘️А что же с концентрированной H2SO4?медь с ней в очень хороших отношениях????
Cu+2H2SO4=CuSO4+SO2+2H2O
Зачем в вино добавляют диоксид серы и не вредно ли это?
Ценитель искусства, за бокалом вина познаю великие картины прославленных…
В 99% бутылок с вином содержится диоксид серы (серный ангидрид). Это вещество добавляют почти все производители, начиная от крымских виноделов и заканчивая французскими мастерами. Теоретически они могут обойтись и без серы, но тогда напиток получится очень дорогим и потребует специфических условий хранения, которые сложно обеспечить в обычных магазинах.
Диоксид серы (Sulphur Dioxide, E220) – бесцветный газ неприятного запаха, который используется пищевой промышленностью в качестве консерванта, предотвращающего размножение грибков и микроорганизмов. В современном виноделии диоксид серы (в виде газа, порошка или водного раствора) используется сразу на 4-х этапах промышленного производства вина: при сборе урожая, прессовании ягод, брожении (ферментации) и разлива по бутылкам.
В зависимости от этапа добавление серы в вино останавливает брожение, препятствует образованию уксусной кислоты, стабилизирует вкус и цвет, увеличивает срок хранения. Адекватной и безвредной замены этому веществу пока не найдено.
Вредно не само наличие сульфитов, а их количество в напитке. Согласно стандартам США, максимально допустимая концентрация диоксида серы в вине – 400 мг/л.
В Европейском Союзе производители не обязаны указывать количество сульфитов. Отсутствие соответствующей надписи вводит в заблуждение покупателей, считающих, что все европейские вина не содержат диоксида серы. На самом деле это не так. Даже стандарты производства органических вин (самых экологически чистых) допускают наличие сульфитов. Но их концентрация ниже – от 10 до 210 мг/л в зависимости от стандарта.
Но стоит знать, что диоксид серы оказывает негативное воздействие на астматиков даже при таких малых дозах, как 1мгл. По этой причине некоторые доктора на всякий случай рекомендуют астматикам вообще отказаться от употребления вина. Для большинства же людей диоксид серы безопасен – в тех дозах, какие применяются в виноделии.
Чтобы выбрать вино с минимальным количеством диоксида серы, следует помнить о следующем:
- сульфитов меньше в красных винах, поскольку благодаря высокому содержанию танинов им требуется минимум консервантов;
- больше всего серы добавляют в сладкие и полусладкие вина, чтобы остановить их брожение;
- в винах с винтовой пробкой меньше консервантов, чем в напитках с классической (деревянной) пробкой;
- лучше не покупать вина из регионов, где поблизости находятся вулканы, так как почва местных виноградников богата серой.
Прочитать ещё 2 ответа
Для чего нужна сера?
Увлеченный своей работой переводчик, ролевик и биолог. Люблю путешествовать…
Сера — химических элемент, используемых издавна и для различных целей. Чистая сера, без примесей, идет в различные красители и светящиеся составы. Кроме того, сера — горючее вещество. Головки бытовых спичек, например, покрыты составом, содержащим в том числе серу.
С чем взаимодействуют кислоты?
Подготовила к ЕГЭ по химии 5000 учеников. С любого уровня до 100 в режиме онлайн 🙂 · vk.com/mendo_him
???? Растворы кислот кислые на вкус, изменяют окраску индикаторов:
???? лакмуса в красный цвет
????метилового оранжевого – в розовый
цвет фенолфталеина не изменяется
ХИМИЧЕСКИЕ СВОЙСТВА
???? Взаимодействуют с металлами
▫️Ca + 2HCl = CaCl2 + H2
⚠️ Металл должен стоять левее водорода в ряду напряжений
⚠️ Кислоты-окислители – азотная и серная конц., реагируют с металлами по-другому
????Реагируют с основными оксидами:
▫️CaO + 2HCl = CaCl2 + H2O
????С основаниями (реакция нейтрализации):
▫️H2SO4 + 2KOH = K2SO4 + 2H2O
????С солями (не обязательно растворимыми в воде):
▫️Na2CO3 + 2HCl = 2NaCl + CO2↑ + H2O
⚠️ Реакция пойдёт только при условии выделения газа или выпадения осадка
???? У кислот есть и специфические свойства, которые связаны с окислительно-восстановительными реакциями
Прочитать ещё 1 ответ
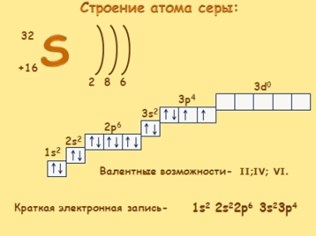
Сера — элемент VIa группы 3 периода периодической таблицы Д.И. Менделеева. Относится к
группе халькогенов — элементов VIa группы.
Сера — S — простое вещество имеет светло-желтый цвет. Использовалась еще до нашей эры в составе священных курений при
религиозных обрядах.

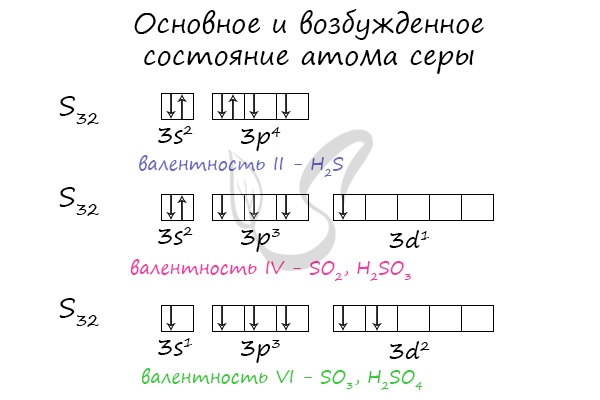
Основное и возбужденное состояние атома серы
Электроны s- и p-подуровня способны распариваться и переходить на d-подуровень. Как и всегда, количество валентных
электронов отражает количество возможных связей у атома.
В разных электронных конфигурациях сера способна принимать валентности: II, IV и VI.
Природные соединения
- FeS2 — пирит, колчедан
- ZnS — цинковая обманка
- PbS — свинцовый блеск (галенит), Sb2S3 — сурьмяный блеск, Bi2S3 — висмутовый блеск
- HgS — киноварь
- CuFeS2 — халькопирит
- Cu2S — халькозин
- CuS — ковеллин
- BaSO4 — барит, тяжелый шпат
- CaSO4 — гипс
В местах вулканической активности встречаются залежи самородной серы.

Получение
В промышленности серу получают из природного газа, который содержит газообразные соединения серы: H2S,
SO2.
H2S + O2 = S + H2O (недостаток кислорода)
SO2 + C = (t) S + CO2
Серу можно получить разложением пирита
FeS2 = (t) FeS + S
В лабораторных условиях серу можно получить слив растворы двух кислот: серной и сероводородной.
H2S + H2SO4 = S + H2O
Химические свойства
- Реакции с неметаллами
- Реакции с металлами
- Реакции с кислотами
- Реакции с щелочами
На воздухе сера окисляется, образуя сернистый газ — SO2. Реагирует со многими неметаллами, без нагревания —
только со фтором.
S + O2 = (t) SO2
S + F2 = SF6
S + Cl2 = (t) SCl2
S + C = (t) CS2

При нагревании сера бурно взаимодействует со многими металлами с образованием сульфидов.
K + S = (t) K2S
Al + S = Al2S3
Fe + S = (t) FeS
При взаимодействии с концентрированными кислотами (при длительном нагревании) сера окисляется до сернистого газа или серной кислоты.
S + H2SO4 = (t) SO2 + H2O
S + HNO3 = (t) H2SO4 + NO2 + H2O
Сера вступает в реакции диспропорционирования с щелочами.
S + KOH = (t) K2S + K2SO3 + H2O
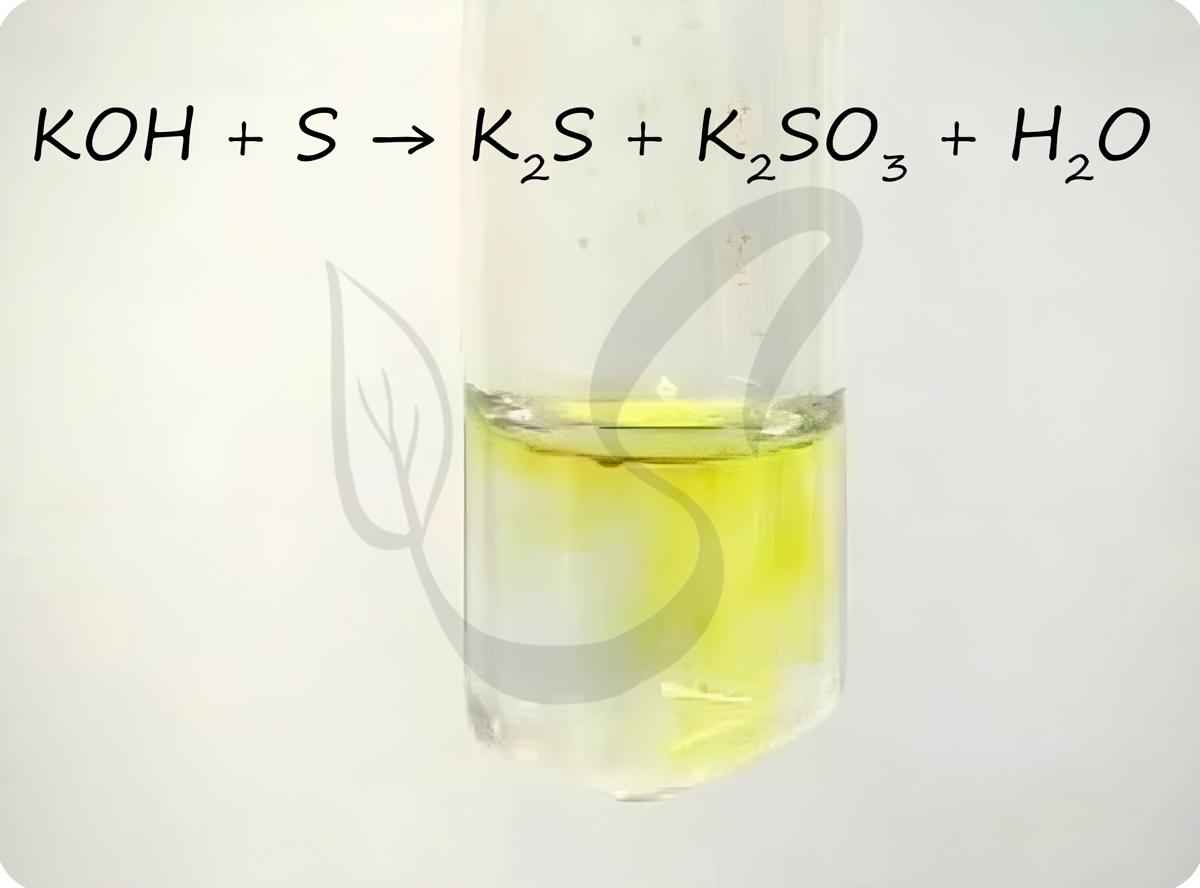
Сероводород — H2S
Бесцветный газ с характерным запахом тухлых яиц. Огнеопасен. Используется в химической промышленности и в лечебных целях (сероводородные
ванны).

Получение
Сероводород получают в результате реакции сульфида алюминия с водой, а также взаимодействия разбавленных кислот с сульфидами.
Al2S3 + H2O = (t) Al(OH)3↓ + H2S↑
FeS + HCl = FeCl2 + H2S↑

Химические свойства
- Кислотные свойства
- Восстановительные свойства
- Качественная реакция
Сероводород плохо диссоциирует в воде, является слабой кислотой. Реагирует с основными оксидами, основаниями с образованием средних и кислых солей (зависит
от соотношения основания и кислоты).
MgO + H2S = (t) MgS + H2O
KOH + H2S = KHS + H2O (гидросульфид калия, избыток кислоты)
2KOH + H2S = K2S + 2H2O
Металлы, стоящие в ряду напряжений до водорода, способны вытеснить водород из кислоты.
Ca + H2S = (t) CaS + H2
Сероводород — сильный восстановитель (сера в минимальной степени окисления S2-). Горит в кислороде синим пламенем, реагирует с кислотами.
H2S + O2 = H2O + S (недостаток кислорода)
H2S + O2 = H2O + SO2 (избыток кислорода)
H2S + HClO3 = H2SO4 + HCl

Качественной реакцией на сероводород является реакция с солями свинца, при котором образуется сульфид свинца.
H2S + Pb(NO3)2 = PbS↓ + HNO3
Оксид серы — SO2
Сернистый газ — SO2 — при нормальных условиях бесцветный газ с характерным резким запахом (запах загорающейся
спички).

Получение
В промышленных условиях сернистый газ получают обжигом пирита.
FeS2 + O2 = (t) FeO + SO2
В лаборатории SO2 получают реакцией сильных кислот на сульфиты. В ходе подобных реакций образуется сернистая кислота,
распадающаяся на сернистый газ и воду.
K2SO3 + H2SO4 = (t) K2SO4 + H2O + SO2↑
Сернистый газ получается также в ходе реакций малоактивных металлов с серной кислотой.
Cu + H2SO4(конц.) = (t) CuSO4 + SO2 + H2O
- Кислотные свойства
- Восстановительные свойства
- Как окислитель
С основными оксидами, основаниями образует соли сернистой кислоты — сульфиты.
K2O + SO2 = K2SO3
NaOH + SO2 = NaHSO3
2NaOH + SO2 = Na2SO3 + H2O

Химически сернистый газ очень активен. Его восстановительные свойства продемонстрированы в реакциях ниже.
Fe2(SO4)3 + SO2 + H2O = FeSO4 + H2SO4
SO2 + O2 = (t, кат. — Pt) SO3
В присутствии сильных восстановителей SO2 способен проявлять окислительные свойства (понижать степень окисления).
CO + SO2 = CO2 + S
H2S + SO2 = S + H2O
Сернистая кислота
Слабая, нестойкая двухосновная кислота. Существует лишь в разбавленных растворах.
Получение
SO2 + H2O ⇄ H2SO3
Химические свойства
- Диссоциация
- Кислотные свойства
- Окислительные свойства
- Восстановительные свойства
Диссоциирует в водном растворе ступенчато.
H2SO3 = H+ + HSO3-
HSO3- = H+ + SO32-
В реакциях с основными оксидами, основаниями образует соли — сульфиты и гидросульфиты.
CaO + H2SO3 = CaSO3 + H2O
H2SO3 + 2KOH = 2H2O + K2SO3 (соотношение кислота — основание, 1:2)
H2SO3 + KOH = H2O + KHSO3 (соотношение кислота — основание, 1:1)
С сильными восстановителями сернистая кислота принимает роль окислителя.
H2SO3 + H2S = S↓ + H 2O
Как и сернистый газ, сернистая кислота и ее соли обладают выраженными восстановительными свойствами.
H2SO3 + Br2 = H2SO4 + HBr

Оксид серы VI — SO3
Является высшим оксидом серы. Бесцветная летучая жидкость с удушающим запахом. Ядовит.
Получение
В промышленности данный оксид получают, окисляя SO2 кислородом при нагревании и присутствии катализатора
(оксид ванадия — Pr, V2O5).
SO2 + O2 = (кат) SO3
В лабораторных условиях разложением солей серной кислоты — сульфатов.
Fe2(SO4)3 = (t) SO3 + Fe2O3
Химические свойства
- Кислотные свойства
- Окислительные свойства
Является кислотным оксидом, соответствует серной кислоте. При реакции с основными оксидами и основаниями образует ее соли — сульфаты и
гидросульфаты. Реагирует с водой с образованием серной кислоты.
SO3 + 2KOH = K2SO4 + 2H2O (основание в избытке — средняя соль)
SO3 + KOH = KHSO4 + H2O (кислотный оксид в избытке — кислая соль)
SO3 + Ca(OH)2 = CaSO4 + H2O

SO3 + Li2O = Li2SO4
SO3 + H2O = H2SO4
SO3 — сильный окислитель. Чаще всего восстанавливается до SO2.
SO3 + P = SO2 + P2O5
SO3 + H2S = SO2 + H2O
SO3 + KI = SO2 + I2 + K2SO4

© Беллевич Юрий Сергеевич 2018-2020
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение
(в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов
без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования,
обратитесь, пожалуйста, к Беллевичу Юрию.
Выберите схемы химических реакций, в которых сероводород проявляет восстановительные
свойства.
2H2S + SO2 → 3S + 2H2O
H2S + Cl2 → S + 2HCl
2H2S + 3O2 → 2SO2 + 2H2O
H2S + 2KOH → K2S + 2H2O
H2S + CuSO4 → CuS + H2SO4
При взаимодействии с какими веществами сера проявляет окислительные свойства?
Железо
Водород
Хлор
Магний
Азотная кислота
Кислород
Вставьте пропущенные слова.
Водный раствор сероводорода проявляет свойства, при взаимодействии сероводорода с гидроксидом лития в соотношении 1:1 образуется лития. Гидросульфид лития – соль.
кислотные
гидросульфид
кислая
основные
сульфид
средняя
Из приведенных утверждений выберите те, которые относятся к характеристике химического
элемента серы.
Минимальная степень окисления равна –2
Для простого вещества не характерно явление аллотропии
Содержит 4 электрона на внешнем уровне
Максимальное число неспаренных электронов, а значит и максимальная валентность, может быть равно шести
Окислительные свойства выражены сильнее, чем у хлора
Имеет больший радиус атома, чем кислород
Впишите ответ.
Сумма коэффициентов в уравнении химической реакции S + HNO3 = H2SO4 + NO2 + H2O
равна
.
Впишите ответ, округлив его до десятых.
Масса осадка, образующаяся при взаимодействии 300 г раствора нитрата свинца (II)
с массовой долей соли 33,1% с избытком сероводорода, составляет
г.
Установите соответствие между химической реакцией и изменением степени окисления
серы в ней.
H2S + Ba(OH)2 → BaS + 2H2O
Дополните предложение, выбрав верный ответ.
Объем кислорода, который потребуется для сжигания технической серы массой 10 г, содержащей 20% примесей, составляет , л.
Электронное строение атома.
Сера относится к элементу, находящемуся в VI-й группе главной подгруппы периодической системы Д.И.Менделеева. Его электронная конфигурация атома 1s22s22p63s23p4.

Нахождение в природе.
В обычных условиях сера представляет собой лёгкие, жёлтые кристаллы, нерастворимые в воде, но хорошо растворимые в сероуглероде. Кристаллическая решётка серы – молекулярная, в узлах которой находится циклическая молекула S8. Сера имеет ряд аллотропных модификаций.
Вышеуказанная форма серы называется моноклинной серой, при охлаждении которой переходит в устойчивые кристаллы ромбической серы.
Если расплавленную серу влить в холодную воду, то образуется ещё одна аллотропная модификация – пластическая сера. Температура кипения серы +445оС. В парах расплавленной серы содержатся молекулы S8, S6, S4, S2.
В природе сера встречается в трёх формах:

1) Самородная сера
2) Сульфидная сера:
FeS2 – серный или железный колчедан, пирит.
CuS – медный блеск.
CuFeS2 – халькопирит или медный колчедан.
PbS – свинцовый блеск.
ZnS – цинковая обманка.
HgS – киноварь.
3) Сульфатная сера:
CaSO4x2H2O – гипс.
CaSO4xH2O – алебастр.
Na2SO4x10H2O – глауберова соль.
MgSO4x 7H2O – горькая соль.
Химические свойства.
1. Свойства простого вещества.
Сера может проявлять как окислительные, так и восстановительные свойства. Окислителем сера является в первую очередь по отношению к металлам:
S + 2Na = Na2S
S + Ca = CaS
3S +2Al = Al2S3
В качестве окислителя сера проявляет свои свойства и при взаимодействии с неметаллами:
S + H2 = H2S
3S + 2P = P2S3
2S + C = CS2
Однако с неметаллами, имеющими электроотрицательность бóльшую, чем у серы, она реагирует в качестве восстановителя:
S +3F2 = SF6
S + Cl2 = SCl2
Сера реагирует со сложными веществами, как правило, окислителями. Причём азотная кислота окисляет её до серной кислоты:
S + 6HNO3 = H2SO4 + 6NO2 + 2H2O
Другие окислители окисляют серу до степени окисления (+4):
S + 2H2SO4 = 3SO2 + 2H2O
3S + 2KClO3 = 3SO2 + 2KCl
По механизму реакции ДИСПРОПОРЦИОНИРОВАНИЯ сера реагирует с щелочами. В процессе этой реакции образуются соединения серы (-2) и (+4):
3S + 6KOH = K2SO3 + 2K2S + 3H2O
Непосредственно с водой сера не реагирует, однако при нагревании подвергается дисмутации в атмосфере водяного пара.
Сера может быть получена в процессе реакций:
SO2 + 2CO = S + 2CO2
Na2S2O3 + 2HCl = S + SO2 + 2NaCl + H2O
2. Соединения серы (-2).
У серы в степени окисления (-2) соединения называются сульфидами. Это бинарные соединения, в которых одним из элементов является металл: Na2S, ZnS, Al2S3, PbS2 и др.
Соединение серы (-2) с водородом называется сероводород – H2S. Сероводород – газ без цвета, неприятного запаха, тяжелее воздуха, очень ядовит, мало растворим в воде. Сероводород можно получить различными способами. Oбычно, в лаборатории, сероводород получают, действуя на сульфиды сильными кислотами:
FeS + 2HCl = FeCl2 + H2S
Для сероводорода и его солей характерны восстановительные свойства:
H2S + SO2 = 3S + 2H2O
В указанной реакции сера образуется по механизму конпропорционирования ( из двух атомов серы, имеющих различные степени окисления (-2) и (+4) образуется соединение серы со степенью окисления (0).
SO2 + 2CO = S + 2CO2
Na2S2O3 + 2HCl = S + SO2 + 2NaCl + H2O
В лаборатории сероводород получают:
FeS + 2HCl = FeCl2 + H2S
При сгорании в кислороде он образует различные продукты:
2H2S + O2 = 2H2O + 2S (недостаток кислорода)
2H2S + 3O2 = 2H2O + 2SO2 (избыток кислорода)
Cероводород легко окисляется галогенами, оксидом серы, хлоридом железа (III):
H2S + Cl2 = 2HCl + S
2H2S + SO2 = 2H2O + 3S
H2S + 2FeCl3 = 2FeCl2 + S + 2HCl
На воздухе сероводород окисляет серебро, чем и объясняется почернение серебряных изделий со временем:
2H2S + 4Ag + O2 = 2Ag2S + 2H2O
Водные растворы сероводорода являются слабой кислотой. Диссоциирует в две стадии, образует два типа солей: гидросульфиды и сульфиды:
H2S ↔ HS-1 + H+
HS-1 ↔ H+ + S-2
Сульфиды большинства металлов нерастворимы и имеют различную окраску. Это является фактором, благодаря которому можно распознавать те или иные катионы в растворах:
Чёрные – HgS, Ag2S, PbS, CuS, FeS, NiS;
Коричневые – SnS, Bi2S3;
Оранжевые – Sb2S3, Sb2S5;
Жёлтые – As2S3, As2S5, SnS2, CdS;
Розовые — MnS
Белые – ZnS, Al2S3, BaS, CaS;
Cульфиды в водной среде проявляют восстановительные свойства, обычно окисляясь до серы: 
3H2S + 2KMnO4 = 3S + 2MnO2 + 2KOH + 2H2O
H2S + 2HNO3 = S + 2NO2 + 2H2O
3H2S + 2FeCl3 = S + FeS + 6HCl
H2S + J2 = S + 2HJ
При взаимодействии с более сильными окислителями сульфиды окисляются до соединений со степенью окисления (+6):
H2S + 4H2O + Cl2 = H2SO4 + 8HCl
MnS + 3HNO3 = MnSO4 + 8NO2 + 4H2O
PbS + 4H2O2 = PbSO4 + 4H2O
3. Соединение серы (+4).
Из соединений серы со степенью окисления (+4) наиболее характерны оксид серы (SO2) или сернистый газ и сернистая кислота (H2SO3) и её соли. Оксид серы представляет собой газ с резким запахом, бесцветный, тяжелее воздуха, хорошо растворяется в воде. Получают при неполном горении сероводорода или при окислении сульфидов. В лаборатории его получают при взаимодействии меди с концентрированной серной кислотой:
Cu + H2SO4 = CuSO4 + SO2 + H2O
Na2SO3 + 2HCl = 2NaCl + SO2 + H2O
Для оксида серы (+4) характерны как окислительные:
SO2 + H2S = 3S + 2H2O
так и восстановительные свойства:
2SO2 + O2 = 2SO3
2SO2 + 2H2O + Br2 = H2SO4 + 2HBr
SO2 + Cl2 = SO2Cl2
SO2 + 2HNO3 = H2SO4 + 2NO2
Оксид серы (+4) – типичный кислотный оксид, он реагирует с основания-ми с образованием солей, с водой образует сернистую кислоту:
SO2 + 2NaOH = Na2SO4 + H2O
SO2 + H2O = H2SO3
Сернистая кислота – слабая кислота, диссоциирует в две стадии, образует два типа солей: кислые — гидросульфитыи средние —сульфиты :
H2SO3 ↔ HSO3- + H+
HSO3-↔ SO32- + H+
Соли сернистой кислоты неустойчивы, разлагаются при действии более сильных кислот и при нагревании:
Na2SO3 + HNO3 = 2NaNO3 + SO2 + H2O
K2SO3 = K2O + SO2
В растворах сульфит-ионы проявляют чаще всего восстановительные свойства:
Na2SO3 + 2KOH + KMnO4 = Na2SO4 + 2K2MnO4 + H2O
4. Соединения серы (+6)
Из соединений серы в степени окисления (+6) наиболее характерны оксид серы — SO3 или серный ангидрид и H2SO4 — cерная кислота. SO3 — бесцветный газ с характерным резким запахом, тяжелее воздуха, хорошо растворим в воде.
Оксид серы (+6) получают окислением оксида серы (+4) в присутствии катализатора и высоком давлении:
2SO2 + O2 = 2SO3
SO3 + H2O = H2SO4
Оксид серы (+6) является сильным окислителем:
SO3 + 2KJ = J2 + K2SO3
SO3 + H2S = 4SO2 + H2O2
5SO3 + 2P = P2O5 + 5SO2
Кроме того, он проявляет кислотные свойства, так как является кислотным оксидом:
SO3 + ZnO = ZnSO4
SO3 + KOH = KHSO4
SO3 + 2KOH = K2SO4 + H2O
Серная кислота, её соли.
Серная кислота представляет собой бесцветную маслообразную жидкость, максимальная плотность которой 1,84 г/мл. Исходным сырьём для получения серной кислоты является серный колчедан или пирит:
4FeS2 + 11O2 = 2Fe2O3 + 8SO2
Далее, под воздействием катализатора — V2O5 происходит окисление оксида серы (+4) до оксида серы (+6):
2SO2 + O2 = 2SO3
Полученная безводная серная кислота называется олеум, т.к. в действительности, оксид серы (+4) растворяют в 98%-ной серной кислоте.
SO3 + H2O = H2SO4
Концентрированная серная кислота проявляет сильное водоотнимающее действие. Это свойство положено в основу многочисленных химических процессов, особенно в органической химии (получение спиртов, простых и сложных эфиров, альдегидов и т.д.). Концентрированная серная кислота является сильным окислителем. Например, при взаимодействии с просты-ми веществами, она окисляет их до кислот или оксидов:
2P + 5H2SO4 = 2H3PO4 + 5SO2 + 2H2O
C + H2SO4 = 2SO2 + CO2 + 2H2O
При обычной температуре она окисляет галогенводороды и сероводород:
H2SO4 + 8HJ = 4J2 + H2S + 4H2O
H2SO4 + 2HBr = Br2 + SO2 + 2H2O
H2SO4 + H2S = S + SO2 + 2H2O
Серная кислота термически устойчива и не летуча, поэтому способна вытеснять другие кислоты из их солей:
H2SO4 + KClO3 = KHSO4 + HClO4
Cерная кислота диссоциирует в две стадии, образует два типа солей:
кислые – гидросульфатыи средние – сульфаты:
H2SO4 ↔ HSO4- + H+
HSO4- ↔ SO42- + H+
Серная кислота проявляет свойства, характерные для остальных кислот: она реагирует с металлами, оксидами металлов, гидроксидами, солями слабых кислот. Качественной реакцией на сульфат-ионы в растворах является взаимодействие её с ионами бария Ва2+, в результате чего выпадает белый осадок:
Ba2+ + SO42- = BaSO4
При прокаливании сульфаты разлагаются на различные классы соединений в зависимости от металла, входящего в состав соли. Сульфаты щелочных металлов плавятся без разложения. Сульфаты металлов средней активности разлагаются на соответствующие оксиды:
ZnSO4 = ZnO + SO3
Сульфат железа (II) разлагается по механизму внутримолекулярной ОВР:
4FeSO4 = 2Fe2O3 + 4SO2 + O2
Сульфаты наиболее тяжёлых или малоактивных металлов разлагаются с образованием простых веществ – металла и кислорода:
HgSO4 = Hg + SO2 + O2
Некоторые сульфаты, являясь окислителями, реагируют с простыми веществами:
CaSO4 + C = CaO + SO2 + CO
BaSO4 + 4C = BaS + 4CO
Большое значение в промышленности, лабораторных исследованиях имеет взаимодействие серной кислоты с металлами. Эта тема заслуживает особого внимания, т.к. образуются различные продукты реакции в зависимости от положения реагируемого металла в ряду напряжений, степени разбавленности кислоты, температуры, катализаторов.
Разбавленная серная кислота с металлами, стоящими в ряду активности до водорода, при обычной температуре образует соль и водород:
H2SO4 + Zn = ZnSO4 + H2
Разбавленная кислота не реагирует с металлами, стоящими в ряду активности после водорода (медь, серебро, ртуть), но концентрированная кислота образует с ними соль, оксид серы (+4) и воду:
H2SO4 + Cu = CuSO4 + SO2 + H2O
Такие же продукты реакции концентрированная серная кислота образует при взаимодействии с металлами, стоящими в ряду активности до водорода:
2H2SO4 + Zn = ZnSO4 + SO2 + 2H2O
Однако, концентрированная серная кислота реагирует не со всеми металлами. Алюминий, железо, свинец и олово она пассивирует с образованием на их поверхности тонких оксидных плёнок, предотвращающих дальнейшее растворение металла:
H2SO4 + Al = Al2O3 + SO2 + H2O
Активные щелочные и щелочноземельные металлы могут образовывать с разбавленной кислотой не только водород. Например, магний с очень разбавленной серной кислотой на холоду образует соль, серу и воду:
H2SO4 + Mg = MgSO4 + S + H2O
Натрий при обычной температуре с очень разбавленной серной кислотой образует соль, серу и воду:
H2SO4 + Na = Na2SO4 + S + H2O,
а при охлаждении образует сероводород:
H2SO4 + Na = Na2SO4 + Н2S + H2O
Соли серной кислоты находят большое применение в промышленности, сельском хозяйстве, в быту.
Na2SO4x 10H2O – глауберова соль, применяется в медицине в качестве слабительного,
(NH4)2SO4 – азотное удобрение для сельского хозяйства,
CaSO4 – безводный гипс, применяется в строительстве.
CaSO4x 2H2O – водный гипс,
2CaSO4 xH2O – алебастр, продукт получения гипса,
MgSO4 – горькая соль, применяется в медицине как слабительное и гипотензивное средство,
BaSO4 – баритова каша, средство, применяемое как рентгеноконтрастное средство.
CuSO4 x 5H2O – медный купорос, применяется в строительстве,
FeSO4x 7H2O – железный купорос,
ZnSO4 x 7H2O – цинковый купорос,
KАl(SO4)2 x 12H2O – алюмокалиевые квасцы.
© blog.tutoronline.ru,
при полном или частичном копировании материала ссылка на первоисточник обязательна.
