Оксид азота 2 это какой оксид химические свойства
Эта статья описывает оксиды азота как химические соединения; об образовании и способах сокращения выбросов оксидов азота при горении см. NOx (оксиды азота).
Окси́ды азо́та — неорганические бинарные соединения азота с кислородом.
Список оксидов[править | править код]
Известны 10 соединений азота с кислородом. Кроме пяти классических оксидов азота — закиси азота N2O, окиси азота NO, оксида азота(III) N2O3, диоксида азота NO2 и оксида азота(V) N2O5 — известны также димер диоксида азота N2O4 и 4 малостабильных соединения: нитрозилазид NON3, нитрилазид NO2N3, тринитрамид N(NO2)3 и нитратный радикал NO3.
N2O[править | править код]
Несолеобразующий оксид. При нагревании разлагается на азот и кислород. При высоких концентрациях N2O возбуждает нервную систему («веселящий газ»). В медицине N2O применяют как слабое средство для наркоза, в высоких концентрациях токсичен. Также N2O называют закисью азота. Закись азота иногда используется для улучшения технических характеристик двигателей внутреннего сгорания. В случае автомобильных применений вещество, содержащее закись азота, и горючее впрыскиваются во впускной (всасывающий) коллектор двигателя, что приводит к следующим результатам:
- снижает температуру всасываемого в двигатель воздуха, обеспечивая плотный поступающий заряд смеси;
- увеличивает содержание кислорода в поступающем заряде;
- повышает скорость (интенсивность) сгорания в цилиндрах двигателя.
NO[править | править код]
Оксид азота NO (монооксид азота) — бесцветный газ, незначительно растворим в воде. Не взаимодействует с водой, растворами кислот и щелочей. Оксид азота(II) — очень реакционное соединение, может вступать в реакции присоединения с рядом солей (нитрозосоли), с галогенами (напр., нитрозилхлорид NOCl), органическими соединениями. При обычной температуре NO соединяется с кислородом с образованием NO2. Оксид NO получают каталитическим окислением аммиака при производстве азотной кислоты. В больших количествах очень ядовит, обладает удушающим действием.
N2O3[править | править код]
Оксид N2O3 (триоксид диазота, азотистый ангидрид) — темно-синяя жидкость, неустойчивая при обычных условиях, взаимодействует с водой, образуя азотистую кислоту HNO2.
NO2[править | править код]
Оксид азота NO2 (диоксид азота) — бурый ядовитый газ тяжелее воздуха, легко сжижается. При комнатной температуре NO2 находится в смеси с его бесцветным димером N2O4, приблизительно 1:1. Взаимодействует с водой:
и растворами щелочей:
N2O5(V)[править | править код]
Оксид азота N2O5 (пентаоксид диазота, азотный ангидрид) — бесцветное кристаллическое вещество, легко разлагается на NO2 и О2. Сильный окислитель. В воде легко растворяется с образованием азотной кислоты HNO3.
Литература[править | править код]
- Химическая энциклопедия / Редкол.: И. Л. Кнунянц и др.. — М.: Советская энциклопедия, 1988. — Т. 1 (Абл-Дар). — 623 с.
- Леонтьев А. В., Фомичева О. А., Проскурнина М. В., Зефиров Н. С. Современная химия оксида азота(I) (рус.) // Успехи химии. — Российская академия наук, 2001. — Т. 70, № 2. — С. 107—122.
- Weller, Richard, Could the sun be good for your heart? Архивы TedxGlasgow. Filmed March 2012, posted January 2013
- Roszer, T (2012) The Biology of Subcellular Nitric Oxide. ISBN 978-94-007-2818-9
- Stryer, Lubert. Biochemistry, 4th Edition. — W.H. Freeman and Company, 1995. — P. 732. — ISBN 0-7167-2009-4.
- Plant-based Diets | Plant-based Foods | Beetroot Juice | Nitric Oxide VegetablesАрхивы . Berkeley Test.
- Ghosh, S. M.; Kapil, V.; Fuentes-Calvo, I.; Bubb, K. J.; Pearl, V.; Milsom, A. B.; Khambata, R.; Maleki-Toyserkani, S.; Yousuf, M.; Benjamin, N.; Webb, A. J.; Caulfield, M. J.; Hobbs, A. J.; Ahluwalia, A. Enhanced Vasodilator Activity of Nitrite in Hypertension: Critical Role for Erythrocytic Xanthine Oxidoreductase and Translational Potential (англ.) // Hypertension : journal. — 2013. — Vol. 61, no. 5. — P. 1091—1102. —
Оксиды азота
При описании свойств азота отмечалось, что при непосредственном взаимодействии азота с кислородом образуется только оксид азота (II) NO. Однако существуют оксиды азота со всеми возможными степенями окисления (от +1 до +5).
N2O — оксид азота (I), «веселящий газ»
При обычной температуре N2O — бесцветный газ со слабым приятным запахом и сладковатым вкусом; обладает наркотическим действием, вызывая сначала судорожный смех, затем — потерю сознания.
Способы получения
1. Разложение нитрата аммония при небольшом нагревании:
NH4NO3 = N2O↑ + 2Н2О
2. Действие HNO3 на активные металлы
10HNO3(конц.) + 4Са = N2O↑ + 4Ca(NO3)2 + 5Н2О
Химические свойства
N2O не проявляет ни кислотных, ни основных свойств, т. е. не взаимодействует с основаниями, с кислотами, с водой (несолеобразующий оксид).
При Т > 500’С разлагается на простые вещества. N2O — очень сильный окислитель. Например, способен в водном растворе окислить диоксид серы до серной кислоты:
N2O + SO2 + Н2О = N2↑ + H2SO4
NO — оксид азота (II), монооксид азота.
При обычной температуре NO — бесцветный газ без запаха, малорастворимый в воде, очень токсичный (в больших концентрациях изменяет структуру гемоглобина).
Способы получения
1. Прямой синтез из простых веществ может быть осуществлен только при очень высокой Т:
N2 + O2 = 2NО — Q
2. Получение в промышленности (1-я стадия производства HNO3).
4NH3 + 5O2 = 4NО + 6Н2О
3. Лабораторный способ — действие разб. HNO3 на тяжелые металлы:
8HNO3 + 3Cu = 2NO + 3Cu(NO3)2 + 4Н2О
Химические свойства
NO — несолеобразующий оксид (подобно N2О). Обладает окислительно-восстановительной двойственностью.
2NO + SO2 + Н2О = N2O↑ + H2SO4
2NO + 2H2 = N2 + 2Н2О (со взрывом)
2NO + O2 = 2NO2
10NO + 6KMnO4 + 9H2SO4 = 10HNO3 + 3K2SO4 + 6MnSO4 + 4Н2О
NO2 — оксид азота (IV), диоксид азота
При обычной температуре NO2 — красно-бурый ядовитый газ с резким запахом. Представляет собой смесь NO2 и его димера N2O4 в соотношении -1:4. Диоксид азота хорошо растворяется в воде.
Способы получения
I. Промышленный — окисление NO: 2NO + O2 = 2NO2
II. Лабораторные:
действие конц. HNO3 на тяжелые металлы: 4HNO3 + Сu = 2NO2↑ + Cu(NO3)2 + 2Н2О
разложение нитратов: 2Pb(NO3)2 = 4NO2↑ + O2↑ + 2РbО
Химические свойства
NO2 взаимодействует с водой, основными оксидами и щелочами. Но реакции протекают не так, как с обычными оксидами — они всегда окислительно — восстановительные. Объясняется это тем, что не существует кислоты со С.О. (N) = +4, поэтому NO2 при растворении в воде диспропорционирует с образованием 2-х кислот — азотной и азотистой:
2NO2 + Н2О = HNO3 + HNO2
Если растворение происходит в присутствии O2, то образуется одна кислота — азотная:
4NO2 + 2Н2О + O2 = 4HNO3
Аналогичным образом происходит взаимодействие NO2 со щелочами:
в отсутствие O2: 2NO2 + 2NaOH = NaNO3 + NaNO2 + Н2О
в присутствии O2: 4NO2 + 4NaOH + O2 = 4NaNO3 + 2Н2О
По окислительной способности NO2 превосходит азотную кислоту. В его атмосфере горят С, S, Р, металлы и некоторые органические вещества. При этом NO2 восстанавливается до свободного азота:
10NO2 + 8P = 5N2 + 4P2O5
2NO2 + 8HI = N2 + 4I2 + 4Н2О (возникает фиолетовое пламя)
В присутствии Pt или Ni диоксид азота восстанавливается водородом до аммиака:
2NO2 + 7Н2 = 2NH3 + 4Н2О
Как окислитель NO2 используется в ракетных топливах. При его взаимодействии с гидразином и его производными выделяется большое количество энергии:
2NO2 + 2N2H4 = 3N2 + 4Н2О + Q
N2O3 и N2O5 — неустойчивые вещества
Оба оксида имеют ярко выраженный кислотный характер, являются соответственно ангидридами азотистой и азотной кислот.
N2O3 как индивидуальное вещество существует только в твердом состоянии ниже Т пл. (-100С).
С повышением температуры разлагается: N2O3 → NO + NO2
N2O5 при комнатной температуре и особенно на свету разлагается так энергично, что иногда самопроизвольно взрывается:
2N2O5 = 4NO2 + O2
Оксиды азота. Общая характеристика, химические свойства.

Данный урок посвящен оксидам азота, которые при взаимодействии с водой образуют кислоты, и соответственно, являются солеобразующими, — NO2 и N2O5.
NO2 представляет собой типичный кислотный оксид, который обладает высокой химической активностью, и при взаимодействии с неметаллами (сера, фтор, водород) ведет себя как сильный окислитель; также применяется при производстве серной кислоты (нитрозный метод), окисляя сернистый газ в олеум (SO3), и азотистой кислоты (HNO2).
N2O5 — это высший оксид азота, очень летуч, взаимодействует с органическими веществами, поэтому его нужно хранить в стеклянной посуде (!Важно! плавиковая кислота (HF) наоборот хранится в полимерной таре по причине того, что разъедает стекло), легко разлагается до ядовитого NO2 со взрывом; используется при получении азотной кислоты (HNO3).
Важно знать, что все оксиды азота токсичны!
Более детально изучить химические свойства предлагаю при помощи таблицы, в которой собраны все необходимые реакции для сдачи ЕГЭ.
Солеобразующие оксиды азота | ||
1) Формула | NO2 | N2O5 |
2) Характеристика | NO2 (Nitrogen dioxide, диоксид азота)– красно — бурый газ, ядовит, с характерным острым запахом; Хорошо растворяется в воде; | N2O5 (Dinitrogen pentoxide, пентаоксид азота)– бесцветные, летучие кристаллы, взрывчатые; Хорошо растворяется в воде; |
3) Получение в лаборатории | 1) 2Pb(NO3)2 = 2PbO + 4NO2 + O2 (200-470 C); 2) Me + 4HNO3(к) = Me(NO3)2 + 2NO2 + 2H2O (Me= правее водорода); | 1) 2HNO3(к) + P2O5 = N2O5 + 2HPO3 (-10 C); 2) 4AgNO3 + 2Cl = 4AgCl + 2N2O5 + O2; |
4) Получение в промышленности | NO+ O2 = NO2 (на воздухе — мгновенно); | 2NO2 + O3 = N2O5 (-78 C); |
5) Химические свойства | 1) Разложение: 2NO2 = 2NO + O2 (140-600 C) 2) C кислотами: 2NO2 + 4HCl = 2NOCl + Cl2 + 2H2O; 2NO2 + 8HI = N2 + 4I2 + 4H2O; 2NO2 + 2H2S = N2 + 2S + 2H2O (350 C); 3) С металлами: 2NO2 + Na = NaNO3 + NO (22 C); 2NO2 + 4Cu = N2 + 4CuO (600 C); 2NO2 + 4Zn = 4ZnO + N2; NO2 + K = KNO2; 4) С неметаллами: NO2 + O2 ≠ В присутствии воды реакция идет (образование HNO3): 4NO2 + O2 + 2H2O = 4HNO3; 4NO2 + O2 + 4NaOH = 4NaNO3 + 2H2O; 2NO2 + O3 = N2O5 + O2; 2NO2 + 2C = N2 + 2CO2 (t); 2NO2 + 7H2 = 2NH3 + 4H2O (kat.: Pt, Ni); 10NO2 + 8P = 5N2 + 4P2O5 (150 C); 2NO2 + 2S = N2 + 2SO2 (150 C); 2NO2 + F2 = NO2F (нитронил фтористый); 2NO2 + F2 + H2O = 2HNO3 + 2HF; 5) С солями: 3NO2 + CaCO3 = Ca(NO3)2 + NO + CO2 (+Q); 2NO2 + KГ = KNO3 + NOГ (Г= Cl, Br); 14NO2 + 16FeSO4 + 8H2SO4 = 8HNO3 + 8Fe2(SO4)2 + 3N2 + 4H2O; 5NO2 + KMnO4 + 2H2SO4 + H2O = 5HNO3 + MnSO4 + KHSO4 6) С оксидами: 2NO2 + H2O = HNO3 + HNO2; 2NO2 + SO2 = N2 + 2SO3 (22 C) 2NO2 + SO2 = SO3 + NO (t) 7) C основаниями: 2NO2 + 2KOH = KNO3 + KNO2 + H2O | 1) Разложение: N2O5 = 4NO + O2 (взрыв); 2) С кислотами: N2O5 + 3H2S = 3H2SO4 + 4N2 + 4O2; 3) С металлами: N2O5 + 3Zn = 3ZnO + O2 + N2 (t) N2O5 + 5Cu = N2 + 5CuO (500 C) N2O5 + Na = NaNO3 + NO2 4) С неметаллами: N2O5 + O2 ≠ N2O5 + I2 = I2O5 + N2 5) С солями: 2N2O5 + 2KI = I2 + 2NO2 + 2KNO3 6) С оксидами: N2O5 + H2O = 2HNO3 + Q N2O5 + 3SO2 = 3SO3 + O2 + N2 N2O5 + Al2O3 = 2Al(NO3)3 (40 C) N2O5 + CaO = Ca(NO3)2 7) С основаниями: N2O5 + 2NH4OH = 2NH4NO3 + H2O N2O5 + 2KOH = 2KNO3 + H2O |
6) Применение | 1) Используется при производстве H2SO4 и HNO3; 2) Окислитель в жидком ракетном топливе; 3) Вместе с другими оксидами азота образует «лисий хвост» — выбросы химического производства, и из выхлопных труб автомобилей; 4) Токсичен, вызывает отек легких. | 1) Применение ограничено из-за взрывоопасной природы оксида азота (V); 2) Используется в качестве нитрующего агента (в органической химии). |
Следующее занятие будет посвящено задачам по этой теме.
Если возникнут вопросы, пиши в коменты)
Солеобразующие оксиды азота. Задачи с объяснениями.
Введение
Если внимательно взглянуть на азот в периодической системе химических элементов Д. И. Менделеева, то можно заметить, что он имеет переменную валентность. Это значит, что азот образует сразу несколько бинарных соединений с кислородом. Некоторые из них были открыты недавно, а некоторые — изучены вдоль и поперек. Существуют малостабильные и устойчивые оксиды азота. Химические свойства каждого из этих веществ совершенно разные, поэтому при их изучении нужно рассматривать как минимум пять оксидов азота. Вот о них и пойдет речь в сегодняшней статье.
Оксид азота (I)
Формула — N2O. Иногда его могут называть оксонитридом азота, оксидом диазота, закисью азота или веселящим газом.
Свойства
В обычных условиях представлен бесцветным газом, имеющим сладковатый запах. Его могут растворять вода, этанол, эфир и серная кислота. Если газобразный оксид одновалентного азота нагреть до комнатной температуры под давлением 40 атмосфер, то он сгущается до бесцветной жидкости. Это несолеобразующий оксид, разлагающийся во время нагревания и показывающий себя в реакциях как восстановитель.
Получение
Этот оксид образуется, когда нагревают сухой нитрат аммония. Другой способ его получения — термическое разложение смеси «сульфаминовая + азотная кислота».
Применение
Используется в качестве средства для ингаляционного наркоза, пищевая промышленность знает этот оксид как добавку E942. С его помощью также улучшают технические характеристики двигателей внутреннего сгорания.
Оксид азота (II)
Формула — NO. Встречается под названиями монооксида азота, окиси азота и нитрозил-радикала
Свойства
При нормальных условиях имеет вид бесцветного газа, который плохо растворяется в воде. Его трудно сжижить, однако в твердом и жидком состояниях это вещество имеет голубой цвет. Данный оксид может окисляться кислородом воздуха
Получение
Его довольно просто получить, для этого нужно нагреть до 1200-1300оС смесь азота и кислорода. В лабораторных условиях он образуется сразу при нескольким опытах:
- Реакция меди и 30%-ного раствора азотной кислоты.
- Взаимодействие хлорида железа, нитрита натрия и соляной кислоты.
- Реакция азотистой и иодоводородной кислот.
Применение
Это одно из веществ, из которых получают азотную кислоту.
Оксид азота (III)

Формула — N2O3. Также его могут называть азотистым ангидридом и сесквиоксидом азота.
Свойства
В нормальных условиях является жидкостью, которая имеет синий цвет, а в стандартных — бесцветным газом. Чистый оксид существует только в твердом агрегатном состоянии.
Получение
Образуется при взаимодействии 50%-ной азотной кислоты и твердого оксида трехвалентного мышьяка (его также можно заменить крахмалом).
Применение
С помощью этого вещества в лабораториях получают азотистую кислоту и ее соли.
Оксид азота (IV)
Формула — NO2. Также его могут называть диоксидом азота или бурым газом.
Свойства
Последнее название соответствует одному из его свойств. Ведь этот оксид имеет вид или красно-бурого газа или желтоватой жидкости. Ему присуща высокая химическая активность.
Получение
Данный оксид получают при взаимодействии азотной кислоты и меди, а также во время термического разложения нитрата свинца.
Применение
С помощью него производят серную и азотную кислоты, окисляют жидкое ракетное топливо и смесевые взрывчатые вещества.
Оксид азота (V)
Формула — N2O5. Может встречаться под названиями пентаоксида диазота, нитрата нитроила или азотного ангидрида.
Свойства
Имеет вид бецветных и очень летучих кристаллов. Они могут плавиться при температуре 32,3оС.
Получение
Этот оксид образуется при нескольких реакциях:
- Дегидрация азотной кислоты оксидом пятивалентного фосфора.
- Пропускание сухого хлора над нитратом серебра.
- Взаимодействие озона с оксидом четырехвалентного азота.
Применение
Из-за своей крайней неустойчивости в чистом виде нигде не используется.
Заключение
В химии существует девять оксидов азота, приведенные выше являются только классическими соединениями этого элемента. Остальные четыре — это, как уже было сказано, нестабильные вещества. Однако их все объединяет одно свойство — высокая токсичность. Выбросы оксидов азота в атмосферу приводят к ухудшению состояния здоровья живущих поблизости от промышленных химических предприятий людей. Симптомы отравления каким-либо из этих веществ — токсический отек легких, нарушение работы центральной нервной системы и поражение крови, причина которого — связывание гемоглобина. Поэтому с оксидами азота необходимо осторожно обращаться и в большинстве случаев использовать средства защиты.
Оксид азота (II), оксид (II) оксид, окись азота — неорганическое соединение состава NO. При обычных условиях является бесцветным, токсичным и негорючей газом. В жидком и твердом состояниях соединение димеризуеться с образованием оксида N 2 O 2.
Монооксид азота относится к несолетвирних оксидов: с водой он не образует кислоту или основание, а непосредственно реагируя с основами и с кислотами, не образует солей.
Физические свойства
Оксид азота NO при обычных условиях является бесцветным газом с очень низкой температурой кипения (-151,8 ° С) и температурой плавления (-163,6 ° С). В твердом состоянии, благодаря наличию неспаренного электрона, соединение полностью димеризуеться с образованием оксида N 2 O 2, а в жидком — примерно на четверть.
В воде растворяется трудно: при обычной температуре лишь около 5 см³ в 100 г воды.
Получение
Промышленный метод
В промышленных масштабах синтез оксида азота (II) является одной из стадий в получении азотной кислоты. Его получают окислением аммиака кислородом воздуха в присутствии катализаторов:
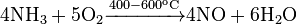
Количество преобразованного в NO аммиака составляет примерно 93-98%. Другими, побочными, реакциями является образование азота и оксида азота (I):
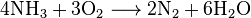
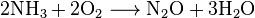
Кроме этого, может происходить частичное разложение конечного продукта, NO, а также его взаимодействие с аммиаком:
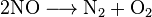
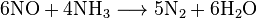
Согласно одной из самых распространенных теорий механизма окисления, предложенной Максом Боденштейном, аммиак окисляется атомарным кислородом, адсорбированным на катализаторе с образованием гидроксиламина, который постепенно разлагается с образованием NO:
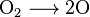
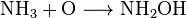
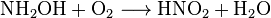
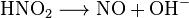
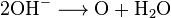
Основными применяемыми катализаторами являются платина и, в меньшей степени, родий и палладий. Несмотря на их высокую стоимость, они имеют преимущество в высшем выходе реакции и меньшей склонности к отравлению.
Лабораторные методы
В лабораториях монооксид азота обычно добывают взаимодействием разбавленной азотной кислоты с медью при некотором нагревании по реакции:
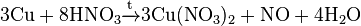
Применяются также реакции восстановления нитритов в разведенной серной кислоте:
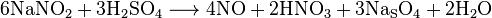
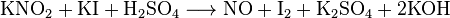
Полученный такими методами NO может быть загрязнен примесями (прежде всего, N 2 O), поэтому он требует дополнительной очистки.
Химические свойства
Наиболее характерной свойством монооксида азота является его способность легко сочетаться при обычных условиях с кислородом воздуха с образованием диоксида азота (реакция имеет большое значение при производстве азотной кислоты):
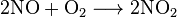
При высокотемпературном нагреве и в присутствии катализатора BaO, газообразные NO разлагается на простые соединения. Жидкий NO с течением времени может диспропорционуваты с образованием оксидов азота (I) и азота (III):
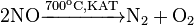
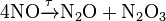
При взаимодействии с галогенами или серной кислотой (в присутствии кислорода), NO окисляется с образованием соединений нитрозила:
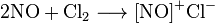
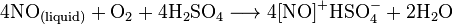
Аналогично он образует нитрозильни комплексы с металлами в водных растворах солей:
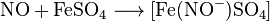
Оксид азота восстанавливается до свободного азота графитом, красным фосфором, неметаллическими соединениями-восстановителями, а также некоторыми металлами:
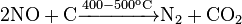
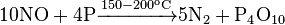
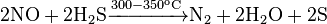
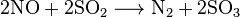
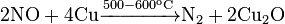
Роль в живых организмах
Роль оксида азота (II) как сигнальной молекулы в живых организмах была открыта в 1980-х годах, а в 1998 Роберт Ферчготт, Луис Игнарро и Ферид Мурад получили Нобелевскую премию по физиологии или медицине за выяснение его функций в сердечно-сосудистой системе. Монооксид азота является паракринным фактором благодаря своей способности быстро диффундировать через мембраны клеток, однако из-за высокой реакционность расстояние такой диффузии ограничена 1 мм а время полжизни молекул NO составляет 5-10 секунд. Азот мооноксид выполняет сигнальную функцию как у животных, так и у растений, даже некоторые бактерии могут чувствовать очень небольшие его концентрации и двигаться в сторону от источника этого соединения.
У млекопитающих NO задействован в ряде физиологических процессов, таких как регуляция артериального давления, передача нервных импульсов, свертывания крови и иммунный ответ. Синтез оксида азота (II) осуществляется путем деаминирование аминокислоты аргинина и обеспечивается ферментом NO-синтазы (NOS), что у млекопитающих трех изоформы: нейрональная (nNOS), индуцибельной (iNOS) и эндотелиальной (eNOS). nNOS и eNOS экспрессируются в соответствующих типах клеток конститутивно и резко увеличивают свою активность в ответ на рост концентрации Ca 2+. Зато активация iNOS осуществляется на уровне транскрипции под влиянием эндотоксинов или цитокинов воспаления, в частности в таких клетках как макрофаги и нейтрофилы, и не зависит от цитоплазматического уровня кальция.
Одной из мишеней монооксида азота в клетках млекопитающих, в том числе и гладких мышцах, является фермент гуанилатциклазы, в активном центре которого он присоединяется к атому железа и таким образом увеличивает энзиматическую активность. Циклический ГМФ, что является продуктом гуанилатциклазы, является вторичным посредником и запускает в клетке каскад реакций, обеспечивающих физиологическую ответ, в случае гладких мышц — их расслабление.
NO может действовать также и цГМФ-независимым путем, например изменять активность белков путем ковалентной нитрозилювання тиольных групп (-SH) специфических остатков цистеина в их составе.
Защитная функция монооксида азота
У растений NO участвует в защитных реакциях во время повреждений и инфекций. Также монооксид азота играет роль в функционировании иммунной системы животных. Активированные макрофаги и нейрофилов (а также клетки эндотелия) производят его в больших количествах во время воспалительных процессов. Вместе с NO они выделяют супероксид-он (O-2), эти два соединения соединяясь образуют очень токсичен пероксинитрит (OONO -) нужен для того, чтобы убить поглощены бактерии.
Медицинские препараты, влияющие на сигналювання NO
Из препаратов, влияющих на сигнальный путь монооксида азота, первым начал использоваться еще в XIX веке нитроглицерин для борьбы со стенокардией. Это соединение медленно расщепляется в организме и действует как источник NO длительное время. NO в свою очередь обеспечивает расширение сосудов и уменьшения нагрузки на сердце. Такое действие нитроглицерина была открыта благодаря наблюдению, что больные стенокардией работники фабрик, на которых изготавливали это соединение, сильнее страдали от боли на выходных. Врачи настолько часто слышали такие сообщения пациентов, обратили внимание на терапевтический эффект нитроглицерина. С тех пор было разработано много других нитровазодиляторив. Сам NO не имеет терапевтического действия при стенокрадии, через очень небольшое время полжизни, однако его иногда используют в вдыхаемой форме для облегчения легочной гипертензии.
Существуют также препараты, имеющие другие мишени в сигнальном пути NO. Например, силденафил подавляет деятельность фосфодиэстеразы, которая расщепляет цГМФ, таким образом продолжая продолжительность действия сигнала. Это соединение была впервые предложена для лечения стенокрадии, однако выяснилось, что она наиболее эффективно влияет на изоформу цГМФ-фосфодиэстеразы, експресуетсья в сосудах пениса, и вызывает их расширение и, соответственно, эрекцию. Поэтому силденафил (под названием Виагра) стал использоваться для лечения эректильной дисфункции.
Токсичность
Оксид NO раздражает дыхательные пути и глаза. Симптомы отравления зьявляють только через определенный период задержки в несколько часов. Ими являются: раздражение горла, затрудненное дыхание, головная боль, тошнота. Дальнейшие осложнения при отсутствии лечебных мероприятий могут вызывать полную потерю сил, непостоянство дыхания, цианоз, а также смерть в результате отека легких.
Пораженного NO необходимо убрать из опасной территории, провентилировать легкие кислородом. Дальнейшие 72 часа необходимо обеспечить надзор и исключить любую физическую деятельность, поскольку это может привести к развитию отека легких. При попадании вещества в ое или на кожу, необходимо тщательно промыть пораженное место теплой водой и обратиться к врачу.
Мерами безопасности при работе с оксидом азота (I) является наличие защитных резиновых (тефлоновых) перчаток, герметичных очков, респиратора.
