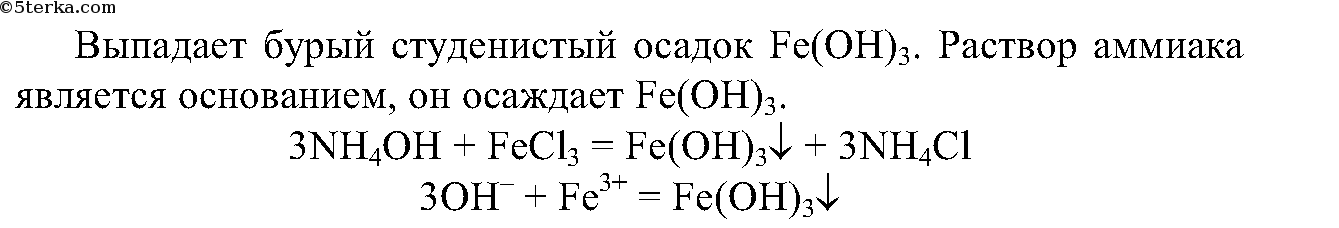О каких свойствах водного раствора аммиака свидетельствует его

Получение аммиака и растворение его в воде
1) В фарфоровой ступке хорошо перемешайте приблизительно равные объёмы кристаллического хлорида аммония NH4Cl и порошка гидроксида кальция Ca(OH)2 (опыт удаётся лучше, если известь слегка влажная). Приготовленную смесь насыпьте в пробирку на 1/3 её объёма. Закройте пробирку пробкой с газоотводной трубкой; конец которой опущен в другую сухую пробирку, закреплённую в штативе открытым концом вниз (рис. 22). Нагрейте смесь в пробирке.
2) Как только почувствуете острый запах (нюхать осторожно!), пробирку с газом, не переворачивая, закройте пробкой, погрузите её в сосуд с водой и откройте пробку.
3) После заполнения пробирки водой закройте её отверстие пробкой и выньте пробирку из воды. Половину полученного раствора перелейте в другую пробирку. В одну пробирку поместите красную лакмусовую бумагу. В другую пробирку добавьте несколько капель раствора фенолфталеина, а затем немного разбавленной соляной кислоты.
О каких свойствах водного раствора аммиака свидетельствует его действие на индикаторы? Как это можно объяснить с позиций теории электролитической диссоциации?
Что происходит при действии кислоты на водный раствор аммиака? Составьте уравнение соответствующей химической реакции
Горение аммиака в кислороде
Снова слегка нагрейте пробирку со смесью хлорида аммония и гидроксида кальция. Газоотводную трубку введите в стеклянный цилиндр с кислородом и при помощи лучинки подожгите газ (рис. 23).
Какие вещества образуются в процессе горения аммиака? Напишите уравнение соответствующей реакции. Подчеркните в уравнении одной чертой окислитель, а двумя — восстановитель.
Взаимодействие аммиака с кислотами
В приборе для получения газов замените пробирку с использованной смесью хлорида аммония и гидроксида кальция на пробирку со свежей порцией смеси. Пробирку слегка нагрейте. Газоотводную трубку последовательно введите в пробирки, в которых налито по 1 мл концентрированных азотной, соляной и серной кислот. Конец газоотводной трубки должен находиться на расстоянии 5-6 мм от поверхности кислоты.
Как объяснить появление белого дыма? Напишите уравнения соответствующих реакций.
Почему конец газоотводной трубки нельзя погружать в кислоту, а можно лишь приближать к ней.
Ответ
Получение аммиака и растворение его в воде
1)
2NH4Cl + Ca(OH)2 t ⟶ CaCl2 + 2H2O + 2NH3↑
2)
NH3 + H2O ⇄ NH4OH
3)
Лакмусовая бумага в растворе аммиака окрасилась в синий цвет, а фенолфталеин окрасил раствор в малиновый цвет, это говорит о том, что аммиак проявляет щелочные свойства, так как в результате диссоциации образовываются гидроксид-анионы (OH-):
NH4OH ⇄ NH4+ + OH-
При добавлении кислоты происходит обесцвечивание фенолфталеина, т. к. аммиак вступает в реакцию с кислотой:
NH3 + HCl ⟶ NH4Cl
Горение аммиака в кислороде
В процессе горения аммиака образуется азот и вода.
| 4NH3 + 3O2 ⟶ 2N2 + 6H2O | ||
| O20 + 4ē ⟶ 2O-2 | 3 | окислитель (восстановление) |
| 2N-3 — 6ē ⟶ N20 | 2 | восстановитель (окисление) |
Взаимодействие аммиака с кислотами
Аммиак реагирует с парами хлороводорода, при этом образуется густой белый дым – соль хлорид аммония:
NH3 + HCl ⟶ NH4Cl
Конец газоотводной трубки нельзя погружать в кислоту, так как хлорид аммония является растворимой солью.
Аммиак – NH3

Аммиак
(в европейских языках его название звучит как «аммониак») своим
названием обязан оазису Аммона в Северной Африке, расположенному на
перекрестке караванных путей. В жарком климате мочевина (NH2)2CO,
содержащаяся в продуктах жизнедеятельности животных, разлагается
особенно быстро. Одним из продуктов разложения и является аммиак. По
другим сведениям, аммиак получил своё название от древнеегипетского
слова амониан. Так называли людей, поклоняющихся богу Амону. Они во время своих ритуальных обрядов нюхали нашатырь NH4Cl, который при нагревании испаряет аммиак.
1. Строение молекулы


Молекула аммиака имеет форму тригональной пирамиды с
атомом азота в вершине. Три неспаренных
p-электрона атома азота участвуют в образовании полярных ковалентных
связей с 1s-электронами трёх атомов водорода (связи N−H), четвёртая пара
внешних электронов является неподелённой, она может образовать
донорно-акцепторную связь с ионом водорода, образуя ион аммония NH4+.
Вид химической связи: ковалентная полярная, три одинарные σ — сигма связи N-H
2. Физические свойства аммиака
При нормальных условиях
— бесцветный газ с резким характерным запахом (запах нашатырного спирта), почти
вдвое легче воздуха, ядовит. По
физиологическому действию на организм относится к группе веществ удушающего и
нейротропного действия, способных при ингаляционном поражении вызвать
токсический отёк лёгких и тяжёлое поражение нервной системы. Пары аммиака сильно раздражают
слизистые оболочки глаз и органов дыхания, а также кожные покровы. Это мы и
воспринимаем как резкий запах. Пары аммиака вызывают обильное слезотечение,
боль в глазах, химический ожог конъюктивы и роговицы, потерю зрения, приступы
кашля, покраснение и зуд кожи. Растворимость NH3 в воде чрезвычайно
велика — около 1200 объёмов (при 0 °C) или 700 объёмов (при 20 °C) в объёме
воды.
3. Получение аммиака
В лаборатории | В |
Для получения аммиака в лаборатории NH4Cl (NH4)2SO4 Внимание! Гидроксид аммония неустойчивое основание, При получении аммиака держите пробирку — приёмник дном кверху, так как аммиак легче воздуха: | Промышленный способ получения аммиака N2(г) + 3H2(г) ↔ 2NH3(г) Условия: катализатор температура давление Это так называемый процесс Габера (немецкий |
4. Химические свойства аммиака
Для аммиака характерны реакции:
- с
изменением степени окисления атома азота (реакции окисления) - без
изменения степени окисления атома азота (присоединение)
Реакции N-3 → N0 → N+2 NH3 – сильный |
с кислородом 1. Горение аммиака (при нагревании) 4NH3 + 3O2 → 2N2 + 6H20 2. Каталитическое окисление амииака (катализатор Pt – Rh, температура) 4NH3 + 5O2 → 4NO + 6H2O Видео — Эксперимент » Окисление аммиака в |
с оксидами металлов 2 NH3 |
с сильными окислителями 2NH3 + 3Cl2 = N2 + 6HCl |
аммиак – непрочное соединение, при 2NH3↔ N2 + 3H2 |
5. Применение аммиака
По объемам производства
аммиак занимает одно из первых мест; ежегодно во всем мире получают около 100
миллионов тонн этого соединения. Аммиак выпускается в жидком виде или в виде
водного раствора – аммиачной воды, которая обычно содержит 25% NH3.
Огромные количества аммиака далее используются для получения азотной кислоты, которая идет на производство удобрений и множества других продуктов. Аммиачную воду
применяют также непосредственно в виде удобрения, а иногда поля поливают из
цистерн непосредственно жидким аммиаком. Из аммиака получают различные соли аммония, мочевину, уротропин. Его применяют также в качестве дешевого
хладагента в промышленных холодильных установках.
Аммиак используется
также для получения синтетических
волокон, например, найлона и капрона. В легкой промышленности он используется при очистке и крашении хлопка,
шерсти и шелка. В нефтехимической промышленности аммиак используют для
нейтрализации кислотных отходов, а в производстве природного каучука аммиак
помогает сохранить латекс в процессе его перевозки от плантации до завода.
Аммиак используется также при производстве соды по методу Сольве. В
сталелитейной промышленности аммиак используют для азотирования – насыщения
поверхностных слоев стали азотом, что значительно увеличивает ее твердость.
Медики
используют водные растворы аммиака (нашатырный спирт)
в повседневной практике: ватка, смоченная в нашатырном спирте, выводит человека
из обморочного состояния. Для человека аммиак в такой дозе не опасен.
ТРЕНАЖЁРЫ
Тренажёр №1 «Горение аммиака»
Тренажёр №2 «Химические свойства аммиака»
ЗАДАНИЯ ДЛЯ ЗАКРЕПЛЕНИЯ
№1. Осуществить превращения по схеме:
а) Азот→ Аммиак → Оксид азота (II)
б) Нитрат аммония → Аммиак → Азот
в) Аммиак → Хлорид аммония → Аммиак → Сульфат аммония
Для ОВР составить е-баланс, для РИО полные, ионные уравнения.
№2. Напишите четыре уравнения химических реакций, в результате которых образуется аммиак.
I Постановка целей и задач урока.
На уроке мы должны получить аммиак реакцией ионного обмена и изучить свойства этого газа и его водного раствора – гидроксида аммония.
II. Повторение правил техника безопасности
1.Экономное расходование веществ.
2.При выяснении запаха веществ не подносите сосуд близко к лицу, иначе вдыхание паров и газов может вызвать раздражение дыхательных путей.
3.Проводите опыты только над столом, нагревая пробирку с жидкостью, держите её так, чтобы открытый конец её был направлен в сторону и от самого себя и от соседей.
4.Не приступайте к выполнению опыта, не зная, что и как нужно делать.
III. Практическая работа
1. Получение аммиака.
На лист бумаги или в небольшую фарфоровую чашку (можно ступку) насыпьте хлорид аммония и гидроксид кальция объемом по одной ложечке (ложечка для сжигания веществ).
Смесь перемешайте стеклянной палочкой и высыпьте в сухую пробирку. Закройте ее пробкой с газоотводной трубкой и укрепите в лапке штатива.
При укреплении прибора в лапке штатива обратите внимание на наклон пробирки относительно ее отверстия. На газоотводную трубку наденьте сухую пробирку для собирания аммиака.
Пробирку со смесью хлорида аммония и гидроксида кальция прогрейте сначала всю (2—3 движения пламени), а затем нагрейте в том месте, где находится смесь.
Почему пробирка вверх дном? ( NH3 легче воздуха в 2 раз).
Как вы узнаете, что получили NH3?
1)по запаху (резкий запах);
2)поднесите к отверстию перевёрнутой вверх дном пробирки влажную фенолфталеиновую бумажку(она стала малиновой).
1). 2NH4CI + Ca (OH )2 = CaCI2 + 2NH3↑ + 2H2O
2)Не переворачивая пробирку, быстро опустите её в чашку с водой отверствием вниз, подержите так, капните фенолфталеин. Что произошло? Какое вещество мы получили?
Аммиак очень хорошо растворим в воде!
NH3 + H2O = NH4OH
аммиачная вода,
нашатырный спирт,
среда щелочная,
3)Получение „дыма без огня”
NH3 + HCI = NH3 + HNO3 =
В результате этих реакций мы получили какие вещества? (соли аммония).
Вывод:
получили аммиак, обнаружили по резкому запаху, имеет основной
характер, хорошо растворим в воде, образуя основание, аммиачную
воду, взаимодействует с кислотами, образуя соли.
Изучение свойств водного раствора аммиака.
1. NH4OH + 2,3 капли фенолфталеина → малиновая окраска
Почему?
t
NH4OH → NH3 ↑+H2O
2.NH4OH + 2,3 капли фенолфталеина → малиновая окраска, + HCI
Как изменился цвет? Почему?
NH4OH +HCI = NH4CI + H2O
NH4 + + OH- + H+ + CI- = NH4 + + CI- + Н2О
Н+ + ОН- = Н2О реакция нейтрализации
3.АICI3 + 3NH4OH = 3NH4CI + AI (OH)3↓
AI3+ + 3CI- + 3NH4+ + 3OH- = 3NH4+ + 3CI- + AI (OH)3↓
AI3+ + 3OH- = AI (OH)3↓
Вывод:
при изучении свойств водного раствора NH3 выяснили, что это
основание, разлагается при нагревании, взаимодействует
с кислотами и солями.
IV Подведение итога урока.
Вывод по уроку:чему научились?
Получили аммиак, изучили его свойства, а также свойства нашатырного спирта.
Дата добавления: 2017-03-12; просмотров: 1351 | Нарушение авторских прав | Изречения для студентов
Читайте также:
Рекомендуемый контект:
Поиск на сайте:
© 2015-2020 lektsii.org — Контакты — Последнее добавление
Анонимный вопрос · 15 марта 2019
12,0 K
Имею естественно научное образование, в юношестве прикипел к литературе, сейчас…
Физические свойства NH3:
- Бесцветный газ
- Резких спиртовой запах
- Растворим в воде
- Легче воздуха
- Плотность концентрированного раствора аммиака 0,91 г/см3
Химические свойства NH3:
- Активен
- Вступает в реакции взаимодействия с разными веществами
- Проявляет восстановительные свойства
- Степень окисления азота в аммиаке «-3»
- В присутствии катализатора окисляется до азота 3
- При нагревании аммиака с галогенами, оксидами тяжелых металлов и кислородом получает азот
- Не имеет кислотных свойств
- Имеет неподеленную пару электронов
- При взаимодействии с кислотами образует соли аммония
А учебник Химия 9 класс уже не катит? У аммиака оснОвные свойства… Уравнения характерных реакций запоминают и… Читать дальше
Нитрид водорода с формулой NH3 называется аммиаком. Это лёгкий (легче воздуха) газ с резким запахом. Строение молекулы определяет физические и химические свойства аммиака. Если один атом водорода заменить углеводородным радикалом (CnHm), получится новое органическое вещество – амин. Замещаться может не только один атом водорода, но и все три. В зависимости от количества… Читать далее
Чем по агрегатному состоянию является огонь?
Специалист в области атомных электрических станций, инженер-контролер на ХАЭС
Огонь — процесс окисления, сопровождающийся излучением в видимом диапазоне. В узком смысле (как говорит википедия) — совокупность раскалённых газов и плазмы, выделяющихся в результате нагревания некоторого материала до определенной температуры при наличии окислителя, или же химической реакции (взрыва, например), или электрическая дуга (электрический разряд в газе).
Если с газами ещё более менее понятно (горит газ, окисляется газом + необходимая температура), то плазма — это частично или полностью ионизированный газ, образованный из нейтральных атомов (или молекул) и заряженных частиц (ионов и электронов). А ионизированный значит, что от некоторой части атомов отделён по крайней мере один электрон.
Так же плазма это: молния, ионосфера, северное сияние — природные источники, а ещё же искусственных сколько…
Т.е. агрегатных состояний два.
Как правильно поливать лук нашатырем?
Видеоблогер, канал https://www.youtube.com/channel/UCsiexG1QLrw30VV2OS_Y9qg · ogorod42.ru
Если вы заметили желтое перо, то, возможно, это — нехватка азота, нужно подкормить мочевиной (карбамидом). Но, если на пере прочерки, разрываете его, а там крохотный червячок. Это — скрытнохоботник. Он повреждает не только перо, но и луковицу, и лук легко заболевает грибковыми заболеваниями и плохо хранится. Нужно поврежденные листья оборвать, сжечь, а лук подкормить мочевиной, чтобы ускорить развитие нового пера. Можно взять на лейку неполный стакан аммиачной воды (нашатырного спирта) и поливаем по листьям, по всем поверхностям. Это и подкормка: азотные удобрения. И безвредно для людей и самих растений.
Прочитать ещё 1 ответ
Как определить тип химической связи?
А. · 400
Люблю простые слова для вещей, toki pona.
Алгоритм такой: смотрим на атомы вещества, если они одинаковы, далее два варианта, если элемент, образующий вещество — металл (Na, Al), связь металлическая, если — неметалл, ковалентная неполярная (O2, J2).
Если атомы вещества различны, то выбор будет между ионной связью (когда электроотрицательность элементов очень далека друг от друга (>= 1,7), например, металл и неметалл, NaCl) и ковалентной полярной (когда электроотрицательность элементов близка (HCl).
Кроме того атомы водорода одой молекулы могут образовывать связь с неподелённой парой электронов другой молекулы, если эта пара принадлежит весьма электроотрицательному элементу (H-F, H20). Кстати, именно из-за этой связи, вода плотнее льда и зимой насквозь реки не промерзают.
Прочитать ещё 1 ответ
Как отличить этиловый спирт от метилового в домашних условиях?
Главный редактор издания «Популярный университет», химик по образованию, продвигаю массы… · popuni.ru
Можно воспользоваться очень надежным старым методом всех химиков: нагреть жидкость и посмотреть, при какой температуре она будет кипеть. Для метилового спирта это почти 65 градусов, для этилового — 78. Разница достаточная, чтобы ее заметить. Другое дело, что без хорошей химической посуды и вытяжки этого лучше не делать, так как даже пары метанола токсичны (в 200 раз токсичнее паров этанола).
Есть еще один, более химический способ (хотя если у вас завалялся медный купорос на кухне, вы тоже можете его использовать). Надо добавить немного медного купороса CuSO4 к каждому из веществ. Тот, в котором кристаллы растворятся и дадут синий раствор – метанол.
Прочитать ещё 3 ответа
Задания. 1. Получите аммиак по реакции гидроксида кальция с хлоридом аммония.
2. Изучите некоторые физические свойства аммиака (цвет, запах, относительную плотность, растворимость в воде).
3. Изучите взаимодействие аммиака с водой, азотной и соляной кислотами.
4. Проделайте реакции:а) между раствором аммиака в воде и серной кислотой;б) между гидроксидом аммония и раствором хлорида железа (III).
Соблюдайте правила техники безопасности при проведении опытов!
Оборудование. Детали прибора для получения аммиака, лабораторный штатив, штатив с пробирками, фарфоровая ступка с пестиком, ложечка или шпатель, стеклянные палочки (2 шт.), пробка с держателем, нагревательный прибор.
Вещества. Кристаллические гидроксид кальция и хлорид аммония; концентрированная соляная, концентрированная азотная и 20% -я серная кислоты; вода (в стакане), раствор фенолфталеина, раствор хлорида железа (III).
Выполнение работы
Получение аммиака. Соберите прибор для получения аммиака (рис. 22.1), испытайте на герметичность. За
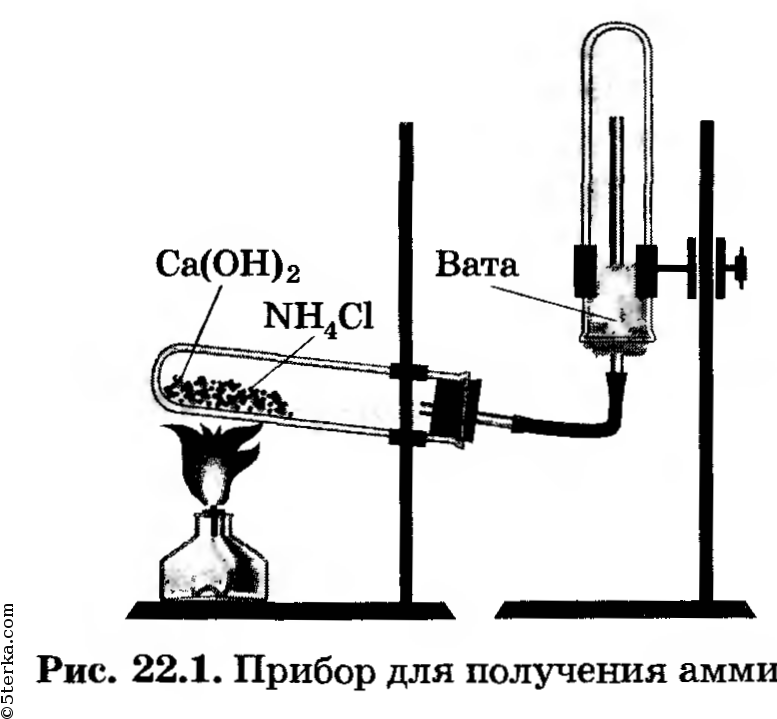
крепите его в штативе так, чтобы удобно было нагревать пробирку. Решите, какое положение пробирки (рис. 22.2, а, б, в или г) является правильным.
Приготовьте три сухих (почему?) пробирки, которые предстоит наполнить аммиаком. Закройте их пробками.
В ступку насыпьте по одной ложечке хлорида аммония и гидроксида кальция, перемешайте их, разотрите пестиком. Затем перенесите порцию смеси в пробирку прибора, заполнив ее не более чем на 1/3.
Начните нагревать содержимое пробирки, при этом сначала обогрейте пламенем горелки всю пробирку, затем пламя направьте так, чтобы нагревалась поверхность смеси.
Наполните три пробирки аммиаком, заткните их пробками с держателями; прекратите нагревание и, не разбирая прибора, перенесите его в вытяжной шкаф.
Изучение свойств аммиака.
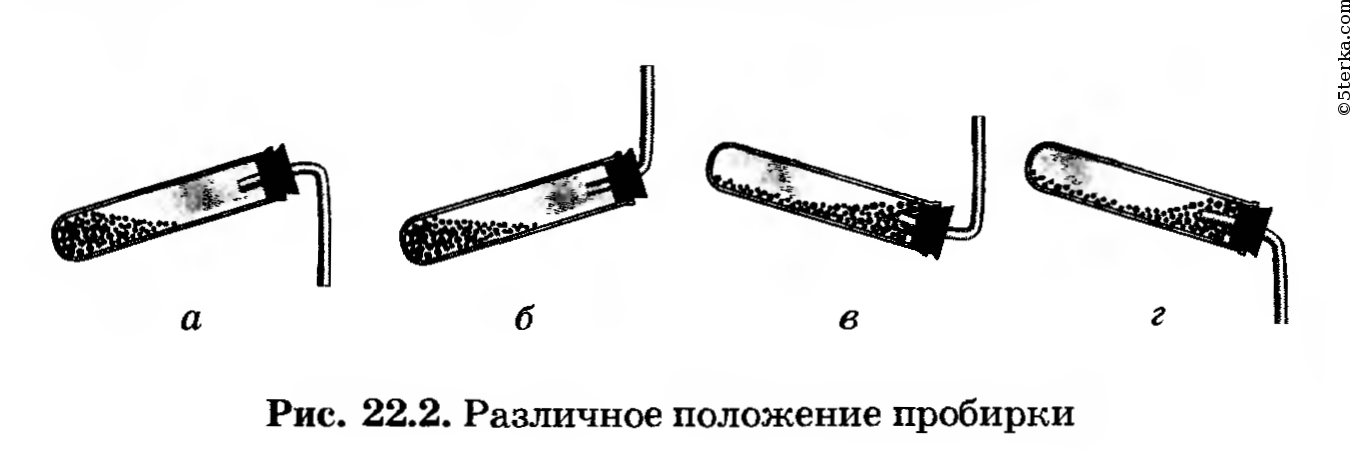
1. Исследуйте растворимость, взаимодействие аммиака с водой. Для этого опустите пробирку с аммиаком в стакан с водой и под водой откройте ее, как это показано на рисунке 22.3.
Что вы наблюдаете?
Не вынимая пробирку, закройте ее также под водой пробкой с держателем, после чего поставьте в штатив. К полученному раствору добавьте 2—3 капли раствора фенолфталеина.
Составьте уравнение реакции взаимодействия аммиака с водой.
2. Смочите стеклянную палочку концентрированной соляной кислотой, другую — концентрированной азотной кислотой. Внесите их поочередно в пробирки с аммиаком. Что вы наблюдаете?
Составьте уравнения происходящих реакций.
Почему опыт не получится при использовании серной и фосфорной кислот?
3. Разлейте полученный водный раствор аммиака в воде в две пробирки. В одну пробирку добавьте несколько капель раствора фенолфталеина и осторожно прилейте серную кислоту до исчезновения окраски индикатора. Что вы наблюдаете?
Составьте уравнения реакций образования сульфата и гидросульфата аммония.
4. В другую пробирку с раствором аммиака добавьте раствор хлорида железа (III). Что вы наблюдаете?
Запишите ионные уравнения реакций.
Получение аммиака:
Правильное положение пробирки под б). Во-первых, NH3 легче, чем воздух, он будет подниматься вверх, поэтому газоотводная трубка должна также быть направлена вверх. Во-вторых, мы будем нагревать вещество в пробирке, поэтому оно не должно соприкасаться с пробиркой, которая от огня может расплавиться.
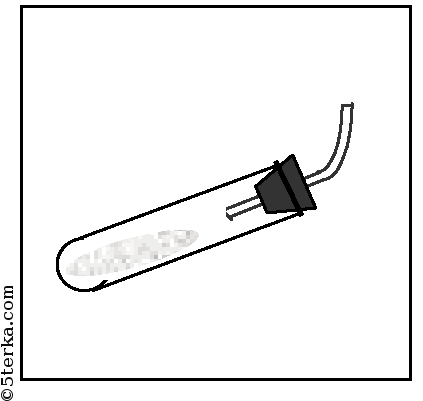
Пробирки должны быть сухими, т.к. аммиак реагирует с водой и в результате образуется гидроксид аммония.
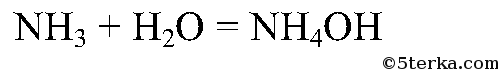
Реакция получения аммиака:
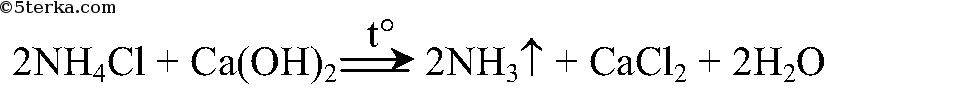
Изучение свойств аммиака:
1.
Аммиак хорошо растворяется в воде:
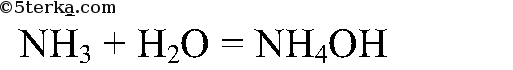

2.
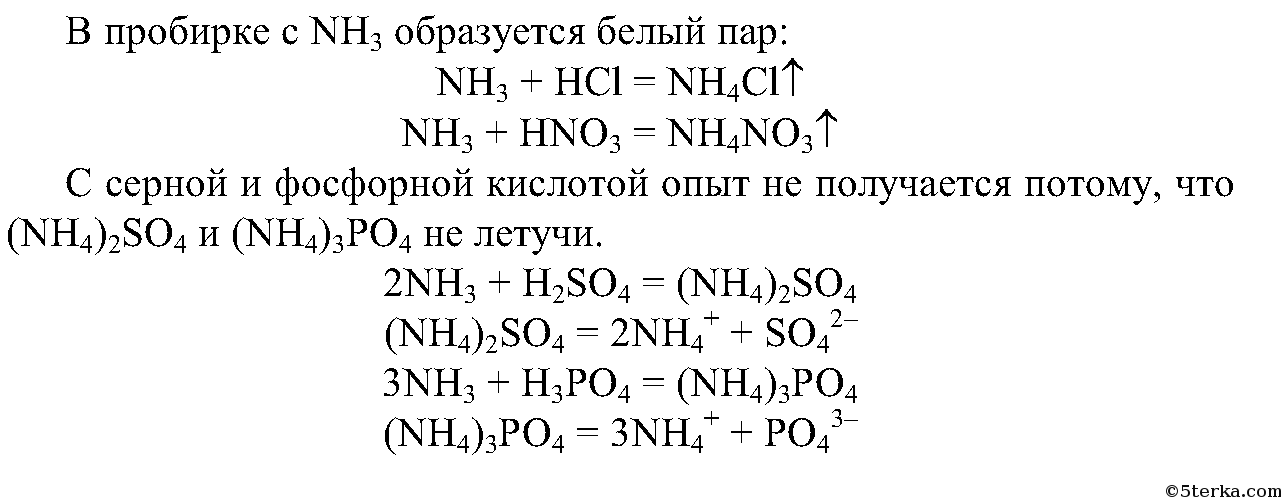
3.
Раствор обесцвечивается, поскольку серная кислота нейтрализует аммиак, т.е. среда становится нейтральной. В нейтральной и кислой среде фенолфталеин бесцветный.
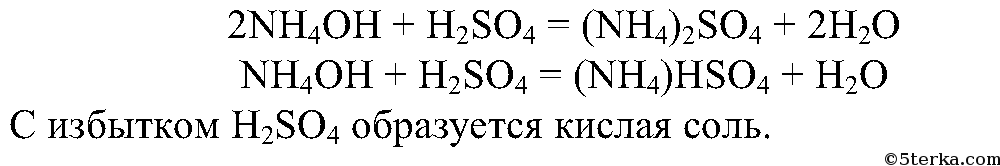
4.