На каких свойствах основано применение водорода

Современную промышленность сложно представить без применения технических газов на различных этапах производства. На сегодняшний день водород входит в тройку наиболее востребованных промышленностью газов, уступая лишь кислороду и азоту.
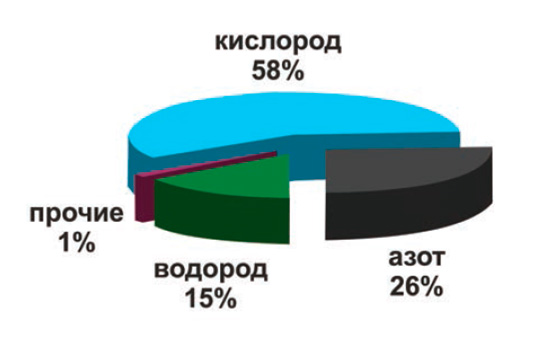 |
| Структура производства промышленных газов в России, % |
Водород относится к числу важнейших видов сырья химической и нефтехимической промышленности. Свойства этого газа обуславливают его применение и в других отраслях промышленности: металлургической, пищевой, стекольной, электронной, электротехнической.
Структура потребления водорода в России в 2013 г.
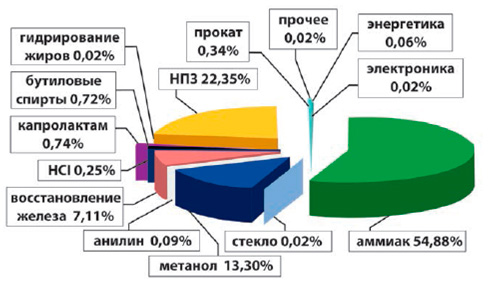
| Аммиак | 54,88% |
| Нефтеперерабатывающие заводы | 22,35% |
| Метанол | 13,30% |
| Восстановление железа | 7,11% |
| Капролактам | 0,74% |
| Бутиловые спирты | 0,72% |
| Прокат | 0,34% |
| HCl | 0,25% |
| Анилин | 0,09% |
| Энергетика | 0,06% |
| Гидрогенизация жиров | 0,02% |
| Электроника | 0,02% |
| Стекло и керамика | 0,02% |
| Прочее | 0,02% |
Перейти в раздел «Водородные компрессоры»
Химическая промышленность
В России основная область потребления водорода – производство химических продуктов, прежде всего аммиака и метанола.
Лидерами по потреблению водорода являются предприятия, производящие аммиак NH
3
. Сейчас на 28 предприятиях в России используется 2,46 млн.т. водорода в год.
Потребление водорода при синтезе метанола CH
3
OH составило 0,6 млн.т. в 2013 г.
Потребление водорода в остальных сегментах химической промышленности не превышает 90 тыс.т. – 3% от объема потребления.
Нефтеперерабатывающая промышленность
Повышается потребность НПЗ в водороде, необходимом для получения топлив из тяжелого высокосернистого сырья. Огромное количество водорода требуется для установок гидрообессеривания, гидрокрекинга дистиллятов, гидроочистки, изомеризации, производств смазочных материалов. Кроме того, водород на НПЗ используется для активации катализаторов риформинга и регенерации катализаторов изомеризации.
Металлургия
Основной областью применения водорода в металлургии является производство металлизированного сырья методом прямого восстановления железа. Сейчас в этом процессе потребляется около 320 тыс.т. водорода.
Значительные объемы водорода расходуются в технологических процессах прокатного производства (при термической обработке холоднокатаного проката). Потребление водорода – около 15 тыс.т. в год.
Водород на металлургических предприятиях используется также для создания защитной азотно-водородной атмосферы при термообработке труб.
Стекольная промышленность
В стекольной промышленности водород применяется при производстве листового стекла float-методом, а также для получения кварцевого стекла, которое изготавливают плавлением чистого горного хрусталя, кварца или синтетического оксида кремния в водородно-кислородном пламени.
Энергетика
В энергетике водород используется для охлаждения мощных турбогенераторов, благодаря его высокой теплопроводности и коэффициенту диффузии, а также нетоксичности. По оценкам, в энергетике на ТЭЦ, АЭС потребляется около 4-5 тыс.т. водорода в год.
Пищевая промышленность
В пищевой промышленности водород используется в процессах гидрогенизации масел и жиров при получении твердых жиров (маргарина). Объем потребления водорода масложировыми комбинатами оценивается на уровне 1,5 тыс.т. в год.
Среди прочих потребителей водорода – обогатительные комбинаты, заводы, занимающиеся фабрикацией ядерного топлива, предприятия электронной и электротехнической промышленности, транспортные и газовые компании, фармацевтика.
Машина без выхлопных газов. Это Mirai производства Toyota. Автомобиль работает на водородном топливе.

Из выхлопных труб выходят лишь нагретый воздух и водяной пар. Машина будущего уже ездит по дорогам, хоть и испытывает проблемы с дозаправкой.
Хотя, учитывая распространенность водорода во Вселенной, такой загвоздки не должно быть.
Мир состоит из 1-го вещества таблицы Менделеева на три четверти. Так что, свой порядковый номер элемент водород оправдывает. Сегодня, все внимание ему.
Свойства водорода
Будучи первым элементом, водород порождает первое вещество. Это вода. Ее формула, как известно, H2O.
На греческом название водорода пишется, как hidrogenium, где hidro – вода, а genium – порождать.
Однако, имя элементу дали не греки, а французский естествоиспытатель Лоран Лавуазье. До него, водород исследовали Генри Кевендишь, Никола Лемери и Теофраст Парацельс.
Последний, собственно, оставил науке первое упоминание о 1-ом веществе. Запись датирована 16-ым веком. К каким же выводам пришли ученые по поводу водорода?
Характеристика элемента – двойственность. У атома водорода всего 1 электрон. В ряде реакций вещество отдает его.
Это поведение типичного металла из первой группы. Однако, водород способен и достраивать свою оболочку, не отдавая, а принимая 1 электрон.
В этом случае, 1-ый элемент ведет себя, как галогены. Они располагаются в 17-ой группе периодической системы и склонны к образованию солей.
В каких из них можно найти водород? К примеру, в гидросульфиде натрия. Его формула: — NaHS.
Это соединение элемента водорода основано на серной кислоте. Как видно, атомы водорода вытеснены из нее натрием лишь частично.
Наличие всего одного электрона и способность его отдать превращает атом водорода в протон. В ядре тоже всего одна частица с положительным зарядом.
Относительная масса протона с электроном равна 2-ум. Показатель в 14 раз меньше, чем у воздуха. Без электрона вещество и того легче.
Вывод, что водород – газ, напрашивается сам собой. Но, у элемента есть и жидкая форма. Сжижжение происходит при температуре -252,8 градусов Цельсия.
За счет своих малых размеров химический элемент водород обладает способностью просачиваться сквозь другие вещества.

Так, если надуть воздушный шар не гелием, или обычным воздухом, а чистым элементом №1, игрушка сдуется уже через пару дней.
Частицы газа без труда пройдут в поры резины. Проходит водород и в некоторые металлы, к примеру, платину и палладий.
Накапливаясь в их структуре, вещество испаряется при повышении температуры.
Хоть водород входит в состав воды, растворяется он плохо. Не зря в лабораториях элемент выделяют путем вытеснения влаги. А как добывают 1-е вещество промышленники? Этому посвятим следующую главу.
Добыча водорода
Формула водорода позволяет добывать его минимум 6-ю способами. Первый – паровая конверсия метана и природного газа.
Берутся легроиновые фракции нефти. Чистый водород из них извлекается каталитическим путем. Для этого необходимо присутствие паров воды.
Второй путь добычи 1-го вещества – газификация угля. Твердое топливо нагревают до 1500 градусов, преобразуя в горючие газы.
Для этого требуется окислитель. Достаточно обычного атмосферного кислорода.
Третий путь получения водорода – электролиз воды. Через нее пропускают ток. Он помогает выделить на электродах нужный элемент.
Воспользоваться можно и пиролизом. Это термическое разложение соединений. Распасться заставляют, как органику, так и неорганические вещества, к примеру, ту же воду. Процесс происходит под действием высоких температур.
Пятый путь получения водорода – частичное окисление, а шестой – биотехнологии.
Под последними, понимается добыча газа из воды путем ее биохимического расщепления. Помогают специальные водоросли.
Нужен замкнутый фотобиореактор, поэтому, 6-ым способом пользуются редко. Популярен, собственно, лишь метод паровой конверсии.
Он наиболее дешев и прост. Однако, наличие массы альтернатив делает водород желанным сырьем для промышленности, ведь нет зависимости от конкретного источника элемента.
Применение водорода
Водород используют для синтеза аммиака. Это соединение является хладагентом в морозильной технике, известно, как составляющая нашатырного спирта, применяется в качестве нейтрализатора кислот.
Водород пускают, так же, на синтез хлороводородной кислоты. Это второе название соляной.
Она нужна, к примеру, для очистки поверхностей металлов, их полировки. В пищевой промышленности хлороводородная кислота – регулятор кислотности Е507.
В качестве пищевой добавки зарегистрирован и сам водород. Его название на упаковках продуктов – Е949.

Применяется, в частности, на производстве маргарина. Система гидрогенезации, собственно, делает маргарин твердым.
В жирных кислотах из растительных масел разрывается часть связей. На местах разрыва встают атомы водорода. Это и преобразует текучую субстанцию в относительно твердую.
В роли топливного элемент водород применяется, пока, не столько в автомобилях, сколько ракетах.
Первое вещество сгорает в кислороде, что и дает энергию для движения космических аппаратах.
Так, одна из самых мощных российских ракет «Энергия» работает именно на водородном топливе. Первый элемент в нем сжижен.
Реакция горения водорода в кислороде пригождается и при сварочных работах. Можно скреплять самые тугоплавкие материалы.
Температура реакции в чистом виде – 3000 градусов Цельсия. С использованием специальных горелок удается достичь 4000 градусов.
«Сдастся» любой сплав, любой металл. Кстати, металлы с помощью 1-го элемента тоже получают. Реакция основана на выделении ценных веществ из их оксидов.
В ядерной промышленности жалуют изотопы водорода. Их всего 3. Один из них – тритий. Он радиоактивен.
Есть еще нерадиоактивные протий и дейтерий. Хоть тритий и излучает опасность, но встречается в естественной среде.

Изотоп образуется в верхних слоях атмосферы, на которые действуют космические лучи. Это приводит к ядерным реакциям.
В реакторах же на поверхности земли тритий – итог нейтронного облучения лития.
Цена водорода
Чаще всего, промышленники предлагают газообразный водород, естественно, в сжатом состоянии и в специальной таре, которая не пропустит мелкие атомы вещества.
Первый элемент делят на технический и очищенный, то есть, высший сорт. Есть даже марки водорода, к примеру, «А».
Для нее действует ГОСТ 3022-80. Это технический газ. За 40 кубических литров производители просят чуть меньше 1000 рублей. За 50 литров дают 1300.
ГОСТ для чистого водорода – Р 51673-2000. Чистота газа составляет 9,9999%. Технический элемент, правда, немногим уступает.
Его чистота – 9,99%. Однако, за 40 кубических литров чистого вещества дают уже больше 13000 рублей.
По ценнику видно, как непросто дается промышленникам финальная стадия очистки газа. За 50-литровый баллон придется отдать 15000-16000 рублей.
Жидкий водород почти не используется. Слишком затратно, потери велики. Поэтому, и предложений о продаже, или покупке не найти.
Сжиженный водород не только трудно получить, но и хранить. Температура в минус 252 градуса – не шутки.
Поэтому, шутить никто и не собирается, пользуясь эффективным и простым в обращении газом.
Анонимный вопрос · 16 декабря 2018
11,8 K
Получил математическое и богословское образование. Есть дети, соответсвенно и…
Водород широко применяется в нефтепереработке — с его помощью из различных нефтепродуктов удаляются соединения серы. Большой объём этого газа используется для получения аммиака (необходимого, например, для производства удобрений). Также реакция водорода с хлором даёт хлороводород, водный раствор которого известен нам как соляная кислота. С помощью водорода также осуществляется восстановление металлов из их оксидов. Этот газ — важная составляющая при производстве метилового спирта.
Водород используется и в пишевой промышленности — для производства маргарина из растительных масел.
Температура сгорания водорода в кислороде — около 3000 градусов, а в специальных горелках её можно довести и до 4000. Поэтому водород используется для сварки тугоплавких металлов. Также жидкий водород — ракетное топливо.
При сгорании водород образует безопасный водяной пар, поэтому в перспективе он может стать экологичным топливом для автомобилей. Правда в настоящий момент его использование невозможно из-за многих технических ограничений.
Применяется он очень широко, все и не описать. Большая часть (около 54%) уходит на проихводство аммиака и метанола, которые нужны для поизводства пластмасс, удобрений и взрывчатки. Еще 35% тратят при переработки нефти. Остальное приходится на: пищевую, косметическую, авиационную промышленность, производство электроники, охлаждение мощных электрогенераторов и т.д… Читать далее
Да знаю
Реально водородсодержащих газ можно получить в специализированной установке, автор которого изобретатель Г.Г.Аракелян. Он успешно эксплуатирует у себя на производстве сушки ЖБК эти установки. Смотрите в Ютубе
Широкого применения в РФ его изобретение не применяется по известной причине.
.
Могут ли существовать неизвестные элементы, более тугоплавкие, чем вольфрам и углерод?
Все элементы, имеющие хоть какое-то практическое значение, давно открыты, их физические свойства хорошо изучены. Надежды синтезировать новый трансурановый элемент, тугоплавкостью превосходящий вольфрам тщетны. У известных трансуранов наблюдается тенденция падения температур плавления с увеличением атомного номера. Да и как, вообще, можно говорить о температуре плавления вещества, когда учёные могут располагать, буквально, несколькими атомами сверхтяжёлых элементов.
Соединения элементов могут быть более тугоплавкими, чем сами элементы. Такими, на пример, являются карбид тантала (C+Ta) и карбид тантала-гафния (C+Ta+Hf), с температурами плавления около 3900 и 4000 градусов, а карбонитрид тантала (C+N+Ta) превосходит по тугоплавкости даже эти соединения, его температура плавления (расчётная) достигает 4200 градусов.
Прочитать ещё 2 ответа
Правда ли, что водородные топливные ячейки — это тупиковая ветвь технологии, потому что у баллона с водородом слишком низкая удельная энергетическая ёмкость?
Researcher, Institute of Physics, University of Tartu
Правда то, что хранение водорода в баллонах — это тупиковая ветвь для водородных топливных ячеек 🙂 И даже не в связи с емкостью в расчете на вес баллона, а в связи с огромными проблемами с безопасностью. Если баллон, значит, забудьте о машинах, забудьте о жилых помещениях и бытовой технике и т.д.
В связи с этим, сейчас разрабатываются кучи технологий по а) способам получения водорода «на месте» из каких-то менее опасных реагентов, б) различным альтернативным способам хранения водорода. Ветвь исследований а) как самостоятельная сейчас несколько утратила популярность в связи с высокими энергозатратами на выделение водорода. В некоторой степени она слилась с ветокой б), поскольку точную грань между прочным физическим связыванием и химическим связыванием провести трудно. Таким образом, основная задача выглядит так: как найти способ хранения водорода а) безопасный, б) рециклируемый (чтобы можно было заряжать много раз), в) достаточно емкий, г) с низкими энергозатратами на извлечение водорода и во многих случаях — д) быстрой загрузкой водорода после разрядки.
Направления исследования — гидриды (металлов и неметаллов, например, бора), пористые матрицы типа цеолитов или аэрогелей, клатраты на основе льда или льдообразных материалов (достаточно экзотическая штука, но потенциально дают возможность 100% извлечения при комнатной температуре), полимерные матрицы и многое другое. Хорошего во всех отношениях решения на данный момент, насколько я знаю, нет, хотя есть уже даже промышленные технологии хранения на основе гидридов металлов и на основе пористых материалов. Там основная проблема, насколько я понимаю, высокая энергия извлечения и рециклируемость (в первый раз извлекаете 85%, второй 85% от 85% и т.д.).
Прочитать ещё 1 ответ
Есть ли будущее у автомобилей, работающих на водороде?
Стажер исследователь ОИВТ РАН, лаборатория водородной и возобновляемой энергетики… · t.me/century_arch
Машины, работающие на водороде, называют Fuel Cell Electric Vehicles или FCEV, на автомобильном рынке уже представлено несколько подобных решений. Конкретные коммерческие модели: Toyota Mirai и Honda FCX Clarity. Такая машина имеет так называемый топливный элемент (электрохимический генератор), являющийся своеобразной “батарейкой”, в которую поступает водород, после чего он окисляется и в результате на выходе мы имеем чистый водяной пар с нулевым содержанием углекислого газа. В остальном здесь все практически так же, как в обычном электромобиле, но в случае с водородной установкой используется куда более компактная батарея – емкость литий-ионного аккумулятора в водородных автомобилях в 10 раз меньше, поскольку он используется только для холодного старта и буферизации энергии, полученной при рекуперативном торможении.
По оценкам Hydrogen council (совет по водородным технологиям), к 2050 году мировой рынок водорода будет составлять порядка 18% от общего спроса на электроэнергию. При этом в транспортном секторе количество легковых автомобилей на водородном топливе составит 400 млн, 15-20 млн грузовых и 5 млн автобусов.
Китай планирует к 2030 году установить 1000 водородных заправочных станций, обслуживающих более 1 млн FCEV.
Так же активно инвестируют в водородную инфраструктуру Южная Корея, ведь всю страну можно пересечь на одном баке водорода.
В следующем году в Токио будет проходить олимпиада, японское правительство пообещало, что вся инфраструктура будет обслуживаться исключительно водородным топливом, уже переданы первые два автобуса на с топливным элементом на борту.
Несмотря на дешевизну ископаемого топлива, многие страны обделены природными ископаемыми, это вынуждает их отказаться от экспортного ископаемого топливо во благо энергетической безопасности страны, тот же водород можно получать дорогим способом электролиза воды — разложением воды на водород и кислород
Так же в мире появляется все больше компаний, которые внедряют водородные технологии в промышленность, и даже в некоторых случаях (Твердооксидные топливные элементы) создаются целые электрические станции, работающие на водородном топливе.
Прочитать ещё 1 ответ
Как на организм человека влияет водород?
Молекулярный водород (Н2) — это самый маленький элемент и самая легкая молекула во Вселенной. Его главная работа в плане влияния на человеческий организм заключается в следующем:
- Молекулярный водород почти мгновенно превращает токсичные гидроксил-радикалы, находящиеся в организме, в воду. Он легко проникает в клетки и нейтрализует цитотоксические кислородные радикалы, защищая тем самым ДНК, РНК и белки от оксидативного стресса.
- Молекулярный водород поддерживает гомеостатический уровень собственных антиоксидантов в организме человека, вызывает активацию или регулирование дополнительных антиоксидантных энизимов (например, глутатиона, супероксиддисмутазы, каталазы и др.) и /или белков тела, защищающих клетки.
- Молекулярный водород выступает сигнальной молекулой, которая влияет на межклеточную коммуникацию, метаболизм клеток и экспрессию генов. Он обладает противовоспалительным, антиаллергическим и анти-апоптотическим действиями.
- Молекулярный водород, благодаря мельчайшим водным кластерам, изменяя электрический заряд в воде, заставляет молекулы воды образовывать небольшие группы, что позволяет легче осуществлять увлажнение организма и транспортировку витаминов и минералов.
Больше химических фактов вы можете найти в нашем справочнике по химии.
Прочитать ещё 3 ответа
