Какой продукт реакции нитрования бензола

Физические свойства
Бензол и его ближайшие гомологи – бесцветные жидкости
со специфическим запахом. Ароматические углеводороды легче воды и в ней не
растворяются, однако легко растворяются в органических растворителях – спирте,
эфире, ацетоне.
Бензол и его гомологи сами являются хорошими
растворителями для многих органических веществ. Все арены горят коптящим
пламенем ввиду высокого содержания углерода вих молекулах.
Физические свойства некоторых аренов представлены
в таблице.
Таблица.
Физические свойства некоторых аренов
Название | Формула | t°.пл., | t°.кип., |
Бензол | C6H6 | +5,5 | 80,1 |
Толуол | С6Н5СH3 | -95,0 | 110,6 |
Этилбензол | С6Н5С2H5 | -95,0 | 136,2 |
Ксилол | С6Н4(СH3)2 | ||
орто- | -25,18 | 144,41 | |
мета- | -47,87 | 139,10 | |
пара- | 13,26 | 138,35 | |
Пропилбензол | С6Н5(CH2)2CH3 | -99,0 | 159,20 |
Кумол | C6H5CH(CH3)2 | -96,0 | 152,39 |
Стирол | С6Н5CH=СН2 | -30,6 | 145,2 |
Бензол – легкокипящая (tкип = 80,1°С), бесцветная жидкость, не растворяется в воде
Внимание! Бензол – яд, действует на почки, изменяет формулу крови (при
длительном воздействии), может нарушать структуру хромосом.
Большинство ароматических углеводородов опасны для
жизни, токсичны.
Получение
аренов (бензола и его гомологов)
В лаборатории
1. Сплавление солей
бензойной кислоты с твёрдыми щелочами
C6H5-COONa
+ NaOH t → C6H6 + Na2CO3
бензоат натрия
2. Реакция Вюрца-Фиттинга:
(здесь
Г – галоген)
С6H5-Г
+ 2Na + R-Г → C6H5—R + 2NaГ
С6H5-Cl
+ 2Na + CH3-Cl → C6H5-CH3 + 2NaCl
В промышленности
- выделяют
из нефти и угля методом фракционной перегонки, риформингом; - из
каменноугольной смолы и коксового газа
1. Дегидроциклизацией
алканов с числом атомов углерода больше 6:
C6H14 t, kat→ C6H6 + 4H2

2. Тримеризация ацетилена
(только для бензола) – р. Зелинского:
3С2H2 600°C, акт. уголь →
C6H6

3. Дегидрированием
циклогексана и его гомологов:
Советский
академик Николай Дмитриевич Зелинский установил, что бензол образуется из
циклогексана (дегидрирование циклоалканов
C6H12 t,
kat→ C6H6 +
3H2

C6H11-CH3
t, kat→ C6H5-CH3 + 3H2
метилциклогексан толуол
4. Алкилирование бензола
(получение гомологов бензола) – р
Фриделя-Крафтса.
C6H6 +
C2H5-Cl t, AlCl3→ C6H5-C2H5
+ HCl
хлорэтан этилбензол
Химические
свойства аренов
I. РЕАКЦИИ
ОКИСЛЕНИЯ
1. Горение (коптящее пламя):
2C6H6 + 15O2t →
12CO2 + 6H2O + Q
2. Бензол при обычных условиях не обесцвечивает
бромную воду и водный раствор марганцовки
3. Гомологи бензола окисляются перманганатом калия
(обесцвечивают марганцовку):
А) в кислой среде до
бензойной кислоты
При действии на гомологи бензола перманганата калия и
других сильных окислителей боковые цепи окисляются. Какой бы сложной ни была
цепь заместителя, она разрушается, за исключением a -атома углерода, который окисляется в карбоксильную группу.
Гомологи бензола с одной боковой цепью дают бензойную
кислоту:
Гомологи, содержащие две боковые цепи, дают
двухосновные кислоты:
5C6H5-C2H5
+ 12KMnO4 + 18H2SO4 → 5C6H5COOH
+ 5CO2 + 6K2SO4 + 12MnSO4+28H2O
5C6H5-CH3
+ 6KMnO4 + 9H2SO4 → 5C6H5COOH
+ 3K2SO4 + 6MnSO4 +14H2O
Упрощённо:
C6H5-CH3
+ 3O KMnO4 → C6H5COOH
+ H2O
Б) в нейтральной и
слабощелочной до солей бензойной кислоты
C6H5-CH3
+ 2KMnO4 → C6H5COOК + KОН + 2MnO2 + H2O
II. РЕАКЦИИ
ПРИСОЕДИНЕНИЯ (труднее, чем у алкенов)
1. Галогенирование
C6H6 +3Cl2hν → C6H6Cl6(гексахлорциклогексан —
гексахлоран)

2. Гидрирование
C6H6 + 3H2 t,Pt или Ni → C6H12 (циклогексан)

3. Полимеризация
III. РЕАКЦИИ
ЗАМЕЩЕНИЯ – ионный механизм (легче, чем у алканов)
1. Галогенирование —
a) бензола
C6H6 + Cl2 AlCl3→ C6H5-Cl + HCl (хлорбензол)

C6H6
+ 6Cl2 t ,AlCl3→ C6Cl6
+ 6HCl (гексахлорбензол)
C6H6
+ Br2 t,FeCl3→ C6H5-Br + HBr (бромбензол)

б) гомологов бензола при облучении
или нагревании
По химическим свойствам алкильные радикалы подобны
алканам. Атомы водорода в них замещаются на галоген по свободно-радикальному
механизму. Поэтому в отсутствие катализатора при нагревании или УФ-облучении
идет радикальная реакция замещения в боковой цепи. Влияние бензольного кольца
на алкильные заместители приводит к тому, что замещается всегда атом водорода у атома углерода, непосредственно
связанного с бензольным кольцом (a -атома углерода).
1) C6H5-CH3
+ Cl2hν→ C6H5-CH2-Cl +
HCl
2)
в) гомологов бензола в
присутствии катализатора
C6H5-CH3 + Cl2 AlCl3→ (смесь орта, пара производных) + HCl
2. Нитрование (с азотной кислотой)
C6H6
+ HO-NO2 t, H2SO4→ C6H5-NO2 +
H2O
нитробензол — запахминдаля!

C6H5-CH3
+ 3HO-NO2 t, H2SO4→ СH3-C6H2(NO2)3
+ 3H2O
2,4,6-тринитротолуол (тол, тротил)
Применение бензола и его гомологов
Бензол C6H6 – хороший
растворитель. Бензол в качестве добавки улучшает качество моторного топлива.
Служит сырьем для получения многих ароматических органических соединений –
нитробензола C6H5NO2 (растворитель, из него
получают анилин), хлорбензола C6H5Cl, фенола C6H5OH,
стирола и т.д.
Толуол C6H5–CH3 – растворитель,
используется при производстве красителей, лекарственных и взрывчатых веществ
(тротил (тол), или 2,4,6-тринитротолуол ТНТ).
Ксилолы C6H4(CH3)2.
Технический ксилол – смесь трех изомеров (орто-, мета— и пара-ксилолов) –
применяется в качестве растворителя и исходного продукта для синтеза многих
органических соединений.
Изопропилбензол C6H5–CH(CH3)2
служит для получения фенола и ацетона.
Хлорпроизводные
бензола используют для защиты
растений. Так, продукт замещения в бензоле атомов Н атомами хлора –
гексахлорбензол С6Сl6 – фунгицид; его применяют для
сухого протравливания семян пшеницы и ржи против твердой головни. Продукт
присоединения хлора к бензолу – гексахлорциклогексан (гексахлоран) С6Н6Сl6 –
инсектицид; его используют для борьбы с вредными насекомыми. Упомянутые
вещества относятся к пестицидам – химическим средствам борьбы с
микроорганизмами, растениями и животными.
Стирол C6H5 – CH = CH2
очень легко полимеризуется, образуя полистирол, а сополимеризуясь с
бутадиеном – бутадиенстирольные каучуки.
ВИДЕО-ОПЫТЫ
Изучение физических свойств бензола
Горениебензола
Изучениеотношения бензола к бромной воде и раствору перманганата калия
Бромирование бензола
Нитрование бензола
Хлорированиебензола (получение гексахлорана)
1. Реакции замещения в бензольном кольце
Первая группа реакций реакции замещения. Мы говорили, что арены не имеют кратных связей в структуре молекулы, а содержат сопряженную систему из шести электронов, которая очень стабильна и придает дополнительную прочность бензольному кольцу. Поэтому в химических реакциях происходит в первую очередь замещение атомов водорода, а не разрушение бензольного кольца.
С реакциями замещения мы уже сталкивались при разговоре об алканах, но для них эти реакции шли по радикальному механизму, а для аренов характерен ионный механизм реакций замещения.
Первое химическое свойство галогенирование. Замещение атома водорода на атом галогена хлора или брома.
Реакция идет при нагревании и обязательно с участием катализатора. В случае с хлором это может быть хлорид алюминия или хлорид железа три. Катализатор поляризует молекулу галогена, в результате чего происходит гетеролитический разрыв связи и получаются ионы.
![]()
Положительно заряженный ион хлора и вступает в реакцию с бензолом.
Если реакция происходит с бромом, то катализатором выступает бромид железа три или бромид алюминия.

Важно отметить, что реакция происходит с молекулярным бромом, а не с бромной водой. С бромной водой бензол не реагирует.
У галогенирования гомологов бензола есть свои особенности. В молекуле толуола метильная группа облегчает замещение в кольце, реакционная способность повышается, и реакция идет в более мягких условиях, то есть уже при комнатной температуре.
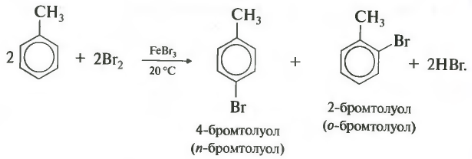
Важно отметить, что замещение всегда происходит в орто- и пара-положениях, поэтому получается смесь изомеров.
Второе свойство нитрование бензола, введение нитрогруппы в бензольное кольцо.
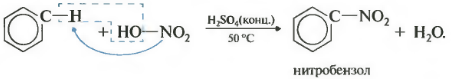
Образуется тяжелая желтоватая жидкость с запахом горького миндаля нитробензол, поэтому реакция может быть качественной на бензол. Для нитрования используется нитрующая смесь концентрированной азотной и серной кислот. Реакция проводится при нагревании.
Напомню, что для нитрования алканов в реакции Коновалова использовалась разбавленная азотная кислота без добавления серной.
При нитровании толуола, также как и при галогенировании, образуется смесь орто- и пара- изомеров.
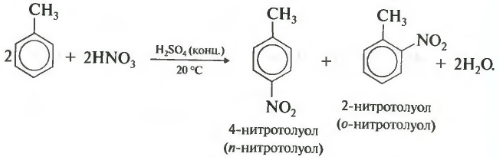
Третье свойство алкилирование бензола галогеналканами.
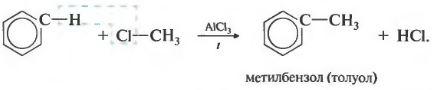
Эта реакция позволяет ввести углеводородный радикал в бензольное кольцо и может считаться способом получения гомологов бензола. В качестве катализатора используется хлорид алюминия, способствующий распаду молекулы галогеналкана на ионы. Также необходимо нагревание.
Четвертое свойство алкилирование бензола алкенами.
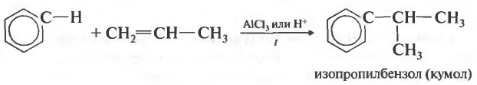
Таким способом можно получить, например, кумол или же этилбензол. Катализатор хлорид алюминия.
2. Реакции присоединения к бензолу
Вторая группа реакций реакции присоединения. Мы говорили, что эти реакции не характерны, но они возможны при достаточно жестких условиях с разрушением пи-электронного облака и образованием шести сигма-связей.
Пятое свойство в общем списке гидрирование, присоединение водорода.
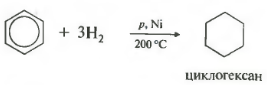
Температура, давление, катализатор никель или платина. Таким же образом способен реагировать толуол.
Шестое свойство хлорирование. Обратите внимание, что речь идет именно о взаимодействии с хлором, поскольку бром в эту реакцию не вступает.
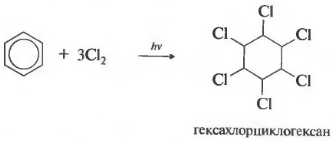
Реакция протекает при жестком ультрафиолетовом облучении. Образуется гексахлорциклогексан, другое название гексахлоран, твердое вещество.
Важно помнить, что для бензола не возможны реакции присоединения галогеноводородов (гидрогалогенирование) и присоединение воды (гидратация).
3. Замещение в боковой цепи гомологов бензола
Третья группа реакций касается только гомологов бензола это замещение в боковой цепи.
Седьмое свойство в общем списке галогенирование по альфа-атому углерода в боковой цепи.
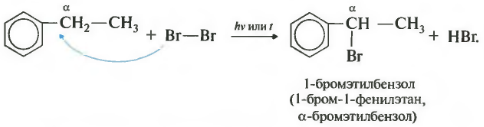
Реакция происходит при нагревании или облучении и всегда только по альфа-углероду. При продолжении галогенирования, второй атом галогена снова встанет в альфа-положение.
4. Окисление гомологов бензола
Четвертая группа реакций окисление.
Бензольное кольцо слишком прочное, поэтому бензол не окисляется перманганатом калия не обесцвечивает его раствор. Это очень важно помнить.
Зато гомологи бензола окисляются подкисленным раствором перманганата калия при нагревании. И это восьмое химическое свойство.
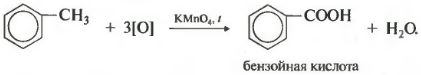
Получается бензойная кислота. Наблюдается обесцвечивание раствора. При этом, какой бы длинной не была углеродная цепь заместителя, всегда происходит ее разрыв после первого атома углерода и альфа-атом окисляется до карбоксильной группы с образованием бензойной кислоты. Оставшаяся часть молекулы окисляется до соответствующий кислоты или, если это только один атом углерода, до углекислого газа.
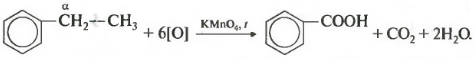
Если гомолог бензола имеет больше одного углеводородного заместителя у ароматического кольца, то окисление происходит по тем же правилам окисляется углерод, находящийся в альфа-положении.
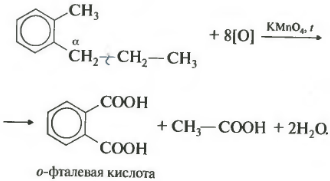
В данном примере получается двухосновная ароматическая кислота, которая называется фталевая кислота.
Особым образом отмечу окисление кумола, изопропилбензола, кислородом воздуха в присутствии серной кислоты.
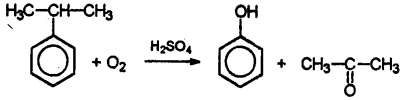
Это так называемый кумольный способ получения фенола. Как правило, сталкиваться с этой реакцией приходится в вопросах, касающихся получения фенола. Это промышленный способ.
Девятое свойство горение, полное окисление кислородом. Бензол и его гомологи сгорают до углекислого газа и воды.
Запишем уравнение горения бензола в общем виде.
![]()
По закону сохранения массы атомов слева должно быть столько же, сколько атомов справа. Потому что ведь в химических реакциях атомы никуда не деваются, а просто изменяется порядок связей между ними. Так вот молекул углекислого газа будет столько же, сколько и атомов углерода в молекуле арена, поскольку в состав молекулы входит один атом углерода. То есть n молекул CO2. Молекул воды будет в два раза меньше, чем атомов водорода, то есть (2n-6)/2, а значит n-3.
Атомов кислорода слева и справа одинаковое количество. Справа их 2n из углекислого газа, потому что в каждой молекуле два атома кислорода, плюс n-3 из воды, итого 3n-3. Слева атомов кислорода столько же 3n-3, а значит молекул в два раза меньше, потому как в состав молекулы входят два атома. То есть (3n-3)/2 молекул кислорода.
Таким образом, мы составили уравнение сгорания гомологов бензола в общем виде.
Что такое нитробензол? Это органическое соединение, которое представляет собой ароматическое ядро и присоединенную к нему нитрогруппу. По внешнему виду, в зависимости от температуры, — это ярко-желтые кристаллы или маслянистая жидкость. Имеет миндальных запах. Токсичен.
Структурная формула нитробензола
Нитрогруппа — это очень сильный акцептор электронной плотности. Поэтому молекула нитробензола обладает отрицательным индуктивным и отрицательным мезомерным эффектом. Нитрогруппа довольно сильно притягивает на себя электронную плотность ароматического ядра, дезактивируя его. Электрофильные реагенты уже не так сильно притягиваются к ядру, и потому нитробензол не так активно вступает в подобные реакции. Чтобы напрямую присоединить к нитробензолу еще одну нитрогруппу, необходимы очень жесткие условия, гораздо более жесткие, чем при синтезе мононитробензола. Тоже самое касается галогенов, сульфогруппы и др.
 Вам будет интересно:Математика: действия с дробями. Действия с десятичными и обыкновенными дробями
Вам будет интересно:Математика: действия с дробями. Действия с десятичными и обыкновенными дробями
Из структурной формулы нитробензола видно, что одна связь азота с кислородом одинарная, а другая — двойная. Но на самом деле, из-за мезомерного эффекта, они обе равнозначны и имеют одинаковую длину 0,123 нм.

Получение нитробензола в промышленности
Нитробензол — важный промежуточный продукт в синтезе многих веществ. Поэтому его производят в промышленных масштабах. Основной способ получения нитробензола — это нитрование бензола. Обычно для этого используют нитрующую смесь (смесь концентрированных серной и азотной кислоты). Реакцию ведут 45 минут при температуре примерно 50 °C. Выход нитробензола составляет 98 %. Именно поэтому данный способ в основном применяют в промышленности. Для его реализации существуют специальные установки как периодического, так и непрерывного типа. На 1995 г производство нитробензола в США составляло 748 000 тонн в год.
Нитрование бензола можно также вести просто концентрированной азотной кислотой, но в таком случае выход продукта будет ниже.

Получение нитробензола в лаборатории
Существует еще один способ получения нитробензола. В качестве сырья здесь используется анилин (аминобензол), который окисляют пероксисоединениями. Благодаря этому аминогруппа заменяется на нитрогруппу. Но в ходе этой реакции образуется несколько побочных продуктов, что мешает эффективно использовать данный способ в промышленности. Тем более, нитробензол в основном и используют для синтеза анилина, поэтому применять анилин для производства нитробензола не имеет смысла.
Физические свойства
 Вам будет интересно:Единое водное пространство, разделяющее материки
Вам будет интересно:Единое водное пространство, разделяющее материки
При комнатной температуре нитробензол представляет из себя бесцветную маслянистую жидкость с запахом горького миндаля. При температуре 5,8 °C она затвердевает, превращаясь в желтые кристаллы. При 211 °C нитробензол кипит, а при 482 °C самовоспламеняется. Данное вещество, почти как любое ароматическое соединение, нерастворимо в воде, зато хорошо растворимо в органических соединениях, особенно в бензоле. Также он может перегоняться водяным паром.

Электрофильное замещение
Для нитробензола, как и для любого арена, характерны реакции электрофильного замещения в ядро, хотя они и несколько затруднены по сравнению с бензолом из-за влияния нитрогруппы. Так, из нитробензола можно получить динитробензол путем дальнейшего нитрования смесью азотной и серой кислот при повышенной температуре. Полученный продукт будет преимущественно (93 %) состоять из мета-динитробензола. Возможно даже получение тринитробензола прямым путем. Но для этого необходимо использовать еще более жесткие условия, а также трехфтористый бор.
Точно так же нитробензол может сульфироваться. Для этого используют очень сильный сульфирующий реагент — олеум (раствор оксида серы VI в серной кислоте). Температура реакционной смеси должна составлять не менее 80 °C. Еще одна реакция электрофильного замещения — прямое галогенирование. В качестве катализаторов используют сильные кислоты Льюиса (хлорид алюминия, трехфтористый бор и др.), а также повышенную температуру.

Нуклеофильное замещение
Как видно из структурной формулы, нитробензол может вступать в реакции с сильными электронодонорными соединениями. Это возможно из-за влияния нитрогруппы. Примером такой реакции может служить взаимодействие с концентрированными или твердыми гидроксидами щелочных металлов. Но в этой реакции не образуется нитробензол натрия. Химическая формула нитробензола предполагает скорее присоединение гидроксильной группы в ядро, т. е. образование нитрофенола. Но происходит это только при достаточно жестких условиях.
 Вам будет интересно:Какое уравнение не имеет корней? Примеры уравнений
Вам будет интересно:Какое уравнение не имеет корней? Примеры уравнений
Подобная реакция протекает и с магнийорганическими соединениями. Углеводородный радикал присоединяется к ядру в орто- или пара- положения к нитрогруппе. Побочным процессом в этом случае является восстановление нитрогруппы до аминогруппы. Реакции нуклеофильного замещения идут проще, если нитрогрупп несколько, так как они еще сильнее будут оттягивать на себя электронную плотность ядра.

Реакция восстановления
Как известно, нитросоединения могут восстанавливаться до аминов. Не является исключением и нитробензол, формула которого предполагает возможность этой реакции. Она часто применяется в промышленности для синтеза анилина.
Но нитробензол может давать и очень много других продуктов восстановления. Чаще всего используют восстановление атомарным водородом в момент его выделения, т. е. в реакционной смеси проводят реакцию взаимодействия кислоты с металлом, и выделяющийся водород вступает в реакцию с нитробензолом. Обычно при таком взаимодействии получается анилин.
Если на нитробензол подействовать цинковой пылью в растворе хлорида аммония, то продуктом реакции будет являться N-фенилгидроксиламин. Это соединение довольно легко может быть восстановлено стандартным способом до анилина, либо же окислено обратно в нитробензол сильным окислителем.

Восстановление также может вестись в газовой фазе молекулярным водородом в присутствии платины, палладия или никеля. В этом случае также получается анилин, но существует вероятность восстановления самого бензольного ядра, что зачастую нежелательно. Иногда также применяют такой катализатор, как никель Ренея. Он представляет из себя пористый никель, насыщенный водородом и содержащий 15 % алюминия.
При восстановлении нитробензола алкоголятами калия или натрия образуется азоксибензол. Если использовать более сильные восстановители в щелочной среде, то получается азобензол. Эта реакция также довольно важна, так как с ее помощью синтезируют некоторые красители. Азобензол может быть подвергнут дальнейшему восстановлению в щелочной среде до образования гидразобензола.
Изначально восстановление нитробензола проводилось сульфидом аммония. Этот способ в 1842 г предложил Зинин Н. Н., поэтому реакция носит его имя. Но в настоящий момент ее уже редко применяют на практике из-за низкого выхода.
Применение
Сам по себе нитробензол применяют очень редко, только как селективный растворитель (например, для эфиров целлюлозы) или мягкий окислитель. Иногда его добавляют в полировочные растворы для металлов.
Почти весь производимый нитробензол используется для синтеза других полезных веществ (например, анилина), которые, в свою очередь, используются для синтеза лекарственных препаратов, красителей, полимеров, взрывчатых веществ и др.

Опасность
Из-за своих физических и химических свойств, нитробензол — очень опасное соединение. Он имеет третий уровень опасности для здоровья из четырех по стандарту NFPA 704. Помимо того, что он может попасть в организм при дыхании или через слизистые оболочки, он также всасывается через кожу. При отравлении большой концентрацией нитробензола человек может потерять сознание и умереть. При небольших концентрациях симптомами отравления являются недомогание, головокружение, шум в ушах, тошнота и рвота. Особенность отравления нитробензолом — высокая скорость заражения. Симптомы проявляются очень быстро: нарушаются рефлексы, кровь приобретает темно-бурый цвет из-за образования в ней метгемоглобина. Иногда могут присутствовать высыпания на коже. Концентрация, достаточная для отправления, очень мала, хотя точных данных по смертельной дозе нет. В специальной литературе часто встречается информация, что 1-2 капли нитробензола хватает, чтобы убить человека.
Лечение
При отравлении нитробензолом пострадавшего необходимо немедленно удалить из токсичной зоны и избавить его от зараженной одежды. Тело омывают теплой водой с мылом, чтобы удалить нитробензол с кожи. Каждые 15 минут пострадавшему делают ингаляцию карбогеном. При легких отравлениях необходимо принимать цистамин, пиридоксин или липоевую кислоту. В более тяжелых случаях рекомендуется использовать метиленовую синь или хромосмон внутривенно. При отравлении нитробезнолом через рот необходимо немедленно вызывать рвоту и промыть желудок теплой водой. Противопоказано принимать какой-либо жир, в том числе и молоко.
