Какой химический элемент по свойствам подобен силицию

На чтение 10 мин. Просмотров 335 Опубликовано 13.01.2020
Как самостоятельный химический элемент кремний стал известен человечеству всего лишь в 1825 году. Что, конечно, не мешало применять соединения кремния в таком количестве сфер, что проще перечислить те, где элемент не используется.

Данная статья прольет свет на физические, механические и полезные химические свойства кремния и его соединений, области применения, также мы расскажем о том, как влияет кремний на свойства стали и иных металлов.
Что такое кремний?
Для начала давайте остановимся на общей характеристике кремния. От 27,6 до 29,5% массы земной коры составляет кремний. В морской воде концентрация элемента тоже изрядная – до 3 мг/л.
По распространенности в литосфере кремний занимает второе почетное место после кислорода. Однако наиболее известная его форма – кремнезем, является диоксидом, и именно его свойства и стали основой для столь широкого применения.
Понятие и особенности
Кремний – неметалл, однако при разных условиях может проявлять и кислотные, и основные свойства. Является типичным полупроводником и чрезвычайно широко используется в электротехнике. Физические и химические его свойства во многом определяются аллотропным состоянием.
Чаще всего дело имеют с кристаллической формой, поскольку ее качества более востребованы в народном хозяйстве:
- Кремний – один из базовых макроэлементов в человеческом теле. Его нехватка губительно сказывается на состоянии костной ткани, волос, кожи, ногтей. Кроме того, кремний оказывает влияние на работоспособность иммунной системы.
- В медицине элемент, вернее говоря, его соединения нашли свое первое применение именно в этом качестве. Вода из колодцев, выложенных кремнием, отличались не только чистотой, но и положительно сказывалась на стойкости к инфекционным болезням. Сегодня соединение с кремнием служат основой для препаратов против туберкулеза, атеросклероза, артрита.
- В целом неметалл малоактивен, однако и в чистом виде встретить его сложно. Связано это с тем, что на воздухе он быстро пассивируется слоем диоксида и перестает реагировать. При нагревании химическая активность увеличивается. В результате человечество гораздо ближе знакомо с соединениями вещества, а не с ним самим.
Так, кремний образует сплавы практически со всеми металлами – силициды. Все они отличаются тугоплавкостью и твердостью и применяются на соответствующих участках: газовые турбины, нагреватели печей.
Размещается неметалл в таблице Д. И. Менделеева в 6 группе вместе с углеродом, германием, оловом, что указывает на определенную общность с этими веществами. Так, с углеродом его «роднит» способность к образованию соединений по типу органических. При этом кремний, как и германий может проявить свойства металла в некоторых химических реакциях, что используется в синтезе.
Плюсы и минусы
Как и всякое другое вещество с точки зрения применения в народном хозяйстве, кремний обладает определенными полезными или не слишком качествами.
Важны они именно для определения области использования:
- Немалым достоинством вещества является его доступность. В природе он, правда, находится не в свободном виде, но все же, технология получения кремния не так уж и сложна, хотя и энергозатратна.
- Второе важнейшее достоинство – образование множества соединений с необыкновенно полезными свойствами. Это и силаны, и силициды, и диоксид, и, конечно, разнообразнейшие силикаты. Способность кремния и его соединений образовывать сложные твердые растворы практически бесконечна, что позволяет бесконечно же получать самые разные вариации стекла, камня и керамики.
- Полупроводниковые свойства неметалла обеспечивает ему место базового материала в электро- и радиотехнике.
- Неметалл является нетоксичным, что допускает применение в любой отрасли промышленности, и при этом не превращает технологический процесс в потенциально опасный.
К недостаткам материала можно отнести лишь относительную хрупкость при хорошей твердости. Кремний не используется для несущих конструкций, но зато это сочетание позволяет обрабатывать должным образом поверхность кристаллов, что важно для приборостроения.
Свойства и характеристики

Поскольку в промышленности чаще всего эксплуатируется кристаллический кремний, то именно его свойства и являются более важными, и именно они и приводятся в технических характеристиках.
Физические свойства вещества
- температура плавления – 1417 С;
- температура кипения – 2600 С;
- плотность составляет 2,33 г/куб. см, что свидетельствует о хрупкости;
- теплоемкость, как и теплопроводность не постоянны даже на самых чистых пробах: 800 Дж/(кг·К), или 0,191 кал/(г·град) и 84-126 вт/(м·К), или 0,20-0,30 кал/(см·сек·град) соответственно;
- прозрачен для длинноволнового ИК-излучения, что используется в инфракрасной оптике;
- диэлектрическая проницаемость – 1,17;
- твердость по шкале Мооса – 7.
Электрические свойства неметалла сильно зависят от примесей. В промышленности эту особенность используют, модулируя нужный тип полупроводника. При нормальной температуре кремний хрупок, но при нагревании выше 800 С возможна пластическая деформация.
Свойства аморфного кремния разительно отличаются: он сильно гигроскопичен, намного активнее вступает в реакцию даже при нормальной температуре.
Химические свойства кремния
В большинстве соединений кремний проявляет степени окисления -4, +2, +4. При низких температурах химически инертен. На воздухе покрывается тонкой плёнкой оксида, в атмосфере кислорода окисляется при нагревании свыше 400°С.
С фтором взаимодействует в обычных условиях, с остальными галогенами, азотом, углеродом — при нагревании. В воде, кислотах (за исключением смеси HF+HNO3) не растворяется. Щёлочи переводят кремний в соли кремниевых кислот с выделением водорода. Растворим во многих расплавленных металлах, с некоторыми из них даёт соединения, называемые силицидами.
С водородом образует весьма реакционноспособные соединения общей формулы SinH2n+2 (где n=1-8) — силаны. Известны многочисленные кремнийорганические соединения (силиконы, органосилоксаны и т.д.). Большое значение имеют кремниевые кислоты.
В свободном состоянии выделены мета-(Н2SiO3), орто-(Н2SiO4) и двуметакремниевая (Н2Si2О5) кислоты. Соли кремниевых кислот широко распространены в природе: минералы класса силикатов природных. При изоморфном замещении в их структуре части кремния алюминием образуются алюмосиликаты.
Состав и структура
![]()
Кремний существует в двух аллотропных формах, одинаково устойчивых при нормальной температуре.
- Кристаллический имеет вид темно-серого порошка. Вещество, хотя и имеет алмазоподобную кристаллическую решетку, является хрупким – из-за чересчур длинной связи между атомами. Интерес представляют его свойства полупроводника.
- При очень высоких давлениях можно получить гексагональную модификацию с плотностью 2,55 г/куб. см. Однако эта фаза практического значения пока не нашла.
- Аморфный – буро-коричневый порошок. В отличие от кристаллической формы намного активнее вступает в реакцию. Связано это не столько с инертностью первой формы, сколько с тем, что на воздухе вещество покрывается слоем диоксида.
Кроме того, необходимо учитывать и еще один тип классификации, связанный с величиной кристалла кремния, которые в совокупности образуют вещество. Кристаллическая решетка, как известно, предполагают упорядоченность не только атомов, но и структур, которые эти атомы образуют – так называемый дальний порядок. Чем он больше, тем более однородным по свойствам будет вещество.
- Монокристаллический – образец представляет собой один кристалл. Структура его максимально упорядочена, свойства однородны и хорошо предсказуемы. Именно такой материал наиболее востребован в электротехнике. Однако он же относится к самому дорогому виду, поскольку процесс его получения сложен, а скорость роста низка.
- Мультикристаллический – образец составляет некоторое количество крупных кристаллических зерен. Границы между ними формируют дополнительные дефектные уровни, что снижает производительность образца, как полупроводника и приводит к более быстрому износу. Технология выращивания мультикристалла проще, потому и материал дешевле.
- Поликристаллический – состоит из большого количества зерен, расположенных хаотически относительно друг друга. Это наиболее чистая разновидность промышленного кремния, применяется в микроэлектронике и солнечной энергетике. Довольно часто используется в качестве сырья для выращивания мульти- и монокристаллов.
- Аморфный кремний и в этой классификации занимает отдельную позицию. Здесь порядок расположения атомов удерживается только на самых коротких дистанциях. Однако в электротехнике он все же используется в виде тонких пленок.
Далее мы расскажем вам про сырье для производства кремния, вредность добычи, технологию его изготовления в мировых масштабах и в России.

Получить чистый кремний не так уж и просто, учитывая инертность его соединений и высокую температуру плавления большинства из них. В промышленности чаще всего прибегают к восстановлению углеродом из диоксида. Проводят реакцию в дуговых печах при температуре 1800 С. Таким образом получают неметалл чистотой в 99,9%, что для его применения недостаточно.
Полученный материал хлорируют с тем, чтобы получить хлориды и гидрохлориды. Затем соединения очищают всеми возможными методами от примесей и восстанавливают водородом.
Очистить вещество можно и за счет получения силицида магния. Силицид подвергают действию соляной или уксусной кислоты. Получают силан, а последний очищают различными способами – сорбционным, ректификацией и так далее. Затем силан разлагают на водород и кремний при температуре в 1000 С. В этом случае получают вещество с долей примеси 10-8–10-6%.
Применение вещества
![]()
Для промышленности наибольший интерес представляют электрофизические характеристики неметалла. Его монокристаллическая форма является непрямозонным полупроводником. Свойства его определяются примесями, что позволяет получать кристаллы кремния с заданными свойствами.
Так, добавка бора, алюминия, индия дает возможность вырастить кристалл с дырочной проводимостью, а введение фосфора или мышьяка – кристалл с электронной проводимостью.
- Кремний в буквальном смысле слова служит основой современной электротехники. Из него изготавливают транзисторы, фотоэлементы, интегральные схемы, диоды и так далее. Причем функциональность прибора определяет практически всегда только приповерхностный слой кристалла, что обуславливает весьма специфические требования именно к обработке поверхности.
- В металлургии технический кремний применяют и как модификатор сплавов – придает большую прочность, и как компонент – в бронзах, например, и как раскислитель – при производстве чугуна.
- Сверхчистый и очищенный металлургический составляют основу солнечной энергетики.
- Диоксид неметалла встречается в природе в очень разных формах. Его кристаллические разновидности – опал, агат, сердолик, аметист, горный хрусталь, нашли свое место в ювелирном деле. Не столь привлекательные внешне модификации – кремень, песок, кварц, используются и в металлургии, и в строительстве, и в радиоэлектротехнике.
- Соединение неметалла с углеродом – карбид, применяется и в металлургии, и в приборостроении, и в химической промышленности. Он является широкозональным полупроводником, отличается высокой твердостью – 7 по шкале Мооса, и прочностью, что и позволяет применять его в качестве абразивного материала.
- Силикаты – то есть, соли кремниевой кислоты. Неустойчивы, легко разлагаются под действием температуры. Примечательность их в том, что они образуют многочисленные и разнообразные соли. А вот последние являются основой при производстве стекла, керамики, фаянса, хрусталя, цемента и бетона. Можно смело сказать, что современное строительство зиждется на разнообразных силикатах.
- Стекло представляет здесь наиболее интересный случай. Основой его служат алюмосиликаты, но ничтожные примеси других веществ – обычно оксидов, придают материалу массу разных свойств, в том числе и цвет. Керамика – клинкер, фаянс, фарфор, по сути, имеет ту же формулу, хотя и с другим соотношением компонентов, и ее разнообразие тоже поразительно.
- Неметалл обладает еще одной способностью: образует соединения по типу углеродных, в виде длинной цепочки из атомов кремния. Такие соединения носят название кремнийорганических. Сфера их применения не менее известна – это силиконы, герметики, смазки и так далее.
Кремний – очень распространенный элемент и имеет необыкновенно большое значение в очень многих сферах народного хозяйства. Причем активно используется не только само вещество, но все его разнообразные и многочисленные соединения.
Источники:
https://stroyres.net/metallicheskie/vidyi/vspomogatelnyie-veshhestva/kremniy.html
https://www.mining-enc.ru/k/kremnij-/
Ïîõîæèå ïîñòû
Ñóëüôèä æåëåçà(II) (FeS) — âåùåñòâî, êîòîðîå îáðàçóåòñÿ ïðè âçàèìîäåéñòâèè æåëåçà ñ ñåðîé. Ïðèìåíÿåòñÿ êàê ñûðüå â ïðîèçâîäñòâå ÷óãóíà, à òàêæå ÿâëÿåòñÿ òâåðäûì èñòî÷íèêîì ñåðîâîäîðîäà. Íà ôîòîãðàôèÿõ ìîæíî çàìåòèòü ÷àñòèöû ìåòàëëè÷åñêîãî æåëåçà, êîòîðîå íå ïðîðåàãèðîâàëî ñ ñåðîé.
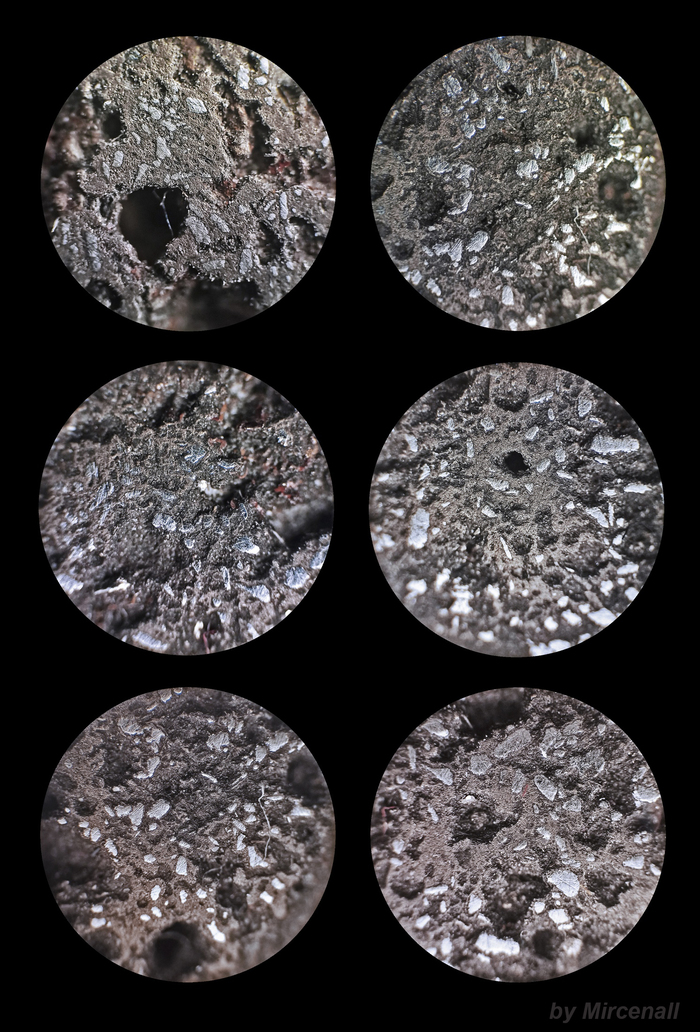
 ïðèðîäå ñóëüôèä æåëåçà(II) âñòðå÷àåòñÿ êðàéíå ðåäêî, îäíàêî ðàñïðîñòðàí¸í äèñóëüôèä æåëåçà(II) (FeS2), èçâåñòíûé êàê ìèíåðàë ïèðèò èëè ñåðíûé êîë÷åäàí.
vk.com/mircenall

Ïîêàçàòü ïîëíîñòüþ
3
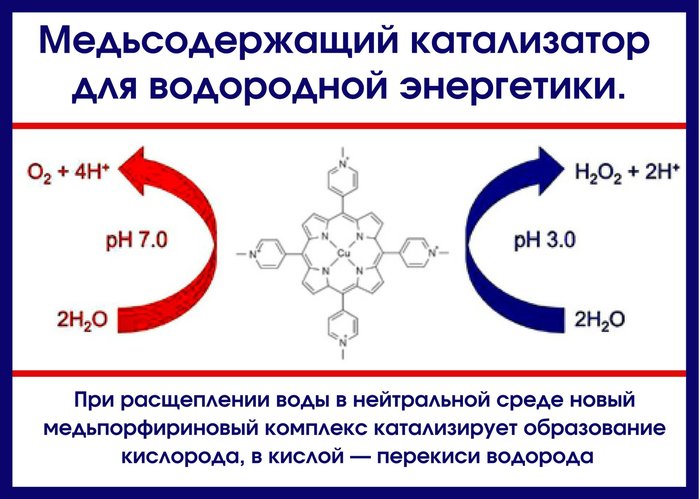
Íîâûé ìåäüñîäåðæàùèé êîìïëåêñ, èäåþ ñòðîåíèÿ êîòîðîãî ïîäñêàçàëà ïðèðîäà, ýôôåêòèâíî ðàñùåïëÿåò âîäó â íåéòðàëüíîé ñðåäå. Ýòî îòêðûòèå ìîæåò ñäåëàòü áîëåå äîñòóïíûì ïîëó÷åíèå âîäîðîäà ñ ïîìîùüþ âîññòàíîâëåíèÿ âîäû.
Ìîëåêóëÿðíûé âîäîðîä äàâíî ðàññìàòðèâàþò êàê àëüòåðíàòèâó íåôòè è ãàçó. Åäèíñòâåííûé ïðîäóêò ñãîðàíèÿ âîäîðîäà âîäà, êîòîðàÿ ñàìà ìîæåò áûòü èñòî÷íèêîì âîäîðîäà. Ìíîãèå èññëåäîâàòåëüñêèå ãðóïïû ïî âñåìó ìèðó ñòàðàþòñÿ ðàçðàáîòàòü êàòàëèçàòîðû, ñïîñîáíûå ïîíèçèòü ýíåðãèþ âîññòàíîâëåíèÿ âîäû äî ìîëåêóëÿðíîãî âîäîðîäà è îáëåã÷èòü ïðîòåêàíèå ýòîé ðåàêöèè. Íàèáîëåå ýôôåêòèâíûå êàòàëèçàòîðû ðàñùåïëåíèÿ âîäû â íàñòîÿùåå âðåìÿ êîîðäèíàöèîííûå ñîåäèíåíèÿ ðóòåíèÿ è èðèäèÿ. Ê íåäîñòàòêàì îáîèõ ìåòàëëîâ ìîæíî îòíåñòè èõ íèçêèå êîíöåíòðàöèè â çåìíîé êîðå è âûñîêóþ ñòîèìîñòü.
Íîâîå èññëåäîâàíèå äåìîíñòðèðóåò, ÷òî â ïðèñóòñòâèè ïîðôèðèíîâîãî êîìïëåêñà ìåäè ýëåêòðîêàòàëèòè÷åñêîå ðàñùåïëåíèå âîäû ïðîèñõîäèò ïðè íåéòðàëüíûõ çíà÷åíèÿõ ðÍ è ïðè íèçêîì çíà÷åíèè ýëåêòðîäíîãî ïîòåíöèàëà. Ïðè 310 ì è ðÍ 7 âîäà îêèñëÿåòñÿ ñ âûäåëåíèåì ìîëåêóëÿðíîãî êèñëîðîäà, à â êèñëîé ñðåäå (ïðè òîì æå ýëåêòðîäíîì ïîòåíöèàëå) äî ïåðåêèñè âîäîðîäà. Õîòÿ ìåäíûé êîìïëåêñ è íå ïðåâîñõîäèò ïî ïðîèçâîäèòåëüíîñòè êîìïëåêñû áëàãîðîäíûõ ìåòàëëîâ, âñå æå ýòî áîëüøîé øàã âïåðåä ìåíüøàÿ ýôôåêòèâíîñòü ïðîèçâîäíûõ ìåäè êîìïåíñèðóåòñÿ åå áîëüøåé ðàñïðîñòðàíåííîñòüþ è äåøåâèçíîé. Êàòàëèçàòîðû ðàñùåïëåíèÿ âîäû íà îñíîâå ìåäè áûëè èçâåñòíû è ðàíåå, íî îíè ðàáîòàëè â ñèëüíîùåëî÷íîé ñðåäå è ïðè áîëüøîì çíà÷åíèè ýëåêòðîäíîãî ïîòåíöèàëà.
Èññëåäîâàòåëè èñõîäèëè èç òîãî, ÷òî â ïðîöåññå ôîòîñèíòåçà êëþ÷åâóþ ðîëü â îêèñëåíèè âîäû è âûäåëåíèè êèñëîðîäà èãðàåò ìàãíèéïîðôèðèíîâûé êîìïëåêñ. Òåì íå ìåíåå ñïîñîáíîñòü ìåäüïîðôèðèíîâîãî êîìïëåêñà êàòàëèçèðîâàòü îêèñëåíèå âîäû îêàçàëàñü ïðèÿòíîé íåîæèäàííîñòüþ äëÿ ìíîãèõ õèìèêîâ êàê ñïåöèàëèñòîâ ïî õèìèè ïîðôèðèíîâûõ êîìïëåêñîâ, òàê è òåõ, êòî çàíèìàëñÿ ðàñùåïëåíèåì âîäû. Åùå îäíà íåîáû÷íàÿ ÷åðòà ýòîãî êàòàëèçàòîðà îêèñëåíèå âîäû äî ïåðåêèñè âîäîðîäà ïðè íèçêèõ çíà÷åíèÿõ ðÍ. Ýòîò ïðîöåññ íå ñòîèò ðàññìàòðèâàòü êàê íîâûé ñïîñîá ïîëó÷åíèÿ H2O2, è âñå æå îí òðåáóåò âíèìàíèÿ. Óñòàíîâèâ, êàê îáðàçóåòñÿ ïåðåêèñü âîäîðîäà, èññëåäîâàòåëè ñìîãóò îïðåäåëèòü ìåõàíèçì ýòîé êàòàëèòè÷åñêîé ðåàêöèè è âûÿñíèòü, êàê ïîâûñèòü ýôôåêòèâíîñòü ðàñùåïëåíèÿ âîäû.

Ïîêàçàòü ïîëíîñòüþ
3
 îäíîì èç ïîñòîâ îá îëîâå ïèêàáóøíèêîâ çàèíòåðåñîâàëà òàêàÿ äåòàëü — ïðè òåìïåðàòóðå íèæå 13.2°C êîâêîå è ïëàñòè÷íîå îëîâî ïåðåõîäèò â äðóãóþ «ñåðóþ» àëëîòðîïíóþ ìîäèôèêàöèþ.

Ïðè ýòîì ïåðåõîä ñîïðîâîæäàåòñÿ óâåëè÷åíèåì îáúåìà íà 25,6 %, â ñâÿçè ñ ÷åì âîçíèê âîïðîñ
Ñîáñòâåííî ýòî ÿ è ðåøèë ïðîâåðèòü.
Ïåðâûì äåëîì íàøåë â ëàáîðàòîðèè ÷èñòîå îëîâî (ïðîâîëîêà ïðèïîÿ íå ïîäîéäåò, èáî îíà ñîäåðæèò ñâèíåö, êîòîðûé êàê ðàç òàêè ïðåäîòâðàùàåò ðàçðóøåíèå). Îëîâî õðàíèòñÿ â âèäå ìàëåíüêèõ ãðàíóë, íî ÿ ïåðåïëàâèë åãî â êóñîê ïîáîëüøå.

Äåëàòü èäåàëüíóþ äåðåâÿííóþ êîðîáêó áûëî áû ñëèøêîì äîëãî, òàê ÷òî ðåøèë çàëèòü êóñîê ìåòàëëà â ãèïñ è âûñòàâèòü íà ìîðîç íà äîëãîå âðåìÿ â çàêðûòîé êîðîáêå.


Êðîìå òîãî, ÷åì íèæå òåìïåðàòóðà, òåì áûñòðåå îñóùåñòâëÿåòñÿ ïåðåõîä (íàèáîëåå áûñòðîå ïðåâðàùåíèå íàáëþäàåòñÿ ïðè òåìïåðàòóðå íèæå -33°C). Ïîñêîëüêó íà÷àëî çèìû â ñòîëèöå âûäàëîñü òåïëûì, ÿ ðåøèë ïðîâîäèòü ýòîò ýêñïåðèìåíò ñ ñåðåäèíû ÿíâàðÿ. Ãèïñîâûé ñëåïîê ñ îëîâîì ÿ ïîëîæèë â êîðîáêó (äàáû çàùèòèòü åãî îò âîäû) è îñòàâèë íà ïîäîêîííèêå, ðåøèâ îòêðûòü ñïóñòÿ ìåñÿö.

×åðåç ìåñÿö ôîðìà îñòàëàñü ëåæàòü, êàê ëåæàëà. Îäíàêî êàê ðàç ñ ñåðåäèíû ôåâðàëÿ óäàðèëè ñèëüíûå ìîðîçû è ïðîöåññ äîëæåí áûë óñêîðèòüñÿ (òåì âðåìåíåì ïèêàáó íà÷àëî íàïîìèíàòü î ñåáå)

Îòêðûâ êîðîáêó óæå â ìàðòå, ÿ óâèäåë æåëàííîå èçìåíåíèå — òðåùèíó, ðàçäåëèâøóþ ñëåïîê íà äâå ïîëîâèíû!

Àêêóðàòíî äîñòàâ åãî, ÿ ðàçäåëèë ïîëîâèíêè ôîðìû è îòòóäà ïîñûïàëñÿ òåìíûé ïîðîøîê ñ ìåòàëëè÷åñêèì áëåñêîì (è îñòàòîê êóñêà áåëîãî îëîâà, ïîâåðõíîñòü êîòîðîãî áûëà òàêæå âñÿ â ñåðîé ìîäèôèêàöèè ).  êîíöå êîíöîâ îíî-òàêè ðàçîðâàëî ãèïñ.

Ñåðîå îëîâî ñêîðåå ïîõîæå íà ãðàôèò ñ áëåñêîì ñâèíöà, ÷åì íà ìåòàëë. ×òîáû íàãëÿäíî ïðîäåìîíñòðèðîâàòü îòëè÷èå, ÿ âûñûïàë ðÿäîì ïîðîøîê áåëîãî îëîâà è ïîëó÷åííîå ñåðîå. Îäíàêî âåðíóòü åìó èñõîäíîå ñîñòîÿíèå íå ñîñòàâëÿåò òðóäà — òðåáóåòñÿ ëèøü ðàñïëàâèòü α-îëîâî è ñëèòîê ñíîâà áóäåò ÿâëÿòüñÿ áåëûì β-îëîâîì

Òàêèì îáðàçîì ïðåäïîëîæåíèå î ðàçðûâàþùåì êîíòåéíåðå îëîâå ïîäòâåðæäåíî

P.S. îòäåëüíàÿ áëàãîäàðíîñòü ñåäüìîé ïàðòèè ãðàíóëèðîâàííîãî îëîâà Óðàëüñêîãî çàâîäà õèìðåàêòèâîâ îò íîÿáðÿ 1977 ãîäà. Èíà÷å áû ýêñïåðèìåíò íå ñîñòîÿëñÿ.


Ïîêàçàòü ïîëíîñòüþ
12
Êðèñòàëëû ñåðåáðà íà ìåäè.

Ñåðåáðî âûäåëÿåòñÿ íà òðåóãîëüíûõ ìåäíûõ ïëàñòèíêàõ, ïîãðóæåííûõ â ðàñòâîð íèòðàòà ñåðåáðà

Ìåäü
Öèíê

Ñåðåáðî

Îëîâî

Ñâèíåö

Ïîêàçàòü ïîëíîñòüþ
2
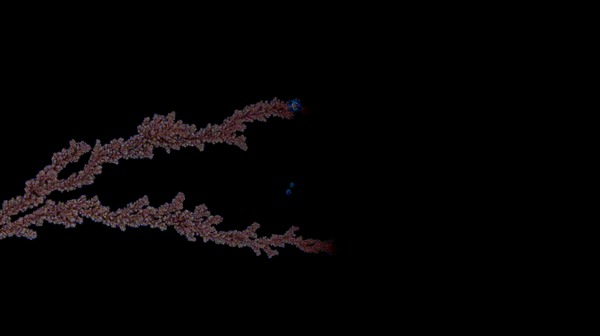
Îáðàçîâàíèå êðèñòàëëîâ îëîâà ïðè ýëåêòðîëèçå ðàñòâîðà õëîðèäà îëîâà â ñåðíîé êèñëîòå

Îáðàçîâàíèå îëîâÿííûõ êðèñòàëëîâ ïîä ìèêðîñêîïîì
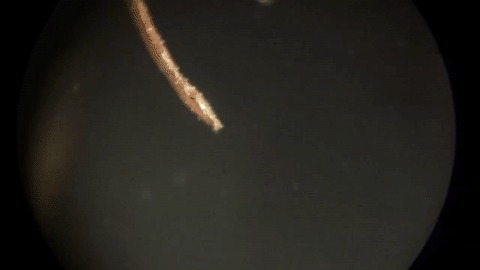
Îáðàçîâàíèå îëîâÿííûõ êðèñòàëëîâ ïðè íèçêîé êîíöåíòðàöèè õëîðèäà îëîâà è ìàëûõ îáúåìàõ ðàñòâîðà (òàêæå óâåëè÷åíî)

Ðåàêöèÿ îëîâà ñ àçîòíîé êèñëîòîé

Ðåàêöèÿ îëîâà ñ ñîëÿíîé êèñëîòîé

Ðåàêöèÿ îëîâà ñ öàðñêîé âîäêîé (ñìåñü àçîòíîé è ñîëÿíîé êèñëîòû) ïðîòåêàåò, îäíàêî, áîëåå áóðíî

«Îëîâÿííàÿ ÷óìà» — îñîáîå ñâîéñòâî ýëåìåíòà, êîòîðîå çàêëþ÷àåòñÿ â òîì, ÷òî ïðè òåìïåðàòóðå íèæå 13,2 °C ìåòàëëè÷åñêîå (áåëîå) îëîâî (β-Sn) ïåðåõîäèò â äðóãîå ôàçîâîå ñîñòîÿíèå ñåðîå îëîâî (α-Sn), â êðèñòàëëè÷åñêîé ðåø¸òêå êîòîðîãî àòîìû ðàñïîëàãàþòñÿ ìåíåå ïëîòíî. Ïðîèñõîäèò ýòî ïðî ïðè÷èíå óâåëè÷åíèÿ óäåëüíîãî îáú¸ìà ÷èñòîãî îëîâà íà 25,6 %

Îëîâî èìååò íåáîëüøóþ òåìïåðàòóðó ïëàâëåíèÿ (232 °C) è ëåãêî ïåðåõîäèò â æèäêîå ñîñòîÿíèå ïîä äåéñòâèåì ïëàìåíè ãîðåëêè

Ãîðåíèå ìàëåíüêîãî êóñî÷êà îëîâà (ìîìåíòàëüíîå îêèñëåíèå)

Ïîêàçàòü ïîëíîñòüþ
6

Ðîñò êðèñòàëëîâ ñåðåáðà íà ìåäíîé ïðîâîëîêå (â ðàñòâîðå íèòðàòà ñåðåáðà)

Ðåàêöèÿ ñåðåáðà ñ àçîòíîé êèñëîòîé (ñ âûäåëåíèåì äèîêñèäà àçîòà)

Îáðàçîâàíèå õëîðèäà ñåðåáðà

Ðåàêöèÿ «Ñåðåáðÿíîå çåðêàëî» (â ïðèñóòñòâèè àëüäåãèäîâ èäåò âîññòàíîâëåíèå ìåòàëëà èç àììèà÷íîãî êîìïëåêñà)

Îáðàçîâàíèå ñóëüôèäà ñåðåáðà ïðè äîáàâëåíèè òèîñóëüôàòà

Îáðàçîâàíèå õðîìàòà ñåðåáðà

Âçðûâ îò íàãðåâàíèÿ àöåòèëåíèäà ñåðåáðà

Îáðàçîâàíèå áðîìèäà è èîäèäà ñåðåáðà

Ñåðåáðî ìîæíî ðàñïëàâèòü õîðîøåé ãàçîâîé ãîðåëêîé

Ïîêàçàòü ïîëíîñòüþ
6
Ðåàêöèÿ
