Какой бывает газ и его свойства

Ïðî íåäàâíåå èçâåñòíîå ñîáûòèå íà Óðàëå — íå áóäó… Òàì ìíîãî âîïðîñîâ áåç îòâåòà…
×òî âîîáùå òàêîå «áûòîâîé ãàç»?
Ýòî ðàçëè÷íûå ãîðþ÷èå ñìåñè, ãàçîîáðàçíûå, îáû÷íî, ïðè òåìïåðàòóðàõ íèæå 0°Ñ, ñ ïîäàâëÿþùèì ñîäåðæàíèåì óãëåâîäîðîäîâ.
 íåêîòîðûõ ãîñóäàðñòâàõ áûòîâîé ãàç ïîëó÷àþò ïóòåì òåðìè÷åñêîé îáðàáîòêè êàìåííîãî óãëÿ…
 Ðîññèè «áûòîâîé ãàç» ïðåäñòàâëåí äâóìÿ îñíîâíûìè òèïàìè ãàçîâûõ ñìåñåé:
— «ìàãèñòðàëüíûì» ïðèðîäíûì ãàçîì — î÷èùåííûì èñêîïàåìûì ìåòàíîì, ñîïðîâîæäàåìûì ðÿäîì ïðèìåñåé;
— ïðîïàí-áóòàíîâûìè ñìåñÿìè äëÿ áûòîâûõ ãàçîâûõ áàëëîíîâ.
Ìåòàí èñòèííî ïðèðîäíûé ãàç, îí íå òîëüêî ñîñòàâëÿåò îñíîâó ñîäåðæàíèÿ ãàçîâîé ôðàêöèè íåôòåãàçâûõ ìåñòîðîæäåíèé (çà ðóáåæîì ÷àñòî èìåíóåòñÿ «íåôòÿíîé ãàç»), íî òàêæå îáðàçóåòñÿ â ïðîöåññå ðàçëîæåíèÿ «ìåòàíîâûìè» áàêòåðèÿìè ïðàêòè÷åñêè âñåãî ñïåêòðà òêàíåé ðàñòèòåëüíîãî è æèâîòíîãî ïðîèñõîæäåíèÿ.
(Íå ïîäíîñèòå îòêðûòîå ïëÿìÿ ê ìàãèñòðàëÿì êàíàëèçàöèè, íå êóðèòå íà áîëîòå. Âìåðçøèå â ëåä ïðóäà/îçåðà «ïóçûðè âîçäóõà», ýòî òîæå ìåòàí).
Äëÿ áûòîâîãî ïîòðåáëåíèÿ ïðèðîäíûé ìåòàí ïîäàåòñÿ ñ íåêîòîðûìè ïðèìåñÿìè, îñòàþùèìèñÿ ïîñëå ôèëüòàöèè îò íåíóæíûõ â æèëèùå êîìïîíåíòîâ è îäîðîðîâàííûé äëÿ öåëè ðàñïîçíàâàíèÿ, â îñíîâíîì, ìåòàíòèîëîì (ýòèëìåðêàïòàíîì).
Íåñêîëüêî ñëîâ ïðî ìåòàíòèîë: ãîðþ÷, ñðåäíåòîêñè÷åí ïðè âûñîêèõ êîíöåíòðàöèÿõ, ïðèìåíÿåòñÿ â êà÷åñòâå îäîðàíòà áûòîâîãî ãàçà ïî òîé ïðè÷èíå, ÷òî äåøåâ è ðàñïîçíàåòñÿ îáîíÿòåëüíîé ñèñòåìîé ÷åëîâåêà óæå ïðè êîíöåíòðàöèè â âîçäóõå 1/1 000 000 (îäíà äîëÿ ê ìèëëèîíó äîëåé âîçäóõà).
Áûòîâîé ãàç â íàèáîëåå ðàñïðîñòðàíåííûõ áàëëîíàõ íèçêîãî äàâëåíèÿ, ñ ìàëûì ñîîòíîøåíèåì äëèíà/äèàìåðò («ïóçàòûå» áàëëîíû) — ýòî ïðîïàí-áóòàí è åãî èçîìåðû — ïåðåðàáîòàííûé ìåòàí. Äàâëåíèå â çàïðàâëåííîì áàëëîíå ñ ïðîáàí-áóòàíîì, ïðè 20°C -îêîëî 5 àòì.
Ìåòàí ïåðåðàáàòûâàþò â ïðîïàí-áóòàí ïîòîìó, ÷òî ìåòàíîâûå ñìåñè ñæèæàþòñÿ ïðè äàâëåíèè, â ñðåäíåì, â 45 ðàç áîëüøåì, ÷åì ïðîïàí-áóòàíîâûå.
Äëÿ áûòîâîãî «áàëîííîãî» ïðèìåíåíèÿ, äàâëåíèå ïîòðåáëÿåìîé ãàçîâîé ñóáñòàíöèè â 200-250 àòìîñôåð ÿâíî íå ïîäõîäèò è ñåãîäíÿ, à 20, 30, 50 ëåò íàçàä, íå ïîäõîäèëî òåì áîëåå.
Ïðîïàí-Áóíàíîâûå ñìåñè áûòîâîãî ïðèìåíåíèÿ òàêæå äåîäîðèðóþòñÿ ìåòàíòèîëîì.
Äàâëåíèå «íà ôîðñóíêå» áûòîâîé ãàçîâîé ïëèòû, ïðè êîòîðîì ïðîèñõîäèò áûòîâîå ïîòðåáëåíèå òîïëèâíûõ ãàçîâûõ ñìåñåé, ïðèìåðíî îäèíàêîâî è äëÿ ìåòàíà, è äëÿ ïðîïàí-áóòàíà — 0.05 àòì. (Äàâëåíèå íåñïåøíî âûäûõàåìîãî âîçäóõà â íîçäðå ÷åëîâåêà çíà÷èòåëüíî âûøå).
Ïðè ðàñòâîðåíèè â âîçäóõå æèëîãî ïîìåùåíèÿ, ìåòàí â ðàçû ìåíåå âçðûâîîïàñåí, ÷åì ïðîïàí-áóòàí.
Ýòî îñíîâíàÿ ïðè÷èíà, ïî êîòîðîé ìàãèñòðàëüíî-ãàçèôèöèðîâàííîå æèëüå ñíàáæàåòñÿ ìåòàíîâîé ñìåñüþ, à íå ïðîïàí-áóòàíîâîé.
(Çàáëóæäåíèå — ïîëàãàòü, ÷òî àâòîíîìíàÿ ãàçèôèêàöèÿ æèëèùà ïðîïàí-áóòàíîì èäåíòè÷íà ïî áåçîïàñíîñòè ìàãèñòðàëüíîìó ïðèðîäíîìó ãàçó. Íå èäåíòè÷íà. Îïàñíåå. Íàìíîãî.).
Ñîçäàòü âîñïëàìåíÿþùóþñÿ êîíöåíòðàöþ ìåòàíà â æèëîì ïîìåùåíèè, ñ ó÷åòîì îñíîâíûõ âëèÿþùèõ ôàêòîðîâ, â ñðåäíåì, â ïÿòü ðàç ñëîæíåå, ÷åì — êîíöåíòðàöèþ ïðîïàí-áóòàíà.
Ãðóáî ãîâîðÿ, íóæíî âûïóñòèòü â ïîìåùåíèå â ïÿòü ðàç áîëüøå ãàçà.
Ñ ó÷åòîì òîãî, ÷òî îáúåìíîå ñîäåðæàíèå îäîðàíòà áóäåò òàêæå â 5 ðàç áîëüøå, âåðîÿòíîñòü âçðûâà áûòîâîé ìåòàíîâîé ñìåñè â æèëîì ïîìåùåíèè, íà ïðàêòèêå, â 10 — 20 ðàç ìåíüøå, â ñðàâíåíèè ñî ñìåñüþ ïðîïàí-áóòàíà.
Òàêèì îáðàçîì, åñëè äëÿ ïîìåùåíèé ñ ìåòàíîâûì ãàçîñíàáæåíèåì, ñèãíàëèçàòîðîì óòå÷êè ðàñòâîðåííûõ â âîçäóõå óãëåâîäîðîäîâ ìîæíî ïðåíåáðå÷ü, òî ïðè ïðîïàí-áóòàíîâîì ãàçîñíàáæåíèè ãàçîàíàëèçàòîð íàñòîÿòåëüíî ðåêîìåíäóåì!
Ñ òî÷êè çðåíèÿ îñíîâíîé îïàñíîñòè äëÿ çäîðîâüÿ ïðè âäûõàíèè ìåòàí è ïðîïàí-áóòàí ïðàêòè÷åñêè èäåíòè÷íû. Èõ òîêñè÷åñêîå äåéñòâèå îáóñëîâëåíî çàìåùåíèåì ñîáîé ïîòðåáíîãî îðãàíèçìó îáúåìà âîçäóøíîé ãàçîâîé ñìåñè. Êðîìå òîãî, âûçûâàÿ ãèïîêñèþ è ñâÿçàííóþ ñ íåé ýéôîðèþ, íåäûõàòåëüíàÿ ãàçîâàÿ ñìåñü áëîêèðóåò ðàñïîçíàâàíèå ñîçíàíèåì ôàêòîâ ïðîãðåññèðóþùèõ ïåðåáîåâ â ðàáîòå ñåðäöà è îñòàíîâêè äûõàíèÿ.
Ó áîëüøîãî ÷èñëà ëþäåé îòêàç ÖÍÑ è ñåðäå÷íîé ìûøöû ìîæåò íàñòóïàòü ïðåæäå ïðî÷èõ ñèìïòîìîâ ãèïîêñèè, ò.å. åùå äî ýéôîðèè, ÿâëÿþùåéñÿ ñèãíàëèçàòîðîì îòðàâëåíèÿ…
Ñîáëþäàéòå ïðàâèëà… Áåðåãèòå ñåáÿ è áëèçêèõ.
(Ïðî ãàç â áàëëîíàõ ïîñòàðàþñü ñêîðî íàïèñàòü îòäåëüíóþ ñòàòüþ).
Введение 2
Состав
и физические свойства природного газа 3
Химический
состав 3
Физические
свойства 3
Приро́дный
газ — смесь газов, образовавшаяся в
недрах земли при анаэробном разложении
органических веществ. Природный газ
относится к полезным ископаемым, одно
из важнейших горючих ископаемых,
занимающее ключевые позиции в
топливно-энергетических балансах многих
государств. Природный газ является
важным сырьем для химической промышленности.
В пластовых условиях (условиях залегания
в земных недрах) находится в газообразном
состоянии — в виде отдельных скоплений
(газовые залежи) или в виде газовой шапки
нефтегазовых месторождений, либо в
растворённом состоянии в нефти или
воде.
Энергетическая
и химическая ценность природного газа
определяется содержанием в нём
углеводородов. Очень часто в месторождениях
он сопутствует нефти. Разница в составе
природного и попутного нефтяного газа
имеется. В последнем, как правило, больше
сравнительно тяжёлых углеводородов,
которые обязательно отделяются, прежде
чем использовать газ.
Состав и физические свойства природного газа Химический состав
Природные
углеводородные газы представляют собой
смесь предельных углеводородов вида
СnН2n+2. Основную часть природного газа
составляет метан CH4 — до 98 %.
В
состав природного газа могут также
входить более тяжёлые углеводороды —
гомологи метана: — этан (C2H6), — пропан
(C3H8), — бутан (C4H10), а также другие
неуглеводородные вещества: — водород
(H2), — сероводород (H2S), — диоксид углерода
(СО2), — азот (N2), — гелий (Не)
Чистый
природный газ не имеет цвета и запаха.
Чтобы можно было определить утечку по
запаху, в газ добавляют небольшое
количество веществ, имеющих сильный
неприятный запах, так называемых
одорантов. Чаще всего в качестве одоранта
применяется этилмеркаптан.
Физические свойства
Ориентировочные
физические характеристики (зависят от
состава; при нормальных условиях, если
не указано иное):
Плотность:
от
0,68 до 0,85 кг/м³ (сухой газообразный);
400
кг/м³ (жидкий).
Температура
кипения при атмосферном давлении: –162°C
Температура
самовозгорания: 650 °C;
Взрывоопасные
концентрации смеси газа с воздухом от
5 % до 15 % объёмных;
Удельная
теплота сгорания: 28—46 МДж/м³ (6,7—11,0
ккал/м³) (то есть 8-12 квт·ч/м³);
Октановое
число при использовании в двигателях
внутреннего сгорания: 120—130.
Легче
воздуха в 1,8 раз, поэтому при утечке не
собирается в низинах, а поднимается
вверх.
Природные
газы подразделяют на следующие группы:
1.
Газ, добываемый из чисто газовых
месторождений и представляющий собой
сухой газ, свободный от тяжелых
углеводородов.
2.
Газы, добываемые вместе с нефтью
(растворенные или попутные газы). Это
физические смеси сухого газа,
пропанобутановой фракции (жирного газа)
и газового бензина.
3.
Газы, добываемые из газоконденсатных
месторождений — смесь сухого газа и
жидкого углеводородного конденсата.
Углеводородный конденсат состоит из
большого числа тяжелых углеводородов
(С5 + высш., С6 + высш. и т.д.), из которых
можно выделить бензиновые, лигроиновые,
керосиновые, а иногда и более тяжелые
масляные фракции.
4.
Газы газогидратных залежей.
Компонентный
состав и свойства отдельных компонентов
природного газа приведены в таблице 1.
Таблица
1. Основные свойства компонентов природных
газов в стандартных условиях
Свойство | Обозначение | CH4 | C2H6 | C3H8 | i-C4H10 | n-C4H10 |
Молекулярная | М | 16,04 | 30,07 | 44,10 | 58,12 | 58,12 |
Объем | V | 1,40 | 0,74 | 0,51 | 0,39 | 0,39 |
Плотность | 0,554 | 1,038 | 1,522 | 2,006 | 2,006 | |
Масса | m | 0,71 | 1,35 | 1,97 | 2,85 | 2,85 |
Критическое | ркр | 4,58 | 4,86 | 4,34 | 3,85 | 3,57 |
Критическая | Ткр | 191 | 305 | 370 | 407 | 425 |
Во
многих случаях состав природных
углеводородных газов определяется не
полностью, а лишь до бутана (С4Н10) или
гексана (С6Н14) включительно, а все
остальные компоненты объединяются в
остаток (или псевдокомпонент).
Газ,
в составе которого тяжелые углеводороды
составляют не более 75 г/м3, называют
сухим.
При
содержании тяжелых углеводородов более
150 г/м3 газ называют жирным.
Газовые
смеси характеризуются массовыми или
молярными концентрациями компонентов.
Для характеристики газовой смеси
необходимо знать ее среднюю молекулярную
массу, среднюю плотность в килограммах
на кубический метр или относительную
плотность по воздуху.
Молекулярная
масса М
природного
газа:
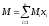 ,
,
где
М – молекулярная масса i-го
компонента; xi
– объемное содержание i-го
компонента, доли ед.
Для
реальных газов обычно М=16 – 20.
Плотность
газа ρг
рассчитывается по формуле:
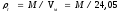 ,
,
где
Vм
– объем 1 моля газа при стандартных
условиях.
Обычно
ρг
находится в пределах 0,73 – 1,0 кг/м3.
Плотность
газа в значительной степени зависит от
давления и температуры, и поэтому для
практического применения этот показатель
неудобен. Чаще пользуются относительной
плотностью газа по воздуху ρг.в.,
равной отношению плотности газа ρг
к плотности воздуха ρв,
взятой при тех же давлении и температуре:
ρг.в.
= ρг
/ ρв,
Если
ρг
и ρв
определяются при стандартных условиях,
то ρв
= 1,293 кг/м3 и ρг.в.
= ρг
/ 1,293.
Плотность
нефтяных газов колеблется от 0,554 (для
метана) до 2,006 (для бутана) и выше.
Вязкость
газа характеризует силы взаимодействия
между молекулами газа, которые
преодолеваются при его движении. Она
увеличивается при повышении температуры,
давления и содержания углеводородных
компонентов. Однако при давлениях выше
3МПа увеличение температуры вызывает
понижение вязкости газа.
Вязкость
нефтяного газа незначительна и при 0оС
составляет 0,000131 пз; вязкость воздуха
при 0оС равна 0,000172 пз.
Уравнения
состояния газов используются для
определения многих физических свойств
природных газов. Уравнением состояния
называется аналитическая зависимость
между параметрами газа, описывающая
поведение газа. Такими параметрами
являются давление, объем и температура.
Состояние
идеальных газов в условиях высоких
давления и температуры определяется
уравнением Клапейрона — Менделеева:
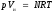 ,
,
где
р
—
давление; Vи
— объем идеального газа, N—
число киломолей газа; R—
универсальная газовая постоянная; Т
—
температура.
Идеальным
называется газ, силами взаимодействия
между молекулами которого пренебрегают.
Реальные углеводородные газы не
подчиняются законам идеальных газов.
Поэтому уравнение Клапейрона—Менделеева
для реальных газов записывается в виде:
pV
= ZNRT,
где
Z
—
коэффициент сверхсжимаемости реальных
газов, зависящий от давления, температуры
и состава газа и характеризующий степень
отклонения реального газа от закона
для идеальных газов.
Коэффициент
сверхсжимаемости Z
реальных
газов — это отношение объемов равного
числа молей реального V
и
идеального Vи
газов при одинаковых термобарических
условиях (т. е. при одинаковых давлении
и температуре):
Z
= V/Vи
Значения
коэффициентов сверхсжимаемости наиболее
надежно могут быть определены на основе
лабораторных исследований пластовых
проб газов. При отсутствии таких
исследований (как это чаще всего бывает
на практике) прибегают к расчетному
методу оценки Z
по
графику Г. Брауна (рис.1). Для пользования
графиком, необходимо знать, так называемые,
приведенные псевдокритическое давление
и псевдокритическую температуру.
Критической
называется
такая температура,
выше
которой газ не может быть превращен в
жидкость ни при каком давлении. Критическим
давлением называется
давление, соответствующее критической
точке перехода газа в жидкое состояние.
С
приближением значений давления и
температуры к критическим свойства
газовой и жидкой фаз становятся
одинаковыми, поверхность раздела между
ними исчезает и плотности их уравниваются.
С
появлением в системе двух и более
компонентов в закономерностях фазовых
изменений возникают особенности,
отличающие их поведение от поведения
однокомпонентного газа. Не останавливаясь
на подробностях, следует отметить, что
критическая температура смеси находится
между критическими температурами
компонентов, а критическое давление
смеси всегда выше, чем критическое
давление любого компонента.
Для
определения коэффициента сверхсжимаемости
Z
реальных газов, представляющих собой
многокомпонентную смесь, находят средние
из значений критических давлений и
температур каждого компонента. Эти
средние называются псевдокритическим
давлением pп.кр.
и псевдокритической температурой Тп.кр.
Они определяются из соотношений:
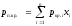 ,
,
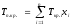 ,
,
природный
газ метан состав
где
ркр. и Ткр. – критические давления и
температура i-го
компонента; xi
– доля i-го
компонента в объеме смеси (в долях
единицы).
Приведенные
псевдокритические давление и температура,
необходимые для пользования графиком
Брауна, представляют собой псевдокритические
значения, приведенные к конкретным
давлению и температуре (к пластовым,
стандартным или каким-либо другим
условиям):
Рпр.
= р/рп.кр.,
Тпр.
= Т/Тп.кр.,
где
р и Т – конкретные давления и температура,
для которых определяется Z.
Коэффициент
сверхсжимаемости Z
обязательно используется при подсчете
запасов газа для правильного определения
изменения объема газа при переходе от
пластовых условий к поверхностным, при
прогнозировании изменения давления в
газовой залежи и при решении других
задач.
Применение
Метан
используется как горючее в газовых
плитах.
Пропан
и бутан – в качестве топлива в некоторых
автомобилях. Также сжиженным пропаном
заполняют зажигалки.
Этан
в качестве горючего используют редко,
основное его применение – получение
этилена.
Этилен
является одним из самых производимых
органических веществ в мире. Он является
сырьём для получения полиэтилена.
Ацетилен
используется для создания очень высокой
температуры в металлургии (сверка и
резка металлов). Ацетилен очень горюч,
поэтому в качестве топлива в автомобилях
не используется, да и без этого условия
его хранения должны строго
соблюдаться.
Сероводород,
несмотря на его токсичность, в малых
количествах применяется в т.н.
сероводородных ваннах. В них используются
некоторые антисептические свойства
сероводорода.
Основным
полезным свойством гелия является его
очень маленькая плотность (в 7 раз легче
воздуха). Гелием заполняют аэростаты и
дирижабли. Водород ещё более лёгок, чем
гелий, но в то же время горюч. Большую
популярность среди детей имеют воздушные
шарики, надуваемые гелием.
Токсичность
Углекислый
газ. Даже большие количества углекислого
газа никак не влияют на здоровье человека.
Однако он препятствует поглощению
кислорода при содержании в атмосфере
от 3% до 10% по объёму. При такой концентрации
начинается удушье и даже смерть.
Гелий.
Гелий абсолютно нетоксичен при нормальных
условиях из-за его инертности. Но при
повышенном давлении возникает начальная
стадия наркоза, похожая на воздействие
веселящего газа.
Сероводород.
Токсичные свойства этого газа велики.
При длительном воздействии на обоняние
возникает головокружение, рвота. Также
парализуется обонятельный нерв, поэтому
возникает иллюзия отсутствия сероводорода,
а на самом деле организм его уже просто
не ощущает. Отравление сероводородом
наступает при концентрации 0,2–0,3 мг/м3,
концентрация выше 1 мг/м3 — смертельна.
Процесс
горения
Все
углеводороды при полном окислении
(избыток кислорода) выделяют углекислый
газ и воду. Например:
CH4
+ 3O2 = CO2 + 2H2O
При
неполном (недостаток кислорода) — угарный
газ и воду:
2CH4
+ 6O2 = 2CO + 4H2O
При
ещё меньшем количестве кислорода
выделяется мелкодисперсный углерод
(сажа):
CH4
+ O2 = C + 2H2O.
Метан
горит голубым пламенем, этан — почти
бесцветным, как спирт, пропан и бутан —
жёлтым, этилен — светящимся, угарный газ
— светло-голубым. Ацетилен — желтоватым,
сильно коптит. Если у Вас дома стоит
газовая плита и вместо обычного голубого
пламени вы видите жёлтое — знайте, это
метан разбавляют пропаном.
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
Áëàãîðîäíûå ãàçû (èíåðòíûå ëèáî ðåäêèå ãàçû) — ãðóïïà õèìè÷åñêèõ ýëåìåíòîâ ñ ïîõîæèìè ñâîéñòâàìè: ïðè íîðìàëüíûõ óñëîâèÿõ îíè ÿâëÿþòñÿ îäíîàòîìíûìè ãàçàìè. Ýòî õèìè÷åñêèå ýëåìåíòû, êîòîðûå îáðàçóþò ãëàâíóþ ïîäãðóïïó 8-é ãðóïïû ïåðèîäè÷åñêîé ñèñòåìû Ìåíäåëååâà.
Ïðè îáû÷íûõ óñëîâèÿõ — ýòî ãàçû áåç öâåòà, âêóñà è çàïàõà, ïëîõî ðàñòâîðèìûå â âîäå, íå âîçãîðàþòñÿ ïðè íîðìàëüíûõ óñëîâèÿõ, ñ î÷åíü íèçêîé õèìè÷åñêîé ðåàêòèâíîñòüþ. Èõ òåìïåðàòóðû ïëàâëåíèÿ è êèïåíèÿ çàêîíîìåðíî óâåëè÷èâàþòñÿ ñ óâåëè÷åíèåì àòîìíîãî íîìåðà.
Ñðåäè âñåõ áëàãîðîäíûõ ãàçîâ ëèøü ó Rn íåò ñòàáèëüíûõ èçîòîïîâ è òîëüêî îí ÿâëÿåòñÿ ðàäèîàêòèâíûì õèìè÷åñêèì ýëåìåíòîì.
Ðåäêèìè (èíåðòíûìè) ãàçàìè ÿâëÿþòñÿ:
- ãåëèé (He) (àòîìíûé íîìåð 2),
- íåîí (Ne) (10),
- àðãîí (Ar) (18),
- êðèïòîí (Kr) (36),
- êñåíîí (Xe) (54)
- ðàäèîàêòèâíûé ðàäîí (Rn) (86).
 ïîñëåäíåå âðåìÿ ê ýòîé ãðóïïå òàêæå ïðè÷èñëÿþò óíóíîêòèé (Uuo) (118).
Âñå èíåðòíûå ãàçû ñîáîé çàâåðøàþò ñîîòâåòñòâóþùèé ïåðèîä â Ïåðèîäè÷åñêîé ñèñòåìå è èìåþò ïîëíîñòüþ çàâåðøåííûé, óñòîé÷èâûé âíåøíèé ýëåêòðîííûé óðîâåíü.
Ó èíåðòíûõ ãàçîâ ýëåêòðîííàÿ êîíôèãóðàöèÿ ns2np6 (ó ãåëèÿ 1s2) è îíè îáðàçóþò VIIIÀ ãðóïïó. Ñ âîçðàñòàíèåì ïîðÿäêîâîãî íîìåðà óâåëè÷èâàþòñÿ ðàäèóñû àòîìîâ è èõ ñïîñîáíîñòü ê ïîëÿðèçóåìîñòè, ÷òî ïðèâîäèò ê óâåëè÷åíèþ ìåæìîëåêóëÿðíûõ âçàèìîäåéñòâèé, ê óâåëè÷åíèþ Òïë è Òêèï, ê óëó÷øåíèþ ðàñòâîðèìîñòè ãàçîâ â âîäå è äðóãèõ ðàñòâîðèòåëÿõ. Äëÿ èíåðòíûõ ãàçîâ ñóùåñòâóþò òàêèå èçâåñòíûå ãðóïïû ñîåäèíåíèé: ìîëåêóëÿðíûå èîíû, ñîåäèíåíèÿ âêëþ÷åíèÿ, âàëåíòíûå ñîåäèíåíèÿ.
Èíåðòíûå ãàçû îòíîñÿòñÿ ê ïîñëåäíåé ïðè ýòîì îíè çàíèìàþò ïåðâûå 6 ïåðèîäîâ è îòíîñÿòñÿ ê 18-é ãðóïïå â ïåðèîäè÷åñêîé òàáëèöå õèìè÷åñêèõ ýëåìåíòîâ. Ôëåðîâèé — ýëåìåíò 14-é ãðóïïû ïîêàçûâàåò íåêîòîðûå ñâîéñòâà áëàãîðîäíûõ ãàçîâ, ïîýòîìó îí ñïîñîáåí çàìåíèòü â ïåðèîäè÷åñêîé òàáëèöå óíóíîêòèé. Áëàãîðîäíûå ãàçû íåàêòèâíû õèìè÷åñêè è ìîãóò ïðèíèìàòü ó÷àñòèå â õèìè÷åñêèõ ðåàêöèÿõ òîëüêî â ýêñòðåìàëüíûõ óñëîâèÿõ.
Öâåòà è ñïåêòðû èíåðòíûõ ãàçîâ.
Öâåòà è ñïåêòðû áëàãîðîäíûõ ãàçîâ.  ïåðâîé ñòðîêå òàáëèöû èçîáðàæåíû áëàãîðîäíûå ãàçû â êîëáàõ, ÷åðåç êîòîðûå ïðîïóùåí òîê, âî âòîðîé — ñàì ãàç â òðóáêå, â òðåòüåé — â òðóáêàõ, êîòîðûå èçîáðàæàþò îáîçíà÷åíèå ýëåìåíòà â ïåðèîäè÷åñêîé òàáëèöå Ìåíäåëååâà.
Ãåëèé | Íåîí | Àðãîí | Êðèïòîí | Êñåíîí |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Ðàñïðîñòðàíåííîñòü èíåðòíûõ (ðåäêèõ) ãàçîâ â ïðèðîäå.
Èç-çà òîãî, ÷òî èíåðòíûå ãàçû îáëàäàþò õèìè÷åñêîé èíåðòíîñòüþ, èõ äîâîëüíî äîëãî íå ïîëó÷àëîñü îáíàðóæèòü, è èõ îòêðûòèå ñîñòîÿëîñü ëèøü âî 2-é ïîëîâèíå XIX âåêà.
Ãåëèé – ÿâëÿåòñÿ âòîðûì (ïîñëå âîäîðîäà) ïî ðàñïðîñòðàíåííîñòè ýëåìåíòîì âî Âñåëåííîé, â çåìíîé êîðå ñîäåðæàíèå ãåëèÿ ñîñòàâëÿåò ëèøü 1 · 10-6 ìàññ. %. Ãåëèé ÿâëÿåòñÿ ïðîäóêòîì ðàäèîàêòèâíîãî ðàñïàäà è ñîäåðæèòñÿ â ïóñòîòàõ ãîðíûõ ïîðîä è â ïðèðîäíîì ãàçå.
Âñå áëàãîðîäíûå ãàçû ÿâëÿþòñÿ ñîñòàâëÿþùèìè âîçäóõà. Â 1 ì3 âîçäóõà íàõîäèòñÿ 9,3 ë àðãîíà, 18 ìë íåîíà, 5 ìë ãåëèÿ, 1 ìë êðèïòîíà è 0,09 ìë êñåíîíà. Ñîëíöå ïðèáëèçèòåëüíî íà 10% ñîñòîèò èç ãåëèÿ, îáðàçóþùèéñÿ èç âîäîðîäà ïî ðåàêöèè ÿäåðíîãî ñèíòåçà:
(β+ — ïîçèòðîí, — àíòèíåéòðèíî).  ñïåêòðå èçëó÷åíèÿ Ñîëíöà äîâîëüíî èíòåíñèâíî ïðîÿâëÿþòñÿ ëèíèè ãåëèÿ, êîòîðûå áûëè âïåðâûå îáíàðóæåíû â 1868 ã. Íà Çåìëå ãåëèé áûë íàéäåí òîëüêî â 1895 ã. ïðè ñïåêòðàëüíîì àíàëèçå ãàçîâ, âûäåëÿþùèõñÿ ïðè ðàñòâîðåíèè â êèñëîòàõ ìèíåðàëà êëåâåèòà U2Î3. Óðàí, âõîäÿùèé â ñîñòàâ ìèíåðàëà, ñàìîïðîèçâîëüíî ðàñïàäàåòñÿ ïî óðàâíåíèþ:
238U → 234Th + 4He.
 íåáîëüøîì êîëè÷åñòâå îíè ïðèñóòñòâóþò â âîçäóõå è íåêîòîðûõ ãîðíûõ ïîðîäàõ, à òàêæå â àòìîñôåðàõ íåêîòîðûõ ïëàíåò-ãèãàíòîâ.
Ïðîìûøëåííîå èñïîëüçîâàíèå èíåðòíûõ ãàçîâ îñíîâàíî íà èõ íèçêîé õèìè÷åñêîé àêòèâíîñòè èëè ñïåöèôè÷åñêèõ ôèçè÷åñêèå ñâîéñòâàõ.
Íåêîòîðûå õàðàêòåðèñòèêè ýëåìåíòîâ VIIIÀ ïîäãðóïïû (èíåðòíûõ ãàçîâ).
Ýëåìåíò | Ðàäèóñ àòîìà, íì | Ïåðâûé ïîòåíöèàë èîíèçàöèè, ýÂ | Tïë., K | Têèï., K | Îòíîñèòåëüíàÿ ïîëÿðèçóåìîñòü àòîìà, óñë. åä. | Ýíåðãèÿ âîçáóæäåííîãî ýëåêòðîíà, ýÂ |
Ãåëèé, He | 0,122 | 24,58 | – | 4,18 | 1 | – |
Íåîí, Ne | 0,160 | 21,56 | 24 | 27,18 | 2 | 16,6 |
Àðãîí, Ar | 0,192 | 15,76 | 34 | 97,29 | 3 | 11,5 |
Êðèïòîí, Kr | 0,198 | 14,00 | 116 | 120,26 | 12 | 9,9 |
Êñåíîí, Xe | 0,218 | 12,13 | 162 | 166,06 | 20 | 8,3 |
Óíèêàëüíûìè ôèçè÷åñêèìè ñâîéñòâàìè îáëàäàåò ãåëèé. Âî ïåðâûõ, ýòî — åäèíñòâåííîå èç èçâåñòíûõ â ïðèðîäå âåùåñòâ, êîòîðîå îñòàåòñÿ æèäêèì ïðè ñàìûõ íèçêèõ òåìïåðàòóðàõ, âïëîòü äî 0 Ê. Îí êðèñòàëëèçóåòñÿ òîëüêî ïîä äàâëåíèåì 25 àòì. Âî-âòîðûõ, ãåëèé èìååò ñàìóþ íèçêóþ èç âñåõ âåùåñòâ òåìïåðàòóðó êèïåíèÿ. Íàêîíåö, ñàìîå èíòåðåñíîå ñâîéñòâî ãåëèÿ — ñâåðõòåêó÷åñòü. Ïðè òåìïåðàòóðàõ íèæå 2,2 Ê æèäêèé 4Íå ñóùåñòâóåò â âèäå ñìåñè äâóõ æèäêîñòåé, îäíà èç êîòîðûõ èìååò îáû÷íûå ñâîéñòâà, à äðóãàÿ — àíîìàëüíûå. Ñâåðõòåêó÷àÿ êîìïîíåíòà æèäêîãî ãåëèÿ èìååò ïðàêòè÷åñêè íóëåâóþ âÿçêîñòü (â 10 ìëðä. ðàç ìåíüøå, ÷åì ó âîäû). Ýòî âåùåñòâî ñïîñîáíî ïðîñà÷èâàòüñÿ ÷åðåç ìåëü÷àéøèå îòâåðñòèÿ â ïîðèñòîì ñîñóäå, îíî ñàìîïðîèçâîëüíî âûòåêàåò èç íåïîðèñòîãî ñîñóäà, ïîäíèìàÿñü ââåðõ ïî åãî ñòåíêàì, è îáëàäàåò ñâåðõâûñîêîé òåïëîïðîâîäíîñòüþ.
Ýëåêòðîííîå ñòðîåíèå áëàãîðîäíûõ ãàçîâ.
Íàçâàíèå | Ýëåêòðîííàÿ êîíôèãóðàöèÿ | Ðàäèóñ àòîìà, íì | Ïîòåíöèàë èîíèçàöèè, ýÂ | Ñòåïåíè îêèñëåíèÿ |
Ãåëèé Íå | 1s2 | 0,122 | 24,6 | |
Íåîí Ne | [Íå]2s22p6 | 0,160 | 21,6 | |
Àðãîí Àr | [Nå]3s23p6 | 0,191 | 15,8 | |
Êðèïòîí Êr | [Ar]3d104s24ð6 | 0,198 | 14,0 | +2,+4 |
Êñåíîí Õå | [Êr]4d105s25p6 | 0,209 | 12,1 | +2,+4,+6,+8 |
Ðàäîí Rn | [Õå]4f145d106s26ð6 | — | 10,8 | +2,+4,+6 |