Какое вещество способно проявлять свойства альдегидов и карбоновых кислот

Химические свойства альдегидов и кетонов
Альдегидами называют соединения, молекулы которых содержат карбонильную группу, соединенную с атомом водорода, т.е. общая формула альдегидов может быть записана как
где R – углеводородный радикал, который может быть разной степени насыщенности, например, предельный или ароматический.
Группу –СНО называют альдегидной.
Кетоны – органические соединения, в молекулах которых содержится карбонильная группа, соединенная с двумя углеводородными радикалами. Общую формулу кетонов можно записать как:
где R и R’ – углеводородные радикалы, например, предельные (алкилы) или ароматические.
Гидрирование альдегидов и кетонов
Альдегиды и кетоны могут быть восстановлены водородом в присутствии катализаторов и нагревании до первичных и вторичных спиртов соответственно:
Окисление альдегидов
Альдегиды легко могут быть окислены даже такими мягкими окислителями, как гидроксид меди и аммиачный раствор оксида серебра.
При нагревании гидроксида меди с альдегидом происходит исчезновение изначального голубого окрашивания реакционной смеси, при этом образуется кирпично-красный осадок оксида одновалентной меди:
В реакции с аммиачным раствором оксида серебра вместо самой карбоновой кислоты образуется ее аммонийная соль, поскольку находящийся в растворе аммиак реагирует с кислотами:
Кетоны в реакцию с гидроксидом меди (II) и аммиачным раствором оксида серебра не вступают. По этой причине эти реакции являются качественными на альдегиды. Так реакция с аммиачным раствором оксида серебра при правильной методике ее проведения приводит к образованию на внутренней поверхности реакционного сосуда характерного серебряного зеркала.
Очевидно, что если мягкие окислители могут окислить альдегиды, то само собой это могут сделать и более сильные окислители, например, перманганат калия или дихромат калия. При использовании данных окислителей в присутствии кислот образуются карбоновые кислоты:
Химические свойства карбоновых кислот
Карбоновыми кислотами называют производные углеводородов, содержащие одну или несколько карбоксильных групп.
Карбоксильная группа:
Как можно видеть, карбоксильная группа состоит из карбонильной группы –С(О)- , соединенной с гидроксильной группой –ОН.
В связи с тем, что к гидроксильной группе непосредственно прикреплена карбонильная, обладающая отрицательным индуктивным эффектом связь О-Н является более полярной, чем в спиртах и фенолах. По этой причине карбоновые кислоты обладают заметно более выраженными, чем спирты и фенолы, кислотными свойствами. В водных растворах они проявляют свойства слабых кислот, т.е. обратимо диссоциируют на катионы водорода (Н+) и анионы кислотных остатков:
Реакции образования солей
С образованием солей карбоновые кислоты реагируют с:
1) металлами до водорода в ряду активности:
2) аммиаком
3) основными и амфотерными оксидами:
4) основными и амфотерными гидроксидами металлов:
5) солями более слабых кислот – карбонатами и гидрокарбонатами, сульфидами и гидросульфидами, солями высших (с большим числом атомов углерода в молекуле) кислот:
Систематические и тривиальные названия некоторых кислот и их солей представлены в следующей таблице:
| Формула кислоты | Название кислоты тривиальное/систематическое | Название соли тривиальное/систематическое |
| HCOOH | муравьиная/ метановая | формиат/ метаноат |
| CH3COOH | уксусная/ этановая | ацетат/ этаноат |
| CH3 CH2COOH | пропионовая/ пропановая | пропионат/ пропаноат |
| CH3 CH2 CH2COOH | масляная/ бутановая | бутират/ бутаноат |
Следует помнить и обратное: сильные минеральные кислоты вытесняют карбоновые кислоты из их солей как более слабые:
Реакции с участием ОН группы
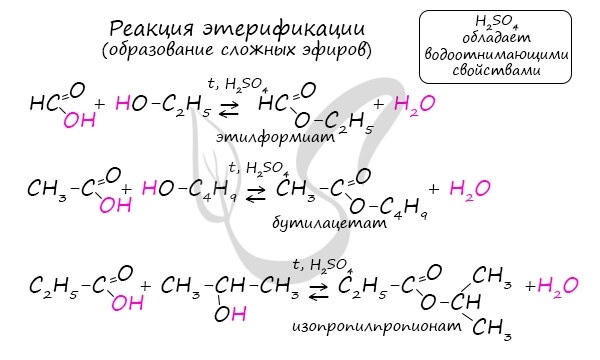
Карбоновые кислоты вступают в реакцию этерификации с одноатомными и многоатомными спиртами в присутствии сильных неорганических кислот, при этом образуются сложные эфиры:
Данного типа реакции относятся к обратимым, в связи с чем с целью смещения равновесия в сторону образования сложного эфира их следует осуществлять, отгоняя более летучий сложный эфир при нагревании.
Обратный реакции этерификации процесс называют гидролизом сложного эфира:
Необратимо данная реакция протекает в присутствии щелочей, поскольку образующаяся кислота реагирует с гидроксидом металла с образованием соли:
Реакции замещения атомов водорода в углеводородном заместителе
При проведении реакций карбоновых с хлором или бромом в присутствии красного фосфора при нагревании происходит замещение атомов водорода при α-атоме углерода на атомы галогена:
В случае большей пропорции галоген/кислота может произойти и более глубокое хлорирование:
Реакции разрушения карбоксильной группы (декарбоксилирование)
Особые химические свойства муравьиной кислоты
Молекула муравьиной кислоты, несмотря на свои малые размеры, содержит сразу две функциональные группы:
В связи с этим она проявляет не только свойства кислот, но также и свойства альдегидов:
При действии концентрированной серной кислоты муравьиная кислота разлагается на воду и угарный газ:
Карбоновые кислоты — класс органических соединений, молекулы которых содержат одну или несколько карбоксильных групп
COOH.
Имеют разнообразное промышленное применение и большое биологическое значение.
Общая формула одноосновных карбоновых кислот CnH2nO2 .
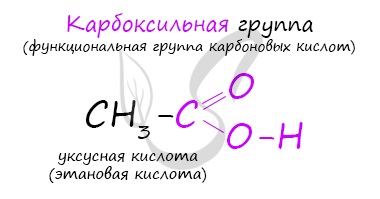
Классификация карбоновых кислот
По количеству карбоксильных групп в молекуле карбоновые кислоты подразделяются на:
- Одноосновные — 1 карбоксильная группа
- Двухосновные — 2 карбоксильных группы
- Трехосновные — 3 карбоксильных группы
Высшие карбоновые кислоты называют жирными кислотами. Более подробно мы изучим их теме, посвященной жирам, в состав
которых они входят.
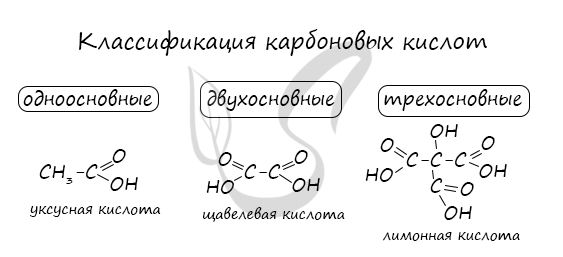
Номенклатура и изомерия карбоновых кислот
Названия карбоновых кислот формируются путем добавления суффикса «овая» к названию алкана с соответствующим числом атомов углерода
и слова кислота: метановая кислота, этановая кислота, пропановая кислота, и т.д.
Многие карбоновые кислоты имеют тривиальные названия. Наиболее известные:
- Метановая — HCOOH — муравьиная кислота
- Этановая — CH3-COOH — уксусная кислота
- Пропановая — C2H5-COOH — пропионовая кислота
- Бутановая — C3H7-COOH — масляная кислота
- Пентановая — C4H9-COOH — валериановая кислота
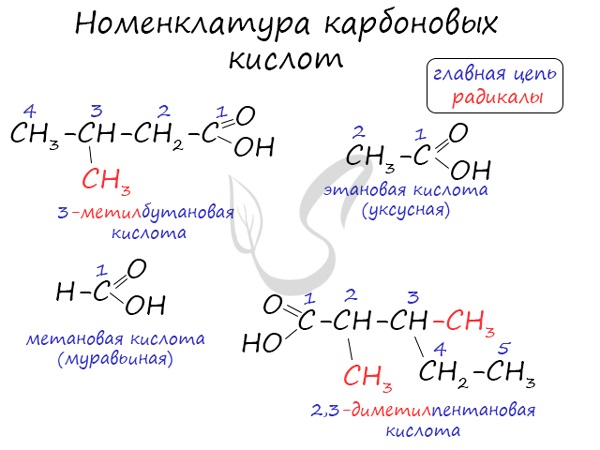
Для предельных карбоновых кислот характерна структурная изомерия: углеродного скелета, межклассовая изомерия со сложными
эфирами.
Получение карбоновых кислот
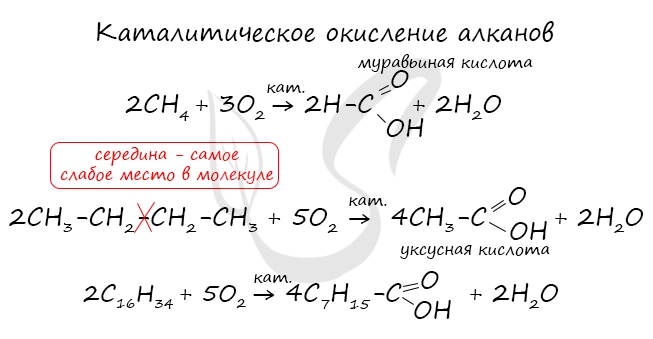
- Окисление алканов
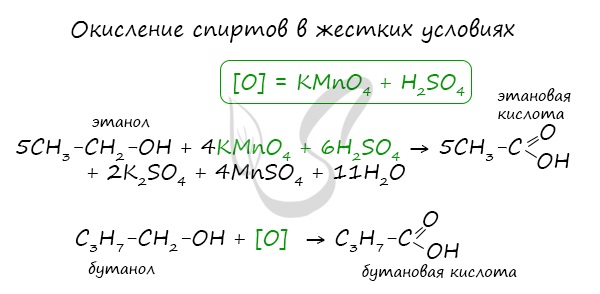
- Окисление спиртов
- Окисление альдегидов
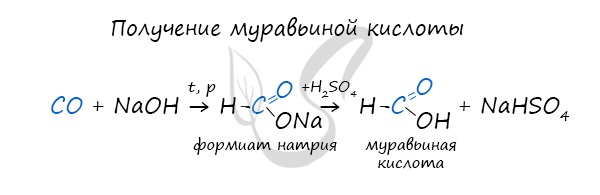
- Синтез муравьиной кислоты
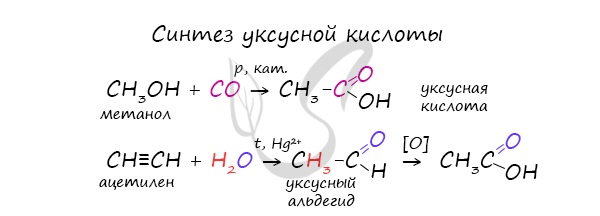
- Синтез уксусной кислоты
При повышенной температуре и в присутствии катализатора становится возможным неполное окисление алканов, в результате которого
образуются кислоты.
При реакции спиртов с сильными окислителями, такими как подкисленный раствор перманганата калия, спирты окисляются
до соответствующих кислот.
При окислении альдегиды образуют соответствующие карбоновые кислоты. Окисление можно проводить качественной реакцией
на альдегиды — реакцией серебряного зеркала.

Обратите особое внимание, что при написании реакции с аммиачным раствором серебра в полном виде, правильнее будет указать не кислоту, а ее аммиачную соль. Это связано с тем, что выделяющийся аммиак, который обладает основными свойствами, реагирует с кислотой с образованием соли.

Окисление альдегидов также может быть успешно осуществлено другим реагентом — свежеосажденным гидроксидом меди II.
В результате такой реакции образуется осадок кирпично-красного цвета оксида меди I.

Существует специфический способ получения муравьиной кислоты, который заключается в реакции щелочи с угарным газом — образуется формиат (соль муравьиной кислоты). В результате добавления раствора серной кислоты к формиату получается
муравьиная кислота.
Специфичность синтеза уксусной кислоты заключается в реакции угарного газа с метанолом, в результате которой она образуется.
Также уксусную кислоту можно получить другим путем: сначала провести реакцию Кучерова, в ходе которой образуется уксусный альдегид.
Окислить его до уксусной кислоты можно аммиачным раствором оксида серебра или гидроксидом меди II.
Химические свойства карбоновых кислот
Для карбоновых кислот не характерны реакции присоединения. Карбоновые кислоты обладают более выраженными кислотными свойствами, чем
спирты.
- Кислотные свойства
- Галогенирование
- Особые свойства муравьиной кислоты
- Разложение муравьиной кислоты
Карбоновые кислоты вступают в реакции с металлами, которые способны вытеснить водород (стоят левее водорода в ряду напряжений
металлов) из кислоты. Реагируют также с основаниями, с солями более слабых кислот, например, угольной кислоты.

Галогенирование происходит по типу замещения в радикале, который соединен с карбоксильной группой. Напомню, что наиболее легко
замещается водород у третичного, чуть сложнее — у вторичного, и значительно сложнее — у первичного атома углерода.

Сила карбоновых кислот тем выше, чем меньше электронной плотности сосредоточено на атоме углерода в карбоксильной группе.
Поэтому самая слабая из трех кислот — уксусная, чуть сильнее — хлоруксусная, за ней — дихлоруксусная и самая сильная —
трихлоруксусная.
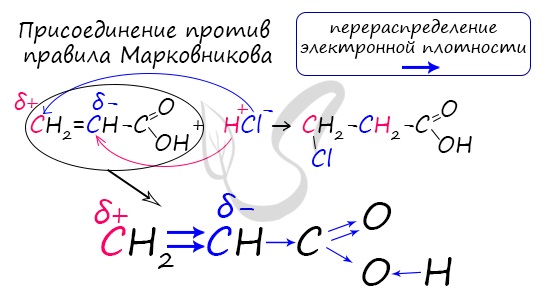
Перераспределение электронной плотности в молекулах этих кислот для лучшего запоминания лучше увидеть наглядно. Это
перераспределение обусловлено большей электроотрицательностью хлора, который притягивает электронную плотность.

Муравьиная кислота отличается от своих гомологов. За счет наличия у нее альдегидной группы, она, единственная из карбоновых кислот,
способна вступать в реакцию серебряного зеркала.
В такой реакции идет ее окисление до нестойкой угольной кислоты, которая распадается на углекислый газ и воду.

При нагревании и в присутствии серной кислоты (водоотнимающего компонента) муравьиная кислота распадается на воду и угарный газ.
HCOOH → (t, H2SO4) CO↑ + H2O
Сложные эфиры
Получение сложных эфиров происходит в реакции этерификации (лат. aether — эфир), заключающейся во взаимодействии карбоновой кислоты
и спирта.
Названия сложных эфиров формируются в зависимости от того, какой кислотой и каким спиртом эфир образован. Примеры:
- Метановая кислота + метанол = метиловый эфир метановой кислоты (метилформиат)
- Этановая кислота + этанол = этиловый эфир уксусной кислоты (этилацетат)
- Метановая кислота + этанол = этиловый эфир метановой кислоты (этилформиат)
- Пропановая кислот + бутанол = бутиловый эфир пропионовой кислоты (бутилпропионат)
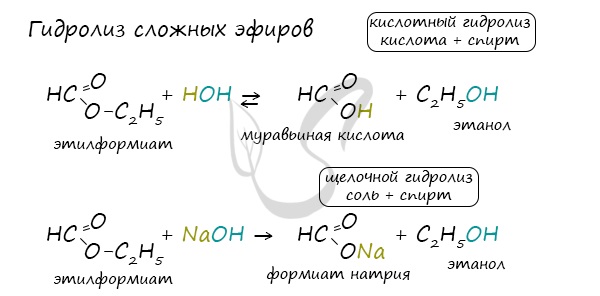
Для сложных эфиров характерной реакцией является гидролиз — их разложение. Возможен щелочной гидролиз, при котором образуется соль
кислоты и спирт, и кислотный гидролиз, при котором образуются исходные спирт и кислота.
Кислотный гидролиз протекает обратимо, щелочной — необратимо.
Реакция щелочного гидролиза по-другому называется реакция омыления, и напомнит о себе, когда мы дойдем до темы жиров.
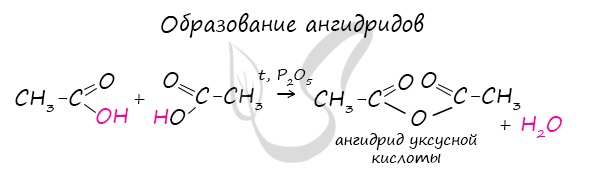
Ангидриды
Ангидриды — химические соединения, производные неорганических и органических кислот, образующиеся при их дегидратации.
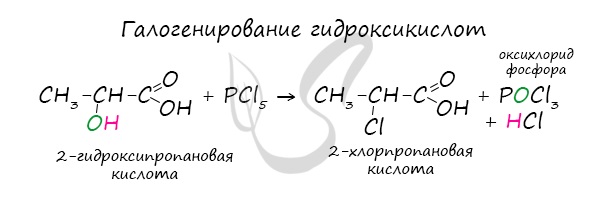
Хлорангидриды карбоновых кислот образуются в реакции карбоновых кислот с хлоридом фосфора V.

Следующая реакция не имеет отношения к ангидридам, однако (из-за их схожести) вы увидите ее здесь для наилучшего запоминания.
Это реакция галогенирования гидроксикислот, в результате которой гидроксогруппа в радикале меняется на атом галогена.
Непредельные карбоновые кислоты
Распределение электронной плотности в молекулах творит чудеса: иногда реакции идут против правила Марковникова. Так происходит
в непредельной акриловой кислоте.
© Беллевич Юрий Сергеевич 2018-2020
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение
(в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов
без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования,
обратитесь, пожалуйста, к Беллевичу Юрию.
- Главная
- Вопросы & Ответы
- Вопрос 4580503
 Гость:
Гость:
9 лет назад
34
1
Лучший ответ:


Гость:
Муравьиная кислота, в ее составе есть и альдегидная и карбоксильная группа
9 Августа в 11:35
Ваш ответ (не менее 20 символов):
Ваше имя (не менее 2 символов):

Лучшее из галереи:































Другие вопросы:
 Гость:
Гость:
(С) ходу взяв скорость,машина промчалась мимо окон. С ходу в этом приложении пишется раздельно или слитно?
9 лет назад
 Гость:
Гость:
3 7/12 — 2 11/12 помогите с решением ◄◄◄◄◄
9 лет назад
Смотреть ответ
3
1
 Гость:
Гость:
Какой ряд состоит из слов в которых пропущены только безударные гласные проверяемые ударением? 1)пок…зался,з…ленеть 2)г…лова,к…пуста 3)т..атр,л..тать
9 лет назад
Смотреть ответ
55
1
 Гость:
Гость:
Каким натуральным числам равны дроби: 16/8;18/2;24/6;30/3;35/35;51/17?
9 лет назад
Смотреть ответ
5
1
 Гость:
Гость:
Помогите решить пример 45+(71-b*9)=80
9 лет назад
Смотреть ответ
13
1
КСУСНУЮ КИСЛОТУ НЕЛЬЗЯ ПОЛУЧИТЬ:
окислением этаналя
окислением бутана
окислением метана
гидролизом этилацетата
2. В КАЧЕСТВЕ АНТИСЕПТИКА ПРИМЕНЯЕТСЯ:
этановая кислота
раствор фенола
диметиловый эфир
бензол
3. МУРАВЬИНАЯ КИСЛОТА СПОСОБНА ПРОЯВЛЯТЬ СВОЙСТВА:
альдегида и спирта
карбоновой кислоты и спирта
карбоновой кислоты и альдегида
карбоновой кислоты и алкена
4.
В СХЕМЕ ПРЕВРАЩЕНИЙ
С2Н2 —> A —> C2H5OH
ВЕЩЕСТВОМ «А» ЯВЛЯЕТСЯ:
СН3СООН
С2Н2Сl2
СН3СНО
С2Н6
5. ИЗОМЕРАМИ ЯВЛЯЮТСЯ:
пентан и пентадиен
уксусная кислота и метилформиат
этан и ацетилен
этанол и этаналь
6. И С АЗОТНОЙ КИСЛОТОЙ И С ГИДРОКСИДОМ МЕДИ (II) БУДЕТ ВЗАИМОДЕЙСТВОВАТЬ:
фенол
глицерин
этанол
метилацетат
7.
УСТАНОВИТЕ К КАКОМУ КЛАССУ ОРГАНИЧЕСКИХ СОЕДИНЕНИЕЙ ПРИНАДЛЕЖИТ ВЕЩЕСТВО
«1,2-ПРОПАНДИОЛ»:
спирты
аминокислоты
фенолы
сложные эфиры
ароматические углеводороды
8. ПРИ ЩЕЛОЧНОМ ГИДРОЛИЗЕ 2-ХЛОРБУТАНА ПРЕИМУЩЕСТВЕННО ОБРАЗУЕТСЯ:
бутанол-2
бутанол-1
бутаналь
бутен-2
9. ПРИ ГИДРИРОВАНИИ АЦЕТАЛЬДЕГИДА ОБРАЗУЕТСЯ:
ацетилен
уксусная кислота
этанол
этиленгликоль
10.
ГОМОЛОГОМ УКСУСНОЙ КИСЛОТЫ ЯВЛЯЕТСЯ КИСЛОТА:
хлоруксусная
муравьиная
олеиновая
бензойная
11. ХАРАКТЕРНОЙ РЕАКЦИЕЙ ДЛЯ МНОГОАТОМНЫХ СПИРТОВ ЯВЛЯЕТСЯ ВЗАИМОДЕЙСТВИЕ С:
H2
Cu
Ag2O (NH3 Р-Р)
Cu(OH)2
12. УСТАНОВИТЕ СООТВЕТСТВИЕ МЕЖДУ ФОРМУЛОЙ ВЕЩЕСТВА «СН3СН2СНО» И ЕГО НАЗВАНИЕМ:
пропан
пропанол
пропаналь
пропанон
пропановая кислота
13. 3,3-ДИМЕТИЛБУТАНАЛЬ ОБРАЗУЕТСЯ ПРИ ОКИСЛЕНИИ:
(СН3)3С-СН2-СН2-ОН
СН3-СН2-С(СН3)2-СН2-ОН
СН3-СН2-СН(СН3)-СН2-ОН
СН3-СН2-СН(СН3)-СН2-ОН
14. ГЛИЦЕРИН В ВОДНОМ РАСТВОРЕ МОЖНО ОБНАРУЖИТ С ПОМОЩЬЮ:
хлорной извести
хлорида железа (III)
гидроксида меди (II)
гидроксида натрия
15. ДЛЯ ПОЛУЧЕНИЯ МЫЛА ИСПОЛЬЗУЮТ РЕАКЦИЮ:
гидрогенизации жиров
щелочного гидролиза жиров
этерификации карбоновых кислот
гидратации алкинов
16. СВЕЖЕПРИГОТОВЛЕННЫЙ ОСАДОК Cu(OH)2 РАСТВОРИТСЯ, ЕСЛИ К НЕМУ ДОБАВИТЬ:
пропандиол-1,2
пропанол-1
пропен
пропанол-2
17. УСТАНОВИТЕ К КАКОМУ КЛАССУ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ ОТНОСИТСЯ ВЕЩЕСТВО «АЦЕТОН»:
спирт
простой эфир
кетон
альдегид
сложный эфир
ароматический углеводород
18. ЭТАНОЛ МОЖНО ПОЛУЧИТЬ ИЗ ЭТИЛЕНА В РЕЗУЛЬТАТЕ РЕАКЦИИ:
гидратации
гидрирования
галогенирования
гидрогалогенирования
19. УКСУСНАЯ КИСЛОТА НЕ ВЗАИМОДЕЙСТВУЕТ С ВЕЩЕСТВОМ, ФОРМУЛА КОТОРОГО:
Mg
Cu(OH)2
Cu
NaOH
20. АТОМ КИСЛОРДА В МОЛЕКУЛЕ ФЕНОЛА ОБРАЗУЕТ:
1 сигма-связь
2 сигма-связи
1 сигма- и 1 пи-связь
2 пи-связи
21. ПРИ ОКИСЛЕНИИ ПРОПАНОЛА ОБРАЗУЕТСЯ:
пропилен
пропанон
пропаналь
пропан
22. УСТАНОВИТЕ СООТВЕТСТВИЕ МЕЖДУ КЛАССОМ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ И НАЗВАНИЕМ ВЕЩЕСТВА «ИЗОПРОПИЛЭТАНОАТ»
спирт
простой эфир
кетон
альдегид
сложный эфир
ароматический углеводород
23. ГИДРОКСИЛЬНАЯ ГРУППА ИМЕЕТСЯ В МОЛЕКУЛАХ:
спиртов и карбоновых кислот
альдегидов и простых эфиров
аминокислот и сложных эфиров
жиров и спиртов
24. ПРИ ГИДРАТАЦИИ ЭТИНА В ПРИСУТСТВИИ СУЛЬФАТА РТУТИ (II) ОБРАЗУЕТСЯ:
этанол
этаналь
этановая кислота
диэтиловый эфир
25. ИЗОМЕРОМ БУТАНОВОЙ КИСЛОТЫ ЯВЛЯЕТСЯ:
бутанол
пентановая кислота
бутаналь
2-метилпропановая кислота
26. МЕЖДУ СОБОЙ МОГУТ ВЗАИМОДЕЙСТВОВАТЬ:
уксусная кислота и карбонат натрия
глицерин и сульфат меди (II)
фенол и гидроксид меди (II)
метанол и углекислый газ
27. ОЛЕИНОВАЯ КИСЛОТА МОЖЕТ ВСТУПАТЬ В РЕАКЦИИ С:
кислородом
хлором
медью
хлоридом цинка
азотом
гидроксидом натрия
28. ФЕНОЛ РЕАГИРУЕТ С:
кислородом
бензолом
гидроксидом натрия
хлороводордом
натрием
29. ОЛЕИНОВАЯ КИСЛОТА МОЖЕТ ВСТУПАТЬ В РЕАКЦИИ С:
водородом
бромоводородом
медью
хлоридом хрома (III)
азотом
карбонатом натрия
30. МЕТАНОЛ ВЗАИМОДЕЙСТВУЕТ С ВЕЩЕСТВАМИ:
хлороводород
карбонат натрия
глицин (аминокислота)
гидроксид железа (III)
