Какое свойство является для природного газа существенным

Сжиженный газ — это продукт, который получается при переработке нефти. Добытая нефть поставляется на нефтеперерабатывающие заводы, и там при переработке на разных этапах получается масло, солярка, бензин и в том числе газ. Этот газ в жидком виде, как и солярка и бензин, в вагонах с заводов отгружается, поступает в хранилище в Московской области. Оттуда приезжает автомобильным транспортом, загружается в машины, и далее его везут по емкостям, по заправочным станциям, где он доходит до потребителя.
По большому счёту сжиженный газ можно сравнить с тем же бензином. Газгольдер, который закапывается у вас на участке, является небольшим хранилищем, куда сливается этот сжиженный газ. И по трубопроводу он уже поступает к вам на котел. Возникает вопрос: А как же сжиженный газ в жидком виде поступает на котел? На самом деле всё очень просто. Сжиженный газ имеет следующее свойство. У него есть жидкая фаза и паровая. Из жидкой фазы он под давлением переходит в паровую фазу, и уже эта паровая фаза в виде газа поступает к вам в дом на котел, где она сгорает, и происходит отопление вашего дома.
Отличие природного газа от сжиженного
Главное его отличие в том, что сжиженный газ измеряется в литрах, потому что он находится в жидком состоянии. А природный газ находится всегда в газообразном. Природный газ добывают из-под земли уже в газообразном состоянии, и по магистралям он по всей территории России, и в принципе по всему миру, уже поступает непосредственно к потребителю.
Что выгоднее
Ещё очень важный вопрос, который постоянно возникает. Стоимость сжиженного газа и природного, что же выгодней? И что же эффективнее использовать? Для того, чтобы это понять, нужно сжиженный газ, который находится у вас в литрах, перевести в газообразное состояние, в газ. Тогда его можно корректно сравнивать с природным газом. То есть там будут кубы, и здесь будут кубы. Сейчас на экранах вы ведите формулу, как правильно перевести сжиженный газ из литров в газообразное состояние и сравнить его с природным газом.
Как же рассчитать
Если вы хотите сами рассчитать, то это в принципе сделать несложно. Вы можете по формулам, которые мы показали, сами просчитать стоимость сжиженного газа и природного газа, и для себя понять разницу. Но если вам не хочется этого делать, можете воспользоваться нашими данными. Мы уже неоднократно это делали, неоднократно просчитали. У нас на канале есть даже видео, и есть отдельная статья, где мы сравниваем разные виды топлива: и дрова, и дизель, и сжиженный газ, и природный газ. Там всё очень подробно рассказано. Заходите, смотрите, изучайте.
Для тех, кто не хочет не считать, не смотреть видео, то просто воспользуйтесь моим советом. Мы уже неоднократно считали сами. Стоимость природного газа где-то примерно в два раза дешевле, чем стоимость отопления на сжиженном газе. Поэтому, если у вас есть возможность подключить природный газ недорого, обязательно его подключайте. Это будет для вас самое выгодное, что может быть на сегодняшний день.
Приведу пример, для отопления дома площадью в 100-150 квадратов природным газом вам потребуется финансов, примерно, 1500-2000 рублей в месяц, это в отопительный сезон зимой. Соответственно, сжиженного газа вам понадобится где-то на 3000-4000 рублей. Поэтому, если у вас есть возможность подключить природный газ, подключайте природный. Но если такой возможности нет, подключайте сжиженный. Ничего страшного в этом нет.
Лень читать? Тогда смотри!
Спасибо за проявленный интерес)
Вы можете подписаться на наши…:
Яндекс Дзен — канал
YouTube — канал
…либо оставить свой комментарий ????
Введение 2
Состав
и физические свойства природного газа 3
Химический
состав 3
Физические
свойства 3
Приро́дный
газ — смесь газов, образовавшаяся в
недрах земли при анаэробном разложении
органических веществ. Природный газ
относится к полезным ископаемым, одно
из важнейших горючих ископаемых,
занимающее ключевые позиции в
топливно-энергетических балансах многих
государств. Природный газ является
важным сырьем для химической промышленности.
В пластовых условиях (условиях залегания
в земных недрах) находится в газообразном
состоянии — в виде отдельных скоплений
(газовые залежи) или в виде газовой шапки
нефтегазовых месторождений, либо в
растворённом состоянии в нефти или
воде.
Энергетическая
и химическая ценность природного газа
определяется содержанием в нём
углеводородов. Очень часто в месторождениях
он сопутствует нефти. Разница в составе
природного и попутного нефтяного газа
имеется. В последнем, как правило, больше
сравнительно тяжёлых углеводородов,
которые обязательно отделяются, прежде
чем использовать газ.
Состав и физические свойства природного газа Химический состав
Природные
углеводородные газы представляют собой
смесь предельных углеводородов вида
СnН2n+2. Основную часть природного газа
составляет метан CH4 — до 98 %.
В
состав природного газа могут также
входить более тяжёлые углеводороды —
гомологи метана: — этан (C2H6), — пропан
(C3H8), — бутан (C4H10), а также другие
неуглеводородные вещества: — водород
(H2), — сероводород (H2S), — диоксид углерода
(СО2), — азот (N2), — гелий (Не)
Чистый
природный газ не имеет цвета и запаха.
Чтобы можно было определить утечку по
запаху, в газ добавляют небольшое
количество веществ, имеющих сильный
неприятный запах, так называемых
одорантов. Чаще всего в качестве одоранта
применяется этилмеркаптан.
Физические свойства
Ориентировочные
физические характеристики (зависят от
состава; при нормальных условиях, если
не указано иное):
Плотность:
от
0,68 до 0,85 кг/м³ (сухой газообразный);
400
кг/м³ (жидкий).
Температура
кипения при атмосферном давлении: –162°C
Температура
самовозгорания: 650 °C;
Взрывоопасные
концентрации смеси газа с воздухом от
5 % до 15 % объёмных;
Удельная
теплота сгорания: 28—46 МДж/м³ (6,7—11,0
ккал/м³) (то есть 8-12 квт·ч/м³);
Октановое
число при использовании в двигателях
внутреннего сгорания: 120—130.
Легче
воздуха в 1,8 раз, поэтому при утечке не
собирается в низинах, а поднимается
вверх.
Природные
газы подразделяют на следующие группы:
1.
Газ, добываемый из чисто газовых
месторождений и представляющий собой
сухой газ, свободный от тяжелых
углеводородов.
2.
Газы, добываемые вместе с нефтью
(растворенные или попутные газы). Это
физические смеси сухого газа,
пропанобутановой фракции (жирного газа)
и газового бензина.
3.
Газы, добываемые из газоконденсатных
месторождений — смесь сухого газа и
жидкого углеводородного конденсата.
Углеводородный конденсат состоит из
большого числа тяжелых углеводородов
(С5 + высш., С6 + высш. и т.д.), из которых
можно выделить бензиновые, лигроиновые,
керосиновые, а иногда и более тяжелые
масляные фракции.
4.
Газы газогидратных залежей.
Компонентный
состав и свойства отдельных компонентов
природного газа приведены в таблице 1.
Таблица
1. Основные свойства компонентов природных
газов в стандартных условиях
Свойство | Обозначение | CH4 | C2H6 | C3H8 | i-C4H10 | n-C4H10 |
Молекулярная | М | 16,04 | 30,07 | 44,10 | 58,12 | 58,12 |
Объем | V | 1,40 | 0,74 | 0,51 | 0,39 | 0,39 |
Плотность | 0,554 | 1,038 | 1,522 | 2,006 | 2,006 | |
Масса | m | 0,71 | 1,35 | 1,97 | 2,85 | 2,85 |
Критическое | ркр | 4,58 | 4,86 | 4,34 | 3,85 | 3,57 |
Критическая | Ткр | 191 | 305 | 370 | 407 | 425 |
Во
многих случаях состав природных
углеводородных газов определяется не
полностью, а лишь до бутана (С4Н10) или
гексана (С6Н14) включительно, а все
остальные компоненты объединяются в
остаток (или псевдокомпонент).
Газ,
в составе которого тяжелые углеводороды
составляют не более 75 г/м3, называют
сухим.
При
содержании тяжелых углеводородов более
150 г/м3 газ называют жирным.
Газовые
смеси характеризуются массовыми или
молярными концентрациями компонентов.
Для характеристики газовой смеси
необходимо знать ее среднюю молекулярную
массу, среднюю плотность в килограммах
на кубический метр или относительную
плотность по воздуху.
Молекулярная
масса М
природного
газа:
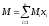 ,
,
где
М – молекулярная масса i-го
компонента; xi
– объемное содержание i-го
компонента, доли ед.
Для
реальных газов обычно М=16 – 20.
Плотность
газа ρг
рассчитывается по формуле:
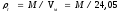 ,
,
где
Vм
– объем 1 моля газа при стандартных
условиях.
Обычно
ρг
находится в пределах 0,73 – 1,0 кг/м3.
Плотность
газа в значительной степени зависит от
давления и температуры, и поэтому для
практического применения этот показатель
неудобен. Чаще пользуются относительной
плотностью газа по воздуху ρг.в.,
равной отношению плотности газа ρг
к плотности воздуха ρв,
взятой при тех же давлении и температуре:
ρг.в.
= ρг
/ ρв,
Если
ρг
и ρв
определяются при стандартных условиях,
то ρв
= 1,293 кг/м3 и ρг.в.
= ρг
/ 1,293.
Плотность
нефтяных газов колеблется от 0,554 (для
метана) до 2,006 (для бутана) и выше.
Вязкость
газа характеризует силы взаимодействия
между молекулами газа, которые
преодолеваются при его движении. Она
увеличивается при повышении температуры,
давления и содержания углеводородных
компонентов. Однако при давлениях выше
3МПа увеличение температуры вызывает
понижение вязкости газа.
Вязкость
нефтяного газа незначительна и при 0оС
составляет 0,000131 пз; вязкость воздуха
при 0оС равна 0,000172 пз.
Уравнения
состояния газов используются для
определения многих физических свойств
природных газов. Уравнением состояния
называется аналитическая зависимость
между параметрами газа, описывающая
поведение газа. Такими параметрами
являются давление, объем и температура.
Состояние
идеальных газов в условиях высоких
давления и температуры определяется
уравнением Клапейрона — Менделеева:
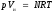 ,
,
где
р
—
давление; Vи
— объем идеального газа, N—
число киломолей газа; R—
универсальная газовая постоянная; Т
—
температура.
Идеальным
называется газ, силами взаимодействия
между молекулами которого пренебрегают.
Реальные углеводородные газы не
подчиняются законам идеальных газов.
Поэтому уравнение Клапейрона—Менделеева
для реальных газов записывается в виде:
pV
= ZNRT,
где
Z
—
коэффициент сверхсжимаемости реальных
газов, зависящий от давления, температуры
и состава газа и характеризующий степень
отклонения реального газа от закона
для идеальных газов.
Коэффициент
сверхсжимаемости Z
реальных
газов — это отношение объемов равного
числа молей реального V
и
идеального Vи
газов при одинаковых термобарических
условиях (т. е. при одинаковых давлении
и температуре):
Z
= V/Vи
Значения
коэффициентов сверхсжимаемости наиболее
надежно могут быть определены на основе
лабораторных исследований пластовых
проб газов. При отсутствии таких
исследований (как это чаще всего бывает
на практике) прибегают к расчетному
методу оценки Z
по
графику Г. Брауна (рис.1). Для пользования
графиком, необходимо знать, так называемые,
приведенные псевдокритическое давление
и псевдокритическую температуру.
Критической
называется
такая температура,
выше
которой газ не может быть превращен в
жидкость ни при каком давлении. Критическим
давлением называется
давление, соответствующее критической
точке перехода газа в жидкое состояние.
С
приближением значений давления и
температуры к критическим свойства
газовой и жидкой фаз становятся
одинаковыми, поверхность раздела между
ними исчезает и плотности их уравниваются.
С
появлением в системе двух и более
компонентов в закономерностях фазовых
изменений возникают особенности,
отличающие их поведение от поведения
однокомпонентного газа. Не останавливаясь
на подробностях, следует отметить, что
критическая температура смеси находится
между критическими температурами
компонентов, а критическое давление
смеси всегда выше, чем критическое
давление любого компонента.
Для
определения коэффициента сверхсжимаемости
Z
реальных газов, представляющих собой
многокомпонентную смесь, находят средние
из значений критических давлений и
температур каждого компонента. Эти
средние называются псевдокритическим
давлением pп.кр.
и псевдокритической температурой Тп.кр.
Они определяются из соотношений:
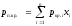 ,
,
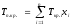 ,
,
природный
газ метан состав
где
ркр. и Ткр. – критические давления и
температура i-го
компонента; xi
– доля i-го
компонента в объеме смеси (в долях
единицы).
Приведенные
псевдокритические давление и температура,
необходимые для пользования графиком
Брауна, представляют собой псевдокритические
значения, приведенные к конкретным
давлению и температуре (к пластовым,
стандартным или каким-либо другим
условиям):
Рпр.
= р/рп.кр.,
Тпр.
= Т/Тп.кр.,
где
р и Т – конкретные давления и температура,
для которых определяется Z.
Коэффициент
сверхсжимаемости Z
обязательно используется при подсчете
запасов газа для правильного определения
изменения объема газа при переходе от
пластовых условий к поверхностным, при
прогнозировании изменения давления в
газовой залежи и при решении других
задач.
Применение
Метан
используется как горючее в газовых
плитах.
Пропан
и бутан – в качестве топлива в некоторых
автомобилях. Также сжиженным пропаном
заполняют зажигалки.
Этан
в качестве горючего используют редко,
основное его применение – получение
этилена.
Этилен
является одним из самых производимых
органических веществ в мире. Он является
сырьём для получения полиэтилена.
Ацетилен
используется для создания очень высокой
температуры в металлургии (сверка и
резка металлов). Ацетилен очень горюч,
поэтому в качестве топлива в автомобилях
не используется, да и без этого условия
его хранения должны строго
соблюдаться.
Сероводород,
несмотря на его токсичность, в малых
количествах применяется в т.н.
сероводородных ваннах. В них используются
некоторые антисептические свойства
сероводорода.
Основным
полезным свойством гелия является его
очень маленькая плотность (в 7 раз легче
воздуха). Гелием заполняют аэростаты и
дирижабли. Водород ещё более лёгок, чем
гелий, но в то же время горюч. Большую
популярность среди детей имеют воздушные
шарики, надуваемые гелием.
Токсичность
Углекислый
газ. Даже большие количества углекислого
газа никак не влияют на здоровье человека.
Однако он препятствует поглощению
кислорода при содержании в атмосфере
от 3% до 10% по объёму. При такой концентрации
начинается удушье и даже смерть.
Гелий.
Гелий абсолютно нетоксичен при нормальных
условиях из-за его инертности. Но при
повышенном давлении возникает начальная
стадия наркоза, похожая на воздействие
веселящего газа.
Сероводород.
Токсичные свойства этого газа велики.
При длительном воздействии на обоняние
возникает головокружение, рвота. Также
парализуется обонятельный нерв, поэтому
возникает иллюзия отсутствия сероводорода,
а на самом деле организм его уже просто
не ощущает. Отравление сероводородом
наступает при концентрации 0,2–0,3 мг/м3,
концентрация выше 1 мг/м3 — смертельна.
Процесс
горения
Все
углеводороды при полном окислении
(избыток кислорода) выделяют углекислый
газ и воду. Например:
CH4
+ 3O2 = CO2 + 2H2O
При
неполном (недостаток кислорода) — угарный
газ и воду:
2CH4
+ 6O2 = 2CO + 4H2O
При
ещё меньшем количестве кислорода
выделяется мелкодисперсный углерод
(сажа):
CH4
+ O2 = C + 2H2O.
Метан
горит голубым пламенем, этан — почти
бесцветным, как спирт, пропан и бутан —
жёлтым, этилен — светящимся, угарный газ
— светло-голубым. Ацетилен — желтоватым,
сильно коптит. Если у Вас дома стоит
газовая плита и вместо обычного голубого
пламени вы видите жёлтое — знайте, это
метан разбавляют пропаном.
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
Учебник для 11 класса
Естествознание
- Назовите важнейшие месторождения природного газа в нашей стране, покажите их на карте.
- Перечислите нетрадиционные источники энергии и страны, где они находят применение.
- Расскажите, какие правила техники безопасности нужно соблюдать при работе с бытовым газом.
Характеристика и свойства алканов. Продолжим характеристику газообразных веществ знакомством с важнейшей группой органических соединений — углеводородами.
Название «углеводороды» говорит само за себя: это вещества, молекулы которых состоят из атомов двух элементов — углерода и водорода. Благодаря уникальной способности атомов углерода соединяться друг с другом в цепи различной длины и формы, таких соединений великое множество. Поэтому их делят на классы. Мы остановимся на краткой характеристике только одного класса — предельные углеводороды, или алканы. И это не случайно, поскольку предельные углеводороды — это основная составная часть природного газа и нефти. Наша страна занимает одно из ведущих мест в мире по запасам, добыче, экспорту и переработке углеводородного сырья (рис. 29).

Рис. 29. Основные месторождения природных источников углеводородов (нефти, газа, каменного угля) в Российской Федерации
Знание этой темы представляет определённый профессиональный интерес не только для тех, кто хочет углублённо изучать естественные науки, но также для будущих юристов и экономистов, обществоведов и политологов, инженеров и экологов. Природные источники углеводородов являются связующим звеном межгосударственных отношений в политической и экономической области и вместе с тем причиной вооружённых конфликтов и войн за контроль над ними.
Итак, вернёмся к характеристике предельных углеводородов.
Алканы (предельные углеводороды, парафины) — это углеводороды, в молекулах которых все валентности атомов углерода, не задействованные на образование простых связей C—C, насыщены атомами водорода; состав алканов соответствует общей формуле CnH2n + 2.
Приведём развёрнутые и сокращённые структурные формулы, а также названия первых трёх представителей ряда алканов:

Свойства предельных углеводородов зависят от состава их молекул, т. е. от относительной молекулярной массы, что наглядно иллюстрирует таблица 1.
Таблица 1
Физические свойства алканов

Нетрудно заметить, что с ростом относительной молекулярной массы у алканов возрастают температура кипения, плотность, а также изменяется агрегатное состояние: первые четыре алкана — газообразные вещества, следующие одиннадцать — жидкости, а начиная с C16H34 — твёрдые вещества.
Состав и использование природного газа. Практически повсеместно на нашей планете в толще Земли встречается природный газ.
Природный газ — это смесь предельных углеводородов и неорганических газов, образующих месторождения.

Рис. 30. Добыча природного газа

Рис. 31. Модели метана: а — объёмная; б — шаростержневая
Содержание каждого компонента зависит от месторождения, однако в любом случае в природном газе (рис. 30) преобладает метан (рис. 31), количество других углеводородов резко сокращается с уменьшением их относительной молекулярной массы (табл. 2).
Таблица 2
Примерный состав природного газа

При сгорании предельных углеводородов выделяется большое количество теплоты, поэтому природный газ служит самым эффективным и дешёвым топливом для тепловых электростанций, котельных установок, доменных и стекловаренных печей. Пропан-бутановая фракция природного газа в сжиженном виде используется как бытовое топливо и топливо для карбюраторных двигателей автомобилей. Кроме того, при полном сгорании алканов воздух практически не загрязняется вредными выбросами, поскольку продуктами их горения являются углекислый газ и водяной пар. В этом нетрудно убедиться, если записать уравнения реакций горения алканов, например метана:
CH4 + 2O2 = CO2 + 2H2O + Q.
Природный газ — это не только высокоэффективное топливо, но и важное сырьё для химической промышленности. Перед вами схема различных вариантов промышленной переработки природного газа.

Сажа. Синтез-газ. При полном разложении метана, основного компонента природного газа, образуются водород и сажа. Около 90% всей получаемой сажи использует резинотехническая промышленность. Резиновые изделия, автомобильные покрышки и камеры имеют чёрный цвет именно потому, что в качестве наполнителя в них добавляют сажу. Кроме того, это вещество входит в состав типографских красок, некоторых типов батареек.
При взаимодействии метана с перегретым водяным паром образуется смесь газов — оксида углерода (II) и водорода в соотношении 1 : 3. Эту смесь называют синтез-газом:

Синтез-газ используется для получения синтетического бензина — смеси предельных углеводородов, содержащих от 6 до 12 атомов углерода в молекуле. Такой бензин называется газовым, он используется в качестве основы низкосортного автомобильного топлива. Кроме того, синтез-газ используется для получения кислородсодержащих органических веществ, в частности метилового спирта:

Этилен. Второй представитель алканов — этан является сырьём для получения ценного газообразного вещества — этилена. У вас сразу возникла ассоциация: полиэтилен. Абсолютно верно: этилен действительно является сырьём для получения этой ценной пластмассы, с которой вы будете знакомиться при изучении полимеров. Покажем, как из этана получается этилен. Для этого сравните формулы первого (C2H6) и второго (C2H4) газов. Очевидно, чтобы из этана получить этилен, нужно из каждой его молекулы отнять два атома (молекулу) водорода, или, как говорят в химии, провести реакцию дегидрирования:
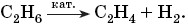
Обратите внимание, что в молекуле этилена все четыре валентности атомов углерода задействованы по-разному: три связаны с другими атомами, а четвёртая образует ещё одну связь между атомами углерода:

Сокращённая структурная формула этилена CH2=CH2 показывает, что его молекула содержит двойную связь, а потому этот углеводород относится к непредельным углеводородам.
Биогаз. В последнее время всё большее внимание привлекают нетрадиционные с технической точки зрения источники энергии: солнечное излучение, морские приливы и многое другое. Некоторые из них, например ветер, находили широкое применение и в прошлом, а сегодня переживают второе рождение. Одним из забытых видов сырья является и биогаз, использовавшийся ещё в Древнем Китае и вновь «открытый» в наше время.
Все природные источники углеводородного сырья, в том числе природный газ, имеют органическое происхождение. Нельзя ли использовать современные растительные и животные остатки для производства газообразных алканов сегодня, не дожидаясь результатов труда матушки-природы? Оказывается, это вполне возможно и в значительных масштабах уже используется во многих странах. Газ, полученный таким способом, и называется биогазом.
На заводах по производству биогаза в качестве сырья используются отходы животного и растительного происхождения — навоз, пищевые отходы, растительные массы, ботва. В генераторах-ферментёрах эти отходы перегнивают под действием анаэробных бактерий.
В отличие от природного газа биогаз содержит значительные количества оксида углерода (IV) — от 25 до 50%. Однако основным его компонентом, как и в природном газе, является метан. Биогаз можно использовать непосредственно для отопления жилищ, приготовления пищи или получения электроэнергии с помощью электрогенератора. Отходы после получения биогаза имеют высокое содержание азота и могут использоваться в качестве высокоэффективных, экологически безопасных удобрений.
Поскольку разложение органических отходов происходит за счёт деятельности определённых типов бактерий, существенное влияние на процесс получения биогаза оказывает окружающая среда. Так, количество вырабатываемого газа в значительной степени зависит от температуры: чем теплее, тем выше скорость и степень ферментации органического сырья. Именно поэтому, вероятно, первые установки для получения биогаза появились в странах с тёплым климатом. Однако применение надёжной теплоизоляции, а иногда и подогретой воды позволяет освоить строительство генераторов биогаза в районах, где температура зимой опускается до -20 °С. Существуют определённые требования и к сырью: оно должно быть подходящим для развития бактерий, содержать биологически разлагающееся органическое вещество и в большом количестве — воду (90—94%). Желательно, чтобы среда была нейтральной и без примеси веществ, мешающих действию бактерий, например мыла, стиральных порошков, антибиотиков. В среднем из 1 кг органического вещества при производстве биогаза получается 250 л метана, 160 л углекислого газа, 200 г воды и 300 г неразложимого остатка.
Запасы природного газа в России. В России находится почти 40% мировых запасов природного газа. Уникальные месторождения расположены на севере в Ямало-Ненецком автономном округе, а также на шельфах арктических морей. Всего в России более 12 нефтегазоносных регионов, занимающих почти половину территории страны (см. рис. 34). Запасы газа значительно больше, чем нефти. По оценкам специалистов на сегодняшний день добыто только около 5% мировых запасов голубого топлива.
Затраты на добычу и транспортировку природного газа постепенно возрастают. Это связано с исчерпанием его запасов в старых месторождениях, необходимостью вкладывать средства в разведку новых. Да и запасы природного сырья на Земле не безграничны.
Далее поговорим подробно о другом ценном полезном ископаемом — нефти и способах её переработки.
Теперь вы знаете
- каковы состав и основные свойства алканов
- состав природного газа
- каковы запасы природного газа в России У что такое биогаз и как он используется
Теперь вы можете
- объяснить, что такое алканы, и перечислить их основные свойства
- дать характеристику природного газа, его состава и количественного содержания его компонентов
- назвать области применения сажи, синтез-газа, этилена, природного газа, биогаза
Выполните задания
- Определите, чем отличаются предельные углеводороды от непредельных.
- Назовите первых трёх представителей ряда алканов, напишите их развёрнутые и сокращённые формулы.
- Объясните, в чём преимущество газообразного топлива перед другими видами топлива.
- Перечислите химические свойства метана, которые лежат в основе его применения, ответ проиллюстрируйте уравнениями соответствующих реакций.
- Приведённую в параграфе схему вариантов промышленной переработки природного газа дополните короткими сообщениями и уравнениями реакций.
Темы для рефератов
- Топливо и его виды.
- Биогаз, его производство и применение.
- Южный и Северный потоки: проблемы и перспективы.
- Роль России в мировой добыче и транспортировке газа.
