Какое количество вещества содержится в одном моле водорода

Количество вещества — физическая величина, характеризующая количество однотипных структурных единиц, содержащихся в веществе. Под структурными единицами понимаются любые частицы, из которых состоит вещество (атомы, молекулы, ионы, электроны или любые другие частицы)[1]. Единица измерения количества вещества в Международной системе единиц (СИ) и в системе СГС — моль[2]. Без конкретизации объекта рассмотрения термин «количество вещества» не используют[K 1].
Применение[править | править код]
Эта физическая величина используется для измерения макроскопических количеств веществ в тех случаях, когда для численного описания изучаемых процессов необходимо принимать во внимание микроскопическое строение вещества, например, в химии, при изучении процессов электролиза, или в термодинамике, при описании уравнений состояния идеального газа.
При описании химических реакций, количество вещества является более удобной величиной, чем масса, так как молекулы взаимодействуют независимо от их массы в количествах, кратных целым числам.
Например, для реакции горения водорода (2H2 + O2 → 2H2O) требуется в два раза большее количество вещества водорода, чем кислорода. При этом масса водорода, участвующего в реакции, примерно в 8 раз меньше массы кислорода (так как атомная масса водорода примерно в 16 раз меньше атомной массы кислорода). Таким образом, использование количества вещества облегчает интерпретацию уравнений реакций: соотношение между количествами реагирующих веществ непосредственно отражается коэффициентами в уравнениях.
Так как использовать в расчётах непосредственно количество молекул неудобно, потому что это число в реальных опытах слишком велико, вместо измерения количества молекул в единицах «штука», их измеряют в молях. Фактическое количество единиц «штука» в 1 моле вещества называется числом Авогадро (NA = 6,02214076⋅1023 «штука»/моль[4]).
Количество вещества обозначается латинской (эн) и не рекомендуется обозначать греческой буквой (ню), поскольку этой буквой в химической термодинамике обозначается стехиометрический коэффициент вещества в реакции, а он, по определению, положителен для продуктов реакции и отрицателен для реагентов[5]. Однако в школьном курсе широко используется именно греческая буква (ню).
Для вычисления количества вещества на основании его массы пользуются понятием молярная масса: , где m — масса вещества, M — молярная масса вещества. Молярная масса — это масса, которая приходится на один моль данного вещества. Молярная масса вещества может быть получена произведением молекулярной массы этого вещества на количество молекул в 1 моле — на число Авогадро. Молярная масса (измеренная в г/моль) численно совпадает с относительной молекулярной массой.
По закону Авогадро, количество газообразного вещества можно также определить на основании его объёма: = V / Vm, где V — объём газа при нормальных условиях, а Vm — молярный объём газа при тех же условиях, равный 22,4 л/моль.
Таким образом, справедлива формула, объединяющая основные расчёты с количеством вещества:
Комментарии[править | править код]
Примечания[править | править код]
- ↑ [dic.academic.ru/dic.nsf/polytechnic/4077/КОЛИЧЕСТВО Количество вещества]. Большой энциклопедический политехнический словарь (2004). Дата обращения 31 января 2014.
- ↑ Деньгуб В. М., Смирнов В. Г. Единицы величин. Словарь-справочник. — М.: Издательство стандартов, 1990. — С. 85. — 240 с. — ISBN 5-7050-0118-5.
- ↑ Пресс И. А., Основы общей химии, 2017, с. 119.
- ↑ Avogadro constant (англ.). Physical Measurement Laboratory. National Institute of Standards and Technology. Дата обращения 7 февраля 2017.
- ↑
Когда теплота реакции записывается так, как это сделано в данном уравнении, подразумевается, что она выражена в килоджоулях на стехиометрическую единицу («моль») реакции по записанному уравнению. В рассматриваемом случае теплота реакции равна 62,8 кДж на моль (+62,8 кДж · моль−1) B5H9 (газообразного), но составляет только 12,56 кДж на моль израсходованного бора (твёрдого кристаллического) или 62,8 кДж на каждые 4,5 моля газообразного водорода. Теплоты реакций всегда табулируются в расчете на моль образующегося соединения.
Литература[править | править код]
- Пресс И. А. Основы общей химии. — 3-е изд., стереотип. — СПб.: Химиздат, 2017. — 352 с. — ISBN 978-5-93808-286-1. (недоступная ссылка)
Некоторые внешние ссылки в этой статье ведут на сайты, занесённые в спам-лист. Эти сайты могут нарушать авторские права, быть признаны неавторитетными источниками или по другим причинам быть запрещены в Википедии. Редакторам следует заменить такие ссылки ссылками на соответствующие правилам сайты или библиографическими ссылками на печатные источники либо удалить их (возможно, вместе с подтверждаемым ими содержимым). Список проблемных доменов |
Каждый, кто уже немного продвинулся в изучении химии, сталкивается с понятием «моль». Правда, большинство сразу думает о моли, которая съела за лето шубу в шкафу, но моль в химии – это совсем другая история. И вот сейчас мы в этом разберёмся.
Фото: formidapps.com
Итак, давайте посмотрим на какую-нибудь химическую реакцию. Например, такую:
Н2+F2=2HF
Здесь 1 молекула водорода H2 реагирует с одной молекулой фтора F2 и получается две молекулы фторида водорода. Напомню, то число молекул или атомов, вступающих в реакцию или получающихся в реакции, определяется коэффициентом, то есть цифрой, стоящей перед формулой вещества. В нашем примере перед водородом не стоит ничего, но на самом деле мы можем поставить здесь единицу, то есть нам нужна 1 молекула водорода. Перед фтором тоже не стоит ничего, значит, нам нужна 1 молекула фтора. А вот перед фторидом водорода HF стоит двойка. Это означает, что у нас получилось 2 молекула фторида водорода. То есть:
Н2 + F2 = 2HF – это то же самое, что и
1 молекула H2 + 1 молекула F2 = 2 молекулы HF.
Но вы знаете, что молекулы так малы, что мы их увидеть не можем. Как же нам считать эти молекулы, вступающие в реакцию? Для этого и ввели понятие МОЛЬ.
Моль – это количество вещества, в котором содержится столько же частиц, сколько атомов содержится в 12 граммах углерода с атомной единицей массы 12.
Это довольно мудрёное определение, но его нужно запомнить. Есть и приятный момент: в одном моле любого вещества содержится число Авогадро частиц. Вот оно, это число:
Такое число представить сложно. Вы только подумайте, миллиард – это 1 000 000 000. А в одном моле частиц 6,02*100 000 000 000 000 000 000 000! (Но чтобы не видеть по ночам кошмаров, просто запомните 6,02*10 в двадцать третьей степени).
Итак, в одном моле любого вещества содержится 6,02*10 в двадцать третьей степени частиц. Но мы же знаем, что атомы разных веществ имеют разное строение, а поэтому и разную массу. Поэтому и массы одного моля у разных веществ различаются. Чтобы разобраться в этом, давайте поедем на дачу и проведём эксперимент.
Мы точно помним, что 1 моль – это всегда одинаковое число частиц (6,02*10 в двадцать третьей степени ). Но в обычной жизни таких чисел нет, поэтому возьмём число поменьше, например, 100. Это будет наш условный экспериментальный моль. Теперь в одну кучу складываем 100 вишен, в другую кучу – 100 груш, в третью – 100 арбузов. Куча – это 1 моль. В каждую кучу мы добросовестно сложили одинаковое число частиц, верно? Но частицы эти разного вида: в одной куче вишни, в другой – груши, в третьей – арбузы. А теперь будем взвешивать. Как вы думаете, будет ли различаться масса 100 вишен, 100 груш и 100 арбузов? Конечно же, будет. При этом обратите внимание: число частиц в каждой куче одинаково, но весят эти кучи по-разному. Почему? Потому что частицы разные!
В химии всё точно так же. Если взять 1 моль водорода, 1 моль кислорода и 1 моль натрия, то масса их будет разной (вспоминаем поездку на дачу). И это важно. Но теперь возникает закономерный вопрос: а как же узнать, какова масса 1 моль водорода, 1 моль кислорода и 1 моль натрия и вообще любого вещества? Для этого вводится понятие молярная масса.
Молярная масса и есть масса 1 моля вещества.
Как её определить? Просто. Это атомная масса или молекулярная масса вещества, которую мы рассчитываем, пользуясь таблицей Менделеева. Молярная масса обозначается буквой М и выражается в г/моль (просто потому, что она показывает сколько граммов вести 1 моль). Примеры из учебника химии.
Пример 1.
Найдите массу одного моля (она же молярная масса) алюминия.
Решаем химию и смотрим в таблицу Менделеева. Видим, что атомная масса алюминия 27. Формула просто вещества алюминия – Al, то есть атом здесь один. Следовательно, молярная масса алюминия совпадает с атомной и равна 27 г/моль.
Пример 2.
Найдите молярную массу фтора.
Фтор у нас в обычных условиях – газ, поэтому молекула фтора состоит из двух атомов и выглядит так: F2. В периодической таблице находим фтор и видим, что его атомная масса 19. Следовательно, молярная масса фтора 2*19=38 г/моль.
Пример 3.
Найдите молярную массу оксида кальция.
Формула оксида кальция СаО. Опять смотрим в таблицу: атомная масса кальция 40, атомная масса кислорода 16. Молярная масса оксида кальция 40+16=56 г/моль.
Пример 4.
Найдите молярную массу оксида кремния.
Формула оксида кремния SiO2. Таблица Менделеева сообщает, что атомная масса кремния 28, кислорода – 16. Будьте внимательны, в этом вопросе подвох! В формуле оксида два атома кислорода, обязательно учтите это, чтобы ответ был верным. И он будет таким: молярная масса оксида кремния 28+16*2=60 г/моль. (16 – масса одного атома кислорода, у нас в формуле их два, поэтому мы и умножили 16 на 2!).
Пример 5.
Сложный пример от репетитора по химии. Но я рекомендую всё-таки вникнуть и разобраться, чтобы прояснить всё окончательно. Итак, ответьте, какова молярная масса серной кислоты.
Здесь придётся сосредоточиться, чтобы не запутаться. Формула серной кислоты H2SO4, то есть у нас имеется:
· 2 атома водорода
· 1 атом серы
· 4 атома кислорода.
Смотрим в периодическую таблицу и определяем атомные массы:
· атомная масса водорода – 1
· атомная масса серы – 32
· атомная масса кислорода – 16.
Переходим к расчёту:
2 атома водорода + 1 атом серы + 4 атома кислорода
2*1 + 1*32 + 4*16
В этом выражении в каждом слагаемом первый множитель – число атомов элемента, второй множитель – атомная масса. Дальше просто математика: 2*1+1*32+4*16=98. И да, молярная масса серной кислоты 98 г/моль.
Уверена, теперь вы различите моль в шкафу и моль в химии. А дальше мы будем разбираться, как взвесить на обычных весах эти моли.
Пишите, пожалуйста, в комментариях, что осталось непонятным, и я обязательно дам дополнительные пояснения. Жалуйтесь на сложности в изучении школьного курса и говорите, что вас испугало в учебнике химии. И тогда следующая статья будет рассказывать именно об этой проблеме.
Моль, молярная масса и граммы – эти понятия как-то связаны? Давайте-ка в этом разберёмся и порешаем задачи на молярную массу. Для начала вспоминаем, что моль – это количество вещества, в котором содержится 6,02*10 в двадцать третьей степени части (это число Авогадро).
Молярная масса показывает, сколько весит 1 моль того или иного вещества в граммах.
Молярная масса совпадает с атомной (если речь о простых вещества) или молекулярной (если речь о веществах сложных и газах, молекулы которых состоят из двух атомов, например, О2).
Это была теория. Но любую теорию нужно применять на практике, иначе зачем она нужна? Вот и займёмся этим.
Фото: pixabay.com
У нас есть химическая реакция:
Н2 + F2 = 2HF
Из уравнения мы видим, что для неё нам нужна 1 молекула водорода и одна молекула фтора. Мы может взять, например, 10 молекул водорода, сколько нам в таком случае понадобится молекул фтора? Тоже 10. Мы можем взять и 100 молекул водорода, тогда потребуется и 100 молекул фтора. Кстати, заодно давайте уж узнаем, сколько молекул фторида водорода мы получим.
Из 1 молекулы водорода и 1 молекулы фтора получается две молекулы фторида водорода
(коэффициент в уравнении перед HF – 2). А если мы берём по 10 молекул водорода и фтора, то сколько получим HF? 20. Ну и взяв по 100 молекул водорода и фтора, мы получим 200 молекул фторида водорода.
Проблема в том, что молекулы настолько малы, что взять даже миллион молекул у человека не получится, это слишком маленькое количество вещества, которое на весах не взвесить. Вот тут и пришёл на помощь моль. Ещё раз запомните: в одном моле любого вещества содержится одно и то же число частиц!
Это очень важно для любых расчётов в химии. В 1 моле водорода содержится число Авогадро частиц, в 1 моле железа содержится число Авогадро частиц, в 1 моле воды содержится число Авогадро частиц, в 1 моле серной кислоты содержится число Авогадро частиц. Но! По массе моли веществ различаются, об это мы говорили раньше. И это обязательно нужно понять.
Теперь вернёмся к нашей реакции:
Н2 + F2 = 2HF
1 молекула Н2 + 1 молекула F2 = 2 молекулы HF
2 молекулы Н2 + 2 молекулы F2 = 4 молекулы HF
100 молекул Н2 + 100 молекул F2 = 200 молекул HF
Всё верно, ведь так?
А теперь вот так:
Н2 + F2 = 2HF
число Авогадро молекул Н2 + число Авогадро молекул F2 = число Авогадро молекул HF
или
1 моль Н2 + 1 моль F2 = 2 моль HF
И как же нам наконец перейти к граммам? Для этого вспоминаем, что молярная масса – это масса 1 моля вещества, совпадающая с атомной или молекулярной. Атомную или молекулярную массу мы определяем по таблице Менделеева: 1 моль водорода весит 2 г (атомная масса водорода 1, формула газообразного водорода Н2, поэтому его молекулярная масса 1*2=2), 1 моль фтора весит 38 г (атомная масса фтора 1, формула газообразного фтора F2, поэтому его молекулярная масса 19*2=38). Таким образом, для того, чтобы произошла реакция, нам нужно взять 2 г водорода и 38 граммов фтора. В этом случае оба вещества прореагируют полностью, образовав 40 граммов фторида водорода.
Теперь ещё пара задач на молярную массу с решениями.
Пример 1.
Сколько граммов оксида кальция и углекислого газа нужно взять, чтобы получить 50 граммов оксида кальция в реакции СаО + СО2 = СаСОз?
Решение.
Первое, что нужно сделать, рассчитать молярные массы всех веществ. Используем периодическую таблицу, чтобы узнать атомные массы:
· молярная масса оксида кальция СаО 40+16=56 г/моль
· молярная масса углекислого газа СО2 12+2*16=44 г/ моль
· молярная масса карбоната кальция СаСО3 40+12+3*16=100 г/моль.
Давайте подумаем, сколько моль карбоната кальция СаСО3 составляют 50 г? 1 моль СаСО3 весит 100 г (см. выше на молярную массу). Следовательно 50г весят 0,5 моль. Это означает, что при проведении реакции в условиях задачи получится 0,5 моль карбоната кальция.
Второе, что нужно сделать, — понять в каком соотношении взяты вещества. Об этом нам говорят коэффициенты в уравнение:
СаО + СО2 = СаСОз
1 моль + 1 моль = 1 моль
Но мы уже выяснили, что в нашем случае мы получим всего 0,5 моль СаСОз. То есть и исходных веществ СаО и СО2 нужно взять по 0,5 моль. Переводя в граммы, получим, что оксида кальция требуется 56 г/моль*0,5 моль=28 г, а углекислого газа – 44 г/моль*0,5 моль=22 г. Это и есть ответ.
Пример 2.
Этот пример не из учебника химии, он сложный, но если вы его поймёте, вас никакой репетитор по химии уже не запугает. Пробуем!
Задача звучит так. Алюминий прореагировал с кислородом с образованием оксида алюминия. Известно, что в реакцию вступило 9 граммов алюминия. Определите, сколько получилось оксида алюминия в граммах.
Решение.
Для начала запишем уравнение 4Al + 3O2 = 2Al2O3 и сразу увидим, что 4 моля алюминия, сгорев, образуют 2 моля оксида алюминия.
Теперь смотрим в таблицу Менделеева и определяемся с молярными массами:
· молярная масса алюминия 27 г/моль, с этим всё просто
· молярная масса оксида алюминия Al2O3 102 г/моль (помните, как мы считаем? 2*27 (это алюминий)+3*16 (это кислород)=54+48=102).
Из условия задачи мы узнали, что в реакцию вступило 9 г алюминия. 1 моль алюминия весит 27 г (это молярная масса). Следовательно, в реакцию вступило 9/27 моль алюминия, или 0,3 моль алюминия. Вернёмся к реакции:
4Al + 3O2 = 2Al2O3
4 моля алюминия при сгорании образуют 2 моля оксида алюминия
0,3 моля алюминия при сгорании образуют Х моля оксида алюминия
Находим Х=0,3*2/4=0,15 моль. Таким образом, если в реакции участвовало 9 г алюминия (или 0,3 моль), то получилось 0,15 моль оксида алюминия. Теперь самое простое – ищем массу в граммах. Припоминаем, что молярная масса оксида алюминия 102 г/моль. То есть 102 г весит 1 моль. А у нас всего 0,15 моль, и весит это количество вещества 102*0,15=15,3 г. Ответ на задачу: при сгорании 9 граммов алюминия получается 15,3 граммов оксида алюминия.
Пишите, пожалуйста, в комментариях, что осталось непонятным, и я обязательно дам дополнительные пояснения. Жалуйтесь на сложности в изучении школьного курса и говорите, что вас испугало в учебнике химии. И тогда следующая статья будет рассказывать именно об этой проблеме.
Задача 53.
Сопоставить числа молекул, содержащихся в 1г NH3 и в 1г N2. В каком случае и во сколько раз число молекул больше?
Решение:
В одном моле любого вещества содержится 6,02 . 1023 молекул этого вещества.
Рассчитаем содержание количества вещества в 1г NH3 и N2 по формуле:
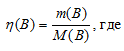
 (B) — количество вещества (В);
(B) — количество вещества (В);
m(B)- масса вещества (В);
M(B) — Молярная масса вещества (В).
М(NH3) = 17г/моль, M(N2) = 28г/моль.
Тогда
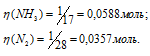
Число молекул NH3 больше числа молекул N2, так как  (NH3) >
(NH3) > (N2) . Теперь рассчитаем, во сколько раз число молекул NH3 больше числа молекул N2:
(N2) . Теперь рассчитаем, во сколько раз число молекул NH3 больше числа молекул N2:
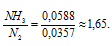
Ответ: в 1,65 раз число молекул NH3 больше числа молекул N2.
Задача 54.
Выразить в граммах массу одной молекулы диоксида серы.
Решение:
Находим молекулярную массу диоксида серы:
M(SO2) = 32 + (16 . 2) = 64г/моль.
Молекулярная масса численно составляет массу одного моля вещества, а значит, вес одного моля численно равен молекулярной массе и составляет 64г. Известно, что в одном моле любого вещества содержится 6,02 . 1023 молекул данного вещества. Исходя из этого, рассчитаем массу в граммах одной молекулы диоксида серы:
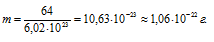
Ответ: масса одной молекулы диоксида серы равна.
Задача 55.
Одинаково ли число молекул в 0,001кг Н2 и в 0,001кг О2? В 1 моле Н2 и в 1 моле 02? В 1л Н2 и в 1л О2 при одинаковых условиях?
Решение:
Молекулярные массы водорода и кислорода равны соответственно 2г/моль и 32г/моль. Отсюда находим количество водорода и кислорода, зная их массы:
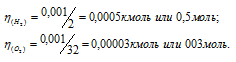
Один моль любого вещества содержит 6,02 .1023 молекул. Следовательно, в 0,001кг водорода и в 0,001кг кислорода содержится разное число молекул:

Так как имеется по одному молю водорода и кислорода, то количество молекул веществ будет одинаково:
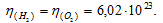
Согласно закону Авогадро в равных объёмах любых газов, взятых при одинаковых условиях, содержится одинаковое число молекул, Один моль любого газа занимает 22,4л, В которых содержится 6,02 . 1023 молекул. Отсюда рассчитаем количество молекул вещества, содержащихся в 1л водорода и в 1л кислорода:
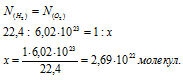
Ответ: а) в 0,001кг водорода и в 0,001кг кислорода содержится разное число молекул; б) в одном моле водорода и в одном моле кислорода содержится одинаковое число молекул: в) в одном литре водорода и в одном литре кислорода содержится одинаковое число молекул.
Задача 56.
Сколько молекул содержится в 1,00 мл водорода при нормальных условиях?
Решение:
Согласно закону Авогадро в равных объёмах любых газов, взятых при одинаковых условиях, содержится одинаковое число молекул, Один моль любого газа занимает 22,4л, В которых содержится 6,02 .1023 молекул. Отсюда рассчитаем количество молекул вещества, содержащихся в 1мл водорода из пропорции:
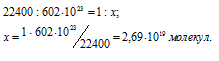
Ответ: 2,69 .1019 молекул.
Задача 57.
Какой объем при нормальных условиях занимают 27 .1021 молекул газа?
Решение:
Согласно закону Авогадро в равных объёмах любых газов, взятых при одинаковых условиях, содержится одинаковое число молекул, Один моль любого газа занимает 22,4л, В которых содержится 6,02 . 1023 молекул. Отсюда находим какой объём при нормальных условиях занимают 27 .1021 молекул газа, составив пропорцию:
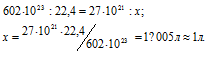
Ответ: V=1л.
Задача 58.
Каково соотношение объемов, занимаемых 1 молем О2 и 1 молем О3 (условия одинаковые)?
Решение:
Согласно закону Авогадро в равных объёмах любых газов, взятых при одинаковых условиях, содержится одинаковое число молекул, Один моль любого газа занимает 22,4л. Следовательно соотношение объёмов, занимаемых одним молем О2 и одним молем О3 иметь вид:
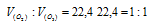
Ответ: 1:1
Задача 59.
Взяты равные массы кислорода, водорода и метана при одинаковых условиях. Найти отношение объемов взятых газов.
Решение:
Согласно закону Авогадро в равных объёмах любых газов, взятых при одинаковых условиях, содержится одинаковое число молекул, Один моль любого газа занимает 22,4л. Мольные массы кислорода, водорода и метана, соответственно равны 32 г/моль; 2г/моль; 16 г/моль.
Так как массы кислорода, водорода и метана одинаковы при одинаковых условиях, то отношение объёмов взятых газов находим из пропорции:
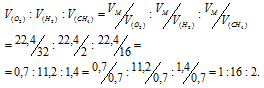
Ответ: 1:16:2.
Задача 60.
На вопрос, какой объем займет 1моль воды при нормальных условиях, получен ответ: 22,4л. Правильный ли это ответ?
Решение:
Согласно закону Авогадро в равных объёмах любых газов, взятых при одинаковых условиях, содержится одинаковое число молекул, Один моль любого газа занимает 22,4л. Так как вода при нормальных условиях находится в жидкой, а не в газообразной фазе, то ответ, что 1моль воды займёт 22,4л не правильный. Учитывая, что молярная масса воды равна 18г/моль, а плотность равна единице, то правильный ответ будет равен:
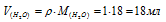
Ответ: 18мл.
Задача 61.
Сколько молекул диоксида углерода находится в 1л воздуха, если объемное содержание СО2 составляет 0,03% (условия нормальные)?
Решение:
При нормальных условиях углекислый газ, содержащийся в 1л воздуха, занимает объём 0,0003л. Зная, что мольный объём любого газа занимает 22,4л, рассчитаем число молей углекислого газа в 0,0003л из пропорции:
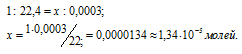
Учитывая, что в одном моле вещества содержится 6,02 . 1023 молекул, находим число молекул в 0,0003л газа:

Ответ: 8,07 .1018 молекул.
