Какое количество молекул двухатомного газа содержится в сосуде объемом

Контрольная работа по теме: «Основы МКТ» 10 класс
1. Что является наиболее наглядным опытным подтверждением существования атомов и молекул? Выберите правильный ответ.
Б. Наблюдение с помощью оптического микроскопа.
В. Капля масла растекается на поверхности воды так, что толщина масляной пленки имеет некоторое минимальное значение.
2. Как изменится давление идеального газа при увеличении концентрации его молекул в 2 раза, если средняя квадратичная скорость молекул остается неизменной? Выберите правильный ответ.
3. Как изменится средняя кинетическая энергия теплового движения молекул идеального газа при увеличении абсолютной температуры в 2 раза? Выберите правильный ответ.
1. Сколько молекул содержится в 1 кг водорода (Н2)?
2. Под каким давлением находится газ в сосуде, если средний квадрат скорости его молекул 106 м 2/ с2, концентрация молекул 3 • 1025 м — 3, а масса каждой молекулы 5 • 10 — 26 кг?
3. В сосуде находится газ при температуре 273 К. Определите среднюю кинетическую энергию хаотического движения молекул газа. На сколько уменьшится кинетическая энергия молекул при уменьшении температуры на 50 К?
1. Какой объем занимают 100 моль ртути?
2. Определить плотность кислорода при давлении 1,3×10 5 Па, если средняя квадратичная скорость его молекул равна 1,4×10 3 м/с.
3. Молекулы какого газа при 20 °С имеют среднюю квадратичную скорость 510 м/с?
4. Найдите количество вещества, содержащееся в алюминиевой отливке массой 135 г.
Какую массу имеет железная отливка, если в ней содержится такое же количество вещества, что и в алюминиевой? Молярная масса алюминия равна 0,027 кг/моль, железа — 0,056 кг/моль.
1. Озеро со средней глубиной 5м и площадью 4км2 «посолили», бросив кристаллик поваренной соли массой 10 мг. Спустя очень длительное время из озера зачерпнули стакан воды объемом 200 см3. Сколько ионов натрия из брошенного кристаллика оказалось в этом стакане?
2. Молекулы одного газа имеют в 2 раз большую массу, чем молекулы другого газа. Сравните их давления при одинаковых концентрациях молекул, если одинаковы: а) средние энергии; б) средние квадратичные скорости их молекул.
3. Какое число молекул двухатомного газа содержится в сосуде объемом 20 см3 при давлении
1,06 •10 4 Па и температуре 27 °С? Какой энергией теплового движения обладают эти молекулы?
4. Вычислите число молекул, содержащихся в углекислом газе (СО2) массой 2 г.
Какова масса воздуха, в которой содержится такое же число молекул, что и в углекислом газе? Во сколько раз масса воздуха меньше массы углекислого газа? Молярная масса воздуха равна 0,029 кг/моль.
Контрольная работа по теме: «Основы МКТ» 10 класс
1. Что является наиболее наглядным опытным подтверждением движения молекул? Выберите правильный ответ.
А. Возникновение сил упругости при деформации тел.
В. Наблюдение с помощью оптического микроскопа.
2. Как изменится давление идеального газа, если при неизменной концентрации средняя квадратичная скорость молекул увеличится в 3 раза? Выберите правильный ответ.
3. При нагревании идеального газа средняя кинетическая энергия теплового движения молекул увеличилась в 3 раза. Как изменилась при этом абсолютная температура газа? Выберите правильный ответ.
1. Какое количество вещества (в молях) содержится в 10 г воды?
2. Как изменится давление газа, если концентрация его молекул увеличится в 3 раза, а средняя квадратичная скорость молекул уменьшится в 3 раза?
3. Определите температуру газа, если средняя кинетическая энергия хаотического движения его равна5,6 • 10 — 21 Дж.
4. Определите температуру газа, если средняя кинетическая энергия хаотического движения его молекул равна 5,6 ×10 — 21 Дж. При какой температуре будет находиться газ, если средняя кинетическая энергия молекул уменьшится на 20%?
1. За 5 суток полностью испарилось 5×10 — 2 кг воды. Сколько в среднем молекул вылетало с поверхности воды за 1 с?
2. Какое давление на стенки сосуда производят молекулы газа, если масса газа 3 • 10 — 3кг, объем 0,5 • 10 -3 м3, средняя квадратичная скорость молекул 500 м/с?
3. Вычислить число молекул воздуха, находящихся в помещении размером 6 × 4 × 2,5 м при температуре 27 °С и давлении 99,8 кПа.
4. Какое количество вещества содержится в водороде объемом 5 м3 при нормальных условиях?
Вычислите объем кислорода, содержащий такое же количество вещества. Температуру и давление газов считать одинаковыми. Плотность водорода равна 0,09 кг/м3, кислорода — 1,43 кг/м3.
1. При комнатной температуре и нормальном атмосферном давлении допускается вытекание метана в бытовой газовой плите не более 1,1 • 10 — 8 м 3/с. Определите количество молекул газа, появившихся в комнате вследствие такого вытекания, если плита была включена в течение трех часов.
2. Изменится ли давление воздуха, если молекулы азота заменить таким же количеством молекул водяного пара при сохранении:
а) средней квадратичной скорости молекул; б) кинетической энергии молекул?
3. Общая кинетическая энергия молекул многоатомного газа равна 3,2 кДж, а масса 0,02 кг. Найти среднюю квадратичную скорость молекул этого газа.
4. Вычислите число частиц, содержащихся в 1 г водорода.
Считая, что диаметр молекул водорода составляет около 2,3×10 — 10 м, подсчитайте, какой длины можно было бы получить нить, если все молекулы водорода расположить в один ряд вплотную друг к другу. Сравните полученное расстояние с расстоянием от Земли до Луны, которое равно 3,844×10 8м.
Контрольная работа по теме: «Основы МКТ» 10 класс
1. Что является наиболее наглядным опытным подтверждением взаимодействия между молекулами? Выберите правильный ответ.
А. Возникновение сил упругости при деформации тел.
2. Как изменится давление идеального газа, если при неизменной концентрации средняя кинетическая энергия молекул увеличится в 3 раза? Выберите правильный ответ.
3. Абсолютная температура идеального газа увеличилась в 4 раза, а концентрация молекул осталась неизменной. Как изменилось давление газа? Выберите правильный ответ.
А. Давление газа осталось неизменным.
Б. Давление газа увеличилось в 2 раза.
В. Давление газа увеличилось в 4 раза.
1. Чему равна масса молекулы азота (N2)?
2. В 1 м 3 газа при давлении 1,2×10 5Па содержится 2 × 1025 молекул, средняя квадратичная скорость которых 600 м/с. Определить массу одной молекулы этого газа.
3. Какое давление производят пары ртути в баллоне ртутной лампы объемом 3 • 10 — 5 м3 при 300 К, если в ней содержится 10 18 молекул?
4. Найдите средние квадратичные скорости молекул водорода и азота при температуре 300 К.
До какой температуры необходимо нагреть азот, чтобы средняя квадратичная скорость его молекул была равна средней квадратичной скорости молекул водорода при 300 К?
1. Где больше атомов: в стакане воды или в стакане ртути? Восколько раз?
2. Какова средняя квадратичная скорость движения молекул газа, который занимает объем 5 м3 при давлении 2 × 105 Па и имеет массу 6 кг?
3. Гелий находится при температуре 580 К. При какой температуре должен находиться водород, чтобы средняя квадратичная скорость молекул этих газов была одна и та же?
4. Зная постоянную Авогадро, вычислите массу атома и молекулы азота. Во сколько раз масса атома и молекулы кислорода больше массы атома и молекулы азота? Молярная масса атома азота равна 0,014 кг/моль, молекулы кислорода — 0,032 кг/моль.
1. Считая, что объем молекул воды равен 1,1 • 10 — 23 см3, найти, какой процент от всего пространства, занятого водой, приходится на долю самих молекул.
2. Часть стенки сосуда покрыли клеем, поглощающим все падающие молекулы газа. Изменится ли давление газа на этом участке стенки? Ответ обосновать.
3. В баллоне радиолампы объемом 10 — 4 м3 находится 4,1 • 1014 молекул воздуха. Определить среднюю квадратичную скорость молекул, если давление в лампе 13,3 мПа.
4.Какое давление производит на стенки сосуда кислород, если средняя квадратичная скорость движения его молекул равна 500 м/с, а концентрация 2,7×1025 м — 3? Как изменится давление молекул на стенки сосуда, если их скорость уменьшится до 400 м/с?
Контрольная работа по теме: «Основы МКТ» 10 класс
1. Что является наиболее наглядным опытным подтверждением существования промежутков между молекулами? Выберите правильный ответ.
А. Наблюдение с помощью оптического микроскопа.
2. Как изменится давление идеального газа при уменьшении концентрации его молекул в 4 раза, если средняя квадратичная скорость молекул остается неизменной? Выберите правильный ответ.
3. Средняя кинетическая энергия молекул идеального газа увеличилась в 2 раза при неизменной концентрации. Выберите правильное утверждение.
А. Средняя квадратичная скорость молекул газа увеличилась в 2 раза.
Б. Температура газа увеличилась в 2 раза.
В. Давление газа увеличилось более чем в 2 раза.
1. Какова масса 200 моль углекислого газа (СО2)?
2. Определить среднюю кинетическую энергию поступательного движения молекул газов воздуха при давлении 10 5 Па. Концентрация молекул воздуха при нормальных условиях 2,7×10 25 м -3 .
3. Современные вакуумные насосы позволяют понижать давление до 1,3 ×10 -10Па. Сколько молекул газа содержится в 1 см3 при указанном давлении и температуре 27 °С?
4. Определите среднюю кинетическую энергию и концентрацию молекул одноатомного газа при температуре 300 К и давлении 101 кПа. Как изменятся кинетическая энергия и концентрация молекул газа, если температура газа уменьшится в 2 раза?
1. Зная число Авогадро, определите объем и диаметр атома золота.
2. Каково давление углекислого газа (СО2), если в баллоне объемом 40 л содержится 5×1024 молекул, а средняя квадратичная скорость молекул 400 м/с?
3. При какой температуре средняя квадратичная скорость молекул углекислого газа СО2 равна 400м/с?
4. Определите число молекул, содержащихся в стакане воды. Вообразим теперь, что все эти молекулы пометили и вылили из стакана в Мировой океан. Если затем перемешать воду в океане и зачерпнуть из него один стакан, то как много в нем будет меченых молекул? В Мировом океане содержится примерно 1,7х1018 м3 воды.
1. Расстояние между центрами соседних атомов золота равно 2,9 • 10 — 10 м. Сколько атомов уложится по толщине листочка золота толщиной 0,1 мкм?
2. В герметично закрытом сосуде находится смесь из одного моля водорода и двух молей кислорода при давлении р0. Между газами происходит реакция с образованием водяного пара. Какое давление установится в баллоне после охлаждения до первоначальной температуры? Пар не конденсируется.
3. Ампула объемом 1 см3, содержащая воздух при нормальных условиях (р0 = 10 5Па и Т0 = 273 К), оставлена в космосе, где давление можно принять равным нулю. В ампуле пробито отверстие. Через какое время давление в ампуле тоже станет равным нулю, если за каждую секунду из нее вылетает 108 молекул?
4. Вычислите среднюю квадратичную скорость движения молекул аргона, если известно, что газ находится в сосуде под давлением 3х105 Па и имеет плотность 1 кг/м3. С какой кинетической энергией движутся молекулы аргона, если молярная масса аргона равна 0,04 кг/моль?
Контрольная работа по теме: «Основы МКТ» 10 класс
1. Перечислите известные вам доказательства существования молекул.
2. Как изменится давление идеального газа, если при неизменной концентрации средняя квадратичная скорость молекул увеличится в 2 раза? Выберите правильный ответ.
3. Абсолютная температура идеального газа увеличилась в 3 раза при неизменной концентрации. Выберите правильное утверждение.
А. Средняя кинетическая энергия молекул газа увеличилась в √3 раз.
Б. Давление газа увеличилось в 3 раза.
В. Средняя квадратичная скорость молекул газа увеличилась в 9 раз.
1. Какую массу имеют 2 • 1023 молекул азота (N2)?
2. Определить среднюю квадратичную скорость молекул газа, находящегося под давлением 6×105 Па, если концентрация молекул 1025 м — 3, а масса каждой молекулы 2 • 10 — 26 кг.
3. При температуре 320 К средняя квадратичная скорость молекул кислорода 500 м/с. Определить массу молекулы кислорода, не пользуясь Периодической системой элементов.
4. В баллоне радиолампы объемом 10 -4 м3 находится 4,1×1014 молекул воздуха. Определите концентрацию молекул, находящихся в лампе. С какой средней квадратичной скоростью движутся молекулы воздуха, если давление в лампе равно 13,3 мПа? Молярная масса воздуха равна 0,029 кг/моль.
1. На деталь, площадь поверхности которой 20 см2, нанесен слой серебра толщиной 1 мкм. Сколько атомов серебра содержится в этом слое?
2. Чему равна средняя кинетическая энергия хаотического движения молекул аргона, если 2 кг его, находясь в сосуде объемом 2м3, оказывают давление 3 • 105 Па (молярная масса аргона 0,04 кг/моль)?
3. Определите средние кинетические энергии поступательного движения и средние квадратичные скорости молекул кислорода и водорода при температуре 27 °С? Какой вывод можно сделать из полученных ответов?
4.Оцените время, за которое запах одеколона (или другого вещества) дойдет до вас. Определите скорость распространения запаха и сравните ее со скоростью движения молекул воздуха.
Объясните с точки зрения МКТ ослабление запаха одеколона с увеличением расстояния.
1. Кристалл поваренной соли имеет кубическую форму и состоит из чередующихся ионов натрия и хлора. Найдите среднее расстояние между ближайшими ионами, если плотность соли 2200 кг/м3.
2. Газ массой 15 кг, молекулы которого состоят из атомов водорода и углерода, содержат 5,64×1026 молекул. Определить массу атомов углерода и водорода, входящих в молекулу этого газа.
3. Определите среднюю квадратичную скорость броуновской частицы при температуре 27 °С. Броуновскую частицу рассматривайте как шарик радиусом 1,5 мкм, плотность которого равна
4. Какое давление на стенки сосуда производят молекулы гелия, если их концентрация равна 2,4× 1022 м — 3, а средняя квадратическая скорость движения 1564 м/с? Изменится ли давление на стенки сосуда, если молекулы гелия заменить молекулами аргона? Ответ обоснуйте. Средние квадратические скорости движения молекул газов считать одинаковыми.
Контрольная работа по теме: «Основы МКТ» 10 класс
1. Приведите факты, свидетельствующие о делимости веществ.
2. Как изменится давление идеального газа, если при неизменной концентрации средняя кинетическая энергия молекул уменьшится в 5 раз? Выберите правильный ответ.
3. Давление идеального газа уменьшилось в 2 раза при неизменной концентрации. Выберите правильное утверждение.
А. Абсолютная температура увеличилась в 2 раза.
Б. Средняя квадратичная скорость молекул газа уменьшилась в √2 раз.
В. Средняя кинетическая энергия молекул газа увеличилась в 2 раза.
1. Определите массу одной молекулу воды.
2. Найти среднюю кинетическую энергию молекулы одноатомного газа при давлении 20 кПа. Концентрация молекул этого газа при указанном давлении составляет 3×10 25 м — 3 .
3. Найти температуру газа при давлении 100 кПа и концентрации молекул 10 25м -3.
4. После того, как в комнате включили электрокамин, температура воздуха повысилась от 15 до 23° С. На сколько увеличилась средняя кинетическая энергия движения молекул? Вычислите, на сколько процентов уменьшилось число молекул воздуха в комнате, если давление осталось прежним.
1. В комнате объемом 60 м3 испарили капельку духов, содержащую 10 — 4 г ароматического вещества. Сколько молекул ароматического вещества попадает в легкие человека при каждом вдохе? Объем вдыхаемого воздуха 1 дм3. Молярная масса ароматического вещества 1 кг/моль.
2. Определите кинетическую энергию хаотического поступательного движения всех молекул любого газа в баллоне емкостью 10 л и давлением 0,4 • 106 Па.
3. После того, как в комнате протопили печь, температура поднялась с 15 °С до 27 °С при неизменном давлении. На сколько процентов изменилось число молекул в этой комнате?
4. Чем отличаются друг от друга молекулы сухого и сырого воздуха? Проведите качественный анализ строения этих молекул. Плотность какого воздуха больше — сырого или сухого? (Считать, что сухой и сырой воздух находятся при заданной температуре и заданном давлении).
1. В помещении площадью 100 м3 и высотой 4 м разлит 1 л ацетона. Сколько молекул ацетона содержится в 1 м3 воздуха, если весь ацетон испарился и равномерно распределился по помещению? Химическая формула ацетона (СН)2СО.
2. Сосуд сообщается с окружающим пространством через малое отверстие. Температура газа в окружающем пространстве Т, давление р. Газ настолько разрежен, что молекулы при пролете в сосуд и из сосуда на протяжении размеров отверстия не сталкиваются друг с другом. В сосуде поддерживается температура 4Т. Каким будет давление в сосуде?
3. Молекула азота при нормальных условиях движется со скоростью 454 м/с. Определите импульс и среднее значение кинетической энергии поступательного движения молекул азота. Сравните импульс и кинетическую энергию молекул азота и кислорода при условии, что молекулы этих веществ движутся с одинаковыми скоростями.

IV. МОЛЕКУЛЯРНАЯ ФИЗИКА И ТЕРМОДИНАМИКА
7.ЗАКОНЫ ИДЕАЛЬНЫХ ГАЗОВ.
МОЛЕКУЛЯРНО-КИНЕТИЧЕСКАЯ ТЕОРИЯ ГАЗОВ
Основные формулы
1. Количество вещества
ν m , или ν N ,
NA
где N – число структурных элементов системы (молекул, атомов, ионов и т. д.); NA – постоянная Авогадро; – молекулярная масса.
2. Уравнение состояния идеальных газов (уравнение Менделеева– Клапейрона)
pV m RT ,
где т – масса газа; – молярная масса газа; R – универсальная газовая постоянная; Т – термодинамическая температура.
3. Закон Дальтона
p p1 p2 … pn,
где р – давление смеси газов; рi – парциальное давление i-го компонента смеси;
п – число компонентов смеси. 4. Молярная масса смеси газов
cм m1 m2 … mn . ν1 ν2 … νn
5. Концентрация частиц (молекул, атомов и т.п.) однородной системы
n N V NA
V NA  .
.
где V – объем системы; – плотность вещества.
6. В МКТ пользуются физической (идеализированной) моделью, называемой идеальным газом, согласно которой:
а) собственный объем молекул газа пренебрежимо мал по сравнению с объемом сосуда.
б) пренебрегают силами взаимодействия между молекулами. Следовательно, потенциальная энергия взаимодействия молекул принимается равной нулю, а внутренняя энергия идеально газа – равной средней кинетической энергии молекул.
в) столкновения молекул газа между собой и со стенками сосуда абсолютно упругие.
68

Заметим, что понятие идеального газа не применимо при очень низких температурах (близких к температуре конденсации данного газа) и при очень высоких давлениях.
Макропараметры газа р, V, T.
Основное уравнение МКТ идеального газа – уравнение, которое связывает макропараметры идеального газа с микропараметрами:
р | 1 | nm V 2 , | (3.1) | ||||||||||||||||||||||||||||||||
3 | ср | ||||||||||||||||||||||||||||||||||
где р – давление газа; m0 – масса молекулы газа m0 | ; n – число моле- | ||||||||||||||||||||||||||||||||||
кул газа в единице объема; Vср2 | NA | ||||||||||||||||||||||||||||||||||
– среднеквадратичная скорость молекул. | |||||||||||||||||||||||||||||||||||
р | 1 | nm V 2 | 2 | nm | Vср2 | 2 | n E | , | (3.2) | ||||||||||||||||||||||||||
2 | |||||||||||||||||||||||||||||||||||
3 | 0 ср | 3 | 3 | кин | |||||||||||||||||||||||||||||||
где Eкин | – средняя кинетическая энергия поступательного движения моле- | ||||||||||||||||||||||||||||||||||
кулы. | 3 | ||||||||||||||||||||||||||||||||||
Eкин | kT, | (3.3) | |||||||||||||||||||||||||||||||||
R | 2 | ||||||||||||||||||||||||||||||||||
где k | – постоянная Больцмана (k = 1,38 · 10–23 Дж/К). | ||||||||||||||||||||||||||||||||||
NA | |||||||||||||||||||||||||||||||||||
Основное управление МКТ можно записать в виде | |||||||||||||||||||||||||||||||||||
р nkT. | (3.4) | ||||||||||||||||||||||||||||||||||
Из уравнения (3.3) следует, что кинетическая энергия не зависит от ро- | |||||||||||||||||||||||||||||||||||
да вещества, а зависит только от температуры. | |||||||||||||||||||||||||||||||||||
7. Скорость молекул: средняя квадратичная | |||||||||||||||||||||||||||||||||||
vкв | , | или | vкв | ; | |||||||||||||||||||||||||||||||
3kT m1 | 3RT | ||||||||||||||||||||||||||||||||||
средняя арифметическая | |||||||||||||||||||||||||||||||||||
v | , | или | v | ; | |||||||||||||||||||||||||||||||
8kT m1 | 8RT | ||||||||||||||||||||||||||||||||||
наиболее вероятная | |||||||||||||||||||||||||||||||||||
v | , | или | v | 2RT | , | ||||||||||||||||||||||||||||||
в | 2kT m | в | |||||||||||||||||||||||||||||||||
1 | |||||||||||||||||||||||||||||||||||
где т1 – масса одной молекулы. | |||||||||||||||||||||||||||||||||||
69
Примеры решения задач
Задача 1. Сколько молекул содержится в 1 м3 водорода при нормальных условиях? Какова масса одной молекулы водорода?
Д а н о:
V = 1 м3
T = 273 ºК р = 1·105 Па
= 2·10–3 кг/моль
п0 = ? т = ?
Р е ш е н и е
Число молекул в одном моле любого газа (число Авогадро) NА = 6,02·1023 1/моль. Объем одного моля любого газа (в том числе и водорода) при нормальных условиях V0 = 22, 4 л/моль = 22,4·10–3 м3/моль.
Следовательно, число молекул водорода, содержащихся в 1 м3 при нормальных условиях, определяется соотношением
n0 NA 2,69 1025 1/моль.
V0
Эта величина одинакова для любого газа и называется числом Лошмидта. Масса одной молекулы водорода
NA
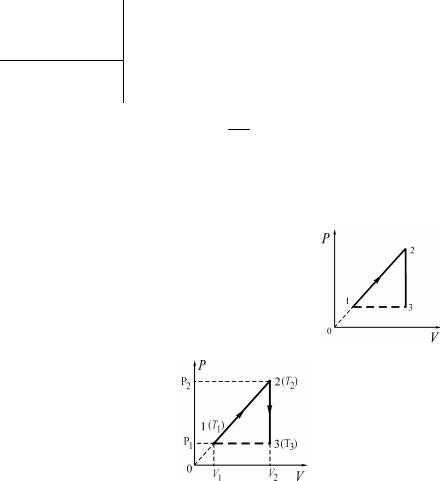
Задача 2. Моль одноатомного идеального газа участвует в процессе 1–2–3, представленном на p–V диаграмме.
Всостоянии 1 температура газа равна Т1 =
=100 ºК, а в состоянии 2 – Т2 = 400 ºК. Определите температуру газа Т3 в точке 3.
Т1 | Дано: | Решение |
= 100 ºК | ||
Т2 | = 400 ºК | V1 p1; |
Т3 = ? | ||
V2 p2. | ||
Запишем уравнение Менделеева–Клапейрона для состояний газа 1 и2:
pV RT ; | p2 RT ; | |||||
1 | 1 | 1 | 1 | 1 | ||
p2 RT | p2 | T | ||||
p V RT , | или | 1 | 1 | . | ||
p2 | ||||||
2 2 | 2 | 2 | 2 | T | ||
2 | 2 | |||||
70 | ||||||
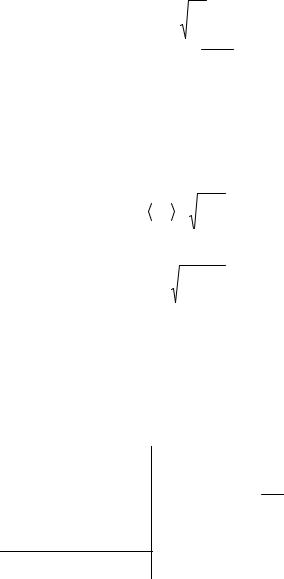
Для изохорического процесса (2–3) можно записать:
p1 | T3 | ; | T1 | T3 | , следовательно, | ||
p2 | T2 | T2 | T2 | ||||
T3 
 T1 T2 200К.
T1 T2 200К.
Задача 3. Температур поверхностного слоя Солнца (фотосферы) – около 6000 ºК. Почему с поверхности Солнца не улетают атомы водорода, из которых в основном состоит фотосфера?
Р е ш е н и е
Средняя квадратичная скорость атомов водорода в фотосфере
Вторая космическая скорость
Как видно, средняя квадратичная скорость в 51 раз меньше второй космической скорости, поэтому большинство атомов водорода не могут вырваться из поля тяготения Солнца.
Задача 4. Определить плотность смеси 4 г водорода и 32 г кислорода при температуре 7 ºС и давлении 700 мм рт.ст.
Д а н о:
m1 = 4 г = 0,004 кг1 = 2·10–3 кг/моль m2 = 32 г = 0,032 кг
2 = 32·10–3 кг/моль T = 280 0К
рсм = 700 мм рт.ст. = = 700·133 = 9,31·104 Па
см = ?
отсюда
Р е ш е н и е
Чтобы найти плотность смеси, необходимо знать ее массу и объем, тогда
cм mсм ; mсм m1 m2 .
V
Объем смеси можно найти, используя уравнение Менделеева–Клапейрона:
p | см | p p | 2 | ; p V | m1 | RT; | p V | m2 | RT ; | |||||||
1 | 1 | 1 | 2 | 2 | ||||||||||||
m | m | 2 | RT | |||||||||||||
pсм | 1 | , | ||||||||||||||
V | ||||||||||||||||
2 | ||||||||||||||||
1 | ||||||||||||||||
71

m | m | ||||||||||
1 | 2 | ||||||||||
1 | 2 | RT | |||||||||
V | , | ||||||||||
и тогда | pсм | ||||||||||
4 10 3 | 32 10 3 9,31 104 | ||||||||||
m1 | m2 pсм | 3 | |||||||||
см | 0,48 кг/м . | ||||||||||
m | m | 2 | 4 10 | 3 | 32 10 | 3 | |||||
1 | RT | 8,31 280 | |||||||||
3 | 3 | ||||||||||
1 | 2 10 | 32 10 | |||||||||
2 | |||||||||||
Задача 5. На осях р-V изображены графически процессы, с помощью которых идеальный газ был переведен из состояния 1 в состояние 4. Начертить, как будут выглядеть эти же процессы 1-2, 2-3 и
3-4 на осях р-Т и V-Т, если 1-2 – изотерма. Расшифруем, графики каких процессов пока-
заны на осях:
1-2 – изотермическое сжатие;
2-3 – изобарическое сжатие;
3-4 – изохорический процесс с понижением давления.
Вычертим графики этих же процессов на других осях.
72
Задачи
7-1. В баллоне объемом 22,4 л находится водород при нормальных условиях. После того как в баллон было дополнительно введено некоторое количество гелия, давление в баллоне возросло до р2 = 0,25 МПа, а температура не изменилась. Определить массу гелия, введенного в баллон.
7-2. Смесь водорода и азота общей массой т = 290 г при температуре Т = 600 ºК и давлении р = 2,46 МПа занимает объем V = 30 л. Определить массу т1 водорода и массу т2 азота.
7-3. Оболочка воздушного шара имеет объем V = 1 600 м3. Найти подъемную силу FП водорода, наполняющего оболочку, на высоте, где давление р = 60 кПа и температура Т = 280 ºК. При подъеме шара водород может выходить через отверстиев нижней части.
7-4. Водород находится при температуре Т = 300 ºК. Найти среднюю кинетическую энергию вращательного движения одной молекулы, а также суммарную кинетическую энергию всех молекул этого газа; количество вещества водорода = 0,5 моль.
7-5. В баллоне объемом 10 л находится гелий под давлением р1 = 1 МПа при температуре Т1 = 300 ºК. После того как из баллона было взято 10 г гелия, температура в баллоне понизилась до Т2 = 290 ºК. Определить давление р2 гелия, оставшегося в баллоне.
7-6. Баллон содержит т1 = 80 г кислорода и т2 = 320 г аргона. Давление смеси р = 1 МПа, температура 300 ºК. Принимая данные газа за идеальные, определить объем баллона.
7-7. Какой объем занимает смесь азота массой т1 = 1 кг и гелия массой т2 = 1 кг при нормальных условиях?
7-8. В баллоне емкостью 15 л находится смесь, содержащая т1 = 10 г водорода, т2 = 54 г водяного пара и т3 = 60 г окиси углерода. Температура смеси 27 ºС. Определить давление.
7-9. Количество вещества гелия = 1,5 моль, температура Т = 120 ºК. Определить суммарную кинетическую энергию поступательного движения всех молекул этого газа.
7-10. Теплоизолированный сосуд объемом V = 2 м3 разделен пористой перегородкой на две равные части. Атомы гелия могут свободно проникать через поры в перегородке, а атомы аргона – нет. В начальный момент в одной части сосуда находится m = 1 кг гелия, а в другой – m = 1 кг аргона, а средняя квадратичная скорость атомов аргона игелия одинакова и составляет1000 м/с.
Определить температуру гелий-аргоновой смеси после установления равновесия в системе.
7-11. Найти плотность газовой смеси водорода и кислорода, если их массовые доли 1 и 2 равны соответственно 1/9 и 8/9. Давление смеси равно 100 кПа, температура Т = 300 ºК.
7-12. В сосуде объемом 2,24 л при нормальных условиях находится кислород. Определить количество вещества и массу т кислорода, а также концентрацию п0 его молекул в сосуде.
73

7-13. В сосуде находится смесь 10 г углекислого газа (СО2) и 15 г азота (N2). Найти плотность этой смеси при температуре 27 0С и давлении 1,5·105 Па.
7-14. Сосуд объемом 20 л содержит смесь водорода и гелия при температуре t = 20 ºС и давлении 2 атм. Масса смеси т = 5 г. Найти отношение массы водорода к массе гелия в данной смеси.
7-15. В баллон емкостью V = 12 л поместили т1 = 1,5 кг азота при температуре t1 = 327 ºС. Какое давление р2 будет создавать азот в баллоне при температуре t2 = 50 ºС, если 35 % азота будет выпущено. Каково было начальное дав-
ление р1?
7-16. На дне сосуда, заполненного воздухом, лежит полыйстальной шарик радиусом r = 2 см. Масса шарика 5 г. До какого давления р надо сжать воздух в сосуде, чтобы шарик поднялся вверх? Считать, что воздух при больших давлениях подчиняется уравнению газового состояния. Температура воздуха t = 20 ºС = = const (сжатие воздуха происходитдостаточно медленно).
7-17. На какой глубине радиус пузырька воздуха вдвое меньше, чем у поверхности воды, если давление у поверхности равно р0?
7-18. Определить температуру газа, находящегося в закрытом баллоне, если его давление увеличилось на 0,4 % первоначально при нагревании на
T = 1 К.
7-19. Тонкостенный резиновый шар собственным весом 0,6 Н наполнен неоном и погружен в озеро на глубину h = 120 м. Найти массу неона, если шар находится в положении равновесия. Атмосферное давление р0 = 1,03·105 Па, температура на глубине озера t = + 4 ºС. Натяжением резины пренебречь.
7-20. В закрытом сосуде емкостью V = 2 м3 находится т1 = 2,7 кг воды и т2 = 3,2 кг кислорода. Найти давление в сосуде при температуре t = 527 ºС, зная, что в этих условиях вся вода превращается в пар (считать, что пар в данном случае подчиняется законам идеального газа).
7-21. В теплоизолированный сосуд объемом V = 2 л, содержащий одноатомный идеальный газ при температуре Т1 = 300 К, помещают кусочек железа массой m = 100 г, нагретый до температуры Т2 = 500 К. Определить давление р2 газа после установления теплового равновесия, если его начальное давление равно р1 = 105 Па. Объемом железа по сравнению с объемом сосуда пренебречь. Удельная теплоемкость железа с = 0,46 · 103 Дж/кг·К.
7-22. В идеальном газе происходят процессы 1-2; 2-3; 3-4. Изобразить эти процессы на координатных осях р–T, р–V.
7-23. В лифте, движущимся с ускорением а = 5 м/с2, направленным вверх, находится цилиндрический сосуд, закрытый поршнем массой М = 20 кг и площадью S = 100 см2. Под поршнем находится идеальный газ. Поршень расположен на расстоянии h = 22 см от дна сосуда. Определите, на
74

какую величину h переместится поршень, если лифт будет перемещаться с тем же по модулю ускорением, направленным вниз. Температура газа не изменяется, атмосферное давление p0 = 105 Па. Ускорение свободного падения поршня g = 10 м/с2. Трением поршня о стенки сосуда пренебречь.
7-24. В цилиндре под невесомым поршнем площадью S = 100 см2 находится 1 моль идеального газа при температуре t1 = 100 ºС. К поршню через два блока на невесомой нерастяжимой нити подвешен груз массой М = 17 кг. На какую высоту h поднимется груз, если охладить газ до температуры t2 = 0 ºС. Атмосферное давление p0 = 105 Па. Трением пренебречь.
7-25. В вертикально расположенном цилиндрическом сосуде находится идеальный газ массой m с молярной массой . Газ отде
