Какое из веществ проявляет наиболее сильные кислотные свойства ch2cl
Инструкция
— Выберите один из вариантов в каждом из 21 вопросов;
— Нажмите на кнопку «Показать результат»;
— Скрипт не покажет результат, пока Вы не ответите на все вопросы;
— Загляните в окно рядом с номером задания. Если ответ правильный, то там (+). Если Вы ошиблись, там (-);
— За каждый правильный ответ начисляется 1 балл;
— Оценки: менее 10.5 баллов — НЕУДОВЛЕТВОРИТЕЛЬНО, от 10.5 но менее 15.75 — УДОВЛЕТВОРИТЕЛЬНО, 15.75 и менее 21 — ХОРОШО, 21 — ОТЛИЧНО;
— Чтобы сбросить результат тестирования, нажать кнопку «Сбросить ответы».
Тест 15. Карбоновые кислоты, сложные эфиры, жиры
- В молекуле этановой кислоты число σ— и π-связей равн:
6 σ-связей и 1 π-связь
6 σ-связей и 2 π-связи
7 σ-связей и 1 π-связь
8 σ-связей и 2 π-связи - В реакцию «серебряного зеркала» вступает кислота:
щавелевая
трихлоруксусная
бензойная
муравьиная - В результате гидролиза жидкого жира образуются:
глицерин и непредельные кислоты
твердые жиры и смесь кислот
глицерин и предельные кислоты
твердые жиры и глицерин - В состав жиров входят:
уксусная кислота
неорганические кислородсодержащие кислоты
высшие предельные и непредельные карбоновые кислоты
бутановая кислота - В схеме органического синтеза СН3-СОН _+Н2_→ X1_+HBr_→ X2, продуктами превращений Х1 и Х2 являются:
уксусная кислота и бромэтан
этанол и бромэтан
этанол и бромэтен
уксусная кислота и бромэтен - В схеме органического синтеза Х1_гидролиз_→ СН3СООК, исходным реагентом Х1 является:
хлорэтан
карбонат калия
этиловый эфир уксусной кислоты
этиловый эфир муравьиной кислоты - В схеме превращений С2Н2 → CH3COH → X → CH3COONa, промежуточным продуктом является:
уксусная кислота
ацетальдегид
этанол
метановая кислота - В схеме превращений СН4 → Х1→ СН3ОН → Х2→ НСООН → НСООС2Н5, промежуточными продуктами Х1 и Х2 являются:
Х1-бромметан, Х2-метаналь
Х1-ацетилен, Х2-формальдегид
Х1-этанол, Х2-ацетальдегид
Х1-этилен, Х2-ацетальдегид - В схеме превращений С6Н12О6 → X → СН3СООН, промежуточным продуктом Х является:
этаналь
пропанол
пропаналь
этанол - В цепочке превращений НС ≡ СН _+Н2О_((HgSO4))→X1__(O)→ X2__CI2 (1моль) → X 3__+NaOH→ X4, формулы веществ Х2 и Х4 соответственно:
CH3 — CHO и СН3-СООН
СН3 — СООН и СН2Cl — COONa
СН3 -СН2ОН и СН3 -СН2ОNa
СН3 -СООН и СН3 -СОCI - Верны ли следующие суждения?
А. Этилацетат образуется при взаимодействии уксусной кислоты с этиленом.
Б. При восстановлении этилацетата образуются спирт и кислота.
верно только А
верно только Б
оба суждения неверны
верны оба суждения - Верны ли следующие суждения?
А. Продуктом дегидратации муравьиной кислоты является угарный газ.
Б. Муравьиную кислоту среди других кислот можно распознать с помощью аммиачного раствора оксида серебра.
верно только А
верно только Б
оба суждения неверны
верны оба суждения - Верны ли следующие утверждения о щавелевой кислоте?
А. Простейшая двухосновная карбоновая кислота, образует средние и кислые соли.
Б. Гомолог муравьиной кислоты.
верно только А
верно только Б
оба утверждения неверны
верны оба утверждения - Взаимодействие между пальмитиновой кислотой и глицерином называется:
омылением
этерификацией
гидратацией
дегидратацией - Взаимодействие уксусной кислоты с натрием является реакцией:
замещения, экзотермической
обмена, экзотермической
замещения, эндотермической
присоединения, экзотермической - Гидроксильная группа отщепляется от молекулы уксусной кислоты при взаимодействии с:
металлами
щелочами
спиртами
карбонатами металлов - Жидкие жиры переводит в твердые:
раствор КОН
водород
раствор KMnO4
бром - Из свойств: 1) при комнатной температуре бесцветная жидкость, 2) газообразное вещество, 3) без запаха, 4) с характерным запахом, 5) плохо растворима в воде, 6) неограниченно растворима в воде, 7) слабый электролит, 8) сильный электролит — верно характеризуют уксусную кислоту следующие:
2,4,5,6,7
1,3,6,8
1,4,5,7
1,4,6,7 - Какое из веществ проявляет наиболее сильные кислотные свойства?
CH2Cl-COOH
CH3-COOH
CCl3-COOH
CHCl2-COOH - Какой из металлов реагирует с уксусной кислотой с максимальной скоростью?
железо
олово
цинк
кальций - Карбоновая кислота строения СН3-СН(С2Н5)-СООН называется:
2-этилпропановая
2-метилбутановая
2-этилпропионовая
2-метилпропановая
Карбоновые кислоты — класс органических соединений, молекулы которых содержат одну или несколько карбоксильных групп
COOH.
Имеют разнообразное промышленное применение и большое биологическое значение.
Общая формула одноосновных карбоновых кислот CnH2nO2 .
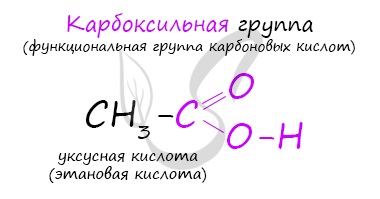
Классификация карбоновых кислот
По количеству карбоксильных групп в молекуле карбоновые кислоты подразделяются на:
- Одноосновные — 1 карбоксильная группа
- Двухосновные — 2 карбоксильных группы
- Трехосновные — 3 карбоксильных группы
Высшие карбоновые кислоты называют жирными кислотами. Более подробно мы изучим их теме, посвященной жирам, в состав
которых они входят.
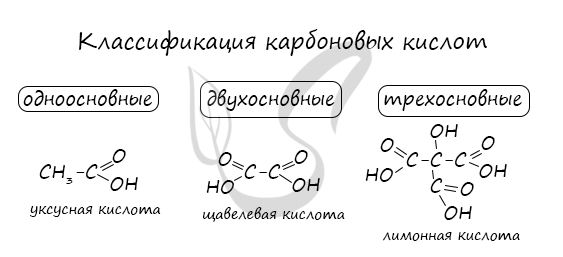
Номенклатура и изомерия карбоновых кислот
Названия карбоновых кислот формируются путем добавления суффикса «овая» к названию алкана с соответствующим числом атомов углерода
и слова кислота: метановая кислота, этановая кислота, пропановая кислота, и т.д.
Многие карбоновые кислоты имеют тривиальные названия. Наиболее известные:
- Метановая — HCOOH — муравьиная кислота
- Этановая — CH3-COOH — уксусная кислота
- Пропановая — C2H5-COOH — пропионовая кислота
- Бутановая — C3H7-COOH — масляная кислота
- Пентановая — C4H9-COOH — валериановая кислота
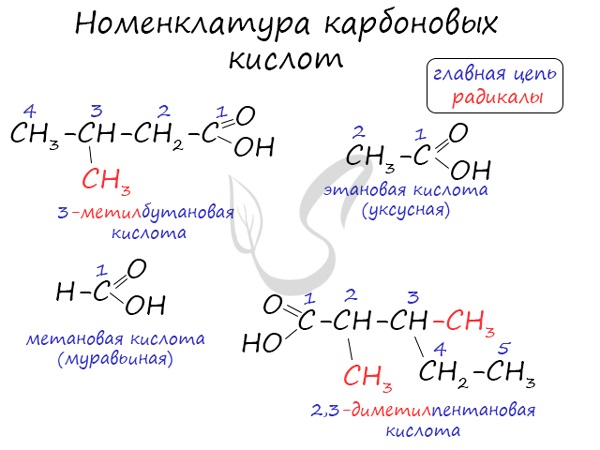
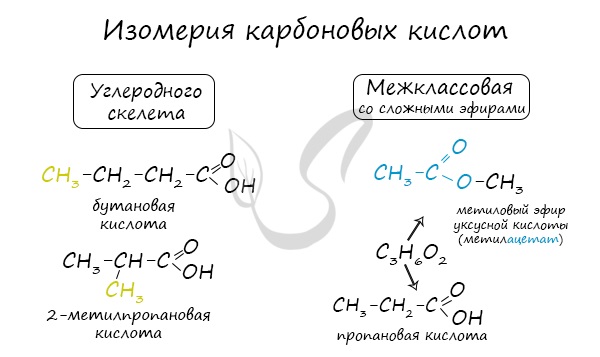
Для предельных карбоновых кислот характерна структурная изомерия: углеродного скелета, межклассовая изомерия со сложными
эфирами.
Получение карбоновых кислот
- Окисление алканов
- Окисление спиртов
- Окисление альдегидов
- Синтез муравьиной кислоты
- Синтез уксусной кислоты
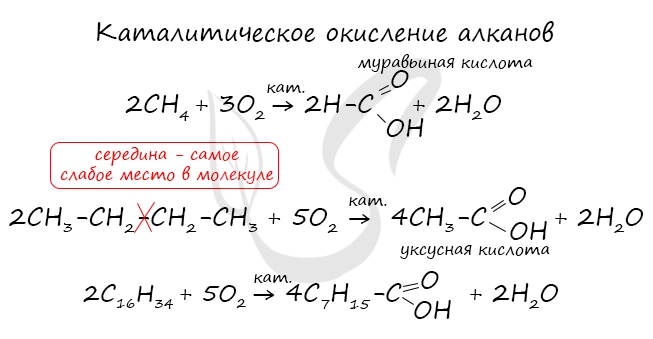
При повышенной температуре и в присутствии катализатора становится возможным неполное окисление алканов, в результате которого
образуются кислоты.
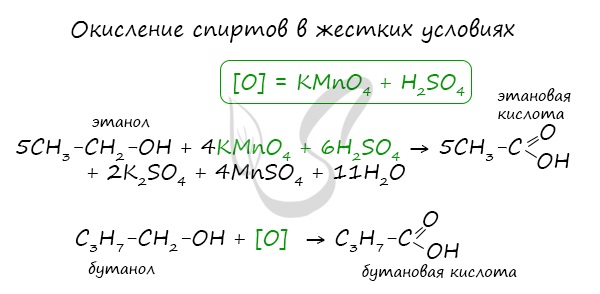
При реакции спиртов с сильными окислителями, такими как подкисленный раствор перманганата калия, спирты окисляются
до соответствующих кислот.
При окислении альдегиды образуют соответствующие карбоновые кислоты. Окисление можно проводить качественной реакцией
на альдегиды — реакцией серебряного зеркала.

Обратите особое внимание, что при написании реакции с аммиачным раствором серебра в полном виде, правильнее будет указать не кислоту, а ее аммиачную соль. Это связано с тем, что выделяющийся аммиак, который обладает основными свойствами, реагирует с кислотой с образованием соли.

Окисление альдегидов также может быть успешно осуществлено другим реагентом — свежеосажденным гидроксидом меди II.
В результате такой реакции образуется осадок кирпично-красного цвета оксида меди I.

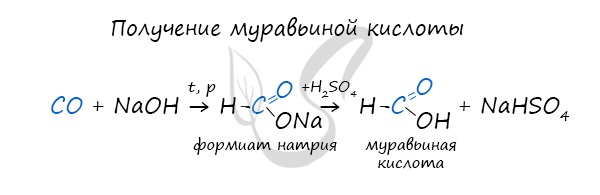
Существует специфический способ получения муравьиной кислоты, который заключается в реакции щелочи с угарным газом — образуется формиат (соль муравьиной кислоты). В результате добавления раствора серной кислоты к формиату получается
муравьиная кислота.
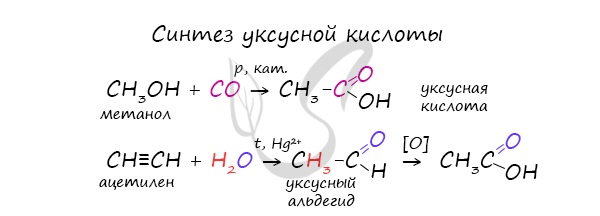
Специфичность синтеза уксусной кислоты заключается в реакции угарного газа с метанолом, в результате которой она образуется.
Также уксусную кислоту можно получить другим путем: сначала провести реакцию Кучерова, в ходе которой образуется уксусный альдегид.
Окислить его до уксусной кислоты можно аммиачным раствором оксида серебра или гидроксидом меди II.
Химические свойства карбоновых кислот
Для карбоновых кислот не характерны реакции присоединения. Карбоновые кислоты обладают более выраженными кислотными свойствами, чем
спирты.
- Кислотные свойства
- Галогенирование
- Особые свойства муравьиной кислоты
- Разложение муравьиной кислоты
Карбоновые кислоты вступают в реакции с металлами, которые способны вытеснить водород (стоят левее водорода в ряду напряжений
металлов) из кислоты. Реагируют также с основаниями, с солями более слабых кислот, например, угольной кислоты.

Галогенирование происходит по типу замещения в радикале, который соединен с карбоксильной группой. Напомню, что наиболее легко
замещается водород у третичного, чуть сложнее — у вторичного, и значительно сложнее — у первичного атома углерода.

Сила карбоновых кислот тем выше, чем меньше электронной плотности сосредоточено на атоме углерода в карбоксильной группе.
Поэтому самая слабая из трех кислот — уксусная, чуть сильнее — хлоруксусная, за ней — дихлоруксусная и самая сильная —
трихлоруксусная.
Перераспределение электронной плотности в молекулах этих кислот для лучшего запоминания лучше увидеть наглядно. Это
перераспределение обусловлено большей электроотрицательностью хлора, который притягивает электронную плотность.

Муравьиная кислота отличается от своих гомологов. За счет наличия у нее альдегидной группы, она, единственная из карбоновых кислот,
способна вступать в реакцию серебряного зеркала.
В такой реакции идет ее окисление до нестойкой угольной кислоты, которая распадается на углекислый газ и воду.

При нагревании и в присутствии серной кислоты (водоотнимающего компонента) муравьиная кислота распадается на воду и угарный газ.
HCOOH → (t, H2SO4) CO↑ + H2O
Сложные эфиры
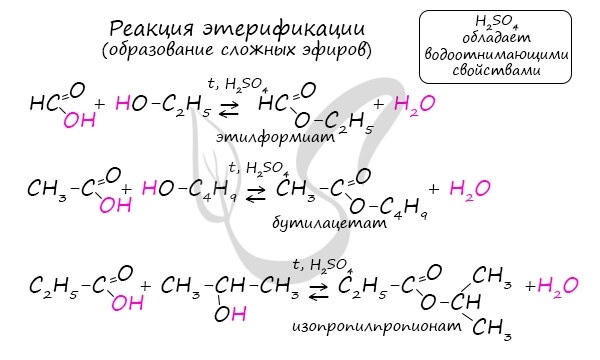
Получение сложных эфиров происходит в реакции этерификации (лат. aether — эфир), заключающейся во взаимодействии карбоновой кислоты
и спирта.
Названия сложных эфиров формируются в зависимости от того, какой кислотой и каким спиртом эфир образован. Примеры:
- Метановая кислота + метанол = метиловый эфир метановой кислоты (метилформиат)
- Этановая кислота + этанол = этиловый эфир уксусной кислоты (этилацетат)
- Метановая кислота + этанол = этиловый эфир метановой кислоты (этилформиат)
- Пропановая кислот + бутанол = бутиловый эфир пропионовой кислоты (бутилпропионат)
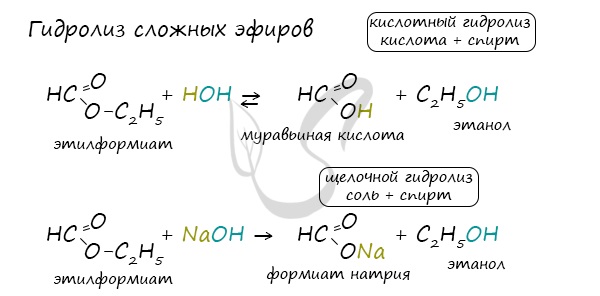
Для сложных эфиров характерной реакцией является гидролиз — их разложение. Возможен щелочной гидролиз, при котором образуется соль
кислоты и спирт, и кислотный гидролиз, при котором образуются исходные спирт и кислота.
Кислотный гидролиз протекает обратимо, щелочной — необратимо.
Реакция щелочного гидролиза по-другому называется реакция омыления, и напомнит о себе, когда мы дойдем до темы жиров.
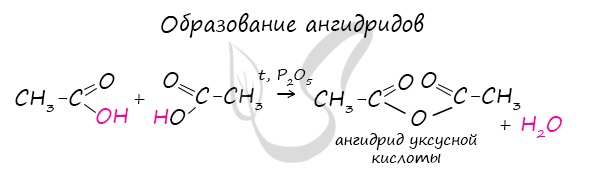
Ангидриды
Ангидриды — химические соединения, производные неорганических и органических кислот, образующиеся при их дегидратации.
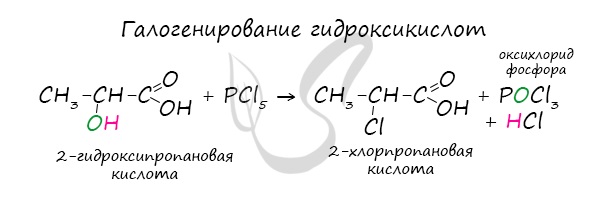
Хлорангидриды карбоновых кислот образуются в реакции карбоновых кислот с хлоридом фосфора V.

Следующая реакция не имеет отношения к ангидридам, однако (из-за их схожести) вы увидите ее здесь для наилучшего запоминания.
Это реакция галогенирования гидроксикислот, в результате которой гидроксогруппа в радикале меняется на атом галогена.
Непредельные карбоновые кислоты
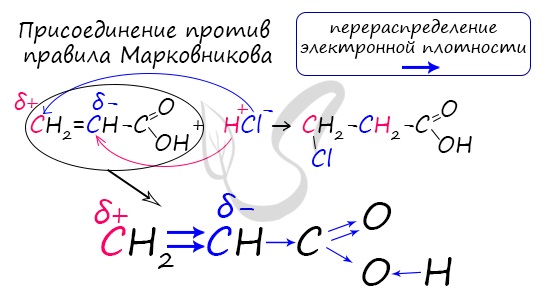
Распределение электронной плотности в молекулах творит чудеса: иногда реакции идут против правила Марковникова. Так происходит
в непредельной акриловой кислоте.
© Беллевич Юрий Сергеевич 2018-2020
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение
(в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов
без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования,
обратитесь, пожалуйста, к Беллевичу Юрию.
Большинство органических соединений можно рассматривать как кислоты, т.к. в их молекулах имеются связи атомов водорода с атомами С, О, N, S. Органические соединения классифицируют по кислотным центрам на С–H, O–H, N–H, S–H кислоты.
Кислотный центр – это элемент и связанный с ним атом водорода. На кислотные свойства органических соединений оказывает влияние стабильность аниона, образующегося при отдаче протона Н+. На стабильность аниона оказывают влияние следующие факторы:
1. Природа элемента в кислотном центре.
а) Электроотрицательность элементов в кислотном центре.
CH3–CH2OH (этанол) pKa=18; СH3–CH2–HNH (этаномин) pKa=30
Чем ниже pKa, тем сильнее кислота. Поскольку О2 является более электроотрицательным элементом, чем азот, то связь О–Н более полярна чем связь N–H, атом водорода в О–Н кислотном центре будет более подвижным, чем в N–Н центре. Исходя из величины pK этанол проявляет более выраженные кислотные свойства по сравнению с этаномином, т.к. образующийся при отщеплении протона алкоксид-ион CH3–CH2O- будет обладать более высокой стабильностью по сравнению с алкиламид-ионом CH3–CH2–HN-. Это объясняется тем, что более электроотрицательный кислород в алкоксид-ионе способен в гораздо большей степени нести отрицательный заряд по сравнению с атомом N в алкиламид-ионе.
б) Поляризуемость элемента в кислотном центре.
CH3–CH2–OH (этанол) pKa=18; CH3–CH2–SH (энантиол) pKa=10,5
Исходя из величины рКа энантиол проявляет более выраженные кислотные свойства по сравнению с этанолом. Если брать во внимание электроотрицательность элемента в кислотном центре, то этанол должен быть более сильной кислотой по сравнению с этантиолом, но в данном случае преобладает не фактор электроотрицательности, а фактор поляризуемости.
Поляризуемость атома – это мера смещения, рассредоточения электронного облака атома под действием внешнего электронного поля.
Поляризуемость атома возрастает с увеличением числа электронов и энергетических уровней. Атом серы более поляризуем, чем атом кислорода, т.к. атом серы имеет 3 энергетических уровня, а атом кислорода — 2. Образующийся при отщеплении протона меркаптид-ион СH3–CH2–S- будет обладать более высокой стабильностью по сравнению с алкоксид-ионом CH3–CH2–O- , т.к. в связи с более высокой поляризуемостью атома серы отрицательный заряд в меркаптид-ионе делокализован в гораздо большем объеме. Поэтому этантиол проявляет более выраженные кислотные свойства по сравнению с этанолом.
2. Стабилизация аниона за счет сопряжения.
C2H5–OH (этанол) рКа=18; C6H5–OH (фенол) рКа=9,9
[этанол с эффектами, (стер11)]
Исходя из величины рКа фенол проявляет более выраженные кислотные свойства по сравнению с этанолом. Для объяснения этого факта рассмотрим влияние электронных эффектов заместителей в молекулах этих соединений.
Под влиянием указанных электронных эффектов заместителей в молекуле этанола электронная плотность смещена к атому кислорода. Образующийся при отщеплении протона алкоксид-ион СH3–CH2–O- будет обладать низкой стабильностью, т.к. отрицательный заряд в этом анионе практически не делокализован по всей системе, а сосредоточен на атоме кислорода, поэтому этанол проявляет слабо выраженные кислотные свойства.
В молекуле же фенола [фенол с эффектами, (стер12)] под влиянием ЭД-заместителя ОН группы электронная плотность смещена от заместителя и делокализована по араматическому кольцу. Образующийся при отщеплении протона фенокси-ион C6H5–O- являясь сопряженной системой, будет обладать более высокой стабильностью по сравнению с алкоксид-ионом CH3–CH2–O-, который не является сопряженной системой. Т.о., образование сопряженной системы способствует делокализации отрицательного заряда в анионе, что повышает его стабильность и усиливает кислотные свойства веществ.
3. Влияние радикала на стабильность аниона.
При одинаковых кислотных центрах появление в радикалах электронноакцепторных заместителей способствует делокализации отрицательного заряда в анионе, что повышает его стабильность и усиливает кислотные свойства веществ. Рассмотрим на примере:
CH3–CH2–COOH (пропионовая к-та) рКа=4,9; молочная к-та рКа=3,83
Исходя из величины рКа молочная к-та (стер13) будет более сильной, чем пропионовая к-та, т.к. наличие в радикале этой кислоты электронноакцепторного заместителя ОН группы способствует делокализации отрицательного заряда в лактат-анион CH3–CH(ОН)–COO- , что повышает его стабильность по сравнению с пропионат-анионом CH3–CH2–COO-, радикал которого не содержит такого заместителя. Поэтому молочная к-та проявляет более выраженные кислотные свойства по сравнению с пропионовой.
4. Влияние растворителя на стабильность аниона.
В водных растворах анионы гидратируются, что повышает их стабильность и усиливает кислотные свойства веществ. Чем меньше радиус аниона, тем он более гидратирован и стабилен, а следовательно будут выше кислотные свойства вещества.
НСООН (муравьиная к-та) рКа=3,7; СН3СООН (уксусная к-та) рКа=4,76; СН3–СН2–СООН (пропионовая к-та) рКа=4,9
Исходя из величины рКа в этом ряду кислот наиболее сильной является муравьиная к-та. Это объясняется тем, что формиат-ион НСОО- имел малые размеры, наиболее гидратирован и стабилен по сравнению с ацетат-ионом CH3–COO- и пропионат-ионом СН3–СН2–СОО-.
Амины
Амины – производные аммиака, в молекуле которого один, два или все три атома водорода замещены на углеводородные радикалы.
По количеству замещенных атомов водорода амины делят на:
По характеру углеводородных заместителей амины делят на
Общие особенности строения аминов
Также как и в молекуле аммиака, в молекуле любого амина атом азота имеет неподеленную электронную пару, направленную в одну из вершин искаженного тетраэдра:
По этой причине у аминов как и у аммиака существенно выражены основные свойства.
Так, амины аналогично аммиаку обратимо реагируют с водой, образуя слабые основания:
Связь катиона водорода с атомом азота в молекуле амина реализуется с помощью донорно-акцепторного механизма за счет неподеленной электронной пары атома азота. Предельные амины являются более сильными основаниями по сравнению с аммиаком, т.к. в таких аминах углеводородные заместители обладают положительным индуктивным (+I) эффектом. В связи с этим на атоме азота увеличивается электронная плотность, что облегчает его взаимодействие с катионом Н+.
Ароматические амины, в случае если аминогруппа непосредственно соединена с ароматическим ядром, проявляют более слабые основные свойства по сравнению с аммиаком. Связано это с тем, что неподеленная электронная пара атома азота смещается в сторону ароматической π-системы бензольного кольца в следствие чего, электронная плотность на атоме азота снижается. В свою очередь это приводит к снижению основных свойств, в частности способности взаимодействовать с водой. Так, например, анилин реагирует только с сильными кислотами, а с водой практически не реагирует.
Химические свойства предельных аминов
Как уже было сказано, амины обратимо реагируют с водой:
Водные растворы аминов имеют щелочную реакцию среды, вследствие диссоциации образующихся оснований:
Предельные амины реагируют с водой лучше, чем аммиак, ввиду более сильных основных свойств.
Основные свойства предельных аминов увеличиваются в ряду.
Вторичные предельные амины являются более сильными основаниями, чем первичные предельные, которые являются в свою очередь более сильными основаниями, чем аммиак. Что касается основных свойств третичных аминов, то то если речь идет о реакциях в водных растворах, то основные свойства третичных аминов выражены намного хуже, чем у вторичных аминов, и даже чуть хуже чем у первичных. Связано это со стерическими затруднениями, существенно влияющими на скорость протонирования амина. Другими словами три заместителя «загораживают» атом азота и мешают его взаимодействию с катионами H+.
Взаимодействие с кислотами
Как свободные предельные амины, так и их водные растворы вступают во взаимодействие с кислотами. При этом образуются соли:
Так как основные свойства предельных аминов сильнее выражены, чем у аммиака, такие амины реагируют даже со слабыми кислотами, например угольной:
Соли аминов представляют собой твердые вещества, хорошо растворимые в воде и плохо в неполярных органических растворителях. Взаимодействие солей аминов с щелочами приводит к высвобождению свободных аминов, аналогично тому как происходит вытеснение аммиака при действии щелочей на соли аммония:
2. Первичные предельные амины реагируют с азотистой кислотой с образованием соответствующих спиртов, азота N2 и воды. Например:
Характерным признаком данной реакции является образование газообразного азота, в связи с чем она является качественной на первичные амины и используется для их различения от вторичных и третичных. Следует отметить, что чаще всего данную реакцию проводят, смешивая амин не с раствором самой азотистой кислоты, а с раствором соли азотистой кислоты (нитрита) и последующим добавлением к этой смеси сильной минеральной кислоты. При взаимодействии нитритов с сильными минеральными кислотами образуется азотистая кислота, которая уже затем реагирует с амином:
Вторичные амины дают в аналогичных условиях маслянистые жидкости, так называемые N-нитрозаминами, но данная реакция в реальных заданиях ЕГЭ по химии не встречается. Третичные амины с азотистой кислотой не взаимодействуют.
Полное сгорание любых аминов приводит к образованию углекислого газа, воды и азота:
Взаимодействие с галогеналканами
Примечательно, что абсолютно такая же соль получается при действии хлороводорода на более замещенный амин. В нашем случае, при взаимодействии хлороводорода с диметиламином:
Получение аминов:
1) Алкилирование аммиака галогеналканами:
В случае недостатка аммиака вместо амина получается его соль:
2) Восстановление металлами (до водорода в ряду активности) в кислой среде:
с последующей обработкой раствора щелочью для высвобождения свободного амина:
3) Реакция аммиака со спиртами при пропускании их смеси через нагретый оксид алюминия. В зависимости от пропорций спирт/амин образуются первичные, вторичные или третичные амины:
Химические свойства анилина
Анилин – тривиальное название аминобензола, имеющего формулу:
Как можно видеть из иллюстрации, в молекуле анилина аминогруппа непосредственно соединена с ароматическим кольцом. У таких аминов, как уже было сказано, основные свойства выражены намного слабее, чем у аммиака. Так, в частности, анилин практически не реагирует с водой и слабыми кислотами типа угольной.
Взаимодействие анилина с кислотами
Анилин реагирует с сильными и средней силы неорганическими кислотами. При этом образуются соли фениламмония:
Взаимодействие анилина с галогенами
Как уже было сказано в самом начале данной главы, аминогруппа в ароматических аминах , втянута в ароматическое кольцо, что в свою очередь снижает электронную плотность на атоме азота, и как следствие увеличивает ее в ароматическом ядре. Увеличение электронной плотности в ароматическом ядре приводит к тому, что реакции электрофильного замещения, в частности, реакции с галогенами протекают значительно легче, особенно в орто- и пара- положениях относительно аминогруппы. Так, анилин с легкостью вступает во взаимодействие с бромной водой, образуя белый осадок 2,4,6-триброманилина:
Данная реакция является качественной на анилин и часто позволяет определить его среди прочих органических соединений.
Взаимодействие анилина с азотистой кислотой
Анилин реагирует с азотистой кислотой, но в виду специфичности и сложности данной реакции в реальном ЕГЭ по химии она не встречается.
Реакции алкилирования анилина
С помощью последовательного алкилирования анилина по атому азота галогенпроизводными углеводородов можно получать вторичные и третичные амины:
Получение анилина
1. Восстановление маталлами нитробензола в присутствии сильных кислот-неокислителей:
C6H5-NO2 + 3Fe + 7HCl = [C6H5-NH3]+Cl- + 3FeCl2 + 2H2O
2. Далее полученную соль обрабатывают щелочью для высвобождения анилина:
[C6H5-NH3]+Cl— + NaOH = C6H5-NH2 + NaCl + H2O
В качестве металлов могут быть использованы любые металлы, находящиеся до водорода в ряду активности.
Реакция хлорбензола с аммиаком:
С6H5−Cl + 2NH3 → C6H5NH2 + NH4Cl
Химические свойства аминокислот
Аминокислотами называют соединения в молекулах которых присутствуют два типа функциональных групп – амино (-NH2) и карбокси- (-COOH) группы.
Другими словами, аминокислоты можно рассматривать как производные карбоновых кислот, в молекулах которых один или несколько атомов водорода замещены на аминогруппы.
Таким образом, общую формулу аминокислот можно записать как (NH2)xR(COOH)y, где x и y чаще всего равны единице или двум.
Поскольку в молекулах аминокислот есть и аминогруппа и карбоксильная группа, они проявляют химические свойства схожие как аминов, так и карбоновых кислот.
Кислотные свойства аминокислот
Образование солей с щелочами и карбонатами щелочных металлов
Этерификация аминокислот
Аминокислоты могут вступать в реакцию этерификации со спиртами:
NH2CH2COOH + CH3OH → NH2CH2COOCH3+ H2O
Основные свойства аминокислот
1. Образование солей при взаимодействии с кислотами
NH2CH2COOH + HCl → [NH3CH2COOH]+Cl—
2. Взаимодействие с азотистой кислотой
NH2-CH2-COOH + HNO2 → НО-CH2-COOH + N2↑ + H2O
Примечание: взаимодействие с азотистой кислотой протекает так же, как и с первичными аминами
3. Алкилирование
NH2CH2COOH + CH3I → [CH3NH2CH2COOH]+I—
4. Взаимодействие аминокислот друг с другом
Аминокислоты могут реагировать друг с другом образуя пептиды – соединения, содержащие в своих молекулах пептидную связь –C(O)-NH-
При этом, следует отметить, что в случае проведения реакции между двумя разными аминокислотами, без соблюдения некоторых специфических условий синтеза, одновременно протекает образование разных дипептидов. Так, например, вместо реакции глицина с аланином выше, приводящей к глицилананину, может произойти реакция приводящая к аланилглицину:
Кроме того, молекула глицина не обязательно реагирует с молекулой аланина. Протекают также и реакции пептизации между молекулами глицина:
И аланина:
Помимо этого, поскольку молекулы образующихся пептидов как и исходные молекулы аминокислот содержат аминогруппы и карбоксильные группы, сами пептиды могут реагировать с аминокислотами и другими пептидами, благодаря образованию новых пептидных связей.
Отдельные аминокислоты используются для производства синтетических полипептидов или так называемых полиамидных волокон. Так, в частности с помощью поликонденсации 6-аминогексановой (ε-аминокапроновой) кислоты в промышленности синтезируют капрон:
Получаемая в результате этой реакции капроновая смола используется для производства текстильных волокон и пластмасс.
Образование внутренних солей аминокислот в водном растворе
В водных растворах аминокислоты существуют преимущественно в виде внутренних солей — биполярных ионов (цвиттер-ионов):
Получение аминокислот
1) Реакция хлорпроизводных карбоновых кислот с аммиаком:
Cl-CH2-COOH + 2NH3 = NH2-CH2-COOH + NH4Cl
2) Расщепление (гидролиз) белков под действием растворов сильных минеральных кислот и щелочей.
