Какое из перечисленных ниже свойств относится к заряду

| |||||||
| |||||||
| |||||||
| |||||||
| |||||||
| |||||||
| |||||||
| |||||||
| |||||||
| |||||||
| |||||||
| |||||||
| |||||||
| |||||||
| |||||||
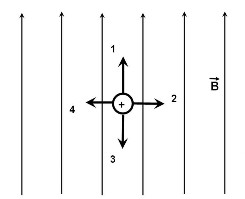
Проволочное кольцо покоится в магнитном поле, линии индукции которого перпендикулярны к плоскости кольца. В первый промежуток времени проекция вектора магнитной индукции на некоторую фиксированную ось линейно растет от B₀ до 5В₀, во второй — за то же время уменьшается от 5В₀ до 0, затем за третий такой же промежуток времени уменьшается от 0 до -5В₀. На каких отрезках времени совпадают направления тока в кольце?
на отрезках 1 и 2
на отрезках 1 и 3
на отрезках 2 и 3
на всех отрезках

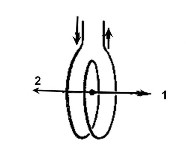
На сердечник в виде сплошной массивной рамки из стали квадратного сечения в двух его частях (см. рисунок) намотана катушка из изолированного проводника и надето кольцо. Где возникает вихревое электрическое поле при пропускании по катушке периодически меняющегося тока?
только вдоль стержней сердечника
только внутри стержней сердечника поперек его сечения
только в кольце по его периметру
в кольце по периметру и в сердечнике поперек его сечения
Укажите устройство, в котором используется явление возникновения силы, действующей на проводник в магнитном поле при прохождении через проводник электрического тока.
реостат
металлоискатель
электродвигатель
электрочайник

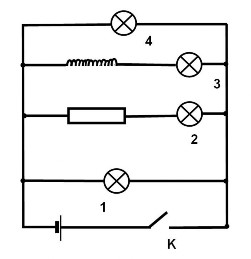
Почему лампочка 2 в схеме, изображенной на рисунке, при замыкании ключа К загорается на 0,5 с позже лампочки 1?
потому что ток по длинному проводу катушки доходит до нее позже
потому что лампочка 2 находится дальше от ключа К
потому что в катушке возникает вихревое электрическое поле, препятствующее нарастанию тока в ней
потому что электроны тормозятся на изогнутых участках цепи
Как изменился магнитный поток в катушке индуктивности, если при увеличении силы тока в катушке в 2 раза энергия магнитного поля катушки увеличилась в 2 раза?
увеличился в 4 раза
уменьшился в 4 раза
увеличился в 2 раза
остался прежним
Сравните индуктивности L₁ и L₂ двух катушек, если при одинаковой силе тока энергия магнитного поля, создаваемого током в
первой катушке, в 9 раз больше, чем энергия магнитного поля, создаваемого током во второй катушке.
L₁ в 9 раз больше, чем L₂
L₁ в 9 раз меньше, чем L₂
L₁ в 3 раза больше, чем L₂
L₁ в 3 раза меньше, чем L₂

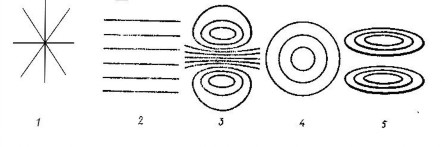
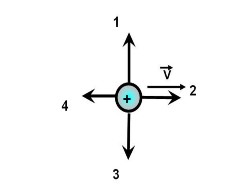
Какой из рисунков соответствует возникновению вихревого электрического поля при возрастании индукции магнитного поля?
1
2
3
4
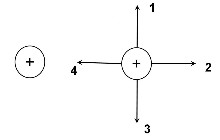
Какое из перечисленных ниже свойств относится только к вихревому электрическому полю, но не к электростатическому?
непрерывность в пространстве
линии напряженности обязательно связаны с электрическими зарядами
работа сил поля при перемещении заряда по любому замкнутому пути равна нулю
работа сил поля при перемещении заряда по замкнутому пути может не быть равной нулю
В катушке с индуктивностью 4 Гн сила тока равна 3 А. Чему будет равна сила тока в этой катушке, если энергия магнитного поля уменьшится в 2 раза?
2,14 А
3 А
1,73 А
1,5 А
В однородном магнитном поле находится плоский виток площадью 10 см², расположенный перпендикулярно к полю. Какой ток потечет по витку, если индукция поля будет убывать с постоянной скоростью 0,01 Тл/с? Сопротивление витка равно 1 Ом.
10⁻⁴ А
10⁵ А
10⁻³ А
0,5 * 10⁻⁵ А
Основные свойства электрического заряда:
1. Заряд инвариантен – его величина одинакова при измерении в любой инерциальной системе отсчёта.
2. Заряд сохраняется – суммарный заряд изолированной систе-мы тел не изменяется.
3. Заряд аддитивен – заряд системы тел равен сумме зарядов отдельных тел.
4. Заряд дискретен – заряд любого тела по величине кратен ми-нимальному заряду, который обозначается символом e и ра —
вен 1,6 10 19 Кл.
12
5. Существуют заряды двух разных «сортов». Заряды одного «сорта» названы положительными, а другого «сорта» – от—рицательными. Одноимённые заряды отталкиваются, а раз-ноимённые – притягиваются.
Если вблизи одной заряженной частицы (заряда q1 ), располо-
женной в начале координат, будет находиться вторая заряженная час-тица (заряд q2 ), то на второй заряд будет действовать электрическая
(кулоновская) F , определяемая законом Кулона:
![]() F 4 q1q2r 2 er ,
F 4 q1q2r 2 er ,
где r – радиус-вектор точки наблюдения;
er – единичный радиус-вектор, направленный в точку наблюде-ния;
0 – электрическая постоянная; – диэлектрическая проницаемость среды (в вакууме 1).
Напряжённость электрического поля – характеристика силового действия электрического поля на заряд. Напряжённость электриче-ского поля, создаваемого зарядом q1 , есть векторная величина, обо-
значаемая символом E(q1 ) и определяемая соотношением:
![]()
F | , |
E(q ) | |
1 | q2 |
где | – сила, действующая на заряд q2 . |
F |
Силовые линии или линии напряжённости – линии, в любой точке которых вектор напряжённости электрического поля направлен по касательной к ним.
Электрическое поле подчиняется принципу суперпозиции: на-пряжённость электрического поля нескольких источников является суммой векторов напряжённости поля, создаваемого независимо каж-дым источником:
E Ei .
i
Потоком электрического поля называется интеграл по некото-рой поверхности S от скалярного произведения напряжённости элек-трического поля на элемент поверхности:
ФЕ EdS ,
S
где вектор dS направлен по нормали к поверхности.
13
Дипольный (электрический) момент есть произведение
Закон Гаусса для электрического поля: поток электрического поля через замкнутую поверхность S0 пропорционален суммарному
заряду, расположенному внутри объёма, ограниченного поверхно-стью интегрирования потока V (S0 ) :
![]() Линии напряжённости электрического поля точечного заряда представляют собой прямые линии, идущие от заряда (положительно-го) или к заряду.
Линии напряжённости электрического поля точечного заряда представляют собой прямые линии, идущие от заряда (положительно-го) или к заряду.
Потенциалом данной точки r электрического поля называется скалярная величина, численно равная работе сил поля по перемеще-нию единичного положительного заряда из данной точки в другую
фиксированную точку r0 , в которой потенциал принят за 0 (напри-мер, в бесконечность):
(r ) Edr .
r
Уравнение, выражающее напряжённость через потенциал:
E grad( ) , где оператор градиента grad | ; | ; | . |
x | y | ||
z |
![]() Диполь есть два одинаковых по величине, но противоположных по знаку точечных заряда q , расположенных на расстоянии L ( L –
Диполь есть два одинаковых по величине, но противоположных по знаку точечных заряда q , расположенных на расстоянии L ( L –
| pe | qL .
Вектор дипольного момента направлен от отрицательного к положи-тельному заряду.
На линии, проходящей через центр диполя, перпендикулярно электрическому моменту диполя и на большом расстоянии r от его центра напряжённость равна:
Методика и порядок измерений
Рассмотрите рисунок 2.1 и зарисуйте необходимое в конспект.
14
Рис. 2.1. Взаимодействие зарядов
Эксперимент 1. Исследование поля точечного заряда
1. Запустите эксперимент «Взаимодействие электрических заря-
дов».
2. Зацепив мышью, перемещайте заряд q1 и зафиксируйте его
вблизи левой границы экспериментального поля. Зацепив мышью, перемещайте движок регулятора величины первого заряда и устано-вите величину заряда q1 , указанную в таблице 2.1, для вашей брига-
ды. Заряд q3 поместите под первым, а его величину установите рав-ной 0. Заряд q2 установите равным 10-8 Кл.
3. Перемещайте, нажав левую кнопку мыши, заряд q2 вправо, устанавливая расстояния r12 до первого заряда, указанные в табли-
це 2.1. Измеренные в данных точках значения E1 | F12 / q2 занесите в | |||
соответствующую строку таблицы 2.2. | ||||
Таблица 2.1 | ||||
Значения величины заряда q 10 8 | Кл (не перерисовывать) | |||
1 | ||||
Бригада | q1, Кл | |||
1 и 5 | 4 | 6 | 8 | 10 |
2 и 6 | 4 | 5 | 9 | 10 |
3 и 7 | -4 | -5 | -7 | -9 |
4 и 8 | -4 | -6 | -8 | -10 |
15 |
Контрольная работа по химии
для групп по специальностям СПО
за 1 семестр обучения.
Цель контрольной работы.
Определение объема и уровня знаний студентами групп по специальностям СПО теоретических основ и основных тем базового курса учебной дисциплины «Химия».
Главный недостаток всех тестовых заданий множественного выбора – возможность угадывания правильного ответа не знающим материала учащимся.
Для уменьшения вероятности угадывания в данных тестах предусматриваются не один, а несколько верных ответов.
В тесты включены задания, которые позволяют выявить навыки практического использования химических знаний, владения основными понятиями курса химии, присутствуют задания повышенного уровня сложности.
В данных тестах использованы задания с выбором ответа, с кратким свободным ответом (в виде цифры, слова), с развернутым свободным ответом, который должен содержать объяснение взаимосвязи состава, строения, свойств конкретных веществ.
I. Тематика соответствует тематическому планированию для первого курса по общеобразовательной дисциплине «Химия» в соответствии с рекомендациями ФИРО.
II. Рекомендуемый объем контрольной работы:
Темы для контроля: введение и общая и неорганическая химия
Время выполнения 45 мин.
Несколько вопросов требуют письменного ответа (без выбора вариантов).
III. Рекомендуемые оценки
26 вопросов
менее 50 % правильных ответов – «2» (неудовлетворительно) (менее 13 правильных ответов)
50 % — 60 % правильных ответов – «3» (удовлетворительно) (от 13 до 16 правильных ответов)
61% — 80 % правильных ответов – «4» (хорошо) (от 17 до 21 правильных ответов)
Более 80 % — «5» (отлично) (от 22 до 26 правильных ответов)
Разработчик: Ивкова Марина Николаевна, преподаватель химии.
ВАРИАНТ 1
Какой из перечисленных элементов является неметаллом:
а) K; б) Na; в) S; г) Zn
Даны смеси:
а) воздух; б) лимонад; в) смесь бензина с водой; г) минеральная вода
Выберите неоднородную смесь.
3. К физическим относится явление:
а) горение свечи; в) растворение сахара в воде;
б) ржавление железа; г) гниение останков живых организмов
4. Какой из перечисленных элементов имеет постоянную валентность:
а) Fe; б) Cu; в) S; г) Al
5. Относительная молекулярная масса CuSO4 равна:
а) 160; б) 80; в) 120; г) 134
6. Дайте название веществу SO3:
а) оксид серы (VI); б) оксид серы (II); в) оксид серы (III); г) оксид серы (IV)
7. В какой из предложенных реакций неверно расставлены коэффициенты, исправьте их:
а) ZnO +2HNO3 = Zn(NO3)2 + H2O; в) 2CuOH = Cu2O + H2O;
б) Al(OH)3+ H2SO4 = Al2(SO4)3 + 3H2O; г) 4P + 5O2 = 2P2O5
8. Выпишите формулу щелочи:
а) Zn(OH)2; б) Al(OH)3; в) KOH; г) Fe(OH)2
9. У какого из перечисленных элементов атом имеет наибольший радиус:
а) №4; б) №5; в) №20; г) №49
10. По номеру периода можно определить:
а) число электронов в атоме; в) высшую валентность;
б) число электронов на последнем уровне; г) число электронных уровней
11. Как изменяются неметаллические свойства в ряду элементов C – N – O – F:
а) не изменяются; б) ослабевают; в) усиливаются; г) периодически повторяются
12. Электронная формула атома имеет вид 1s22s22p63s23p63d104s24p64d104f0 5s25p3:
Какой это элемент?
а) олово; б) сурьма; в) селен; г) нет верного ответа
13. Элемент №16 может проявлять валентность:
а) II, IV; б) IV, VI; в) II, VI, V; г) II, IV,VI
14. Как называется химическая связь, образующаяся между атомами за счет общих электронных пар:
а) ионная; б) ковалентная; в) металлическая г) водородная
15. Назовите вещество с ионной связью:
а) CH4; б) CaCl2; в) CO2; г) нет верного ответа
16. Какой из данных элементов является восстановителем:
а) Zn+2 Zn0; б) Al0 Al+3; в) P+5 P+3; г) Ba+2 → Ba0 .
17. Диссоциации какого вещества соответствует приведенное уравнение?
Н2А = 2Н+ + А2- (А — кислотный остаток)
а) Н2S; б) Н2O; в) НС1; г) правильного ответа нет
18. Какой из данных металлов является щелочноземельным:
а) K; б) Al; в) Fe; г) Ca
19. Какая конфигурация у атома алюминия:
а) 1 s2 2s2 2p1;
б) 1 s2 2s2 2p3;
в) 1 s2 2s2 2p6 3s2 3p1;
г) 1 s2 2s2 2p6 3s2 3p6 3d1 4s2
20. Какой из данных металлов необходимо хранить под слоем керосина:
а) Mg; б) Al; в) Be; г) K
21. Укажите характеристику суспензии:
а) Газообразные частицы распределены в жидкости;
б) Газообразные частицы распределены в газе;
в) жидкость распределена в другой, не растворяя её;
г) твердые частицы распределены в жидкости.
22. Что показывает химическая формула?
23. Рассчитайте относительную молекулярную и молярную массы вещества: Ca3(PO4)2
24. Напишите электронные конфигурации атомов элементов, имеющих порядковые номера 7, 20.
25. Рассчитайте массовую долю элементов в веществе: BaSO4.
26. Дайте определение понятия «вещество».
ВАРИАНТ 2
1. Выберите сложное вещество:
а) Al; б) CuO; в) S; г) O2.
2. Чему равна относительная атомная масса калия:
а) 40; б) 38; в) 39; г) 65
3. Химический символ С обозначает:
а) ртуть; б) медь; в) кальций; г) углерод
4. Простое вещество состоит из:
а) атомов одного и того же химического элемента; в) одинаковых молекул;
б) атомов разных химических элементов; г)разных молекул
5. Какая из приведенных ниже формул составлена по валентности неверно:
а) ZnO; б) Ca2Cl; в) BaJ2 г) H2O
6. Составьте формулу оксида калия:
а) KO2; б) KO; в) K2O2; г) К2О
7. Определите неверно составленную формулу вещества:
а) Cu(OH)2; б) H2NO3; в) Ca3(PO4)2; г) Zn(NO3)2
8. Из приведенного перечня химических свойств выпишите то, которое характерно для
нерастворимых оснований:
а) с кислотными оксидами; в) с водой;
б) термическое разложение; г) с основными оксидами
9. Сколько электронных уровней в атоме цинка:
а) 2; б) 3; в) 4; г) 5
10. У какого элемента наиболее ярко выражены неметаллические свойства:
а) германий; б) мышьяк; в) бром; г) селен
11. Почему свойства элементов периодически повторяются:
а) повторяется число электронов на внешнем энергетическом уровне;
б) увеличивается радиус атома;
в) увеличивается число нейтронов в ядре;
г) увеличивается число энергетических уровней
12. Какая формула соответствует конфигурации атома фосфора:
а) 1s2 2s2 2p6 3s2; в) 1s2 2s2 2p6 3s2 2p4;
б) 1s2 2s2 2p6 3s2 3p3; г) 1s2 2s2 2p6 3s23p1
13. Как изменяются металлические свойства в ряду Be – Mg – Ca –Sr:
а) усиливаются; б) не изменяются; в) периодически изменяются; г) ослабевают
14. Какая связь образуется между атомами неметаллов с одинаковой ЭО:
а) ионная; б) металлическая; в) ковалентная полярная; г) ковалентная неполярная
15. Укажите вещество с ковалентной полярной связью:
а) NaF; б) HI; в) C; г) MgO
16. Какой из перечисленных процессов является окислением:
а) Mg0 Mg+2; б) N+3 N+2; в) N+5 N+4; г) P+5 → P0
17. Какое из приведенных веществ является слабым электролитом?
а) Nа2S04 ; б) HNO3 ; в) Н2S ; г) НС1
18. Алюминий — это:
а) металл; б) неметалл; в) переходный элемент; г) нет верного ответа
19.Какой осадок образуется при взаимодействии растворов солей фосфата натрия и нитрата кальция:
а) NaNO3; б) Ca3(PO4)2; в) Ca(OH)2; г) Na3PO4
20.Какой из данных металлов является щелочным:
а) Ba; б) Be; в) Sr; г) Fr
21.Укажите твердую дисперсную систему:
а) смог; б) сплав; в) лимфа; г) воздух.
22. Какие разновидности химических форму вы знаете?
23. Рассчитайте относительную молекулярную и молярную массы вещества: Zn(NO3)2
24. Напишите электронные конфигурации атомов элементов, имеющих порядковые номера 17, 4.
25. Рассчитайте массовую долю элементов в веществе: NaNO3.
26. Дайте определение понятия «химический элемент».
ВАРИАНТ 3
1. Какой из перечисленных элементов является неметаллом:
а) Ba; б) Ca; в) Fe; г) P
2. Сложное вещество состоит из:
а) разных молекул; в) атомов разных химических элементов;
б) одинаковых молекул; г) атомов одного и того же химического элемента
3. Чему равна относительная атомная масса кальция:
а) 50; б) 40; в) 39; г) 24
4. Выберите однородную смесь среди перечисленных ниже:
а) почва; б) лимонад; в) смесь бензина с водой; г) смесь мела с водой
5. Составьте формулу вещества, содержащего натрий и серу (II):
а) NaS2; б) Na2S; в) Na2S2; г) NaS
6. В состав кислот обязательно входят:
а) атомы водорода; б) атомы кислорода; в) атомы серы; г) атомы металла
7. Выберите формулу нерастворимого основания:
а) Ba(OH)2; б) Fe(OH)3; в) NaOH; г) KOH
8. Определите неверно составленную формулу:
а) Ca(OH)2; б) H2SO4; в) BaCl2; г) H2PO4;
9. Как определить число электронных уровней в атоме:
а) по номеру периода; в) по порядковому номеру химического элемента;
б) по номеру группы; г) правильного ответа нет
10. У какого элемента наиболее ярко выражены металлические свойства:
а) №4; б) №56; в) №12; г) №38
11. Какой из перечисленных элементов образует соединения ЭО2 и H2ЭO3:
а) сера; б) кремний; в) марганец; г) бериллий
12. Какая формула соответствует конфигурации атома неона:
а) 1s2 2s2 2p3; б) 1s2 2p4 3s2; в) 1s2 2s2 2p6; г) 1s2 2s2 2p6 3s2
13. Атом какого элемента имеет строение внешнего уровня 3s2 3p3:
а) №15; б) №16; в) №7; г) №9
14. Как изменяется электроотрицательность элементов с ростом заряда ядра в группах, в главных подгруппах:
а) не изменяется; б) усиливается; в) уменьшается; г) периодически повторяется
15. Определите степень окисления хлора в соединении NaClO2:
а) +2; б) +3; в) +4; г) +1
16. Какой из данных элементов является восстановителем:
а) S0 S+4; б) N+5 N+2; в) Mg+2 Mg0; г) C+4 → C+2
17. Какое вещество диссоциирует в воде в соответствии с приведенным уравнением?
М(ОН)2 = М2+ + 2OН- (М — металл)
а) K2SO4; б) NaOH; в) Ва(ОН)2 ; г) Са(NOз)2
18. Как изменяются металлические свойства в ряду Li – Na – K – Rb:
а) не изменяются; б) ослабевают; в) усиливаются; г) нет верного ответа
19.Какой металл легче окисляется кислородом:
а) K; б) Mg; в) Be; г) Al
20.В какой паре оба гидроксида являются щелочами:
а) NaOH и Al(OH)3;
б) Mg(OH)2 и Ca(OH)2;
в) Ba(OH)2 и KOH;
г) Zn(OH)2 и LiOH
21. Укажите характеристику эмульсии:
а) газообразные частицы, распределенные в жидкости;
б) газообразные частицы распределенные в газе;
в) одна из жидкостей раздроблена в другой, не растворяющей её;
г) твердые частицы распределены в жидкости.
22. Чем отличается молекулярная масса вещества от молярной?
23. Рассчитайте относительную молекулярную и молярную массы вещества: Fe(OH)3
24. Напишите электронные конфигурации атомов элементов, имеющих порядковые номера 12, 33.
25. Рассчитайте массовую долю элементов в веществе: K2SO4 .
26.Охарактеризуйте понятие аллотропия. Приведите примеры аллотропных модификаций.
ВАРИАНТ 4
1. К химическим относится явление:
а) измельчение древесины; в) плавление меди;
б) измельчение сахара; г) прокисание молока.
2. В соединении Zn3P2 валентность фосфора равна:
а) I; б) II; в) III; г) V
3. Химический символ K обозначает:
а) кальций; б) бром; в) калий; г) кремний
4. Относительная молекулярная масса HNO3 равна:
а) 80; б) 120; в) 63; г) 82
5. Выберите простое вещество:
а) Ba; б) CaS; в) N2O5; г) H2О
6. Дайте название соли Fe(NO3)2:
а) нитрат железа; б) нитрит железа (II); в) нитрат железа (II); г) нитрат железа (III)
7. Из данного списка веществ выпишите формулы солей, дайте им названия:
Zn(OH)2, K2CO3, Fe2O3 , Na3PO4, BaCl2, KOH, HNO3, Cu(NO3)2, Ba(OH)2
8. В какой из реакций неверно расставлены коэффициенты, исправьте их:
а) FeO + H2 = Fe + H2O; в) K2O + 2H3PO4 = K3PO4 + 3H2O;
б) N2O3 + H2O = 2HNO2; г) Cu(OH)2 + 2HNO3 = Cu(NO3)2 +2H2O
9. Что обозначает порядковый номер элемента:
а) заряд атомного ядра;
б) число электронов на последнем электронном уровне;
в) количество электронных уровней;
г) нет верного ответа
10. У какого элемента наиболее ярко выражены металлические свойства:
а) кремний; б) алюминий; в) натрий; г) калий
11. Чем определяются свойства химических элементов главных подгрупп:
а) общим числом электронов в атоме; в) числом нейтронов в ядре;
б) количеством электронных уровней: г) числом электронов на последнем уровне в атоме
12. Какая формула соответствует конфигурации атома магния:
а) 1s2 2s2 2p6 3s1; б) 1s2 2s2 2p6 3s2; в) 1s2 2s2 2p6; г) 1s2 2s2 2p6 3s2 3p1
13. Атом какого элемента имеет строение внешней оболочки 2s2 2p2:
а) №18; б) №8; в) №6; г) №4
14. Какой элемент называется окислителем:
а) отдающий электроны; в) не изменяющий степень окисления;
б) принимающий электроны; г) проявляющий степень окисления 0
15. Как называется способность атомов оттягивать к себе электроны от других атомов в соединениях: