Какое химическое свойство характерно для оксида азота 2
- Главная
- Вопросы & Ответы
- Вопрос 4782435
 Гость:
Гость:
9 лет назад
9
1
Лучший ответ:


Гость:
Для NO характерно взаимодействие с кислородом.
2NO + O2 = 2NO2
9 Августа в 11:46
Ваш ответ (не менее 20 символов):
Ваше имя (не менее 2 символов):

Лучшее из галереи:































Другие вопросы:
 Гость:
Гость:
График какой из приведенных ниже функций изображен на рисунке? 1)y=3/x 2)y=-1/3x 3)y=-3/x 4)y=1/3x
9 лет назад
Смотреть ответ
143
1
 Гость:
Гость:
Расстояние между двумя пристанями катер проходит по течению за 2 ч, а против течения – за 3 ч. За сколько часов это расстояние преодолеет плот? Дайте ответ в часах.
9 лет назад
Смотреть ответ
15
1
 Гость:
Гость:
Как решить это уравнение c•100=465+2635
9 лет назад
Смотреть ответ
8
1
 Гость:
Гость:
В понедельник цена акции составляла 2000 руб в среду она уменьшилась на 5% а в пятницу она уменьшилась на 10% по сравнению со средой.Какой была цена акции пятницу?
9 лет назад
Смотреть ответ
6
1
 Гость:
Гость:
Укажите угловой коэффициент прямой, заданной уравнением
9 лет назад
Смотреть ответ
8
1
Оксиды азота. Общая характеристика, химические свойства.

Данный урок посвящен оксидам азота, которые при взаимодействии с водой образуют кислоты, и соответственно, являются солеобразующими, — NO2 и N2O5.
NO2 представляет собой типичный кислотный оксид, который обладает высокой химической активностью, и при взаимодействии с неметаллами (сера, фтор, водород) ведет себя как сильный окислитель; также применяется при производстве серной кислоты (нитрозный метод), окисляя сернистый газ в олеум (SO3), и азотистой кислоты (HNO2).
N2O5 — это высший оксид азота, очень летуч, взаимодействует с органическими веществами, поэтому его нужно хранить в стеклянной посуде (!Важно! плавиковая кислота (HF) наоборот хранится в полимерной таре по причине того, что разъедает стекло), легко разлагается до ядовитого NO2 со взрывом; используется при получении азотной кислоты (HNO3).
Важно знать, что все оксиды азота токсичны!
Более детально изучить химические свойства предлагаю при помощи таблицы, в которой собраны все необходимые реакции для сдачи ЕГЭ.
Солеобразующие оксиды азота | ||
1) Формула | NO2 | N2O5 |
2) Характеристика | NO2 (Nitrogen dioxide, диоксид азота)– красно — бурый газ, ядовит, с характерным острым запахом; Хорошо растворяется в воде; | N2O5 (Dinitrogen pentoxide, пентаоксид азота)– бесцветные, летучие кристаллы, взрывчатые; Хорошо растворяется в воде; |
3) Получение в лаборатории | 1) 2Pb(NO3)2 = 2PbO + 4NO2 + O2 (200-470 C); 2) Me + 4HNO3(к) = Me(NO3)2 + 2NO2 + 2H2O (Me= правее водорода); | 1) 2HNO3(к) + P2O5 = N2O5 + 2HPO3 (-10 C); 2) 4AgNO3 + 2Cl = 4AgCl + 2N2O5 + O2; |
4) Получение в промышленности | NO+ O2 = NO2 (на воздухе — мгновенно); | 2NO2 + O3 = N2O5 (-78 C); |
5) Химические свойства | 1) Разложение: 2NO2 = 2NO + O2 (140-600 C) 2) C кислотами: 2NO2 + 4HCl = 2NOCl + Cl2 + 2H2O; 2NO2 + 8HI = N2 + 4I2 + 4H2O; 2NO2 + 2H2S = N2 + 2S + 2H2O (350 C); 3) С металлами: 2NO2 + Na = NaNO3 + NO (22 C); 2NO2 + 4Cu = N2 + 4CuO (600 C); 2NO2 + 4Zn = 4ZnO + N2; NO2 + K = KNO2; 4) С неметаллами: NO2 + O2 ≠ В присутствии воды реакция идет (образование HNO3): 4NO2 + O2 + 2H2O = 4HNO3; 4NO2 + O2 + 4NaOH = 4NaNO3 + 2H2O; 2NO2 + O3 = N2O5 + O2; 2NO2 + 2C = N2 + 2CO2 (t); 2NO2 + 7H2 = 2NH3 + 4H2O (kat.: Pt, Ni); 10NO2 + 8P = 5N2 + 4P2O5 (150 C); 2NO2 + 2S = N2 + 2SO2 (150 C); 2NO2 + F2 = NO2F (нитронил фтористый); 2NO2 + F2 + H2O = 2HNO3 + 2HF; 5) С солями: 3NO2 + CaCO3 = Ca(NO3)2 + NO + CO2 (+Q); 2NO2 + KГ = KNO3 + NOГ (Г= Cl, Br); 14NO2 + 16FeSO4 + 8H2SO4 = 8HNO3 + 8Fe2(SO4)2 + 3N2 + 4H2O; 5NO2 + KMnO4 + 2H2SO4 + H2O = 5HNO3 + MnSO4 + KHSO4 6) С оксидами: 2NO2 + H2O = HNO3 + HNO2; 2NO2 + SO2 = N2 + 2SO3 (22 C) 2NO2 + SO2 = SO3 + NO (t) 7) C основаниями: 2NO2 + 2KOH = KNO3 + KNO2 + H2O | 1) Разложение: N2O5 = 4NO + O2 (взрыв); 2) С кислотами: N2O5 + 3H2S = 3H2SO4 + 4N2 + 4O2; 3) С металлами: N2O5 + 3Zn = 3ZnO + O2 + N2 (t) N2O5 + 5Cu = N2 + 5CuO (500 C) N2O5 + Na = NaNO3 + NO2 4) С неметаллами: N2O5 + O2 ≠ N2O5 + I2 = I2O5 + N2 5) С солями: 2N2O5 + 2KI = I2 + 2NO2 + 2KNO3 6) С оксидами: N2O5 + H2O = 2HNO3 + Q N2O5 + 3SO2 = 3SO3 + O2 + N2 N2O5 + Al2O3 = 2Al(NO3)3 (40 C) N2O5 + CaO = Ca(NO3)2 7) С основаниями: N2O5 + 2NH4OH = 2NH4NO3 + H2O N2O5 + 2KOH = 2KNO3 + H2O |
6) Применение | 1) Используется при производстве H2SO4 и HNO3; 2) Окислитель в жидком ракетном топливе; 3) Вместе с другими оксидами азота образует «лисий хвост» — выбросы химического производства, и из выхлопных труб автомобилей; 4) Токсичен, вызывает отек легких. | 1) Применение ограничено из-за взрывоопасной природы оксида азота (V); 2) Используется в качестве нитрующего агента (в органической химии). |
Следующее занятие будет посвящено задачам по этой теме.
Если возникнут вопросы, пиши в коменты)
Солеобразующие оксиды азота. Задачи с объяснениями.
Оксиды азота
При описании свойств азота отмечалось, что при непосредственном взаимодействии азота с кислородом образуется только оксид азота (II) NO. Однако существуют оксиды азота со всеми возможными степенями окисления (от +1 до +5).
N2O — оксид азота (I), «веселящий газ»
При обычной температуре N2O — бесцветный газ со слабым приятным запахом и сладковатым вкусом; обладает наркотическим действием, вызывая сначала судорожный смех, затем — потерю сознания.
Способы получения
1. Разложение нитрата аммония при небольшом нагревании:
NH4NO3 = N2O↑ + 2Н2О
2. Действие HNO3 на активные металлы
10HNO3(конц.) + 4Са = N2O↑ + 4Ca(NO3)2 + 5Н2О
Химические свойства
N2O не проявляет ни кислотных, ни основных свойств, т. е. не взаимодействует с основаниями, с кислотами, с водой (несолеобразующий оксид).
При Т > 500’С разлагается на простые вещества. N2O — очень сильный окислитель. Например, способен в водном растворе окислить диоксид серы до серной кислоты:
N2O + SO2 + Н2О = N2↑ + H2SO4
NO — оксид азота (II), монооксид азота.
При обычной температуре NO — бесцветный газ без запаха, малорастворимый в воде, очень токсичный (в больших концентрациях изменяет структуру гемоглобина).
Способы получения
1. Прямой синтез из простых веществ может быть осуществлен только при очень высокой Т:
N2 + O2 = 2NО — Q
2. Получение в промышленности (1-я стадия производства HNO3).
4NH3 + 5O2 = 4NО + 6Н2О
3. Лабораторный способ — действие разб. HNO3 на тяжелые металлы:
8HNO3 + 3Cu = 2NO + 3Cu(NO3)2 + 4Н2О
Химические свойства
NO — несолеобразующий оксид (подобно N2О). Обладает окислительно-восстановительной двойственностью.
2NO + SO2 + Н2О = N2O↑ + H2SO4
2NO + 2H2 = N2 + 2Н2О (со взрывом)
2NO + O2 = 2NO2
10NO + 6KMnO4 + 9H2SO4 = 10HNO3 + 3K2SO4 + 6MnSO4 + 4Н2О
NO2 — оксид азота (IV), диоксид азота
При обычной температуре NO2 — красно-бурый ядовитый газ с резким запахом. Представляет собой смесь NO2 и его димера N2O4 в соотношении -1:4. Диоксид азота хорошо растворяется в воде.
Способы получения
I. Промышленный — окисление NO: 2NO + O2 = 2NO2
II. Лабораторные:
действие конц. HNO3 на тяжелые металлы: 4HNO3 + Сu = 2NO2↑ + Cu(NO3)2 + 2Н2О
разложение нитратов: 2Pb(NO3)2 = 4NO2↑ + O2↑ + 2РbО
Химические свойства
NO2 взаимодействует с водой, основными оксидами и щелочами. Но реакции протекают не так, как с обычными оксидами — они всегда окислительно — восстановительные. Объясняется это тем, что не существует кислоты со С.О. (N) = +4, поэтому NO2 при растворении в воде диспропорционирует с образованием 2-х кислот — азотной и азотистой:
2NO2 + Н2О = HNO3 + HNO2
Если растворение происходит в присутствии O2, то образуется одна кислота — азотная:
4NO2 + 2Н2О + O2 = 4HNO3
Аналогичным образом происходит взаимодействие NO2 со щелочами:
в отсутствие O2: 2NO2 + 2NaOH = NaNO3 + NaNO2 + Н2О
в присутствии O2: 4NO2 + 4NaOH + O2 = 4NaNO3 + 2Н2О
По окислительной способности NO2 превосходит азотную кислоту. В его атмосфере горят С, S, Р, металлы и некоторые органические вещества. При этом NO2 восстанавливается до свободного азота:
10NO2 + 8P = 5N2 + 4P2O5
2NO2 + 8HI = N2 + 4I2 + 4Н2О (возникает фиолетовое пламя)
В присутствии Pt или Ni диоксид азота восстанавливается водородом до аммиака:
2NO2 + 7Н2 = 2NH3 + 4Н2О
Как окислитель NO2 используется в ракетных топливах. При его взаимодействии с гидразином и его производными выделяется большое количество энергии:
2NO2 + 2N2H4 = 3N2 + 4Н2О + Q
N2O3 и N2O5 — неустойчивые вещества
Оба оксида имеют ярко выраженный кислотный характер, являются соответственно ангидридами азотистой и азотной кислот.
N2O3 как индивидуальное вещество существует только в твердом состоянии ниже Т пл. (-100С).
С повышением температуры разлагается: N2O3 → NO + NO2
N2O5 при комнатной температуре и особенно на свету разлагается так энергично, что иногда самопроизвольно взрывается:
2N2O5 = 4NO2 + O2
Азот — неметаллический элемент Va группы периодической таблицы Д.И. Менделеева. Составляет 78% воздуха. Входит в состав
белков, являющихся важной частью живых организмов.
Температура кипения азота составляет -195,8 °C. Однако быстрого замораживания объектов, которое часто демонстрируют в
кинофильмах, не происходит. Даже для заморозки растения нужно продолжительное время, это связано с низкой теплоемкостью
азота.
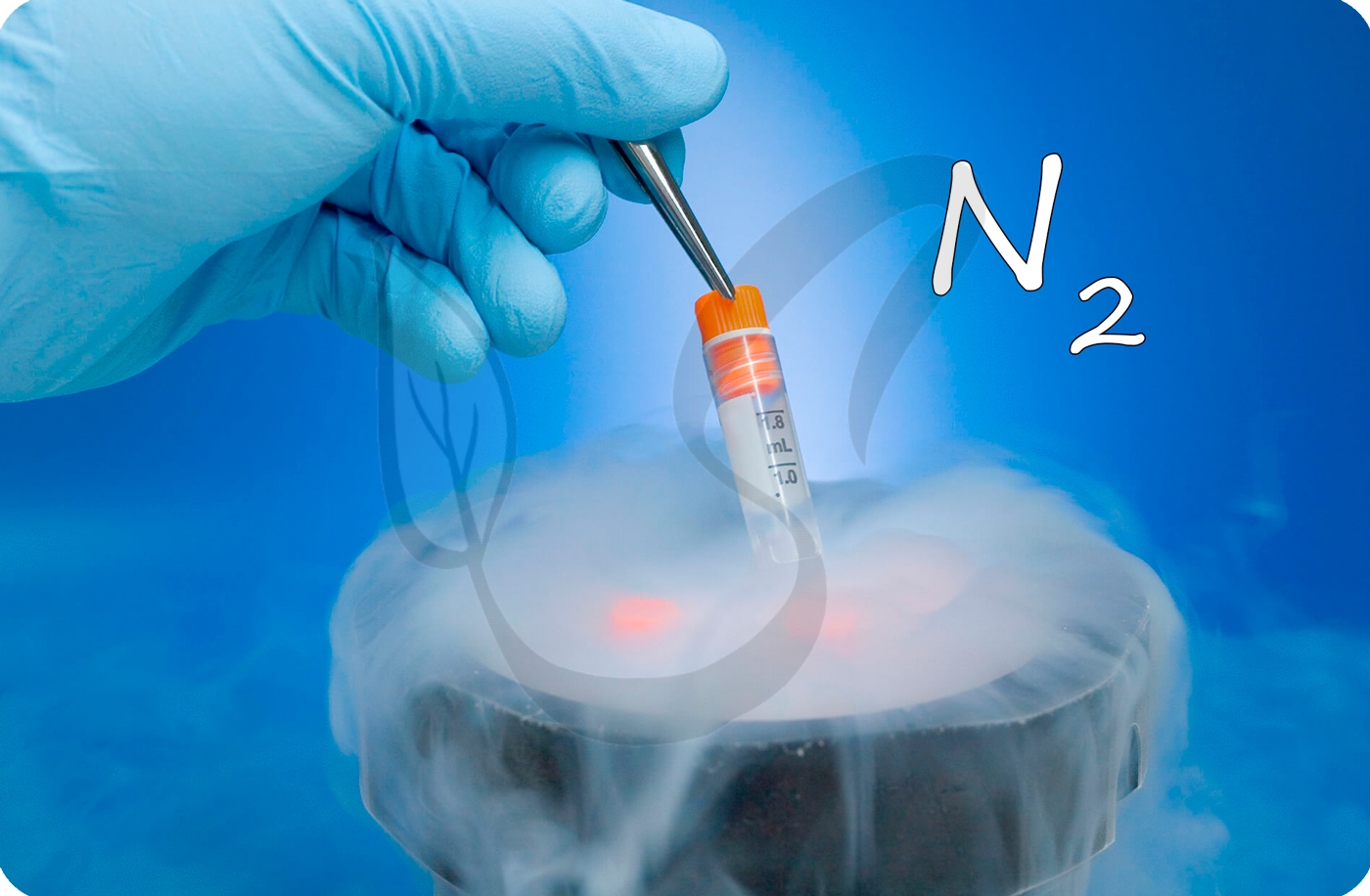
Общая характеристика элементов Va группы
От N к Bi (сверху вниз в периодической таблице) происходит увеличение: атомного радиуса, металлических, основных, восстановительных свойств.
Уменьшается электроотрицательность, энергия ионизация, сродство к электрону.
Азот, фосфор и мышьяк являются неметаллами, сурьма — полуметалл, висмут — металл.
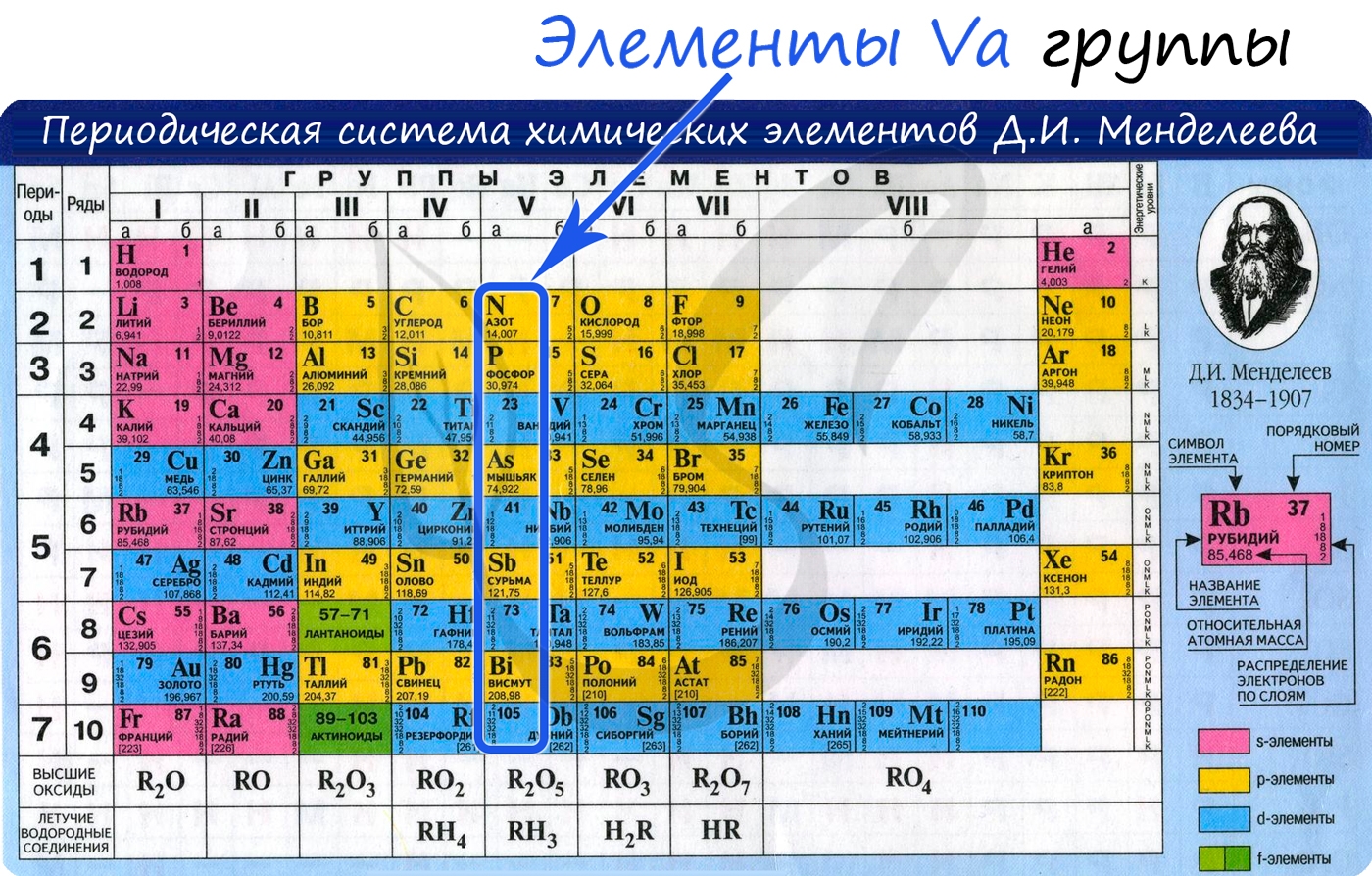
Электронные конфигурации у данных элементов схожи, так как они находятся в одной группе (главной подгруппе!), общая формула ns2np3:
- N — 2s22p3
- P — 3s23p3
- As — 4s24p3
- Sb — 5s25p3
- Bi — 6s26p3
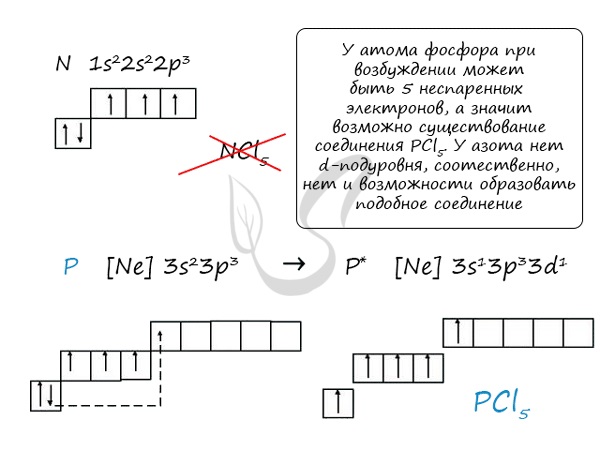
Основное и возбужденное состояние азота
При возбуждении атома азота электроны на s-подуровне распариваются и переходят на p-подуровень. Поскольку азот находится во втором периоде, то
3ий уровень у него отсутствует, что проявляется в особенностях электронной конфигурации возбужденного состояния.
Сравнивая возможности перемещения электронов у азота и фосфора, разница становится очевидна.
Природные соединения
В природе азот встречается в виде следующих соединений:
- Воздух — во вдыхаемом нами воздухе содержится 78% азота
- Азот входит в состав нуклеиновых кислот, белков
- KNO3 — индийская селитра, калиевая селитра
- NaNO3 — чилийская селитра, натриевая селитра
- NH4NO3 — аммиачная селитра (искусственный продукт, в природе не встречается)
Селитры являются распространенными азотными удобрениями, которые обеспечивают быстрый рост и развитие растений, повышают урожайность. Однако,
следует строго соблюдать правила их применения, чтобы не превысить допустимые концентрации.

Получение
В промышленности азот получают путем сжижения воздуха. В дальнейшем путем испарения их сжиженного воздуха получают азот.
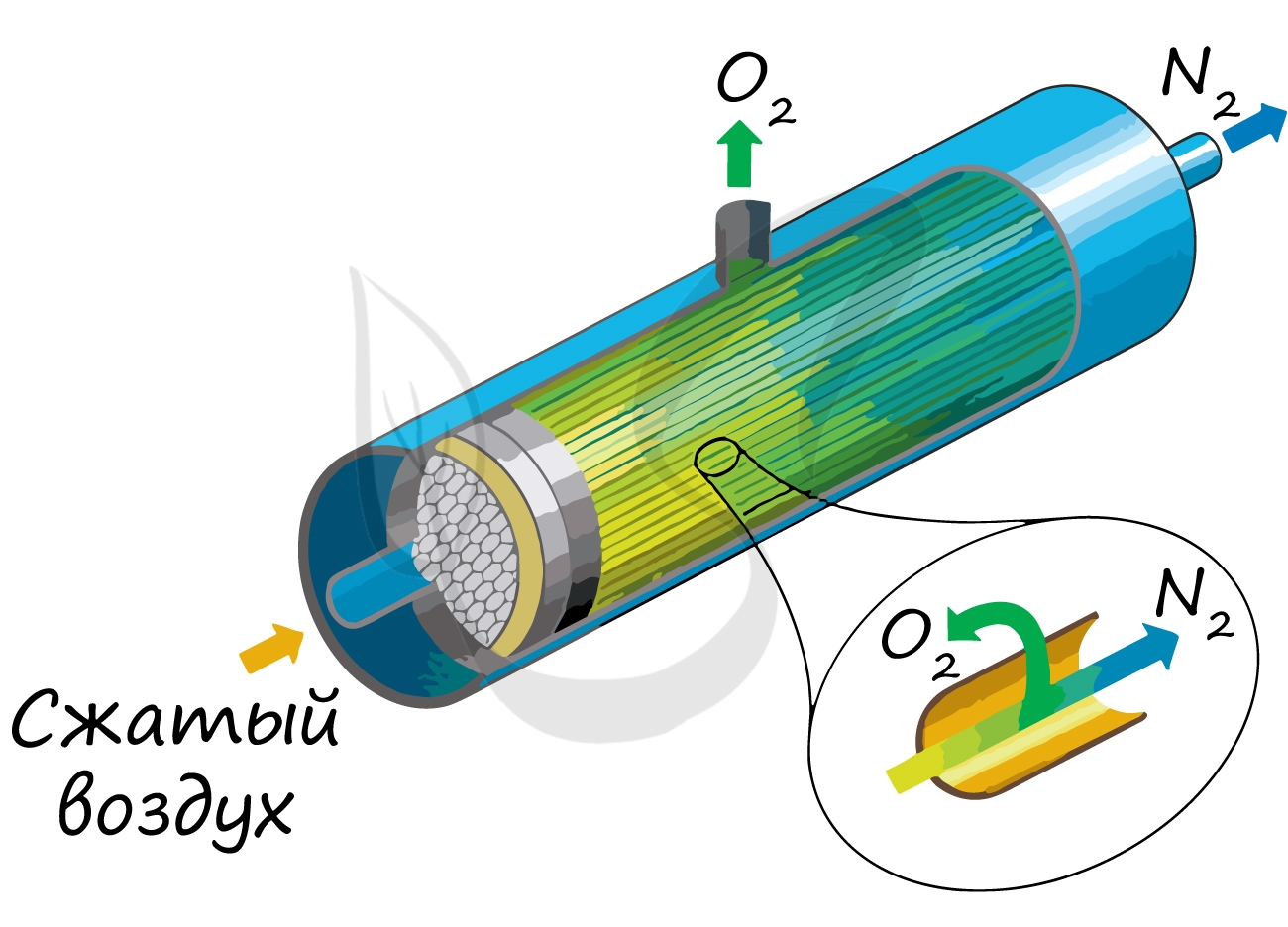
Применяют и метод мембранного разделения, при котором через специальный фильтр из сжатого воздуха удаляют кислород.
В лаборатории методы не столь экзотичны. Чаще всего получают азот разложением нитрита аммония
NH4NO2 → (t) N2 + H2O
Также азот можно получить путем восстановления азотной кислоты активными металлами.
HNO3(разб.) + Zn → Zn(NO3)2 + N2 + H2O

Химические свойства
Азот восхищает — он принимает все возможные для себя степени окисления от -3 до +5.

Молекула азота отличается большой прочностью из-за наличия тройной связи. Вследствие этого многие реакции эндотермичны: даже горение
азота в кислороде сопровождается поглощением тепла, а не выделением, как обычно бывает при горении.

- Реакция с металлами
- Реакция с неметаллами
Без нагревания азот взаимодействует только с литием. При нагревании реагирует и с другими металлами.
N2 + Li → Li3N (нитрид лития)
N2 + Mg → (t) Mg3N2
N2 + Al → (t) AlN
Важное практическое значение имеет синтез аммиака, который применяется в дальнейшим при изготовлении удобрений, красителей, лекарств.
N2 + H2 ⇄ (t, p) NH3
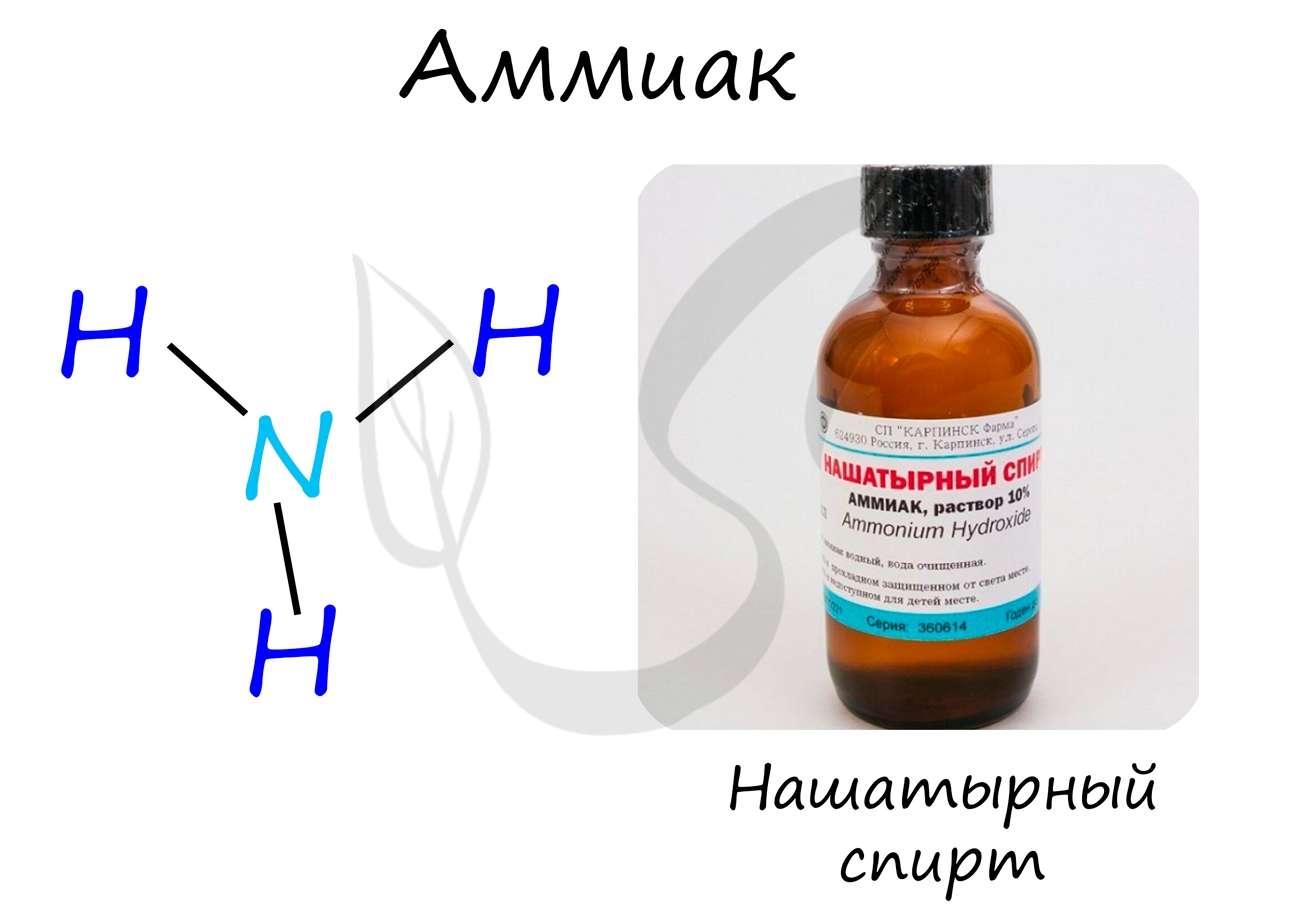
Аммиак
Бесцветный газ с резким едким запахом, раздражающим слизистые оболочки. Раствор концентрацией 10% аммиака применяется в медицинских целях,
называется нашатырным спиртом.

Получение
В промышленности аммиак получают прямым взаимодействием азота и водорода.
N2 + H2 ⇄ (t, p) NH3
В лабораторных условиях сильными щелочами действуют на соли аммония.
NH4Cl + NaOH → NH3 + NaCl + H2O
Химические свойства
Аммиак проявляет основные свойства, окрашивает лакмусовую бумажку в синий цвет.
- Реакция с водой
- Основные свойства
- Восстановительные свойства
Образует нестойкое соединение — гидроксид аммония, слабое основание. Оно сразу же распадается на воду и аммиак.
NH3 + H2O ⇄ NH4OH
Как основание аммиак способен реагировать с кислотами с образованием солей.
NH3 + HCl → NH4Cl (хлорид аммония)
NH3 + HNO3 → NH4NO3 (нитрат аммония)

Поскольку азот в аммиаке находится в минимальной степени окисления -3 и способен только ее повышать, то аммиак проявляет выраженные
восстановительные свойства. Его используют для восстановления металлов из их оксидов.
NH3 + FeO → N2↑ + Fe + H2O
NH3 + CuO → N2↑ + Cu + H2O
Горение аммиака без катализатора приводит к образованию азота в молекулярном виде. Окисление в присутствии катализатора сопровождается
выделением NO.
NH3 + O2 → (t) N2 + H2O
NH3 + O2 → (t, кат) NO + H2O

Соли аммония
Получение
NH3 + H2SO4 → NH4HSO4 (гидросульфат аммония, избыток кислоты)
3NH3 + H3PO4 → (NH4)3PO4
Химические свойства
Помните, что по правилам общей химии, если по итогам реакции выпадает осадок, выделяется газ или образуется вода — реакция идет.
- Реакции с кислотами
- Реакции с щелочами
- Реакции с солями
- Реакция гидролиза
- Реакции разложения
NH4Cl + H2SO4 → (NH4)2SO4 + HCl↑
В реакциях с щелочами образуется гидроксид аммония — NH4OH. Нестойкое основание, которое легко распадается на воду и аммиак.
NH4Cl + KOH → KCl + NH3 + H2O
(NH4)2SO4 + BaCl2 = BaSO4↓ + NH4Cl
В воде ион аммония подвергается гидролизу с образованием нестойкого гидроксида аммония.
NH4+ + H2O ⇄ NH4OH + H+
NH4OH ⇄ NH3 + H2O
NH4Cl → (t) NH3↑ + HCl↑
(NH4)2CO3 → (t) NH3↑ + H2O + CO2↑
NH4NO2 → (t) N2↑ + H2O
NH4NO3 → (t) N2O↑ + H2O
(NH4)3PO4 → (t) NH3↑ + H3PO4

Оксид азота I — N2O
Закись азота, веселящий газ — N2O — обладает опьяняющим эффектом. Несолеобразующий оксид. При н.у. является бесцветным газом с приятным
сладковатым запахом и привкусом. В медицине применяется в больших концентрациях для ингаляционного наркоза.

Получают N2O разложением нитрата аммония при нагревании:
NH4NO3 → N2O + H2O
Оксид азота I разлагается на азот и кислород:
N2O → (t) N2 + O2
Оксид азота II — NO
Окись азота — NO. Несолеобразующий оксид. При н.у. бесцветный газ, на воздухе быстро окисляется до оксида азота IV.
Получение
В промышленных масштабах оксид азота II получают при каталитическом окислении аммиака.
NH3 + O2 → (t, кат) NO + H2O
В лабораторных условиях — в ходе реакции малоактивных металлов с разбавленной азотной кислотой.
Cu + HNO3(разб.) → Cu(NO3)2 + NO + H2O
Химические свойства
На воздухе быстро окисляется с образованием бурого газа — оксида азота IV — NO2.
NO + O2 → NO2

Оксид азота III — N2O3
При н.у. жидкость синего цвета, в газообразной форме бесцветен. Высокотоксичный, приводит к тяжелым ожогам кожи.

Получение
Получают N2O3 в две стадии: сначала реакцией оксида мышьяка III с азотной кислотой, затем
охлаждением полученной смеси газов до температуры — 36 °C.
As2O3 + HNO3 → H3AsO 3 + NO↑ + NO2↑
При охлаждении газов образуется оксид азота III.
NO + NO2 → N2O3
Химические свойства
Является кислотным оксидом. соответствует азотистой кислота — HNO2, соли которой называются нитриты (NO2-).
Реагирует с водой, основаниями.
H2O + N2O3 → HNO2
NaOH + N2O3 → NaNO2 + H2O
Оксид азота IV — NO2
Бурый газ, имеет острый запах. Ядовит.

Получение
В лабораторных условиях данный оксид получают в ходе реакции меди с концентрированной азотной кислотой. Также NO2 выделяется при
разложении нитратов.
Cu + HNO3(конц) → Cu(NO3)2 + NO2 + H2O

Cu(NO3)2 → (t) CuO + NO2 + O2
Pb(NO3)2 → (t) PbO + NO2 + O2
Химические свойства
Проявляет высокую химическую активность, кислотный оксид.
- Окислительные свойства
- Реакции с водой и щелочами
Как окислитель NO2 ведет себя в реакциях с фосфором, углеродом и серой, которые сгорают в нем.
NO2 + C → CO2 + N2
NO2 + P → P2O5 + N2
Окисляет SO2 в SO3 — на этой реакции основана одна из стадий получения серной кислоты.
SO2 + NO2 → SO3 + NO
Оксид азота IV соответствует сразу двум кислотам — азотистой HNO2 и азотной HNO3. Реакции с
водой и щелочами протекают по одной схеме.
NO2 + H2O → HNO3 + HNO2
NO2 + LiOH → LiNO3 + LiNO2 + H2O
Если растворение в воде оксида проводить в избытке кислорода, образуется азотная кислота.
NO2 + H2O + O2 → HNO3

© Беллевич Юрий Сергеевич 2018-2020
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение
(в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов
без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования,
обратитесь, пожалуйста, к Беллевичу Юрию.
