Какими свойствами отличаются моно ди и полисахариды
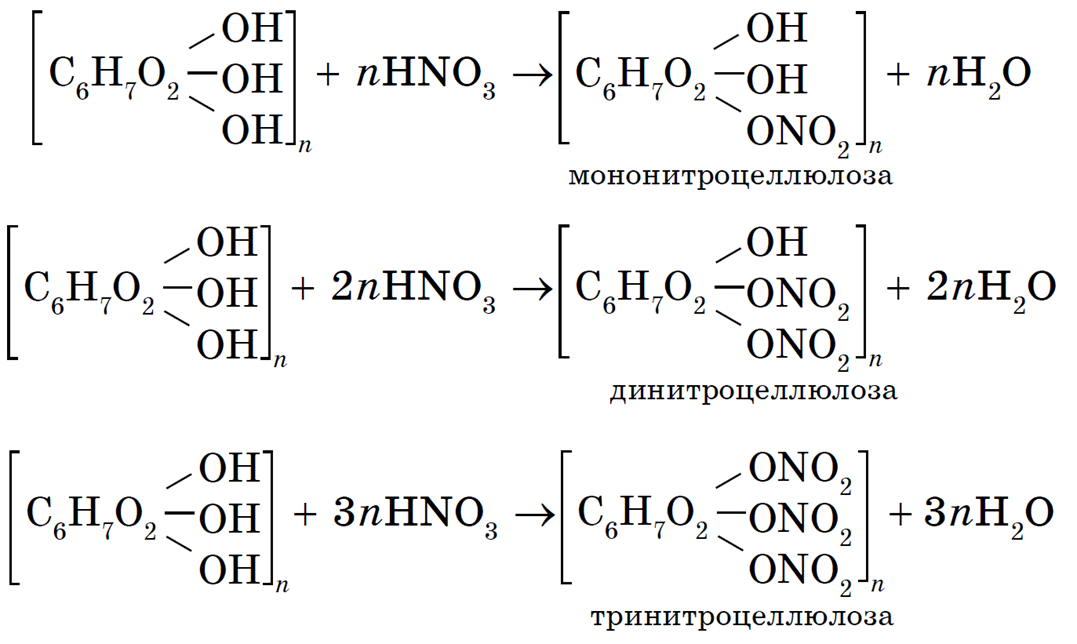
Углеводы — органические соединения, чаще всего природного происхождения, состоящие только из углерода, водорода и кислорода.
Углеводы играют огромную роль в жизнедеятельности всех живых организмов.
Свое название данный класс органических соединений получил за то, что первые изученные человеком углеводы имели общую формулу вида Cx(H2O)y . Т.е. их условно посчитали соединениями углерода и воды. Однако позднее оказалось, что состав некоторых углеводов отклоняется от этой формулы. Например, такой углевод как дезоксирибоза имеет формулу С5Н10О4. В то же время существуют некоторые соединения, формально соответствующие формуле Cx(H2O)y, однако к углеводам не относящиеся, как, например, формальдегид (СН2О) и уксусная кислота (С2Н4О2).
Тем не менее, термин «углеводы» исторически закрепился за данным классом соединений, в связи с чем повсеместно используется и в наше время.
Классификация углеводов
В зависимости от способности углеводов расщепляться при гидролизе на другие углеводы с меньшей молекулярной массой их делят на простые (моносахариды) и сложные (дисахариды, олигосахариды, полисахариды).
Как легко догадаться, из простых углеводов, т.е. моносахаридов, нельзя гидролизом получить углеводы с еще меньшей молекулярной массой.
При гидролизе одной молекулы дисахарида образуются две молекулы моносахарида, а при полном гидролизе одной молекулы любого полисахарида получается множество молекул моносахаридов.
Химические свойства моносахаридов на примере глюкозы и фруктозы
Самыми распространенными моносахаридами являются глюкоза и фруктоза, имеющие следующие структурные формулы:
Как можно заметить, и в молекуле глюкозы, и в молекуле фруктозы присутствует по 5 гидроксильных групп, в связи с чем их можно считать многоатомными спиртами.
В составе молекулы глюкозы имеется альдегидная группа, т.е. фактически глюкоза является многоатомным альдегидоспиртом.
В случае фруктозы можно обнаружить в ее молекуле кетонную группу, т.е. фруктоза является многоатомным кетоспиртом.
Химические свойства глюкозы и фруктозы как карбонильных соединений
Все моносахариды могут реагировать в присутствии катализаторов с водородом. При этом карбонильная группа восстанавливается до спиртовой гидроксильной. Так, в частности, гидрированием глюкозы в промышленности получают искусственный подсластитель – гексаатомный спирт сорбит:
Молекула глюкозы содержит в своем составе альдегидную группу, в связи с чем логично предположить, что ее водные растворы дают качественные реакции на альдегиды. И действительно, при нагревании водного раствора глюкозы со свежеосажденным гидроксидом меди (II) так же, как и в случае любого другого альдегида, наблюдается выпадение из раствора кирпично-красного осадка оксида меди (I). При этом альдегидная группа глюкозы окисляется до карбоксильной – образуется глюконовая кислота:
Также глюкоза вступает и в реакцию «серебряного зеркала» при действии на нее аммиачного раствора оксида серебра. Однако, в отличие от предыдущей реакции вместо глюконовой кислоты образуется ее соль – глюконат аммония, т.к. в растворе присутствует растворенный аммиак:
Фруктоза и другие моносахариды, являющиеся многоатомными кетоспиртами, в качественные реакции на альдегиды не вступают.
Химические свойства глюкозы и фруктозы как многоатомных спиртов
Поскольку моносахариды, в том числе глюкоза и фруктоза, имеют в составе молекул несколько гидроксильных групп. Все они дают качественную реакцию на многоатомные спирты. В частности, в водных растворах моносахаридов растворяется свежеосажденный гидроксид меди (II). При этом вместо голубого осадка Cu(OH)2 образуется темно-синий раствор комплексных соединений меди.
Реакции брожения глюкозы
Спиртовое брожение
При действии на глюкозу некоторых ферментов глюкоза способна превращаться в этиловый спирт и углекислый газ:
Молочнокислое брожение
Помимо спиртового типа брожения существует также и немало других. Например, молочнокислое брожение, которое протекает при скисании молока, квашении капусты и огурцов:
Особенности существования моносахаридов в водных растворах
Моносахариды существуют в водном растворе в трех формах – двух циклических (альфа- и бета-) и одной нециклической (обычной). Так, например, в растворе глюкозы существует следующее равновесие:
Как можно видеть, в циклических формах отсутствует альдегидная группа, в связи с тем что она участвует в образовании цикла. На ее основе образуется новая гидроксильная группа, которую называют ацетальным гидроксилом. Аналогичные переходы между циклическими и нециклической формами наблюдаются и для всех других моносахаридов.
Дисахариды. Химические свойства.
Общее описание дисахаридов
Дисахаридами называют углеводы, молекулы которых состоят из двух остатков моносахаридов, связанных между собой за счет конденсации двух полуацетальных гидроксилов либо же одного спиртового гидроксила и одного полуацетального. Связи, образующиеся таким образом между остатками моносахаридов, называют гликозидными. Формулу большинства дисахаридов можно записать как C12H22O11.
Наиболее часто встречающимся дисахаридом является всем знакомый сахар, химиками называемый сахарозой. Молекула данного углевода образована циклическими остатками одной молекулы глюкозы и одной молекулы фруктозы. Связь между остатками дисахаридов в данном случае реализуется за счет отщепления воды от двух полуацетальных гидроксилов:
Поскольку связь между остатками моносахаридов образована при конденсации двух ацетальных гидроксилов, для молекулы сахара невозможно раскрытие ни одного из циклов, т.е. невозможен переход в карбонильную форму. В связи с этим сахароза не способна давать качественные реакции на альдегиды.
Подобного рода дисахариды, которые не дают качественные реакции на альдегиды, называют невосстанавливающими сахарами.
Тем не менее, существуют дисахариды, которые дают качественные реакции на альдегидную группу. Такая ситуация возможна, когда в молекуле дисахарида остался полуацетальный гидроксил из альдегидной группы одной из исходных молекул моносахаридов.
В частности, в реакцию с аммиачным раствором оксида серебра, а также гидроксидом меди (II) подобно альдегидам вступает мальтоза. Связано это с тем, что в её водных растворах существует следующее равновесие:
Как можно видеть, в водных растворах мальтоза существует в виде двух форм – с двумя циклами в молекуле и одним циклом в молекуле и альдегидной группой. По этой причине мальтоза, в отличие от сахарозы, дает качественную реакцию на альдегиды.
Гидролиз дисахаридов
Все дисахариды способны вступать в реакцию гидролиза, катализируемую кислотами, а также различными ферментами. В ходе такой реакции из одной молекулы исходного дисахарида образуется две молекулы моносахарида, которые могут быть как одинаковыми, так и различными в зависимости от состава исходного моносахарида.
Так, например, гидролиз сахарозы приводит к образованию глюкозы и фруктозы в равных количествах:
А при гидролизе мальтозы образуется только глюкоза:
Дисахариды как многоатомные спирты
Дисахариды, являясь многоатомными спиртами, дают соответствующую качественную реакцию с гидроксидом меди (II), т.е. при добавлении их водного раствора ко свежеосажденному гидроксиду меди (II) нерастворимый в воде голубой осадок Cu(OH)2 растворяется с образованием темно-синего раствора.
Полисахариды. Крахмал и целлюлоза
Полисахариды — сложные углеводы, молекулы которых состоят из большого числа остатков моносахаридов, связанных между собой гликозидными связями.
Есть и другое определение полисахаридов:
Полисахаридами называют сложные углеводы, молекулы которых образуют при полном гидролизе большое число молекул моносахаридов.
В общем случае формула полисахаридов может быть записана как (C6H10O5)n.
Крахмал – вещество, представляющее собой белый аморфный порошок, не растворимый в холодной воде и частично растворимый в горячей с образованием коллоидного раствора, называемого в быту крахмальным клейстером.
Крахмал образуется из углекислого газа и воды в процессе фотосинтеза в зеленых частях растений под действием энергии солнечного света. В наибольших количествах крахмал содержится в картофельных клубнях, пшеничных, рисовых и кукурузных зернах. По этой причине указанные источники крахмала и являются сырьем для его получения в промышленности.
Целлюлоза – вещество, в чистом состоянии представляющее собой белый порошок, не растворимый ни в холодной, ни в горячей воде. В отличие от крахмала целлюлоза не образует клейстер. Практически из чистой целлюлозы состоит фильтровальная бумага, хлопковая вата, тополиный пух. И крахмал, и целлюлоза являются продуктами растительного происхождения. Однако, роли, которые они играют в жизни растений, различны. Целлюлоза является в основном строительным материалом, в частности, главным образом ей образованы оболочки растительных клеток. Крахмал же несет в основном запасающую, энергетическую функцию.
Химические свойства крахмала и целлюлозы
Горение
Все полисахариды, в том числе крахмал и целлюлоза, при полном сгорании в кислороде образуют углекислый газ и воду:
Образование глюкозы
При полном гидролизе как крахмала, так и целлюлозы образуется один и тот же моносахарид – глюкоза:
Качественная реакция на крахмал
При действии йода на что-либо, в чем содержится крахмал, появляется синее окрашивание. При нагревании синяя окраска исчезает, при охлаждении появляется вновь.
При сухой перегонке целлюлозы, в частности древесины, происходит ее частичное разложение с образованием таких низкомолекулярных продуктов как метиловый спирт, уксусная кислота, ацетон и т.д.
Поскольку и в молекулах крахмала, и в молекулах целлюлозы имеются спиртовые гидроксильные группы, данные соединения способны вступать в реакции этерификации как с органическими, так и с неорганическими кислотами:
Оглавление
- Классификация углеводов
- Моносахариды. Глюкоза.
- Строение молекулы глюкозы
- Химические свойства глюкозы
- Полисахариды. Крахмал и целлюлоза.
- Строение крахмала и целлюлозы
- Химические свойства полисахаридов
- Применение углеводов
- Задания для самопроверки
Классификация углеводов
Углеводы — органические вещества, молекулы которых состоят из атомов углерода, водорода и кислорода, причем водород и кислород находятся в них, как правило, в таком же соотношении, как и в молекуле воды (2 : 1).
Общая формула углеводов — Сn(Н2О)m, т. е. они как бы состоят из углерода и воды, отсюда и название класса, которое имеет исторические корни. Оно появилось на основе анализа первых известных углеводов. В дальнейшем было установлено, что имеются углеводы, в молекулах которых не соблюдается указанное соотношение (2 : 1), например дезоксирибоза — С5Н10О4. Известны также органические соединения, состав которых соответствует приведенной общей формуле, но которые не принадлежат к классу углеводов. К ним относятся, например, формальдегид СН2О и уксусная кислота СН3СООН.
Однако название «углеводы» укоренилось и в настоящее время является общепризнанным для этих веществ.
Углеводы по их способности гидролизоваться можно разделить на три основные группы: моно-, ди- и полисахариды.
Моносахариды — углеводы, которые не гидролизуются (не разлагаются водой). В свою очередь, в зависимости от числа атомов углерода, моносахариды подразделяются на триозы (молекулы которых содержат три углеродных атома), тетрозы (четыре углеродных атома), пентозы (пять), гексозы (шесть) и т. д.
В природе моносахариды представлены преимущественно пентозами и гексозами.
К пентозам относятся, например, рибоза — С5Н10О5 и дезоксирибоза (рибоза, у которой «отняли» атом кислорода) — С5Н10О4. Они входят в состав РНК и ДНК и определяют первую часть названий нуклеиновых кислот.
К гексозам, имеющим общую молекулярную формулу С6Н12О6, относятся, например, глюкоза, фруктоза, галактоза.
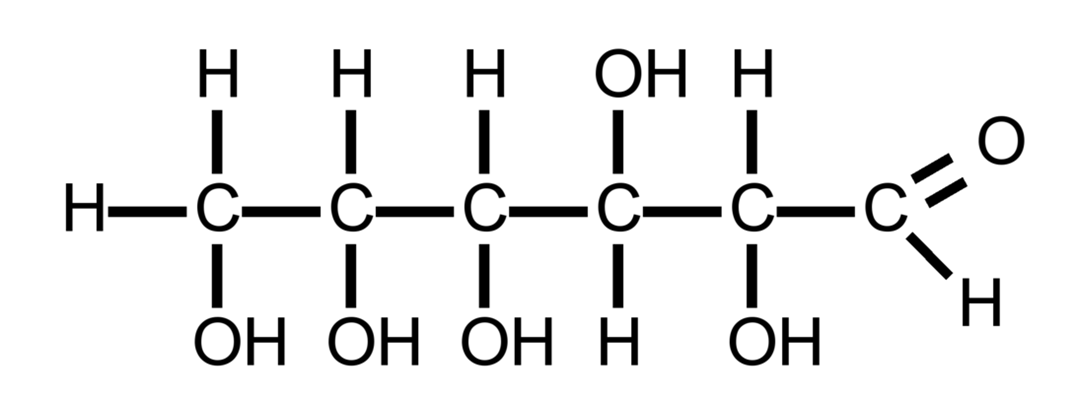 Формула глюкозы
Формула глюкозы
Дисахариды — углеводы, которые гидролизуются с образованием двух молекул моносахаридов, например гексоз. Общую формулу подавляющего большинства дисахаридов вывести несложно: нужно «сложить» две формулы гексоз и «вычесть» из получившейся формулы молекулу воды — С12Н22О11. Соответственно можно записать и общее уравнение гидролиза:
К дисахаридам относятся:
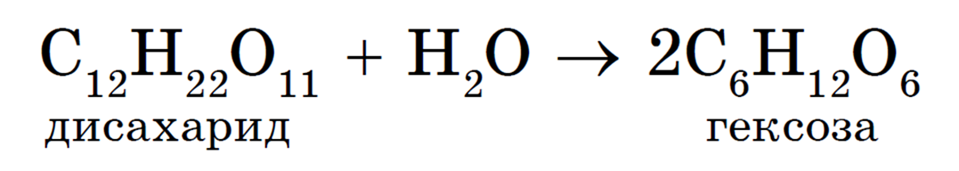
1. Сахароза (обычный пищевой сахар), которая при гидролизе образует одну молекулу глюкозы и молекулу фруктозы. Она содержится в большом количестве в сахарной свекле, сахарном тростнике (отсюда и названия — свекловичный или тростниковый сахар), клене (канадские первопроходцы добывали кленовый сахар), сахарной пальме, кукурузе и т. д.
2. Мальтоза (солодовый сахар), которая гидролизуется с образованием двух молекул глюкозы. Мальтозу можно получить при гидролизе крахмала под действием ферментов, содержащихся в солоде, — пророщенных, высушенных и размолотых зернах ячменя.
3. Лактоза (молочный сахар), которая гидролизуется с образованием молекул глюкозы и галактозы. Она содержится в молоке млекопитающих (до 4-6 %), обладает невысокой сладостью и используется как наполнитель в драже и аптечных таблетках.
Сладкий вкус разных моно- и дисахаридов различен. Так, самый сладкий моносахарид — фруктоза — в 1,5 раза слаще глюкозы, которую принимают за эталон. Сахароза (дисахарид), в свою очередь, в 2 раза слаще глюкозы и в 4-5 раз — лактозы, которая почти безвкусна.
Полисахариды — крахмал, гликоген, декстрины, целлюлоза и т. д. — углеводы, которые гидролизуются с образованием множества молекул моносахаридов, чаще всего глюкозы.
Чтобы вывести формулу полисахаридов, нужно от молекулы глюкозы «отнять» молекулу воды и записать выражение с индексом n: (С6Н10О5)n, ведь именно за счет отщепления молекул воды в природе образуются ди- и полисахариды.
Роль углеводов в природе и их значение для жизни человека чрезвычайно велики. Образуясь в клетках растений в результате фотосинтеза, они выступают источником энергии для клеток животных. В первую очередь это относится к глюкозе.
Многие углеводы (крахмал, гликоген, сахароза) выполняют запасающую функцию, роль резерва питательных веществ.
Кислоты РНК и ДНК, в состав которых входят некоторые углеводы (пентозы-рибозы и дезоксирибоза), выполняют функции передачи наследственной информации.
Целлюлоза — строительный материал растительных клеток — играет роль каркаса для оболочек этих клеток. Другой полисахарид — хитин — выполняет аналогичную роль в клетках некоторых животных: образует наружный скелет членистоногих (ракообразных), насекомых, паукообразных.
Углеводы служат в конечном итоге источником нашего питания: мы потребляем зерно, содержащее крахмал, или скармливаем его животным, в организме которых крахмал превращается в белки и жиры. Самая гигиеничная одежда изготовлена из целлюлозы или продуктов на ее основе: хлопка и льна, вискозного волокна, ацетатного шелка. Деревянные дома и мебель построены из той же целлюлозы, образующей древесину.
В основе производства фото- и кинопленки — все та же целлюлоза. Книги, газеты, письма, денежные банкноты — все это продукция целлюлозно-бумажной промышленности. Значит, углеводы обеспечивают нас всем необходимым для жизни: пищей, одеждой, кровом.
Кроме того, углеводы участвуют в построении сложных белков, ферментов, гормонов. Углеводами являются и такие жизненно необходимые вещества, как гепарин (он играет важнейшую роль — предотвращает свертывание крови), агар-агар (его получают из морских водорослей и применяют в микробиологической и кондитерской промышленности — вспомните знаменитый торт «Птичье молоко»).
Необходимо подчеркнуть, что единственным видом энергии на Земле (помимо ядерной, разумеется) является энергия Солнца, а единственным способом ее аккумулирования для обеспечения жизнедеятельности всех живых организмов является процесс фотосинтеза, протекающий в клетках живых растений и приводящий к синтезу углеводов из воды и углекислого газа. Именно при этом превращении образуется кислород, без которого жизнь на нашей планете была бы невозможна:

Моносахариды. Глюкоза

Глюкоза и фруктоза — твердые бесцветные кристаллические вещества. Глюкоза содержится в соке винограда (отсюда название «виноградный сахар») вместе с фруктозой, которая содержится в некоторых фруктах и плодах (отсюда название «фруктовый сахар»), составляет значительную часть меда. В крови человека и животных постоянно содержится около 0,1 % глюкозы (80-120 мг в 100 мл крови). Большая ее часть (около 70 %) подвергается в тканях медленному окислению с выделением энергии и образованием конечных продуктов — углекислого газа и воды (процесс гликолиза):
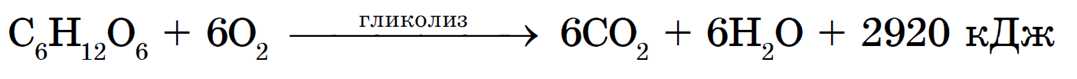
Энергия, выделяемая при гликолизе, в значительной степени обеспечивает энергетические потребности живых организмов.
Превышение содержания глюкозы в крови уровня 180 мг в 100 мл крови свидетельствует о нарушении углеводного обмена и развитии опасного заболевания — сахарного диабета.
Строение молекулы глюкозы
О строении молекулы глюкозы можно судить на основании опытных данных. Она реагирует с карбоновыми кислотами, образуя сложные эфиры, содержащие от 1 до 5 остатков кислоты. Если раствор глюкозы прилить к свежеполученному гидроксиду меди (II), то осадок растворяется и образуется ярко-синий раствор соединения меди, т. е. происходит качественная реакция на многоатомные спирты. Следовательно, глюкоза является многоатомным спиртом. Если же подогреть полученный раствор, то вновь выпадет осадок, но уже красноватого цвета, т. е. произойдет качественная реакция на альдегиды. Аналогично, если раствор глюкозы нагреть с аммиачным раствором оксида серебра, то произойдет реакция «серебряного зеркала». Следовательно, глюкоза является одновременно многоатомным спиртом и альдегидом — алъдегидоспиртом. Попробуем вывести структурную формулу глюкозы. Всего атомов углерода в молекуле C6H12O6 шесть. Один атом входит в состав альдегидной группы:
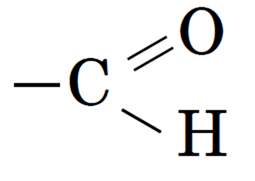
Остальные пять атомов связываются с пятью гидроксигруппами.
И наконец, атомы водорода в молекуле распределим с учетом того, что углерод четырехвалентен:
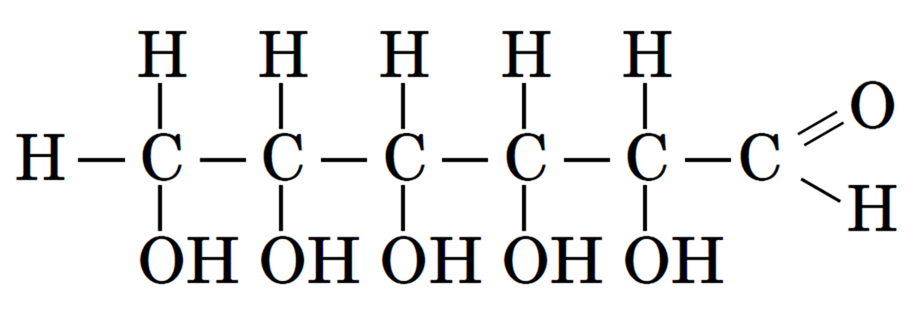
или
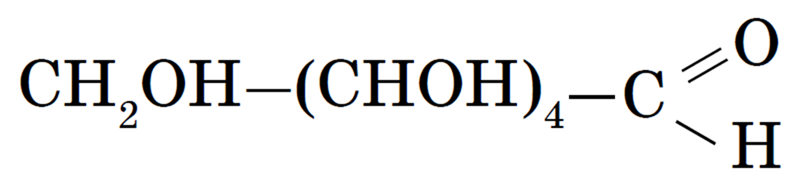
Однако установлено, что в растворе глюкозы помимо линейных (альдегидных) молекул существуют молекулы циклического строения, из которых состоит кристаллическая глюкоза. Превращение молекул линейной формы в циклическую можно объяснить, если вспомнить, что атомы углерода могут свободно вращаться вокруг σ-связей, расположенных под углом 109° 28′. При этом альдегидная группа (1-й атом углерода) может приблизиться к гидроксильной группе пятого атома углерода. В первой под влиянием гидрокси- группы разрывается π-связь: к атому кислорода присоединяется атом водорода, и «потерявший» этот атом кислород гидроксигруппы замыкает цикл:
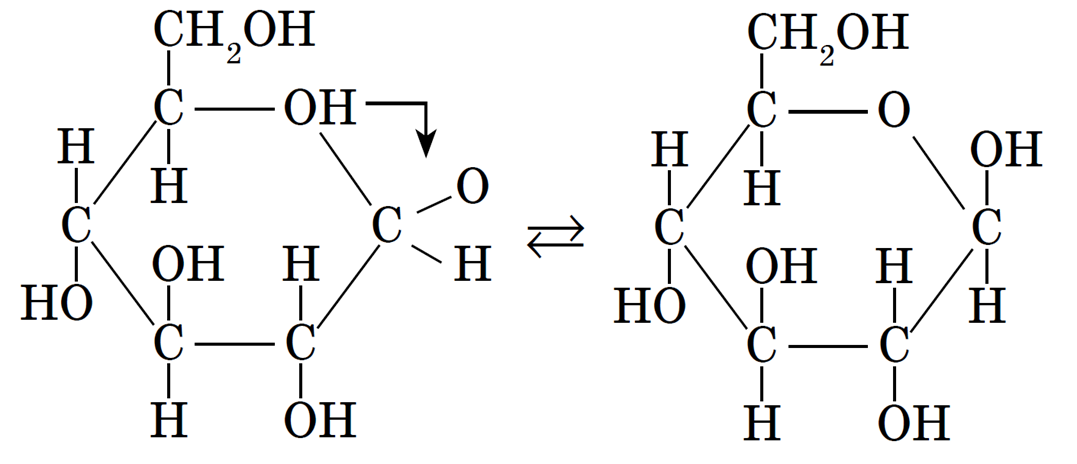
В результате такой перегруппировки атомов образуется циклическая молекула. Циклическая формула показывает не только порядок связи атомов, но и их пространственное расположение. В результате взаимодействия первого и пятого атомов углерода появляется новая гидроксигруппа у первого атома, которая может занять в пространстве два положения: над и под плоскостью цикла, а потому возможны две циклические формы глюкозы:
а) α-форма глюкозы — гидроксильные группы при первом и втором атомах углерода расположены по одну сторону кольца молекулы;
б) β-форма глюкозы — гидроксильные группы находятся по разные стороны кольца молекулы:
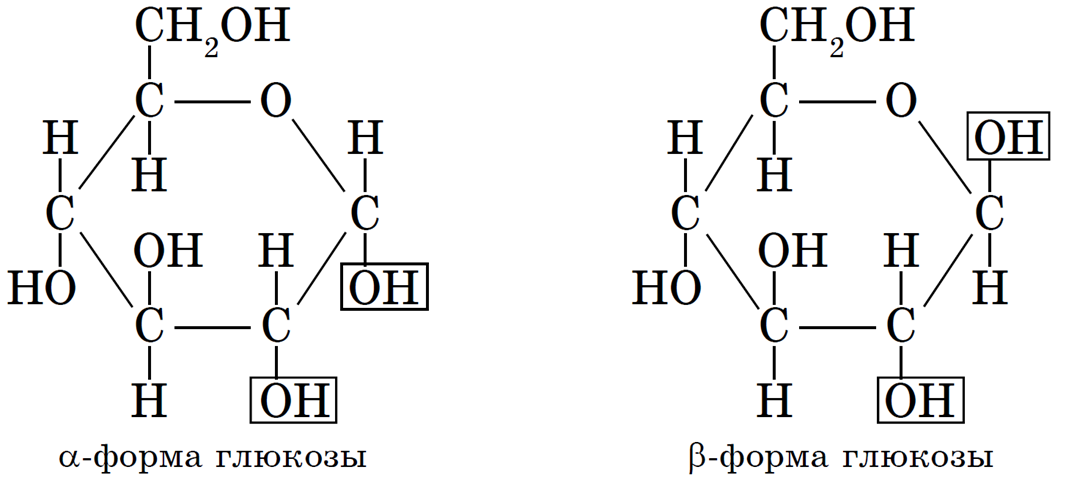
В водном растворе глюкозы в динамическом равновесии находятся три ее изомерные формы — циклическая α-форма, линейная (альдегидная) форма и циклическая β-форма:

В установившемся динамическом равновесии преобладает β-форма (около 63 %), так как она энергетически предпочтительнее — у нее OH-группы у первого и второго углеродных атомов по разные стороны цикла. У α-формы (около 37 %) OH-группы у тех же углеродных атомов расположены по одну сторону плоскости, поэтому она энергетически менее устойчива, чем β-форма. Доля же линейной формы в равновесии очень мала (всего около 0,0026 %).
Динамическое равновесие можно сместить. Например, при действии на глюкозу аммиачного раствора оксида серебра количество ее линейной (альдегидной) формы, которой в растворе очень мало, пополняется все время за счет циклических форм, и глюкоза полностью подвергается окислению до глюконовой кислоты.
Изомером альдегидоспирта глюкозы является кетоноспирт — фруктоза:
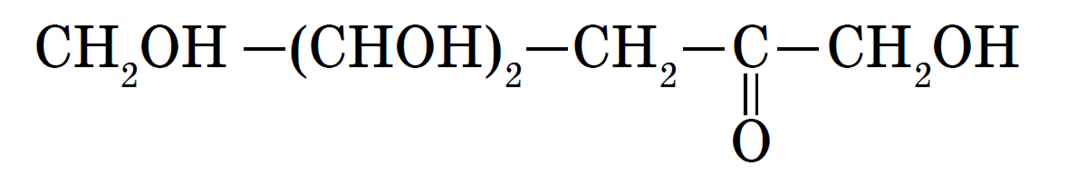
Химические свойства глюкозы
Химические свойства глюкозы, как и любого другого органического вещества, определяются ее строением. Глюкоза обладает двойственной функцией, являясь и альдегидом, и многоатомным спиртом, поэтому для нее характерны свойства и многоатомных спиртов, и альдегидов.
Реакции глюкозы как многоатомного спирта.
Глюкоза дает качественную реакцию многоатомных спиртов (вспомните глицерин) со свежеполученным гидроксидом меди (II), образуя ярко-синий раствор соединения меди (II).
Глюкоза, подобно спиртам, может образовывать сложные эфиры.
Реакции глюкозы как альдегида
1. Окисление альдегидной группы. Глюкоза как альдегид способна окисляться в соответствующую (глюконовую) кислоту и давать качественные реакции альдегидов.
Реакция «серебряного зеркала»:
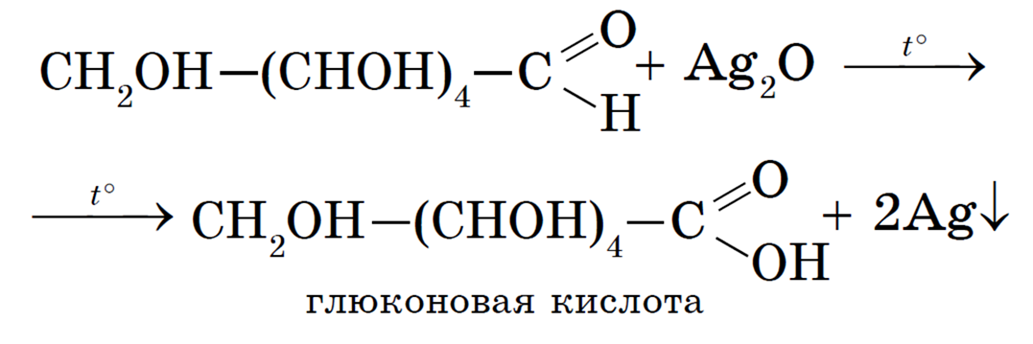
Реакция со свежеполученным Cu(OH)2 при нагревании:
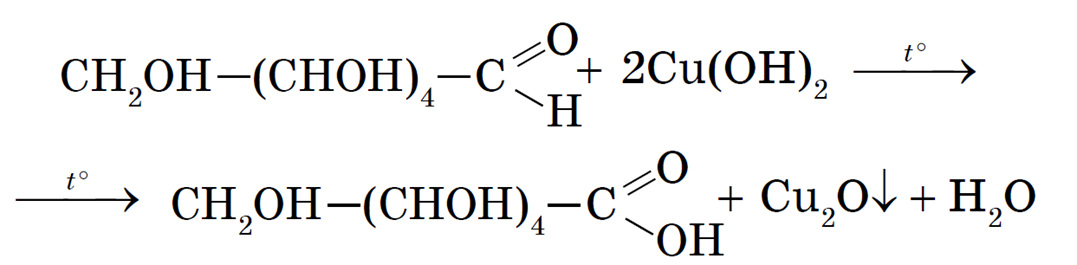
Восстановление альдегидной группы. Глюкоза может восстанавливаться в соответствующий спирт (сорбит):
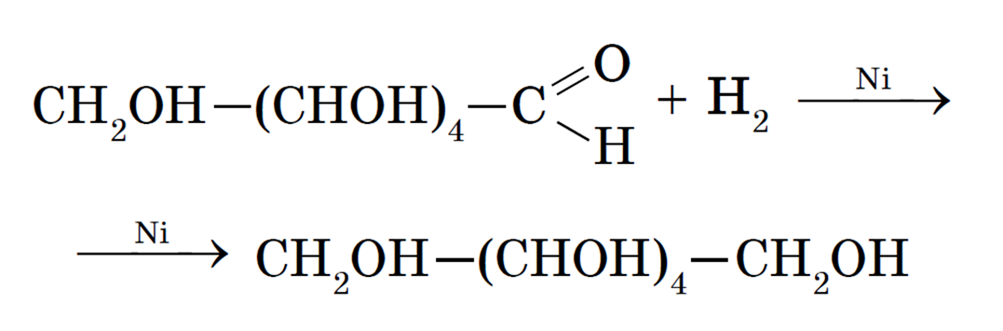
Реакции брожения
Эти реакции протекают под действием особых биологических катализаторов белковой природы — ферментов.
1. Спиртовое брожение:
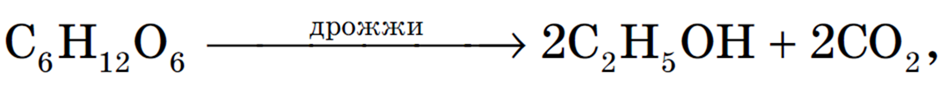
издавна применяемое человеком для получения этилового спирта и алкогольных напитков.
2. Молочнокислое брожение:
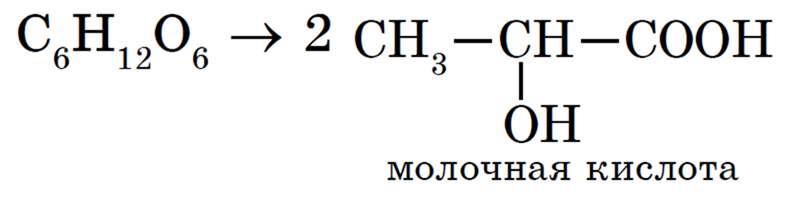
которое составляет основу жизнедеятельности молочнокислых бактерий и происходит при скисании молока, квашении капусты и огурцов, силосовании зеленых кормов.
Химические свойства глюкозы — конспект
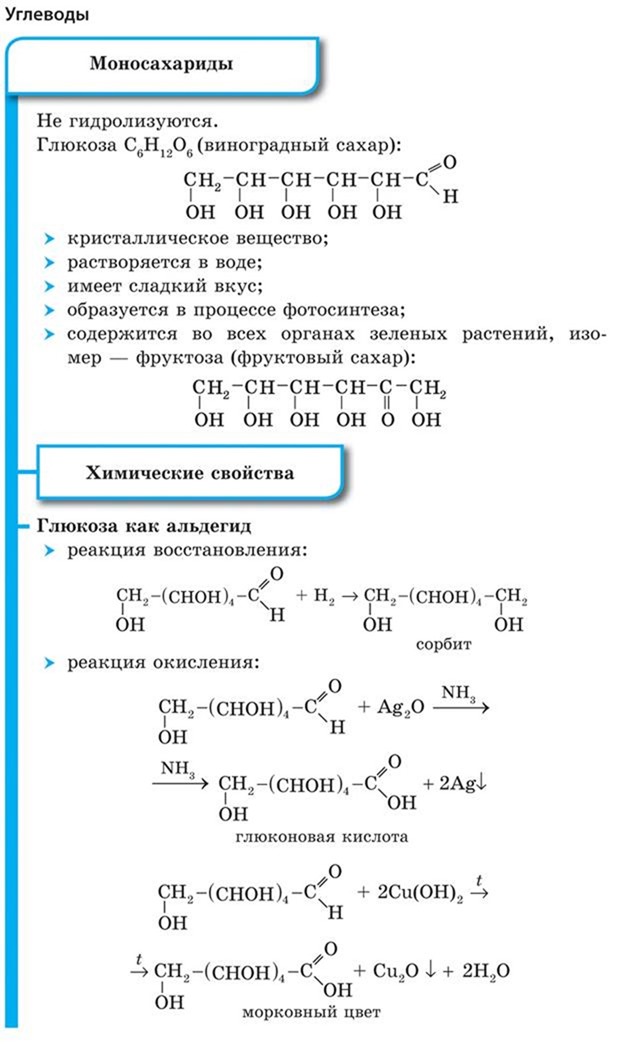

Полисахариды. Крахмал и целлюлоза.

Крахмал — белый аморфный порошок, не растворяется в холодной воде. В горячей воде он разбухает и образует коллоидный раствор — крахмальный клейстер.
Крахмал содержится в цитоплазме растительных клеток в виде зерен запасного питательного вещества. В картофельных клубнях содержится около 20 % крахмала, в пшеничных и кукурузных зернах — около 70 %, а в рисовых — почти 80 %.
Целлюлоза (от лат. cellula — клетка), выделенная из природных материалов (например, вата или фильтровальная бумага), представляет собой твердое волокнистое вещество, нерастворимое в воде.
Оба полисахарида имеют растительное происхождение, однако играют в клетке растений разную роль: целлюлоза — строительную, конструкционную функцию, а крахмал — запасающую. Поэтому целлюлоза является обязательным элементом клеточной оболочки растений. Волокна хлопка содержат до 95 % целлюлозы, волокна льна и конопли — до 80 %, а в древесине ее содержится около 50 %.
Строение крахмала и целлюлозы
Состав этих полисахаридов можно выразить общей формулой (C6H10O5)n. Число повторяющихся звеньев в макромолекуле крахмала может колебаться от нескольких сотен до нескольких тысяч. Целлюлоза же отличается значительно большим числом звеньев и, следовательно, молекулярной массой, которая достигает нескольких миллионов.
Различаются углеводы не только молекулярной массой, но и структурой. Для крахмала характерны два вида структур макромолекул: линейная и разветвленная. Линейную структуру имеют более мелкие макромолекулы той части крахмала, которую называют амилозой, а разветвленную структуру имеют молекулы другой составной части крахмала — амилопектина.
В крахмале на долю амилозы приходится 10— 20 %, а на долю амилопектина — 80-90 %. Амилоза крахмала растворяется в горячей воде, а амилопектин только набухает.
Структурные звенья крахмала и целлюлозы построены по-разному. Если звено крахмала включает остатки α-глюкозы, то целлюлоза — остатки β-глюкозы, ориентированные в природные волокна:
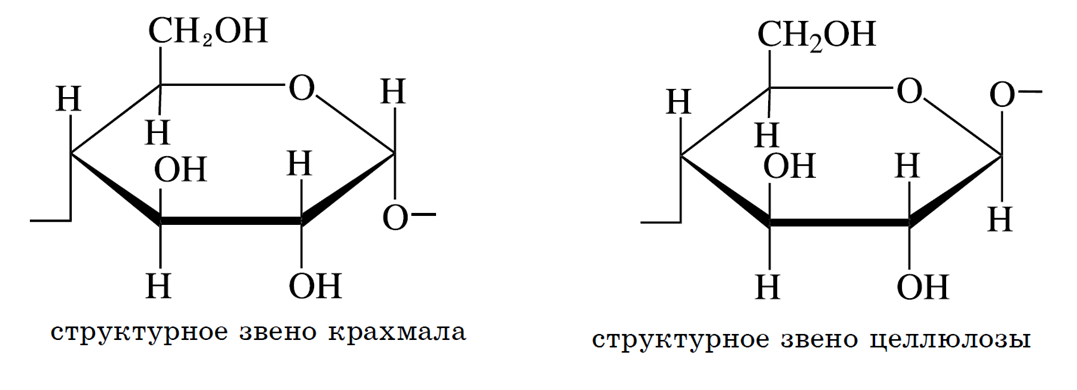
Химические свойства полисахаридов
1. Образование глюкозы. Крахмал и целлюлоза подвергаются гидролизу с образованием глюкозы в присутствии минеральных кислот, например серной:
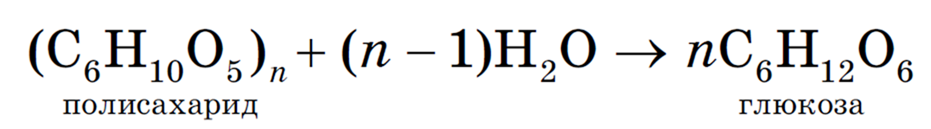
В пищеварительном тракте животных крахмал подвергается сложному ступенчатому гидролизу:
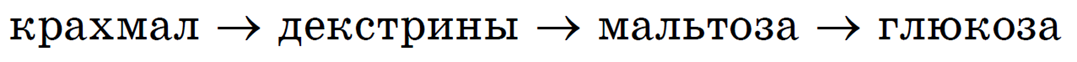
Организм человека не приспособлен к перевариванию целлюлозы, так как не имеет ферментов, необходимых для разрыва связей между остатками β-глюкозы в макромолекуле целлюлозы.
Лишь у термитов и жвачных животных (например, коров) в пищеварительной системе живут микроорганизмы, вырабатывающие необходимые для этого ферменты.
2. Образование сложных эфиров. Крахмал может образовывать эфиры за счет гидроксигрупп, однако эти эфиры не нашли практического применения.
Каждое звено целлюлозы содержит три свободных спиртовых гидроксигруппы. Поэтому общую формулу целлюлозы можно записать таким образом:
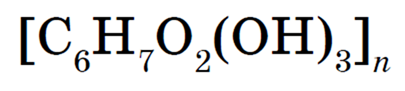
За счет этих спиртовых гидроксигрупп целлюлоза и может образовывать сложные эфиры, которые широко применяются.
При обработке целлюлозы смесью азотной и серной кислот получают в зависимости от условий моно-, ди- и тринитроцеллюлозу:
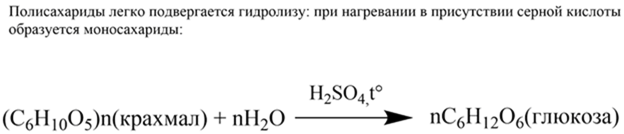
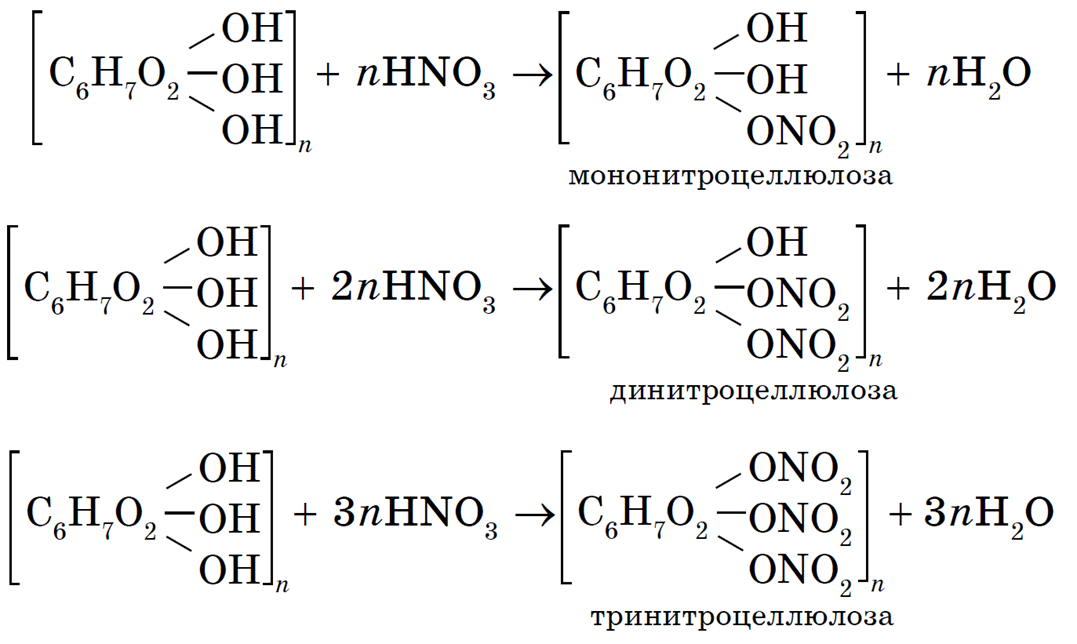
Химические свойства полисахаридов — конспект

Применение углеводов
Смесь моно- и динитроцеллюлозы называют коллоксилином. Раствор коллоксилина в смеси спирта и диэтилового эфира — коллодий — применяют в медицине для заклеивания небольших ран и для приклеивания повязок к коже.
При высыхании раствора коллоксилина и камфары в спирте получается целлулоид — одна из пластмасс, которая впервые стала широко использоваться в повседневной жизни человека (из нее делают фото- и кинопленку, а также различные предметы широкого потребления). Растворы коллоксилина в органических растворителях применяются в качестве нитролаков. А при добавлении к ним красителей получаются прочные и эстетичные нитрокраски, широко используемые в быту и технике.
Как и другие органические вещества, содержащие в составе молекул нитрогруппы, все виды нитроцеллюлозы огнеопасны. Особенно опасна в этом отношении тринитроцеллюлоза — сильнейшее взрывчатое вещество. Под названием «пироксилин» она широко применяется для производства оружейных снарядов и проведения взрывных работ, а также для получения бездымного пороха.
С уксусной кислотой (в промышленности для этих целей используют более мощное этерифицирующее вещество — уксусный ангидрид) получают аналогичные (ди- и три-) сложные эфиры целлюлозы и уксусной кислоты, которые называются ацетилцеллюлозой:
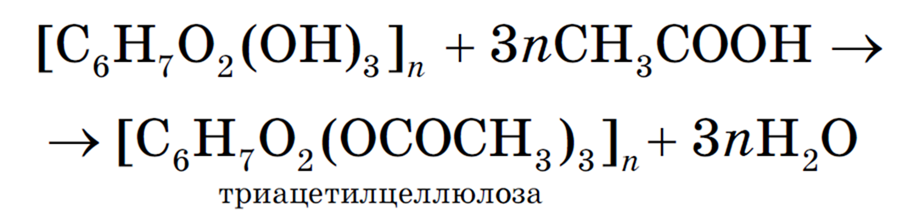
Ацетилцеллюлозу используют для получения лаков и красок, она служит также сырьем для изготовления искусственного шелка. Для этого ее растворяют в ацетоне, а затем этот раствор продавливают через тонкие отверстия фильер (металлических колпачков с многочисленными отверстиями). Вытекающие струйки раствора обдувают теплым воздухом. При этом ацетон быстро испаряется, а высыхающая ацетилцеллюлоза образует тонкие блестящие нити, которые идут на изготовление пряжи.
Крахмал, в отличие от целлюлозы, дает синее окрашивание при взаимодействии с йодом. Эта реакция является качественной на крахмал или йод в зависимости от того, наличие какого вещества требуется доказать.
Справочный материал для прохождения тестирования:

Таблица Менделеева

Таблица растворимости
