Какими свойствами обладают элементы

Электронные аналоги
Периодический закон и система Д.И. Менделеева
В 1869г. Д.И.Менделеев сформулировал периодический закон:«свойства простых веществ, а также формы и свойства соединения элементов находятся в периодической зависимости от величины их атомных весов» и создал систему, отражающую электронное строение атомов.
В 1913г. Мозли определил, что порядковый номер элемента в таблице Д.И.Менделеева численно равен заряду ядра атома. Поэтому современная формулировка периодического закона такова: «свойства химических элементов, а также форма и свойства их соединений находятся в периодической зависимости от порядкового номера элемента».
Периодические изменения в свойствах элементов связаны с периодической повторяемостью электронных структур атомов.
Порядковый номер элемента характеризует заряд ядра атома и количество электронов в оболочке. Элементы располагаются по мере увеличения заряда ядер их атомов.
Периодическая система состоит из периодов и групп. Период– это последовательный горизонтальный ряд элементов с одинаковым значением главного квантового числа. Группа – это вертикальный ряд элементов с одинаковым количеством валентных электронов. Элементы одной группы разделяются на две подгруппы: главную и побочную. В главной подгруппе объединяются элементы, у которых валентные электроны располагаются на s- и p- подуровнях внешнего квантового уровня. В побочную подгруппу – элементы, у которых валентные электроны располагаются на внешнем s- и предвнешнем d-подуровнях.
Химические элементы, у которых имеется одинаковая конфигурация валентных электронов, называются электронными аналогами.
У полных аналогов совпадают электронные конфигурации двух последних периодов.
Например: 32Ge: 1s2 2s2 2p63s2 3p6 4s2 3d10 4p2
50Sn: …………. 4s2 4p6 5s2 4d10 5p2
У неполных аналогов совпадают электронные конфигурации только последнего периода.
Например: 6C: 1s22s22p2
14Si: 1s2 2s2 2p63s2 3p6
Электронные аналоги, являющиеся химическими аналогами, характеризуются одинаковым количеством валентных электронов, которые участвуют в образовании химических связей.
Очень важной характеристикой элемента с точки зрения строения атома является радиус атома. С ростом положительного заряда ядра радиус у элементов изменяется. В периоде слева направо радиус уменьшается вследствие сжатия электронной оболочки (заряд ядра увеличивается, электроны сильнее притягиваются к ядру). В группах сверху вниз радиус увеличивается вследствие увеличения количества квантовых уровней. Чем больше радиус атома, тем слабее удерживаются валентные электроны, тем легче отдает их атом в химических реакциях. Как отдача электронов, так и принятие электронов характеризуется энергетическим эффектом, который определяется тремя видами энергии:
· энергия ионизации (J)– энергия, которая необходима для отрыва валентных электронов от атома и превращения атома в положительно заряженную частицу – ион. Она измеряется в эВ/атом или кДж/моль.
Энергия ионизации зависит от радиуса атома. С увеличением радиуса энергия ионизации уменьшается в группе сверху вниз, увеличивается в периоде с ростом количества валентных электронов. Энергия ионизации характеризует металлические (восстановительные) свойства, его активность. Чем больше величина энергии ионизации, тем меньше металлические свойства;
· энергия сродства к электрону (Е) – энергия (единицы измерения эВ/атом или кДж/моль), которая выделяется при присоединении валентных электронов к атому, при этом атом превращается в отрицательно заряженную частицу. Эта энергия характеризует неметаллические (окислительные) свойства химических элементов; в группе сверху вниз уменьшается, в периоде увеличивается;
· электроотрицательность – это полусумма энергии ионизации и энергии сродства к электрону: Э.О. = (I+E) / 2
Электроотрицательность – способность атома в молекуле притягивать к себе электроны. За единицу принята элетроотрицательность лития Li. В группе электроотрицательность уменьшается cверху вниз, в периоде увеличивается слева направо. Зная значение энергии для каждого из атомов, мы можем дать окислительно-восстановительную характеристику элемента. (Значения электроотрицательности атомов по Полингу представлены в приложении)
Ïîõîæèå ïîñòû
Ñóëüôèä æåëåçà(II) (FeS) — âåùåñòâî, êîòîðîå îáðàçóåòñÿ ïðè âçàèìîäåéñòâèè æåëåçà ñ ñåðîé. Ïðèìåíÿåòñÿ êàê ñûðüå â ïðîèçâîäñòâå ÷óãóíà, à òàêæå ÿâëÿåòñÿ òâåðäûì èñòî÷íèêîì ñåðîâîäîðîäà. Íà ôîòîãðàôèÿõ ìîæíî çàìåòèòü ÷àñòèöû ìåòàëëè÷åñêîãî æåëåçà, êîòîðîå íå ïðîðåàãèðîâàëî ñ ñåðîé.
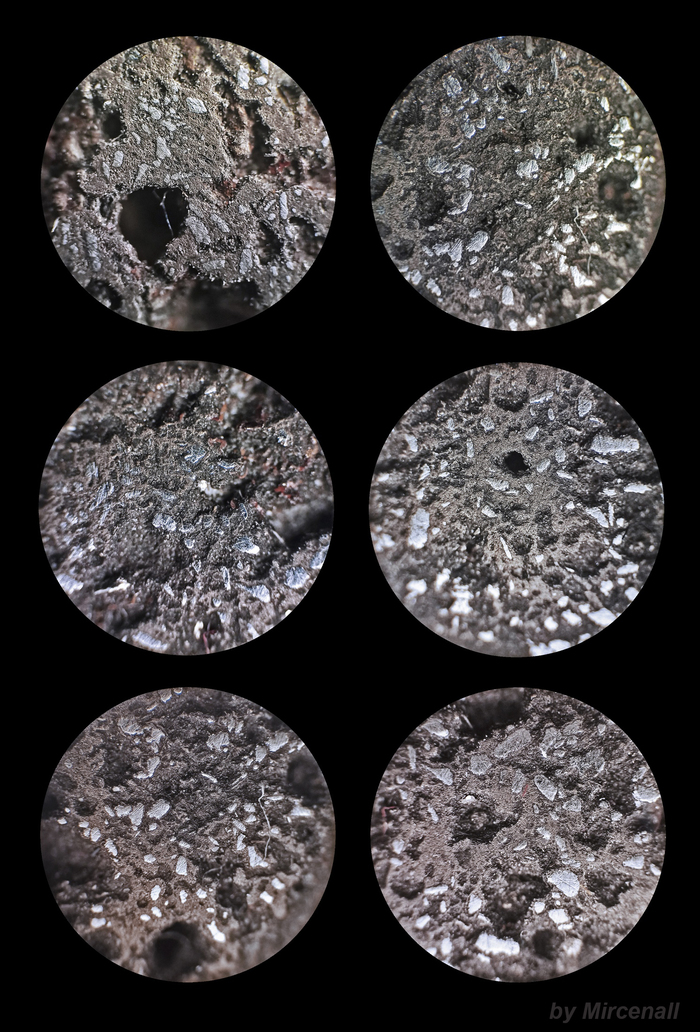
 ïðèðîäå ñóëüôèä æåëåçà(II) âñòðå÷àåòñÿ êðàéíå ðåäêî, îäíàêî ðàñïðîñòðàí¸í äèñóëüôèä æåëåçà(II) (FeS2), èçâåñòíûé êàê ìèíåðàë ïèðèò èëè ñåðíûé êîë÷åäàí.
vk.com/mircenall

Ïîêàçàòü ïîëíîñòüþ
3
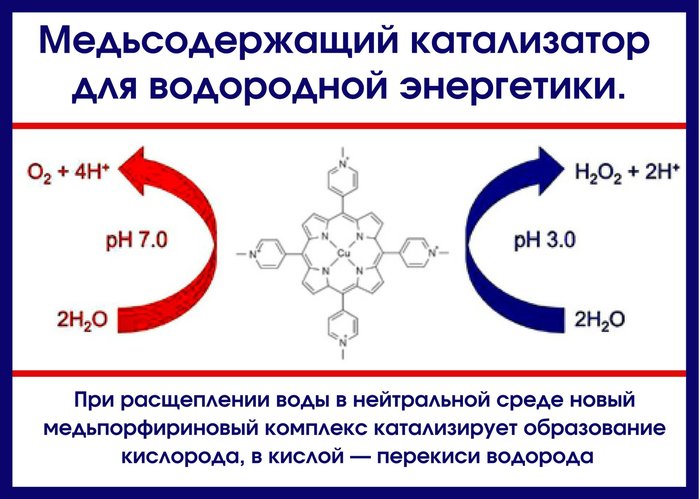
Íîâûé ìåäüñîäåðæàùèé êîìïëåêñ, èäåþ ñòðîåíèÿ êîòîðîãî ïîäñêàçàëà ïðèðîäà, ýôôåêòèâíî ðàñùåïëÿåò âîäó â íåéòðàëüíîé ñðåäå. Ýòî îòêðûòèå ìîæåò ñäåëàòü áîëåå äîñòóïíûì ïîëó÷åíèå âîäîðîäà ñ ïîìîùüþ âîññòàíîâëåíèÿ âîäû.
Ìîëåêóëÿðíûé âîäîðîä äàâíî ðàññìàòðèâàþò êàê àëüòåðíàòèâó íåôòè è ãàçó. Åäèíñòâåííûé ïðîäóêò ñãîðàíèÿ âîäîðîäà âîäà, êîòîðàÿ ñàìà ìîæåò áûòü èñòî÷íèêîì âîäîðîäà. Ìíîãèå èññëåäîâàòåëüñêèå ãðóïïû ïî âñåìó ìèðó ñòàðàþòñÿ ðàçðàáîòàòü êàòàëèçàòîðû, ñïîñîáíûå ïîíèçèòü ýíåðãèþ âîññòàíîâëåíèÿ âîäû äî ìîëåêóëÿðíîãî âîäîðîäà è îáëåã÷èòü ïðîòåêàíèå ýòîé ðåàêöèè. Íàèáîëåå ýôôåêòèâíûå êàòàëèçàòîðû ðàñùåïëåíèÿ âîäû â íàñòîÿùåå âðåìÿ êîîðäèíàöèîííûå ñîåäèíåíèÿ ðóòåíèÿ è èðèäèÿ. Ê íåäîñòàòêàì îáîèõ ìåòàëëîâ ìîæíî îòíåñòè èõ íèçêèå êîíöåíòðàöèè â çåìíîé êîðå è âûñîêóþ ñòîèìîñòü.
Íîâîå èññëåäîâàíèå äåìîíñòðèðóåò, ÷òî â ïðèñóòñòâèè ïîðôèðèíîâîãî êîìïëåêñà ìåäè ýëåêòðîêàòàëèòè÷åñêîå ðàñùåïëåíèå âîäû ïðîèñõîäèò ïðè íåéòðàëüíûõ çíà÷åíèÿõ ðÍ è ïðè íèçêîì çíà÷åíèè ýëåêòðîäíîãî ïîòåíöèàëà. Ïðè 310 ì è ðÍ 7 âîäà îêèñëÿåòñÿ ñ âûäåëåíèåì ìîëåêóëÿðíîãî êèñëîðîäà, à â êèñëîé ñðåäå (ïðè òîì æå ýëåêòðîäíîì ïîòåíöèàëå) äî ïåðåêèñè âîäîðîäà. Õîòÿ ìåäíûé êîìïëåêñ è íå ïðåâîñõîäèò ïî ïðîèçâîäèòåëüíîñòè êîìïëåêñû áëàãîðîäíûõ ìåòàëëîâ, âñå æå ýòî áîëüøîé øàã âïåðåä ìåíüøàÿ ýôôåêòèâíîñòü ïðîèçâîäíûõ ìåäè êîìïåíñèðóåòñÿ åå áîëüøåé ðàñïðîñòðàíåííîñòüþ è äåøåâèçíîé. Êàòàëèçàòîðû ðàñùåïëåíèÿ âîäû íà îñíîâå ìåäè áûëè èçâåñòíû è ðàíåå, íî îíè ðàáîòàëè â ñèëüíîùåëî÷íîé ñðåäå è ïðè áîëüøîì çíà÷åíèè ýëåêòðîäíîãî ïîòåíöèàëà.
Èññëåäîâàòåëè èñõîäèëè èç òîãî, ÷òî â ïðîöåññå ôîòîñèíòåçà êëþ÷åâóþ ðîëü â îêèñëåíèè âîäû è âûäåëåíèè êèñëîðîäà èãðàåò ìàãíèéïîðôèðèíîâûé êîìïëåêñ. Òåì íå ìåíåå ñïîñîáíîñòü ìåäüïîðôèðèíîâîãî êîìïëåêñà êàòàëèçèðîâàòü îêèñëåíèå âîäû îêàçàëàñü ïðèÿòíîé íåîæèäàííîñòüþ äëÿ ìíîãèõ õèìèêîâ êàê ñïåöèàëèñòîâ ïî õèìèè ïîðôèðèíîâûõ êîìïëåêñîâ, òàê è òåõ, êòî çàíèìàëñÿ ðàñùåïëåíèåì âîäû. Åùå îäíà íåîáû÷íàÿ ÷åðòà ýòîãî êàòàëèçàòîðà îêèñëåíèå âîäû äî ïåðåêèñè âîäîðîäà ïðè íèçêèõ çíà÷åíèÿõ ðÍ. Ýòîò ïðîöåññ íå ñòîèò ðàññìàòðèâàòü êàê íîâûé ñïîñîá ïîëó÷åíèÿ H2O2, è âñå æå îí òðåáóåò âíèìàíèÿ. Óñòàíîâèâ, êàê îáðàçóåòñÿ ïåðåêèñü âîäîðîäà, èññëåäîâàòåëè ñìîãóò îïðåäåëèòü ìåõàíèçì ýòîé êàòàëèòè÷åñêîé ðåàêöèè è âûÿñíèòü, êàê ïîâûñèòü ýôôåêòèâíîñòü ðàñùåïëåíèÿ âîäû.

Ïîêàçàòü ïîëíîñòüþ
3
 îäíîì èç ïîñòîâ îá îëîâå ïèêàáóøíèêîâ çàèíòåðåñîâàëà òàêàÿ äåòàëü — ïðè òåìïåðàòóðå íèæå 13.2°C êîâêîå è ïëàñòè÷íîå îëîâî ïåðåõîäèò â äðóãóþ «ñåðóþ» àëëîòðîïíóþ ìîäèôèêàöèþ.
Ïðè ýòîì ïåðåõîä ñîïðîâîæäàåòñÿ óâåëè÷åíèåì îáúåìà íà 25,6 %, â ñâÿçè ñ ÷åì âîçíèê âîïðîñ
Ñîáñòâåííî ýòî ÿ è ðåøèë ïðîâåðèòü.
Ïåðâûì äåëîì íàøåë â ëàáîðàòîðèè ÷èñòîå îëîâî (ïðîâîëîêà ïðèïîÿ íå ïîäîéäåò, èáî îíà ñîäåðæèò ñâèíåö, êîòîðûé êàê ðàç òàêè ïðåäîòâðàùàåò ðàçðóøåíèå). Îëîâî õðàíèòñÿ â âèäå ìàëåíüêèõ ãðàíóë, íî ÿ ïåðåïëàâèë åãî â êóñîê ïîáîëüøå.

Äåëàòü èäåàëüíóþ äåðåâÿííóþ êîðîáêó áûëî áû ñëèøêîì äîëãî, òàê ÷òî ðåøèë çàëèòü êóñîê ìåòàëëà â ãèïñ è âûñòàâèòü íà ìîðîç íà äîëãîå âðåìÿ â çàêðûòîé êîðîáêå.


Êðîìå òîãî, ÷åì íèæå òåìïåðàòóðà, òåì áûñòðåå îñóùåñòâëÿåòñÿ ïåðåõîä (íàèáîëåå áûñòðîå ïðåâðàùåíèå íàáëþäàåòñÿ ïðè òåìïåðàòóðå íèæå -33°C). Ïîñêîëüêó íà÷àëî çèìû â ñòîëèöå âûäàëîñü òåïëûì, ÿ ðåøèë ïðîâîäèòü ýòîò ýêñïåðèìåíò ñ ñåðåäèíû ÿíâàðÿ. Ãèïñîâûé ñëåïîê ñ îëîâîì ÿ ïîëîæèë â êîðîáêó (äàáû çàùèòèòü åãî îò âîäû) è îñòàâèë íà ïîäîêîííèêå, ðåøèâ îòêðûòü ñïóñòÿ ìåñÿö.

×åðåç ìåñÿö ôîðìà îñòàëàñü ëåæàòü, êàê ëåæàëà. Îäíàêî êàê ðàç ñ ñåðåäèíû ôåâðàëÿ óäàðèëè ñèëüíûå ìîðîçû è ïðîöåññ äîëæåí áûë óñêîðèòüñÿ (òåì âðåìåíåì ïèêàáó íà÷àëî íàïîìèíàòü î ñåáå)

Îòêðûâ êîðîáêó óæå â ìàðòå, ÿ óâèäåë æåëàííîå èçìåíåíèå — òðåùèíó, ðàçäåëèâøóþ ñëåïîê íà äâå ïîëîâèíû!

Àêêóðàòíî äîñòàâ åãî, ÿ ðàçäåëèë ïîëîâèíêè ôîðìû è îòòóäà ïîñûïàëñÿ òåìíûé ïîðîøîê ñ ìåòàëëè÷åñêèì áëåñêîì (è îñòàòîê êóñêà áåëîãî îëîâà, ïîâåðõíîñòü êîòîðîãî áûëà òàêæå âñÿ â ñåðîé ìîäèôèêàöèè ).  êîíöå êîíöîâ îíî-òàêè ðàçîðâàëî ãèïñ.

Ñåðîå îëîâî ñêîðåå ïîõîæå íà ãðàôèò ñ áëåñêîì ñâèíöà, ÷åì íà ìåòàëë. ×òîáû íàãëÿäíî ïðîäåìîíñòðèðîâàòü îòëè÷èå, ÿ âûñûïàë ðÿäîì ïîðîøîê áåëîãî îëîâà è ïîëó÷åííîå ñåðîå. Îäíàêî âåðíóòü åìó èñõîäíîå ñîñòîÿíèå íå ñîñòàâëÿåò òðóäà — òðåáóåòñÿ ëèøü ðàñïëàâèòü α-îëîâî è ñëèòîê ñíîâà áóäåò ÿâëÿòüñÿ áåëûì β-îëîâîì

Òàêèì îáðàçîì ïðåäïîëîæåíèå î ðàçðûâàþùåì êîíòåéíåðå îëîâå ïîäòâåðæäåíî

P.S. îòäåëüíàÿ áëàãîäàðíîñòü ñåäüìîé ïàðòèè ãðàíóëèðîâàííîãî îëîâà Óðàëüñêîãî çàâîäà õèìðåàêòèâîâ îò íîÿáðÿ 1977 ãîäà. Èíà÷å áû ýêñïåðèìåíò íå ñîñòîÿëñÿ.


Ïîêàçàòü ïîëíîñòüþ
12
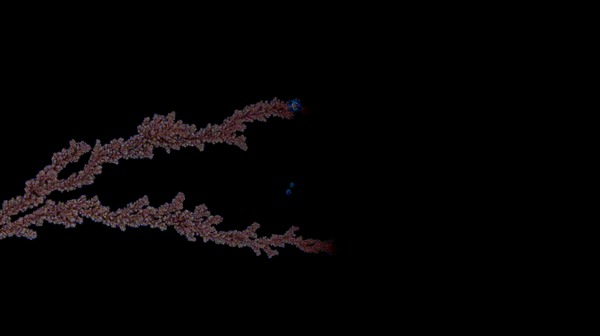
Êðèñòàëëû ñåðåáðà íà ìåäè.

Ñåðåáðî âûäåëÿåòñÿ íà òðåóãîëüíûõ ìåäíûõ ïëàñòèíêàõ, ïîãðóæåííûõ â ðàñòâîð íèòðàòà ñåðåáðà

Ìåäü
Öèíê

Ñåðåáðî

Îëîâî

Ñâèíåö

Ïîêàçàòü ïîëíîñòüþ
2
Îáðàçîâàíèå êðèñòàëëîâ îëîâà ïðè ýëåêòðîëèçå ðàñòâîðà õëîðèäà îëîâà â ñåðíîé êèñëîòå

Îáðàçîâàíèå îëîâÿííûõ êðèñòàëëîâ ïîä ìèêðîñêîïîì
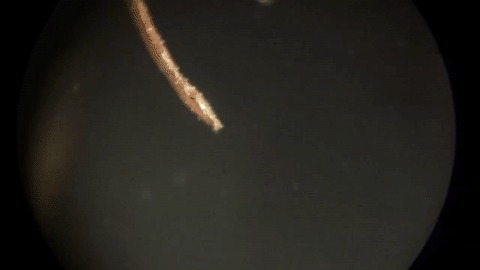
Îáðàçîâàíèå îëîâÿííûõ êðèñòàëëîâ ïðè íèçêîé êîíöåíòðàöèè õëîðèäà îëîâà è ìàëûõ îáúåìàõ ðàñòâîðà (òàêæå óâåëè÷åíî)

Ðåàêöèÿ îëîâà ñ àçîòíîé êèñëîòîé

Ðåàêöèÿ îëîâà ñ ñîëÿíîé êèñëîòîé

Ðåàêöèÿ îëîâà ñ öàðñêîé âîäêîé (ñìåñü àçîòíîé è ñîëÿíîé êèñëîòû) ïðîòåêàåò, îäíàêî, áîëåå áóðíî

«Îëîâÿííàÿ ÷óìà» — îñîáîå ñâîéñòâî ýëåìåíòà, êîòîðîå çàêëþ÷àåòñÿ â òîì, ÷òî ïðè òåìïåðàòóðå íèæå 13,2 °C ìåòàëëè÷åñêîå (áåëîå) îëîâî (β-Sn) ïåðåõîäèò â äðóãîå ôàçîâîå ñîñòîÿíèå ñåðîå îëîâî (α-Sn), â êðèñòàëëè÷åñêîé ðåø¸òêå êîòîðîãî àòîìû ðàñïîëàãàþòñÿ ìåíåå ïëîòíî. Ïðîèñõîäèò ýòî ïðî ïðè÷èíå óâåëè÷åíèÿ óäåëüíîãî îáú¸ìà ÷èñòîãî îëîâà íà 25,6 %
Îëîâî èìååò íåáîëüøóþ òåìïåðàòóðó ïëàâëåíèÿ (232 °C) è ëåãêî ïåðåõîäèò â æèäêîå ñîñòîÿíèå ïîä äåéñòâèåì ïëàìåíè ãîðåëêè

Ãîðåíèå ìàëåíüêîãî êóñî÷êà îëîâà (ìîìåíòàëüíîå îêèñëåíèå)

Ïîêàçàòü ïîëíîñòüþ
6

Ðîñò êðèñòàëëîâ ñåðåáðà íà ìåäíîé ïðîâîëîêå (â ðàñòâîðå íèòðàòà ñåðåáðà)

Ðåàêöèÿ ñåðåáðà ñ àçîòíîé êèñëîòîé (ñ âûäåëåíèåì äèîêñèäà àçîòà)

Îáðàçîâàíèå õëîðèäà ñåðåáðà

Ðåàêöèÿ «Ñåðåáðÿíîå çåðêàëî» (â ïðèñóòñòâèè àëüäåãèäîâ èäåò âîññòàíîâëåíèå ìåòàëëà èç àììèà÷íîãî êîìïëåêñà)

Îáðàçîâàíèå ñóëüôèäà ñåðåáðà ïðè äîáàâëåíèè òèîñóëüôàòà

Îáðàçîâàíèå õðîìàòà ñåðåáðà

Âçðûâ îò íàãðåâàíèÿ àöåòèëåíèäà ñåðåáðà

Îáðàçîâàíèå áðîìèäà è èîäèäà ñåðåáðà

Ñåðåáðî ìîæíî ðàñïëàâèòü õîðîøåé ãàçîâîé ãîðåëêîé

Ïîêàçàòü ïîëíîñòüþ
6
Ðåàêöèÿ ñìåñè æåëåçà è ñåðû îò íàãðåòîé ïàëî÷êè (îáðàçîâàíèå ñóëüôèäà)

Îáðàçîâàíèå ñèëèêàòà æåëåçà, ïðè äîáàâëåíèè õëîðèäà ê ðàñòâîðó ñèëèêàòà íàòðèÿ
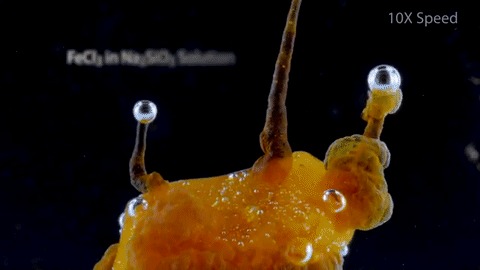
Îáðàçîâàíèå êðàñèòåëÿ «Áåðëèíñêàÿ ëàçóðü» ( äîáàâëåíèå êðàñíîé êðîâÿíîé ñîëè ê ðàñòâîðó æåëåçà 2+)

Ðåàêöèÿ «Êðîâàâîå æåëåçî» (æåëåçíàÿ ïðîâîëîêà â ðàñòâîðå òèîöèàíàòà êàëèÿ, ïåðåêèñè è õëîðîâîäîðîäà)

Ãîðåíèå ñòàëüíîé âàòû

Ãîðåíèå ñòàëüíîé âàòû ïîä óâåëè÷åíèåì
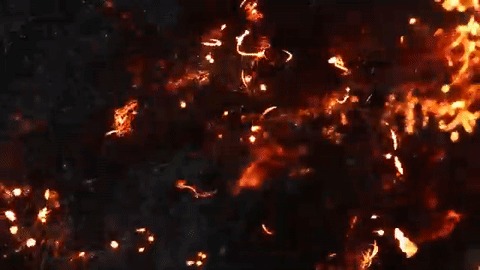
Ðåàêöèÿ ãîðÿùåé ñòàëüíîé âàòû ñ õëîðîì è îáðàçîâàíèå õëîðèäà æåëåçà III

Ãîðåíèå ïèðîôîðíîãî æåëåçà (ìåëêîäèñïåðñíûé ïîðîøîê æåëåçà, êîòîðûé ñàìîâîçãîðàåòñÿ îò êèñëîðîäà âîçäóõà)

Òåðìèòíàÿ ñìåñü îêñèäà æåëåçà III è àëþìèíèÿ

Îõëàæäåíèå ñòàëè íà ïðîèçâîäñòâå

Ïîêàçàòü ïîëíîñòüþ
7
Íàãðåâàíèå è ãîðåíèå ëèòèÿ

Êîððîäèðîâàíèå è ïëàâëåíèå ëèòèÿ íà âîçäóõå ïðè íàãðåâàíèè

Ðåàêöèÿ ëèòèÿ ñ äðåâåñèíîé (âîäîé, çàêëþ÷åííîé â å¸ ñòðóêòóðå)

Ðåàêöèÿ ëèòèÿ ñ àçîòíîé êèñëîòîé

Ëèòèé â âèäå ëåíòû â ëèòèåâûõ áàòàðåéêàõ

Ðåàêöèÿ ëèòèåâîé ëåíòû ñ âîäîé

Ëèòèåâàÿ ëåíòà ñ âîäîé ïðè áîëüøèõ îáüåìàõ

Ðàçðóøåíèå ôàðôîðà â ñëåäñòâèè âûñîêîé òåìïåðàòóðû ãîðåíèÿ ëèòèÿ (áîëåå 2300 Ñ)

Àíàëîãè÷íàÿ òåìïåðàòóðà ìîæåò ðàñïëàâèòü è ñòàëü

Ãîðåíèå ìàòåðèàëà, ïðîïèòàííîãî ñîëÿìè ëèòèÿ
Ïîêàçàòü ïîëíîñòüþ
7

Ïîêàçàòü ïîëíîñòüþ
1

Ìíîãèå ìîãóò äóìàòü, ÷òî æåëåçî ìîæåò îðãàíèçîâûâàòü òîëüêî íåêàçèñòûå ÷åðíûå êàìíè, åäâà îòëè÷èìûå îò çåìëè. Íî ñóùåñòâóþò ìèíåðàëû âåëèêîëåïíîãî âèäà, áëàãîäàðÿ ñîäåðæàíèþ âíóòðè êðèñòàëëè÷åñêîé ðåøåòêè èîíîâ æåëåçà.

Äåñÿòêà ñàìûõ êðàñèâûõ ìèíåðàëîâ æåëåçà:
Àëüìàíäèí Al2Fe3(SiO4)3, ñàìàÿ òâ¸ðäàÿ ðàçíîâèäíîñòü ãðàíàòîâ. ßâëÿåòñÿ Äðàãîöåííûì êàìíåì 4 êàòåãîðèè.

Àíàïàèò Ca2Fe[PO4]2·4H2O, ðåäêèé ìèíåðàë ñ Êðàñíîäàðñêîãî Êðàÿ

Âåçóâèàí (Mg,Fe)2Ca10Al4[OH4(SiO4)5(Si2O7)2], íàéäåí â ëàâå Âåçóâèÿ, îòëè÷àåòñÿ êðàéíå íèçêèì äâóïðåëîìëåíèåì

Ãóìèò (Mg,Fe)7(SiO4)3(F,OH)2, ðåäêèé ìèíåðàë, òàêæå íàéäåííûé â ëàâå Âåçóâèÿ, íî òîëüêî â 19 âåêå.



