Какими свойствами обладают аминокислоты напишите
Аминокислоты – органические бифункциональные соединения, в состав которых входят карбоксильные группы –СООН и аминогруппы –NH2.
Природные аминокислоты можно разделить на следующие основные группы:
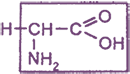
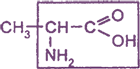
| 1) Алифатические предельные аминокислоты (глицин, аланин) | NH2-CH2-COOH глицин NH2-CH(CH3)-COOH аланин |
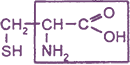
| 2) Серосодержащие аминокислоты (цистеин) |  цистеин |
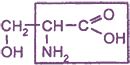
| 3) Аминокислоты с алифатической гидроксильной группой (серин) | NH2-CH(CH2OH)-COOH серин |
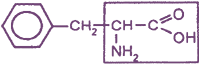
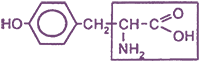
| 4) Ароматические аминокислоты (фенилаланин, тирозин) |  фенилаланин
тирозин |
| 5) Аминокислоты с двумя карбоксильными группами (глутаминовая кислота) | HOOC-CH(NH2)-CH2-CH2-COOH глутаминовая кислота |
| 6) Аминокислоты с двумя аминогруппами (лизин) | CH2(NH2)-CH2-CH2-CH2-CH(NH2)-COOH лизин |
- Для природных α-аминокислот R-CH(NH2)COOH применяются тривиальные названия: глицин, аланин, серин и т. д.
- По систематической номенклатуре названия аминокислот образуются из названий соответствующих кислот прибавлением приставки амино- и указанием места расположения аминогруппы по отношению к карбоксильной группе:
- Часто используется также другой способ построения названий аминокислот, согласно которому к тривиальному названию карбоновой кислоты добавляется приставка амино- с указанием положения аминогруппы буквой греческого алфавита.
Аминокислоты – твердые кристаллические вещества с высокой температурой плавления. Хорошо растворимы в воде, водные растворы хорошо проводят электрический ток.
- Замещение галогена на аминогруппу в соответствующих галогензамещенных кислотах:

- Восстановление нитрозамещенных карбоновых кислот (применяется для получения ароматических аминокислот):

При растворении аминокислот в воде карбоксильная группа отщепляет ион водорода, который может присоединиться к аминогруппе. При этом образуется внутренняя соль, молекула которой представляет собой биполярный ион:
![]()
1. Кислотно-основные свойства аминокислот
Аминокислоты — это амфотерные соединения.
Они содержат в составе молекулы две функциональные группы противоположного характера: аминогруппу с основными свойствами и карбоксильную группу с кислотными свойствами.
Водные растворы аминокислот имеют нейтральную, щелочную или кислую среду в зависимости от количества функциональных групп.
Так, глутаминовая кислота образует кислый раствор (две группы -СООН, одна -NH2), лизин — щелочной (одна группа -СООН, две -NH2).
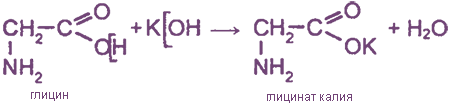
1.1. Взаимодействие с металлами и щелочами
Как кислоты (по карбоксильной группе), аминокислоты могут реагировать с металлами, щелочами, образуя соли:

1.2. Взаимодействие с кислотами
По аминогруппе аминокислоты реагируют с основаниями:

2. Взаимодействие с азотистой кислотой
Аминокислоты способны реагировать с азотистой кислотой.
Например, глицин взаимодействует с азотистой кислотой:
![]()
3. Взаимодействие с аминами
Аминокислоты способны реагировать с аминами, образуя соли или амиды.
![]()
4. Этерификация
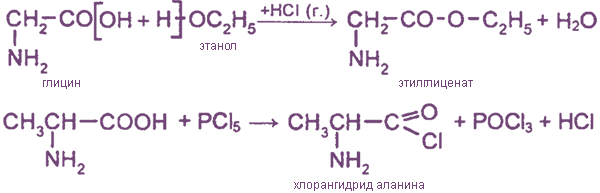
Аминокислоты могут реагировать со спиртами в присутствии газообразного хлороводорода, превращаясь в сложный эфир:
Например, глицин взаимодействует с этиловым спиртом:
![]()
5. Декарбоксилирование
Протекает при нагревании аминокислот с щелочами или при нагревании.
Например, глицин взаимодействует с гидроксидом бария при нагревании:
![]()
Например, глицин разлагается при нагревании:
![]()
6. Межмолекулярное взаимодействие аминокислот
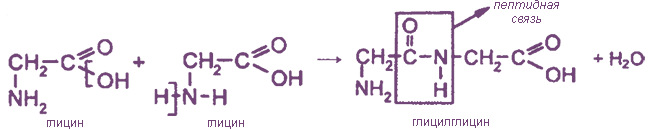
При взаимодействии аминокислот образуются пептиды. При взаимодействии двух α-аминокислот образуется дипептид.
Например, глицин реагирует с аланином с образованием дипептида (глицилаланин):

Фрагменты молекул аминокислот, образующие пептидную цепь, называются аминокислотными остатками, а связь CO–NH — пептидной связью.
Благодаря способности аминокислот к поликонденсации образуются полиамиды – белки, пептиды, а также энант, капрон и нейлон. При поликонденсации ɛ-аминокапроновой кислоты получается полимер капрон. Из капроновой смолы получают не только волокна, но и пластмассовые изделия.
Энант, капрон и нейлон применяются в промышленности при производстве корда, прочных тканей, сетей, канатов, веревок, трикотажных и чулочных изделий.
Аминокислоты широко применяются в медицинской практике в качестве лекарственных средств.
Аминокислоты прописываются при сильном истощении, после тяжелых операций, их используют для питания больных.
Из полиаминокислот получают хороший материал для хирургии.
Аргинин в сочетании с аспартатом или глутаматом помогает при заболевании печени.
Аспарагиновая кислота способствует повышению потребления кислорода сердечной мышцей. В кардиологии применяют панангин – препарат, содержащий аспартат калия и аспартат магния. Панангин применяют для лечения различного рода аритмий, а также ишемической болезни сердца.
В медицинских учреждениях аминокислоты применяются в качестве парентерального питания пациентов с заболеваниями желудочно-кишечного тракта (язва желудка), при лечении болезней печени, ожогов, малокровия, при нервно-психических заболеваниях.
Глутаминовая кислота используется в детской психиатрии для лечения слабоумия и последствий родовых травм, при нарушениях мозгового кровообращения после инсульта, при атеросклерозе мозговых сосудов, потере памяти.
Гистидин иногда применяют для лечения больных гепатитами, язвенной болезнью желудка и двенадцатиперстной кишки.
Глицин является медиатором торможения в ЦНС. В медицинской практике применяется для лечения алкоголизма. Производное глицина – бетаин улучшает процессы пищеварения.
Метионин и его активные производные используются в лечении и профилактике болезней печени. Метионин защищает организм при отравлении бактериальными эндотоксинами и некоторыми другими ядами, в связи с этим используется для защиты организма от токсикантов окружающей среды.
Некоторые аминокислоты используются в качестве самостоятельных лекарственных средств (аргинин, цистеин, ароматические аминокислоты).
Аминокислоты в сельском хозяйстве применяются преимущественно в качестве кормовых добавок. Многие растительные белки содержат недостаточное количество белков. Лизин, лейцин, метионин, треонин, триптофан добавляют в корма сельскохозяйственных животных.
Аминокислоты метионин, глутаминовая кислота и валин применяются для защиты растений от болезней, а аланин и глицин, обладающий гербицидным действием, используется для борьбы с сорняками.
Аминокислоты используются в микробиологической промышленности для приготовления культуральных сред и как реактивы.
В пищевой промышленности аминокислоты применяются в качестве вкусовых добавок.
Наиболее важны добавки лизина, триптофана и метионина к пищевым продуктам, неполноценным по содержанию этих аминокислот.
Добавка глутаминовой кислоты и ее солей к ряду продуктов придает им приятный мясной вкус, что часто используют в пищевой промышленности.
Натриевая соль глутаминовой кислоты (глутамат натрия) известна как «пищевая добавка E621» или «усилитель вкуса».
Глутаминовая кислота является важным компонентом при замораживании и консервировании.
Благодаря присутствию глицина, метионина и валина, во время термической обработки продуктов питания удается получить специфические ароматы хлебобулочных и мясных изделий.
Аминокислоты цистеин, лизин и глицин используются в качестве антиоксидантов, стабилизирующих ряд витаминов, например аскорбиновую кислоту; замедляющих пероксидное окисление липидов.
Глицин применяется при производстве безалкогольных напитков и приправ.
Аминокислоты также являются компонентами спортивного питания (в изготовлении которого применяется, как правило, валин, лейцин, изолейцин, аланин, лизин, аргинин и глутамин), использующегося спортсменами, а также людьми, занимающимися бодибилдингом, фитнесом.
В химической промышленности введение в такие аминокислоты, как глутаминовая или аспарагиновая кислоты, гидрофобных группировок дает возможность получать поверхностно-активные вещества (ПАВ), широко используемые в синтезе полимеров, а также при производстве моющих средств, эмульгаторов, добавок к моторному топливу.

Аминокислоты
Аминокислоты
Аминокислоты — соединения, которые содержат в молекуле одновременно аминогруппу и карбоксильную группу.
Классификация
— моноаминомонокарбоновые кислоты
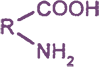
простейший представитель:
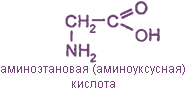
— моноаминодикарбоновые кислоты

Например:
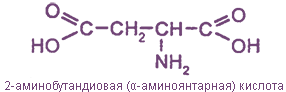
— диаминомонокарбоновые кислоты
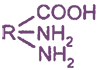
Например:
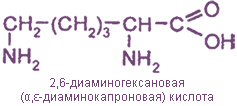
-α-аминокислоты
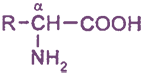
— β-аминокислоты
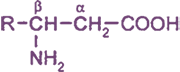
— γ-аминокислоты
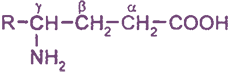
Формулы и названия некоторых α-аминокислот, остатки которых входят в состав белков
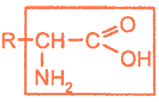
Белки представляют собой природные полимеры, макромолекулы которых построены из большого числа остатков 20 различных α-аминокислот. В биохимии для аминокислот используют, как правило, короткие тривиальные названия и трехбуквенные обозначения.
Моноаминомонокарбоновые кислоты
| Аминоэтановая, или аминоуксусная кислота, или глицин (гликокол) | Gly (Гли) |
| 2-аминопропановая, или α-аминопропионовая кислота, или аланин | Ala (Ала) |
| 2-амино-З-гидроксипропановая, или | Ser (Сер) |
| 2-амино-З-меркаптопропановая кислота, или β-меркаптоаланин, или цистеин | Cys (Цис) |
| 2-амино-З-фенилпропановая кислота, или β-фенилаланин, или фенилаланин | Phe (Фен) |
| 2-амино-3-(4-гидроксифенил)-пропановая кислота, или β-(n-гидроксифенип)-апанин, или тирозин | Tyr (тир) |
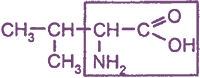
| 2-амино-З-метилбутановая, или α-аминоизовалериановая кислота, или валин | Val (Вал) |
Моноаминодикарбоновые кислоты
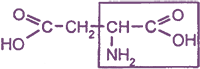 | (2-)аминобутандиовая, или аминоянтарная кислота, или аспарагиновая кислота | Asp (Асп) |
| α-аминоглутаровая кислота, или глутаминовая кислота | Glu (Глу) |
Диаминомонокарбоновая кислота
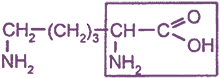 | 2,6-диаминогексановая, или α,ε-диаминокапроновая кислота, или лизин | Lys (Лиз) |
Классификация природных аминокислот
I. Заменимые аминокислоты — могут синтезироваться в организме человека. К ним среди вышеперечисленных относятся: глицин, аланин, серин, цистеин, тирозин, аспарагиновая и глутаминовая кислоты.
II. Незаменимые аминокислоты — не могут синтезироваться в организме человека, должны поступать в организм в составе белков пищи. Фенилаланин, валин, лизин — представители незаменимых аминокислот.
Физические свойства
Большинство аминокислот — бесцветные кристаллические вещества, хорошо растворимые в воде. Многие аминокислоты имеют сладкий вкус. Температуры плавления разных аминокислот лежат в пределах 230-300°C.
Химические свойства
Аминокислоты являются амфотерными соединениями, что обусловлено наличием в их молекулах функциональных групп кислотного (-СООН) и основного (-NH2) характера.
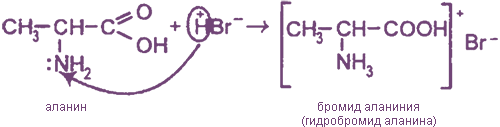
В водных растворах аминокислоты существуют в виде равновесных смесей молекул и биполярных ионов, которые в кислой среде переходят в катионную форму, а в щелочной среде — в анионную форму.
а) Моноаминомонокарбоновые кислоты
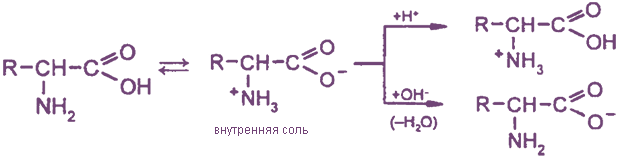
При образовании внутренних солей моноаминомонокарбоновых кислот характер среды не изменяется. Поэтому эти аминокислоты называются нейтральными. Суммарный заряд внутренних солей таких кислот равен нулю.
При добавлении кислоты (Н+) карбоксилат-ион протонируется и остается только положительный заряд на группе -NH. В щелочной среде (ОН-) аминогруппа депротонируется и остается отрицательный заряд на карбоксилат-ионе.
б) Моноаминодикарбоновые кислоты
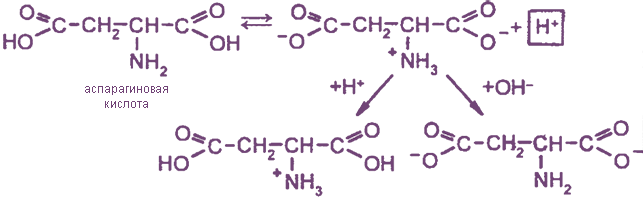
При образовании внутренних солей моноаминодикарбоновых кислот образуется избыток ионов водорода, поэтому водные растворы этих кислот имеют рН Суммарный заряд внутренних солей кислых аминокислот отрицательный.
в) Диаминомонокарбоновые кислоты
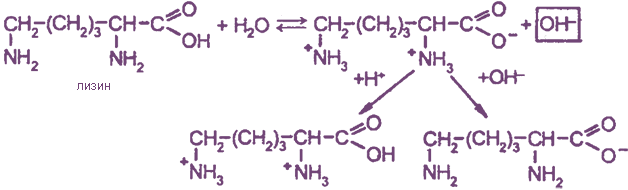
При образовании внутренних солей диаминомонокарбоновых кислот образуется избыток гидроксид-ионов, поэтому их водные растворы имеют рН > 7. Такие аминокислоты называются основными. Суммарный заряд внутренних солей основных аминокислот положительный.
При взаимодействии карбоксильной группы одной молекулы аминокислоты и аминогруппы другой молекулы аминокислоты образуются дипептиды:
При взаимодействии двух разных аминокислот образуется смесь четырех дипептидов; например:
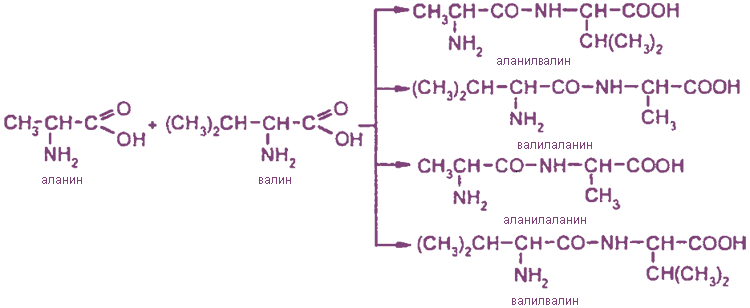
Дипептид, присоединяя еще одну молекулу аминокислоты, может образовать трипептид. Аналогично из трипептида можно получить тетрапептид и т. д.
Как и карбоновые кислоты, аминокислоты могут образовывать сложные эфиры, хлорангидриды и др. Например:

6. Поликонденсация ε-аминокапроновой кислоты
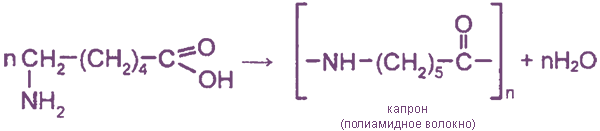
Способы получения
1. Аммонолиз α-галогенкарбоновых кислот
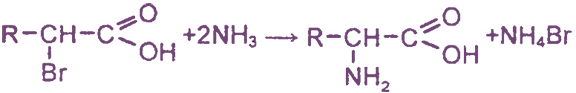
2. Гидролиз белков
![]()
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 5 сентября 2018;
проверки требует 61 правка.
21 протеиногенная α-аминокислота эукариот, сгруппированные согласно радикалам.
Незаменимые аминокислоты — необходимые аминокислоты, которые не могут быть синтезированы в том или ином организме. Для разных видов организмов список незаменимых аминокислот различен. Все белки, синтезируемые организмом, собираются в клетках из 20 базовых аминокислот, только часть из которых может синтезироваться организмом. Невозможность сборки определённого белка организмом приводит к нарушению его нормальной работы, поэтому необходимо поступление незаменимых аминокислот в организм с пищей.
[1]
Незаменимыми для взрослого здорового человека являются 8 аминокислот: валин, изолейцин, лейцин, лизин, метионин, треонин, триптофан и фенилаланин; также часто к незаменимым относят гистидин[2][3]; (F V T W M L I K H). Для детей также незаменимым является аргинин.
6 других аминокислот (R C G Q P Y) считаются условно незаменимыми в питании человека, что означает ограниченные возможности их синтеза в зависимости от состояния организма, например у новорожденных и больных людей.[4].
5 аминокислот (A D N E S) — заменимые у человека, означает что они могут синтезироваться в достаточных количествах в организме.[4]
Роль незаменимых для человека аминокислот[править | править код]
В результате дефицита необходимых аминокислот в организме человека нарушается синтез белков, что приводит к ослаблению функций памяти и умственных способностей, снижению иммунитета (сопротивляемости организма болезням). В то же время избыток потребления несбалансированного белка приводит к перегрузке работы органов, в первую очередь печени и почек. Ценность потребляемого с пищей белка для человека определяется его сбалансированностью по содержанию незаменимых аминокислот.[1]
Рекомендованная суточная норма[править | править код]
Рассчитать требования к рекомендованной суточной норме достаточно сложно; эти значения претерпели значительные изменения за последние 20 лет. Следующая таблица представляет список рекомендованных ВОЗ и Национальной библиотекой медицины США суточных норм для взрослого человека.[5][6]
| Аминокислота(ы) | ВОЗ мг на 1 кг веса тела | ВОЗ мг для веса 70 кг | США мг на 1 кг веса тела | Кодирующий кодон генетического кода |
|---|---|---|---|---|
| H Гистидин | 10 | 700 | 14 | CAU, CAC |
| I Изолейцин | 20 | 1400 | 19 | AUU, AUC, AUA |
| L Лейцин | 39 | 2730 | 42 | UUA, UUG, CUU, CUC, CUA, CUG |
| K Лизин | 30 | 2100 | 38 | AAA, AAG |
| M Метионин + C Цистеин | 10,4 + 4,1 (15 всего) | 1050 всего | 19 всего | Метионин: AUG; Цистеин: UGU, UGC. |
| F Фенилаланин + Y Тирозин | 25 (всего) | 1750 всего | 33 всего | Фенилаланин: UUU, UUC; Тирозин: UAU,UAC . |
| T Треонин | 15 | 1050 | 20 | ACU, ACC, ACA, ACG |
| W Триптофан | 4 | 280 | 5 | UGG |
| V Валин | 26 | 1820 | 24 | GUU, GUC, GUA, GUG |
Рекомендованная суточная норма для детей от 3 лет и старше на 10-20 % выше, чем для взрослого.[5][7]
Продукты с повышенным содержанием отдельных незаменимых аминокислот[править | править код]
- Валин: зерновые, бобовые, арахис, грибы, молочные продукты, мясо.
- Изолейцин: миндаль, кешью, турецкий горох (нут), чечевица, рожь, большинство семян, соя, яйца, куриное мясо, рыба, печень, мясо.
- Лейцин: чечевица, орехи, большинство семян, овёс, бурый (неочищенный) рис, рыба, яйца, курица, мясо.
- Лизин: пшеница, орехи, амарант, гречиха, молочные продукты, рыба, мясо, горох.
- Метионин: бобы, фасоль, чечевица, соя, гречиха, молоко, яйца, рыба, мясо.
- Треонин: орехи, бобы, молочные продукты, яйца.
- Триптофан: бобовые, овёс, сушёные финики[источник не указан 2086 дней], арахис, кунжут, кедровые орехи, молоко, йогурт, творог, рыба, курица, индейка, мясо.
- Фенилаланин: бобовые, орехи, говядина, куриное мясо, рыба, яйца, творог, молоко. Также образуется в организме при распаде синтетического сахарозаменителя — аспартама, активно используемого в пищевой промышленности.
- Аргинин (частично-заменимая аминокислота, образуется из аминокислот, поступающих с пищей, не путать с условно-заменимыми, которые образуются из незаменимых кислот, не поступающих с пищей): семена тыквы, арахис, кунжут, йогурт, швейцарский сыр, свинина, говядина, горох.
- Гистидин (частично-заменимая аминокислота): соевые бобы, арахис, чечевица, тунец, лосось, куриные грудки, свиная вырезка, говяжье филе.
Компенсация незаменимых аминокислот[править | править код]
Несмотря на то, что самостоятельно организм не способен синтезировать незаменимые аминокислоты, их недостаток в некоторых случаях все же может быть частично компенсирован. Так, например, недостаток поступающего вместе с пищей незаменимого фенилаланина может быть частично замещен заменимым тирозином. Гомоцистеин вместе с необходимым количеством доноров метильных групп снижает потребности в метионине, а глутаминовая кислота частично замещает аргинин.
См. также[править | править код]
- Незаменимые жирные кислоты
- Незаменимые пищевые вещества
Примечания[править | править код]
- ↑ 1 2 https://cyberleninka.ru/article/n/metodologiya-otsenki-sbalansirovannosti-aminokislotnogo-sostava-mnogokomponentnyh-pischevyh-produktov.pdf
- ↑ https://www.ncbi.nlm.nih.gov/pubmed/1123426 1975
- ↑ apps.who.int/iris/bitstream/10665/38133/1/9251030979_eng.pdf 1991
- ↑ 1 2 Dietary Reference Intakes: The Essential Guide to Nutrient Requirements Архивировано 5 июля 2014 года.. Institute of Medicine’s Food and Nutrition Board. usda.gov
- ↑ 1 2 FAO/WHO/UNU (2007), PROTEIN AND AMINO ACID REQUIREMENTS IN HUMAN NUTRITION, WHO Press, <https://whqlibdoc.who.int/trs/WHO_TRS_935_eng.pdf>, page 150
- ↑ Institute of Medicine (англ.)русск.. Protein and Amino Acids // Dietary Reference Intakes for Energy, Carbohydrates, Fiber, Fat, Fatty Acids, Cholesterol, Protein, and Amino Acids (англ.). — Washington, DC: The National Academies Press (англ.)русск., 2002. — P. 589—768.
- ↑ Imura K., Okada A. Amino acid metabolism in pediatric patients (неопр.) // Nutrition. — 1998. — Т. 14, № 1. — С. 143—148. — doi:10.1016/S0899-9007(97)00230-X. — PMID 9437700.
Ссылки[править | править код]
- Amino acids / MedlinePlus Encyclopedia, 2015: (англ.) «The 9 essential amino acids are: histidine, isoleucine, leucine, lysine, methionine, phenylalanine, threonine, tryptophan, and valine.»
- https://web.archive.org/web/20150226110517/https://www.uic.edu/classes/phar/phar332/Clinical_Cases/aa%20metab%20cases/PKU%20Cases/essential-nonessential.htm
- ESSENTIAL AMINO ACID REQUIREMENTS: A REVIEW / FAO, 1981
- Recommended Dietary Allowances: 10th Edition., National Research Council (US), National Academies Press 1989. Chapter 6 «Protein and Amino Acids» (англ.)
§17. Аминокислоты. Белки
1. Какие вещества называют аминокислотами, а какие – белками? Что общего между этими классами органических соединений?
Аминокислоты – органические соединения, в молекуле которых одновременно содержатся карбоксильные и аминные группы.
Белки – высокомолекулярные органические вещества, состоящие из альфа-аминокислот, соединенных в цепочку пептидной связью.
Общее между классами данных веществ: качественный состав. Белки состоят из аминокислот.
2. Почему аминокислоты – амфотерные органические соединения?
В связи с наличием кислотной карбоксильной и основной аминогрупп, аминокислоты относят к амфотерным соединениям. В зависимости от условий они могут реагировать как кислоты или основания.
3. На основе примеров, приведенных в параграфе, попробуйте предложить способ образования названий аминокислот.
4. Какими свойствами обладают аминокислоты? Напишите уравнения реакций, характеризующих химические свойства анилина.
5. Назовите области применения аминокислот.
Производство нейлона, капрона, энанта.
Аминокислоты входят в состав спортивного питания и комбикорма. Аминокислоты применяются в пищевой промышленности в качестве вкусовых добавок, например, натриевая соль глутаминовой кислоты.
6. Охарактеризуйте три структуры белка.
 7. Какие химические свойства характерны для белков?
7. Какие химические свойства характерны для белков?
Для белков наиболее характерны реакции гидролиз (разрушение полипептидной цепочки с образованием более простых фрагментов), денатурация (разрушение пространственной структуры белка), ксантопротеиновая и биуретова реакции.
8. Что такое денатурация? Какие внешние факторы могут вызвать ее?
Денатурация – это необратимое разрушение третичной и вторичной структуры белка. Практически любое заметное изменение внешних условий, например, нагревание или существенное изменение pH приводит к последовательному нарушению четвертичной, третичной и вторичной структур белка. Обычно денатурация вызывается повышением температуры, действием сильных кислот и щелочей, солей тяжелых металлов, некоторых растворителей (спирт), радиации и др.
9. Как с помощью одного и того же реактива распознать растворы трех веществ: белка, глюкозы и глицерина?
Гидроксид меди (II). При добавлении к белку дает фиолетовое окрашивание, при сдобавлении к глюкозе и глицерину – синее. Если пробирку с раствором глюкозы нагреть, то происходит обесцвечивание раствора и выпадение красного осадка.
10. Запишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
Этан → этилен → этиловый спирт → уксусный альдегид → уксусная кислота → хлоруксусная кислота → аминоуксусная кислота → полипептид.
11. Вычислите массу соли, которую можно получить при взаимодействии 150 г 5%-го раствора аминоуксусной кислоты с необходимым количеством гидроксида натрия. Сколько граммов 12%-го раствора щелочи потребуется для реакции?