Какими свойствами обладает франций

Франций – это элемент с атомным числом 87. Атомная масса наиболее долгоживущего изотопа – 223. Франций является радиоактивным щелочным металлом, обладает крайне выраженной химической реактивностью.
История открытия франция
Металл был открыт еще в 1939 году сотрудницей парижского Института Радия по имени Маргарита Перей. Она же — видимо, из патриотических чувств — назвала элемент в честь своей Родины. Франций был открыт при изучении искусственно полученного элемента «актиния»: было замечено нехарактерное радиоактивное свечение. Следует ради справедливости отметить, что над созданием этого элемента могли одновременно с ней работать и другие исследователи, но, как говорится, победителей не судят.
Основные характеристики
На сегодняшний день франций является одним из самых редких металлов (да и вообще химических элементов), которые встречаются в природе.
Согласно подсчетам ученых, содержание этого металла в земной коре составляет порядка 340 грамм (меньше содержится только aстата). Связано это главным образом с его физической неустойчивостью. Будучи радиоактивным, он имеет очень короткий период полураспада (у самого стабильного изотопа он составляет 22,3 минуты). Единственное, чем компенсируется его природное содержание, так это тем, что франций является промежуточным звеном распада урана-235 и тория-232. Таким образом, весь франций, который содержится в естественных условиях, является продуктом радиоактивного распада.
Как можно его получить?
Рассмотрим единственный способ получить самый стабильный изотоп франция. Это можно сделать за счет ядерной реакции золота с атомами кислорода. Все остальные способы (имеется в виду радиоактивный распад) нецелесообразны, так как получаются крайне нестабильные изотопы, которые «живут» не более нескольких минут. Получить в домашних условиях этот элемент, как и все его соединения, понятное дело, не получится (да и незачем, собственно). Здесь можно найти множество экспериментов с другими металлами.
Какие химические свойства проявляет франций?
По своим свойствам франций аналогичен цезию. Релятивистские эффекты 6p-оболочки обеспечивают связь франция с кислородом в супероксидах (например, состава FrO2) более ковалентной, относительно супероксидов прочих элементов этой группы. С учетом максимально низкой электроотрицательности из всех ныне существующих франций характеризуется выраженной химической активностью. Все физические свойства этого элемента указаны только теоретически, так как проверить их на практике не представляется возможным по причине короткого периода «жизни» этого элемента (плотность=1,87 г/см³, t плавления=27 °C, t кипения=677 °C, удельная теплота плавления=9,385 кДж/кг). Все соединения этого элемента растворимы в воде (исключения: соли перхлорат, хлороплатинат, пикраткобальтинитрит франция). Франций всегда сокристаллизуется с веществами, в состав которых входит цезий. Наблюдается его соосаждение с нерастворимыми солями цезия (перхлоратом или кремневольфраматом цезия). Извлечение из растворов франция осуществляется:
- хлороплатинатами цезия и рубидия Cs2PtCl6 и Rb2PtCl6;
- хлоровисмутатом Cs2BiCl5, хлоростаннатом Cs2SnCl6 и хлороантимонатом цезия Cs2SbCl5•2,5H2O;
- cвободными гетерополикислотами: кремневольфрамовой и фосфорновольфрамовой.
Какое практическое значение имеет этот элемент?
Несмотря на всю свою уникальность, никакого применения на практике франций пока еще не имеет. Соответственно, в промышленности и каких-либо технологиях не используется. Причиной тому является его чрезвычайно короткий период полураспада. Есть данные, что хлорид франция может быть использован для диагностики онкологических новообразований, однако в виду значительной стоимости этого образования, подобного рода методика не может быть введена в систематическое использование. В принципе, теми же свойствами обладает цезий.
Так что и это свойство франция оказалось невостребованным: его стоимость сравнивается со стоимостью тонны платины или золота. По прогнозам ведущих специалистов, рассматриваемый элемент будет всегда иметь чисто познавательную ценность, не более того.
 Ïåðèîäè÷åñêîé òàáëèöå ñóùåñòâóåò íåìàëî õèìè÷åñêèõ ýëåìåíòîâ, íàçâàííûõ â ÷åñòü ìåñòíîñòåé è ãîñóäàðñòâ. Íàïðèìåð, ãåðìàíèé (â ÷åñòü Ãåðìàíèè), ðóòåíèé (â ÷åñòü Ðîññèè), ñêàíäèé (â ÷åñòü Ñêàíäèíàâèè) è ò.ï.
Ëþáîïûòíî òî, ÷òî â ýòîò ñïèñîê ïûòàëàñü íå ðàç ïîïàñòü è Àâñòðèÿ, íî ïîñòîÿííî òåðïåëà íåóäà÷ó…

Ñåé÷àñ ýòî íåáîëüøàÿ ñòðàíà â Öåíòðàëüíîé Åâðîïå, íî â íà÷àëå XIX âåêà Kaisertum Österreich ïðîñòèðàëàñü îò Ìèëàíà äî Ëüâîâà, òàê ÷òî ìíîãèå ó÷¸íûå, òðóäèâøèåñÿ íà áëàãî ðîäèíû, æåëàëè óâåêîâå÷èòü å¸ â ëèöå ýëåìåíòà «Austrium». Ïî÷åìó æå ýòîãî ñäåëàòü âñ¸-òàêè íå âûøëî?

Ïåðâûì òåðìèí «àâñòðèé» óïîòðåáèë âåíãåðñêèé õèìèê Àíòàë Ðóïðåõò â 1792 ãîäó.
Òàê îí íàçâàë ìåòàëëè÷åñêèå îáðàçöû, êîòîðûå îáíàðóæèë íà äíå òèãëÿ, â êîòîðîì ïðîêàëèë ñìåñü ìàãíåçèè è óãîëüíîãî ïîðîøêà. Îí áûë ïðèâåðæåíöåì òåîðèè, ÷òî «çåìëè» (òàê íàçûâàëè ëþáûå íåðàñòâîðèìûå â âîäå ñûïó÷èå ïîðîäû) íå ôóíäàìåíòàëüíûå ýëåìåíòû, à îêñèäû íåèçâåñòíûõ ìåòàëëîâ è æåëàë äîêàçàòü ýòî ýêñïåðèìåíòàëüíî.
Îäíàêî, êàê îêàçàëîñü ìàãíåçèÿ áûëà çàãðÿçíåíà ñîåäèíåíèÿìè æåëåçà è Ðóïðåõò ïîëó÷èë ôàêòè÷åñêè ÷àñòèöû íåèçâåñòíîãî æåëåçíîãî ñïëàâà, èç êîòîðîãî íåëüçÿ áûëî ÷òî-ëèáî âûäåëèòü.

Íî â 1808 ãîäó àíãëèéñêèé õèìèê Õýìôðè Äýâè ïðîâ¸ë-òàêè óñïåøíûé ýêñïåðèìåíò ïóò¸ì ýëåêòðîëèçà ðàñïëàâà ìàãíåçèè è îêñèäà ðòóòè, îí âûäåëèë àìàëüãàìó íåèçâåñòíîãî ìåòàëëà è äàë åìó èìÿ Magnesium. Òàê ñòàëî ÿñíî, ÷òî «çåìëÿ» èçâåñòíàÿ, êàê «áåëàÿ ìàãíåçèÿ» ÿâëÿåòñÿ îêñèäîì ýòîãî ìåòàëëà. ×èñòûé ìàãíèé ïîëó÷èë ëèøü â 1831 ãîäó ôðàíöóçñêèé õèìèê Àíòóàí Áþññè è çà ýëåìåíòîì îñòàâèëè íàçâàíèå, ïðåäëîæåííîå Äýâè.
Âòîðîé ðàç àâñòðèé ïîÿâëÿåòñÿ â òðóäàõ ïðîôåññîðà Êàðëîâà óíèâåðñèòåòà â Ïðàãå, íåìåöêîãî õèìèêà Ýäóàðäà Ëèííåìàííà â 1886 ãîäó.  ïðîöåññå ðàáîòû ñ îáðàçöàìè ðåäêîãî ìèíåðàëà îðòèòà îí îáíàðóæèë íåîáû÷íûå ñïåêòðàëüíûå ëèíèè ñ äëèíîé âîëíû 416.5 è 403 íì. Ëèííåìàí íå ñìîã îïðåäåëèòü ê êàêîìó èç èçâåñòíûõ íà òîò ìîìåíò ýëåìåíòó îíè ìîãóò îòíîñèòñÿ è ïðåäïîëîæèë, ÷òî îòêðûë íîâûé ýëåìåíò, íàçâàâ åãî àâñòðèåì.

Ê ñîæàëåíèþ â ýòîò æå ãîä ïðîôåññîð ñêîí÷àëñÿ è ñ ðåçóëüòàòàìè èññëåäîâàíèé äðóãèå ó÷¸íûå îçíàêîìèëèñü óæå ïîñëå åãî ñìåðòè. Îäíàêî ôðàíöóçñêèé õèìèê Ïîëü Ýìèëü Ëåêîê äå Áóàáîäðàí ïðåäïîëîæèë, ÷òî ýòè ñïåêòðû ìîãóò ïðèíàäëåæàòü îòêðûòîìó èì ãàëëèþ. Äàííóþ ãèïîòåçó òàêæå ïîäòâåðäèë àâñòðèéñêèé õèìèê Ðè÷àðä Ïðèáðàì — äåéñòâèòåëüíî, ëèíèè ñîîòâåòñòâîâàëè ýòîìó ìåòàëëó.
È â ïîñëåäíèé, òðåòèé ðàç, àâñòðèé óïîìèíàåò â 1889 ãîäó â ñâîåé ðàáîòå ÷åøñêèé õèìèê Áîãóñëàâ Áðàóíåð. Òàê îí íàçâàë íåèçâåñòíûé òÿæ¸ëûé ìåòàëë, ñëåäû êîòîðîãî èì áûëè îáíàðóæåíû â òåëëóðå. Êðîìå òîãî, îí äîïóñêàë, ÷òî ñàì òåëëóð íå ÿâëÿåòñÿ èíäèâèäóàëüíûì ñîåäèíåíèåì, è åãî àòîìíóþ ìàññó «óâåëè÷èâàþò» ïîäîáíûå ïðèìåñè.

Ïîçæå ãèïîòåçà Áðàóíåðà î ãåòåðîãåííîñòè òåëëóðà áûëà ïðèçíàíà îøèáî÷íîé, à ïîñëå îòêðûòèÿ ñóïðóãàìè Êþðè â îáðàçöàõ íàñòóðàíà ýëåìåíòà ïîëîíèÿ, áûëî óñòàíîâëåíî, ÷òî èìåííî åãî ñëåäû Áðàóíåð çàìåòèë â òåëëóðå. Ê ñîæàëåíèþ îí íå ìîã íàñòàèâàòü íà ïåðâåíñòâå, ïî òîìó êàê ëèøü ñîîáùèë î íåèçâåñòíîé ïðèìåñè, à íå êëàññèôèöèðîâàë è ïðåäñòàâèë äîêàçàòåëüñòâà îòêðûòèÿ íîâîãî ìåòàëëà.
Ñ òåõ ïîð àâñòðèé íå ïîÿâëÿëñÿ â íàó÷íîé ëèòåðàòóðå. Âïðî÷åì íå ñòîèò çàáûâàòü, ÷òî è ïî ñåé äåíü Ïåðèîäè÷åñêàÿ òàáëèöà ïîïîëíÿåòñÿ íîâûìè ýëåìåíòàìè, òàê ÷òî è àâñòðèé ìîæåò-òàêè äîæäàòüñÿ êîãäà-íèáóäü ñâîåãî ÷àñà.

Ïîäîáíûå è ïðî÷èå ïîñòû íà ñòðàíèöå ÂÊ:
https://vk.com/mircenall
| Франций | |
|---|---|
| Атомный номер | 87 |
| Внешний вид простого вещества | радиоактивный щелочной металл |
| Свойства атома | |
| Атомная масса (молярная масса) | 223,0197 а. е. м. (г/моль) |
| Радиус атома | n/a пм |
| Энергия ионизации (первый электрон) | 380 кДж/моль (эВ) |
| Электронная конфигурация | [Rn] 7s1 |
| Химические свойства | |
| Ковалентный радиус | n/a пм |
| Радиус иона | (+1e) 180 пм |
| Электроотрицательность (по Полингу) | 0,7 |
| Электродный потенциал | Fr←Fr+ −2,92 В |
| Степени окисления | +1 |
| Термодинамические свойства простого вещества | |
| Плотность | 1,87 г/см³ |
| Молярная теплоёмкость | n/a Дж/(K·моль) |
| Теплопроводность | n/a Вт/(м·K) |
| Температура плавления | 300 K |
| Теплота плавления | ~ 2 кДж/моль |
| Температура кипения | 950 K |
| Теплота испарения | ~ 65 кДж/моль |
| Молярный объём | n/a см³/моль |
| Кристаллическая решётка простого вещества | |
| Структура решётки | кубическая объёмноцентрированая |
| Параметры решётки | n/a Å |
| Отношение c/a | n/a |
| Температура Дебая | n/a K |
Франций — элемент главной подгруппы первой группы седьмого периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 87. Обозначается символом Fr (Francium). Простое вещество франций (CAS-номер: 7440-73-5) — радиоактивный щелочной металл, обладающий высокой химической активностью.
История открытия Франция
Франций был предсказан Д. И. Менделеевым (как Эка-цезий), и был открыт (по его радиоактивности) в 1939 г. Маргаритой Пере, сотрудницей Института радия в Париже. Она же дала ему в 1964 г. название в честь своей родины — Франции.
Нахождение Франция в природе
Франций-223 (самый долгоживущий из изотопов франция, период полураспада 22,3 минуты) содержится в одной из побочных ветвей радиоактивного ряда урана-235 и может быть выделен из природных урановых минералов. Образуется при альфа-распаде актиния-227:
227Ac → 223Fr (сопровождается α-излучением, вероятность распада приблизительно 1,4 %),
227Ac → 227Th (сопровождается β-излучением, вероятность распада около 98,6 %).
Его старое название — «актиний К» (AcK). По оценкам, его равновесное содержание в земной коре равно 340 г.
Кроме того, в одной из побочных ветвей радиоактивного ряда тория содержится франций-224 с периодом полураспада 3,0 минуты. Его равновесное содержание в земной коре составляет лишь 0,5 г.
Получение Франция
Микроскопические количества франция-223 и франция-224 могут быть химически выделены из минералов урана и тория. Другие изотопы франция получают искусственным путём с помощью ядерных реакций.
Физические, химические свойства Франция
Франций похож по свойствам на цезий. Всегда сокристаллизуется с его соединениями. Так как в распоряжении исследователей имеются лишь мельчайшие образцы, содержащие не более 10−7 г франция, то сведения о его свойствах известны с достаточно большой погрешностью, однако они все время уточняются. Согласно последним данным, плотность франция при комнатной температуре составляет 1,87 г/см³, температура плавления 27°C, температура кипения 677°C, удельная теплота плавления 9,385 кДж/кг.
Применение Франция
Соль франция FrCl использовалась для обнаружения раковых опухолей, но по причине чрезвычайно высокой стоимости эту соль в масштабных разработках использовать не выгодно.
Таблица
^
=>>
Маргарита Перрей
(1909 — 1975)

Источник: https://www.liveinternet.ru/ users/kakula/post137818671/
| Поделиться в |
Уранит |
История открытия:
Франций — один из четырех элементов (№№ 43, 61, 85 и 87) которые остались неоткрытыми к 1925 году. Предсказанный еще Меделеевым эка-цезий искали в качестве спутника цезия в цезиевых минералах. С 1929 по 1939 год эка-цезий «находили» несколько раз, называя то виргинием в честь штата США, то молдавием, то алкалинием или руссием. Однако все эти открытия были ошибочными.
В 1939 г. Маргарита Перей из института Кюри в Париже, занимаясь очисткой препарата актиния (Ас-227) от разнообразных продуктов радиоактивного распада, обнаружила b-излучение, которое не могло принадлежать ни одному из известных в то время изотопов.
Когда этот изотоп (период полураспада 21 мин) подвергли химическому исследованию, оказалось, что его свойства соответствуют свойствам эка-цезия.
Окончательно это было подтверждено после второй мировой войны, и в 1946 г. Перей предложила назвать новый элемент францием (Francium) в честь ее родины.
Получение:
Франций-223 (самый долгоживущий из изотопов франция, период полураспада 22,3 минуты) входит в одну из побочных ветвей природного радиоактивного ряда урана-235 и содержится в крайне малых количествах в урановых минералах. Его образование из актиния можно выразить уравнением:
227Ac (-, a ) 223Fr. По оценкам, его равновесное содержание в земной коре равно 340 г. Также в одной из побочных ветвей радиоактивного ряда тория содержится франций-224 с периодом полураспада 3,0 минуты. Его равновесное содержание в земной коре составляет лишь 0,5 г.
С помощью ядерных реакций получают и другие изотопы франция. Одна из наиболее распространённых реакций:
197Au + 18O = 210Fr + 5n
Физические свойства:
Радоактивный металл. Вследствие высокой радиоактивности исследования проводятся с микроскопическими количествами. Согласно последним данным, плотность франция при комнатной температуре составляет 1,87 г/см3, температура плавления 27°C, температура кипения 677°C.
Франций претерпевает b-распад, превращаясь в изотоп радия: 223Fr (-, b ) 223Ra
Химические свойства:
Франций имеет самую низкую электроотрицательность из всех элементов, известных в настоящее время. Электродный потенциал Fr+/Fr = -2,92 В.
Соответственно, франций является и самым химически активным щелочным металлом.
В соединениях проявляет степень окисления +1.
Важнейшие соединения:
Соединения мало изучены вследствие радиоактивности франция. Он обладает большинством свойств, характерных для других щелочных металлов, наиболее похож по свойствам на цезий, всегда сокристаллизуется с его соединениями. Так для выделения франция из смеси с другими продуктами ядерных реакций используется основано на его соосаждении с нерастворимыми солями цезия (перхлоратом или кремневольфраматом цезия). Он извлекается из растворов также хлороплатинатами цезия и рубидия Cs2PtCl6 и Rb2PtCl6, хлоровисмутатом Cs2BiCl5, хлоростаннатом Cs2SnCl6 и хлороантимонатом цезия Cs2SbCl5· 2,5H2O, а также свободными гетерополикислотами – кремневольфрамовой и фосфорновольфрамовой.
Образует растворимые соли и гидроксид.
Применение:
Хлорид франция FrCl использовался для обнаружения раковых опухолей, но по причине чрезвычайно высокой стоимости эту соль в масштабных разработках использовать невыгодно.
В настоящее время франций и его соли применения пока что не имеют, в связи с малым периодом полураспада и высокой радиоактивностью.
Тестова Кристина
ХФ ТюмГУ, 581 группа, 2011 г.
Источники: Франций. Популярная библиотека химических элементов https://n-t.ru/ri/ps/pb087.htm
Франций. Википедия, свободная энциклопедия. https://ru.wikipedia.org/?oldid=34567492.
Ïóáëèêóÿ ãèôêè ñ ðàçëè÷íûìè ðåàêöèÿìè ùåëî÷íûõ ìåòàëëîâ, â êîììåíòàõ äîñòàòî÷íîå êîëè÷åñòâî ëþäåé èíòåðåñîâàëîñü ôðàíöèåì â ýòîì ïëàíå.
Òåïåðü æå, äàáû ðàññòàâèòü âñå òî÷êè íàä i… Ñ ôðàíöèåì, óâû, ãèôîê íåò. Òàê ÷òî âìåñòî ýòîãî ÿ ðàññàæó íåïîñðåäñòâåííî ïðî íåãî, à çàîäíî ïî÷åìó íåò ãèôîê.
Ôðàíöèé — ïîñëåäíèé èç îòêðûòûõ ýëåìåíòîâ ãðóïïû ùåëî÷íûõ ìåòàëëîâ (õîòÿ ãèïîòåòè÷åñêè, ñëåäóþùèé ùåëî÷íîé ìåòàëë (ýëåìåíò ¹ 119) ýòî óíóíåííèé, íî åãî åùå äàæå íå îòêðûëè).
Ôðàíöèé òàêæå áûë ïðåäñêàçàí çàäîëãî äî ñâîåãî îòêðûòèÿ, åùå 1870-õ ãîäàõ. Òîãäà æå è âïëîòü äî åãî îòêðûòèÿ, ôðàíöèé èìåíîâàëè «ýêà-öåçèåì».  íà÷àëå XX âåêà áûëî ìíîæåñòâî íåóäà÷íûõ ïîïûòîê åãî îòêðûòèÿ, òàê êàê çà íåãî ïðèíèìàëè ðàäèîàêòèâíûå èçîòîïû óæå èçâåñòíûõ ùåëî÷íûõ ìåòàëëîâ. Íî âñå æå, â 1939 ãîäó, íåèçâåñòíûé íà òîò ìîìåíò ýëåìåíò, áûë çàìå÷åí Ìàðãàðèòîé Ïåðåé, ñîòðóäíèöîé Èíñòèòóòà Êþðè â Ïàðèæå, êàê ïðîäóêò àëüôà-ðàñïàäà àêòèíèÿ-227, ñîäåðæàùèéñÿ â ìèíåðàëå Íàñòóðàí.
Ïîçæå, 1946 ãîäó ýëåìåíòó äàëè íàçâàíèå «ôðàíöèé», â ÷åñòü ðîäèíû ïåðâîîòêðûâàòåëüíèöû.

Èíòåðåñíûé ôàêò, ÷òî èçíà÷àëüíî ñàìà Ïåðåé, ïðåäëàãàëà íàçâàòü åãî êîòèé (catium), ïîñêîëüêó ýëåìåíò èìååò ñàìûé ýëåêòðîïîëîæèòåëüíûé êàòèîí, íî èç-çà áîëüøåé àññîöèàöèåé ñ êîòàìè, à íå ñ êàòèîíàìè ïðåäëîæåíèå îòêëîíèëè è îñòàíîâèëèñü íà âàðèàíòå ñ ôðàíöèåì

Íà äàííûé ìîìåíò èçâåñòíî 34 èçîòîïà ôðàíöèÿ. Ñàìûå ñòàáèëüíûå èç íèõ ôðàíöèé-223 è ôðàíöèé-221. Ôðàíöèé-223, òîò ñàìûé, ÷òî áûë íàéäåí â íàñòóðàíå, ïðåäñòàâëÿåò èç ñåáÿ ïðîäóêò ñåðèè àêòèíèåâîãî ðàñïàäà. Â òî æå âðåìÿ åãî ïðîäóêòîì ïîñëå áåòà-ðàñïàäà ÿâëÿåòñÿ ðàäèé-223. Ôðàíöèé-221 — ïðîäóêò ñåðèè íåïòóíèåâîãî ðàñïàäà, îáðàçóþùèéñÿ èç àêòèíèÿ 225, è ñàì ðàñïàäàþùèéñÿ íà àñòàò-217. Ïåðèîä èõ ïîëóðàñïàäà 22 ìèíóòû (ó ôðàíöèÿ-223) è 5 ìèíóò (ó ôðàíöèÿ-221), òàêèì îáðàçîì íàéäåííûé Ïåðåé èçîòîï — ñàìûé ñòàáèëüíûé.
(íèæå ïðåäñòàâëåíî èçîáðàæåíèå èñêóññòâåííî-ïîëó÷åííîãî ôðàíöèÿ-223 â ìàãíèòíî-îïòè÷åñêîé ëîâóøêå êîëè÷åñòâîì â 300k àòîìîâ)

«Íî êàê æå îí ñóùåñòâóåò â ïðèðîäå, åñëè ïåðèîä æèçíè ñàìîãî ñòàáèëüíîãî èçîòîïà 22 ìèíóòû?» — ñïðîñèòå âû. Âñå äåëî â íåïðåðûâíîì ðàñïàäå â ðàäèîàêòèâíûõ ìèíåðàëàõ.  íèæåèçîáðàæåííîì îáðàçöå íàñòóðàíà, ôðàíöèÿ âñåãäà, â ëþáîé ìîìåíò âðåìåíè, 3,3 × 10^-20 ãðàìì, èáî «òîò ôðàíöèé, ÷òî áûë 22 ìèíóòû íàçàä» ïðåâðàòèëñÿ â ðàäèé, à íåêîòîðîå êîëè÷åñòâî àêòèíèÿ, ñóùåñòâîâàâøåå 22 ìèíóòû íàçàä ïðåâðàòèëîñü âî ôðàíöèé, òàêèì îáðàçîì åãî âñåãäà îäíî è òî æå êîëè÷åñòâî.

Çíàÿ êîíöåíòðàöèþ óðàíîâûõ ìèíåðàëîâ â çåìëå è êîíöåíòðàöèþ â íèõ ôðàíöèÿ, ìîæíî òàêæå ïîñ÷èòàòü êîëè÷åñòâî âñåãî ôðàíöèÿ â çåìíîé êîðå â ëþáîé ìîìåíò âðåìåíè — ýòî ïðèìåðíî 30 ãðàìì. Ñîáñòâåííî, ýòî è îòâåò íà âîïðîñ, ïî÷åìó íåò ãèôîê ñ íèì.

Íåñìîòðÿ íà ÷ðåçâû÷àéíóþ ðåäêîñòü, íåêîòîðûå ñâîéñòâà ýòîãî ìåòàëëà, êàê óñðåäíåííûå ñâîéñòâà åãî èçîòîïîâ, âñå æå èçâåñòíû…
 öåëîì õèìè÷åñêèå ñâîéñòâà ôðàíöèÿ áûëè áû ïîõîæè íà ñâîéñòâà öåçèÿ, òîëüêî ïðîòåêàëè áû åùå áîëåå áóðíî. Êàê è âñå ùåëî÷íûå ìåòàëëû, ôðàíöèé ðåàãèðîâàë áû ñ êèñëîðîäîì âîçäóõà, îáðàçóÿ îêñèäû è ïåðîêñèäû, à òàêæå ñ âîäîé, îáðàçóÿ ùåëî÷ü.
Ïëîòíîñòü ôðàíöèÿ 1,87 ã/ñì³ (â 3,5 ðàçà áîëüøå, ÷åì ó ëèòèÿ, íî â 1,4 ìåíüøå, ÷åì ó àëþìèíèÿ).
Òåìïåðàòóðà ïëàâëåíèÿ 20Ñ, ÷òî äåëàëî áû åãî òðåòüèì æèäêèì ïðè í.ó. ýëåìåíòîì, êðîìå ðòóòè è áðîìà (ó ãàëëèÿ è öåçèÿ Òïë 28 ãðàäóñîâ, òàê ÷òî îíè ñ÷èòàþòñÿ òâåðäûìè ïðè ñòàíäàðòíûõ 298Ê (25Ñ))
Ôðàíöèé îáëàäàåò ñàìûìè íèçêèìè ïîêàçàòåëÿìè ýëåêòðîîòðèöàòåëüíîñòè, è åñëè áû åãî èñïîëüçîâàëè â õèìèè, òî îí áûë áû ñèëüíåéøèì ñóùåñòâóþùèì âîññòàíîâèòåëåì.
Íåïîäòâåðæäåííîå, íî âñå æå èìåþùåå ìåñòî ïðåäïîëîæåíèå ïîñëåäíèõ ëåò ãëàñèò, ÷òî â òåîðèè ìåòàëëè÷åñêèé ôðàíöèé ìîæåò èìåòü öâåò îò çîëîòèñòîãî (ïîäîáíî öåçèþ) äî âîâñå êðàñíîãî.
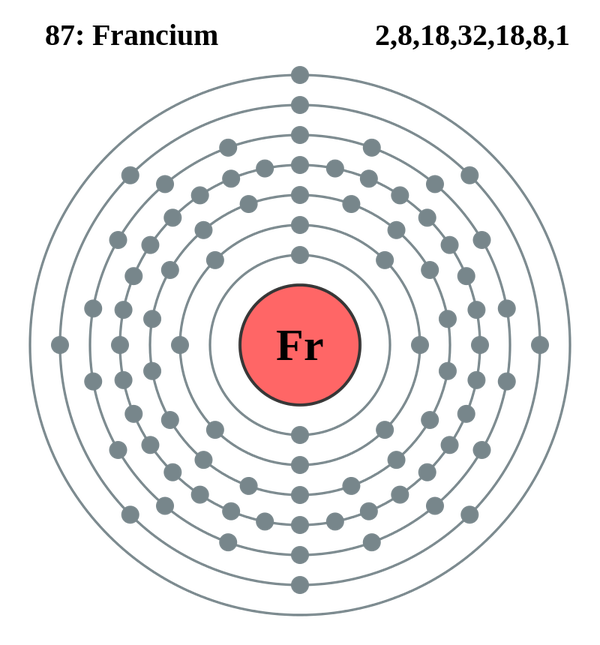
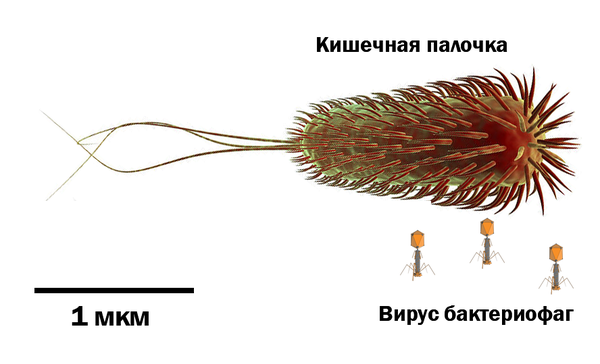
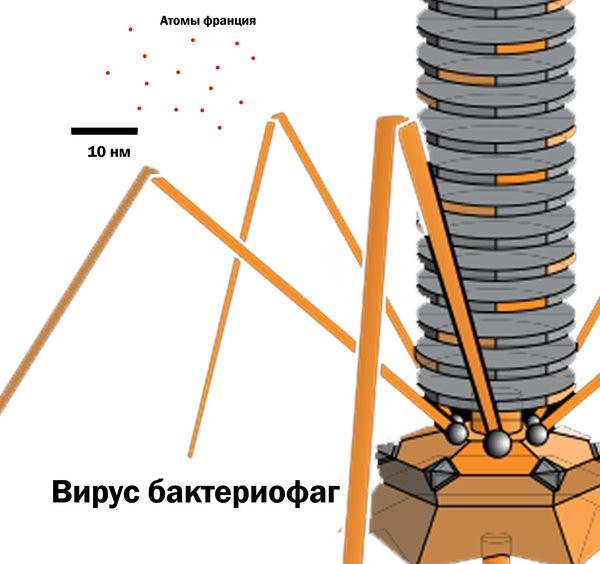
Ôðàíöèé èìååò ñàìûé áîëüøîé ðàçìåð àòîìîâ — 0,54 íì. Ýòî â 2 ðàçà áîëüøå àòîìà óðàíà, â 4,5 ðàçà áîëüøå, ÷åì àòîì êèñëîðîäà è â 8,5 ðàç áîëüøå àòîìà âîäîðîäà.
Óâû, ïî ïîíÿòíûì ïðè÷èíàì, ôðàíöèé íå íàøåë ïðàêòè÷åñêîãî ïðèìåíåíèÿ, îäíàêî áûë ïðîåêò åãî èñïîëüçîâàíèÿ â ëå÷åíèè ðàêîâûõ çàáîëåâàíèé, íî îïÿòü æå èç-çà åãî ðåäêîñòè ïðîåêò ïðèçíàëè íåöåëåñîîáðàçíûì.


