Какими особенностями типа связи свойства металлов обусловлены
Какими свойствами обладают металлы и какими особенностями типа связи эти свойства обусловлены?
Металлы в твердом и отчасти в жидком состоянии обладают рядом характерных свойств:
– высокими теплопроводность и электрической проводимостью;
– положительным температурным коэффициентом электрического сопротивления; с повышением температуры электрическое сопротивление чистых металлов возрастает; большое число металлов обладают сверхпроводимостью (у этих металлов при температуре, близкой к абсолютному нулю, электрическое сопротивление падает скачкообразно, практически до нуля);
– термоэлектронной эмиссией, т. е. способностью испускать электроны при нагреве;
– хорошей отражательной способностью: металлы непрозрачны и обладают металлическим блеском;
– повышенной способностью к пластической деформации.
Данные свойства обусловлены особенностями строения металлов. Согласно теории металлического состояния, металл представляет собой вещество, состоящее из положительных ядер, вокруг которых по орбиталям вращаются электроны. На последнем уровне число электронов невелико и они слабо связаны с ядром. Эти электроны имеют возможность перемещаться по всему объему металла, т.е. принадлежать целой совокупности атомов.
Таким образом, пластичность, теплопроводность и электропроводность обеспечиваются наличием «электронного газа».
Какая температура разделяет районы холодной и горячей пластической деформации и почему? Рассмотрите на примере меди.
В зависимости от отношения температуры деформации к температуре рекристаллизации различают холодную и горячую деформацию.
Холодной деформацией называют такую, которую проводят при температуре ниже температуры рекристаллизации. Поэтому холодная деформация сопровождается упрочнением (наклепом) металла.
Деформацию называют горячей, если ее проводят при температуре выше температуры рекристаллизации для получения для получения полностью рекристаллизованной структуры.
При этих температурах деформация также вызывает упрочнение («горячий наклеп»), которое полностью или частично снимается рекристаллизацией, протекающей при температурах обработки и при последующем охлаждении.
При горячей обработке давлением (прокатке, прессовании, ковке, штамповке и т. д.) упрочнение в результате наклепа (повышение плотности дислокаций) непосредственно в процессе деформации непрерывно чередуется с процессом разупрочнения (уменьшением плотности дислокаций) при динамической полигонизации и рекристаллизации во время деформации и охлаждения. В этом основное отличие динамической полигонизации и рекристаллизации от статической.
Горячую деформацию в зависимости от состава сплава и скорости деформации обычно проводят при температурах (0,7 – 0,75 Тпл).
Полигонизация – процесс деления зерен на части: фрагменты, полигоны в результате скольжения и переползания дислокаций. Рекристаллизация – процесс зарождения и роста новых недеформированных зерен при нагреве наклепанного металла до определенной температуры.
А.А. Бочвар показал, что между температурным порогом рекристаллизации и температурой плавления металлов имеется простое соотношение: рекристаллизация начинается при температуре, составляющей одинаковую для всех металлов долю от температуры плавления по абсолютной шкале, а именно Тп.р. = (0,3¸0,4)Тпл.
Для меди температурный порог рекристаллизации равен
Тп.р. = (1083+273)0,4–273 = 268 °С.
Выше этой температуры деформация называется горячей, ниже – холодной.
Вычертите диаграмму состояния железо-карбид железа, укажите структурные составляющие во всех областях диаграммы, опишите превращения и постройте кривую охлаждения (с применением правила фаз) для сплава, содержащего 4,3% С. Какова структура этого сплава при комнатной температуре и как такой сплав называется?
Первичная кристаллизация сплавов системы железо-углерод начинается по достижении температур, соответствующих линии ABCD (линии ликвидус), и заканчивается при температурах, образующих линию AHJECF (линию солидус).
При кристаллизации сплавов по линии АВ из жидкого раствора выделяются кристаллы твердого раствора углерода в α-железе (δ-раствор). Процесс кристаллизации сплавов с содержанием углерода до 0,1 % заканчивается по линии АН с образованием α (δ)-твердого раствора. На линии HJB протекает перитектическое превращение, в результате которого образуется твердый раствор углерода в γ-железе, т. е. аустенит. Процесс первичной кристаллизации сталей заканчивается по линии AHJE.
При температурах, соответствующих линии ВС, из жидкого раствора кристаллизуется аустенит. В сплавах, содержащих от 4,3 % до 6,67 % углерода, при температурах, соответствующих линии CD, начинают выделяться кристаллы цементита первичного. Цементит, кристаллизующийся из жидкой фазы, называется первичным. B точке С при температуре 1147°С и концентрации углерода в жидком растворе 4,3% образуется эвтектика, которая называется ледебуритом. Эвтектическое превращение с образованием ледебурита можно записать формулой ЖР4,3→Л[А2,14+Ц6,67]. Процесс первичной кристаллизации чугунов заканчивается по линии ECF образованием ледебурита.
Таким образом, структура чугунов ниже 1147°С будет: доэвтектических – аустенит + ледебурит, эвтектических – ледебурит и заэвтектических – цементит (первичный) + ледебурит.
Превращения, происходящие в твердом состоянии, называются вторичной кристаллизацией. Они связаны с переходом при охлаждении γ-железа в α-железо и распадом аустенита.
Линия GS соответствует температурам начала превращения аустенита в феррит. Ниже линии GS сплавы состоят из феррита и аустенита.
Линия ЕS показывает температуры начала выделения цементита из аустенита вследствие уменьшения растворимости углерода в аустените с понижением температуры. Цементит, выделяющийся из аустенита, называется вторичным цементитом.
В точке S при температуре 727°С и концентрации углерода в аустените 0,8 % образуется эвтектоидная смесь состоящая из феррита и цементита, которая называется перлитом. Перлит получается в результате одновременного выпадения из аустенита частиц феррита и цементита. Процесс превращения аустенита в перлит можно записать формулой А0,8П[Ф0,03+Ц6,67].
Линия PQ показывает на уменьшение растворимости углерода в феррите при охлаждении и выделении цементита, который называется третичным цементитом.
Следовательно, сплавы, содержащие менее 0,008% углерода (точкаQ), являются однофазными и имеют структуру чистого феррита, а сплавы, содержащие углерод от 0,008 до 0,03% – структуру феррит + цементит третичный и называются техническим железом.
Доэвтектоидные стали при температуре ниже 727ºС имеют структуру феррит + перлит и заэвтектоидные – перлит + цементит вторичный в виде сетки по границам зерен.
В доэвтектических чугунах в интервале температур 1147–727ºС при охлаждении из аустенита выделяется цементит вторичный, вследствие уменьшения растворимости углерода (линия ES). По достижении температуры 727ºС (линия PSK) аустенит, обедненный углеродом до 0,8% (точка S), превращаясь в перлит. Таким образом, после окончательного охлаждения структура доэвтектических чугунов состоит из перлита, цементита вторичного и ледебурита превращенного (перлит + цементит).
Структура эвтектических чугунов при температурах ниже 727ºС состоит из ледебурита превращенного. Заэвтектический чугун при температурах ниже 727ºС состоит из ледебурита превращенного и цементита первичного.
Правило фаз устанавливает зависимость между числом степеней свободы, числом компонентов и числом фаз и выражается уравнением:
C = K + 1 – Ф,
где С – число степеней свободы системы;
К – число компонентов, образующих систему;
1 – число внешних факторов (внешним фактором считаем только температуру, так как давление за исключением очень высокого мало влияет на фазовое равновесие сплавов в твердом и жидком состояниях);
Ф – число фаз, находящихся в равновесии.
Сплав железа с углеродом, содержащий 4,3% С, называется эвтетическим чугуном. Его структура при комнатной температуре Ледебурит (П+Fe3C).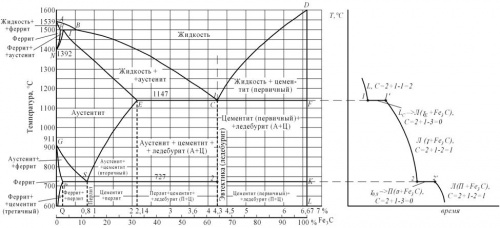
а) б)
Рисунок 1: а-диаграмма железо-цементит, б-кривая охлаждения для сплава, содержащего 4,3% углерода
С помощью диаграммы состояния железо-цементит определите температуру нормализации, отжига и закалки для стали У10. Охарактеризуйте эти виды термической обработки и опишите структуру и свойства стали после каждого режима термообработки.
Отжигом называется нагрев стали выше температур фазовых превращений с последующим медленным охлаждением (обычно вместе с печью). При медленном охлаждении стали приближаются к фазовому и структурному равновесию. Структуры, полученные после отжига, указаны на диаграмме железо-цементит. После отжига сталь имеет низкую твердость и прочность. Основные цели отжига: перекристаллизация стали (измельчение зерна), снятие внутренних напряжений, снижение твердости и улучшение обрабатываемости. При комнатной температуре сталь У10 имеет структуру цементита и перлита. До температуры Аc1 сохраняется исходная структура. При температуре Аc1 происходит превращение перлита в аустенит с содержанием углерода 0,8%. При нагреве выше точки Ас1 происходит растворение цементита в аустените (в соответствии с линией SE). Увеличение температуры выше точки Асm вызывает рост зерна аустенита.
При нагреве заэвтектоидной стали выше Аcm (линия ES) и медленном охлаждении после такого нагрева образуется грубая сетка вторичного цементита, ухудшающая механические свойства. Для устранения грубой сетки вторичного цементита заэвтектоидные стали подвергают нормализации. Критические точки для стали У10: Аc1 = 730°С; Аcm = 800°С. Нормализация заэвтектоидной стали заключается в нагреве стали до температуры выше точки Асm на 40-50°С, в непродолжительной выдержке для прогрева садки и завершения фазовых превращений и охлаждении на воздухе. При температуре нагрева заэвтектоидной стали выше Аcm на 40-50°С имеем структуру аустенита (100%). При снижении температуры до Аrm начинают появляться первые зерна цементита. При дальнейшем снижении температуры до Аr1 из аустенита будут образовываться только зерна цементита, а содержание углерода в остающемся аустените будет уменьшаться и при температуре Аr1 достигнет 0,8%. Ускоренное охлаждение на воздухе способствует тому, что цементит не успевает образовать грубую сетку, понижающую свойства стали. При снижении температуры ниже Аr1 из аустенита будет образовываться перлит. Заэвтектоидная сталь после нормализации имеет структуру перлита и цементита.
Для закалки заэвтектоидные стали нагревают на 50-70°С выше точки Ас1. Таким образом, температура нагрева под закалку составляет 780-800°С. При этих температурах в стали наряду с аустенитом имеется цементит. Поэтому после закалки в структуре заэвтектоидных сталей будет мартенсит с цементитом и небольшое количество остаточного аустенита. Охлаждающая среда при закалке – индустриальное масло. Твердость поверхности после закалки 62-64 HRC. Для снятия напряжений и стабилизации структуры после закалки изделия подвергают низкому отпуску. В результате закалки из аустенита образуется неустойчивая, метастабильная структура мартенсит и цементит. Мартенсит представляет собой пересыщенный твердый раствор углерода в α-железе.
Углеродистые стали 45 и У8 после закалки и отпуска имеют структуру мартенсит отпуска и твердость: первая – 50 HRC, вторая – 60 HRC. Используя диаграмму состояния железо – карбид железа и учитывая превращения, происходящие в этих сталях в процессе закалки и отпуска, объясните, почему сталь У8 имеет большую твердость, чем сталь 45.
Закалка – термическая обработка – заключается в нагреве стали до температуры выше критической (А3 для доэвтектоидной и А1 – для заэвтектоидной сталей) или температуры растворения избыточных фаз, в выдержке и последующем охлаждении со скоростью, превышающей критическую.
В результате закалки из аустенита образуется неустойчивая, метастабильная структура мартенсит. Для стали 45 температура АС3 = 770°С, поэтому температуру закалки выбираем 810-840°С.
Для стали У8 критическая точка АС1 = 720°С, поэтому температура закалки равна 770-790°С.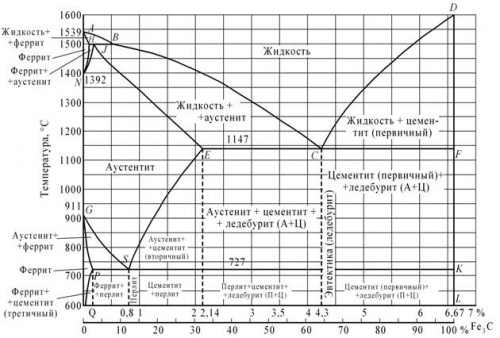
Низкий отпуск снижает закалочные макронапряжения, мартенсит закалки переводится в отпущенный мартенсит, повышается прочность и немного улучшается вязкость без заметного снижения твердости. При отпуске уменьшается степень тетрагональности кристаллической решетки мартенсита вследствие выделения из нее углерода в виде ε-карбида.
Низкий отпуск для обеих сталей проводим при температуре 160-200ºС. Более высокие температуры применять не следует, так как это приводит к снижению твердости, статической и усталостной прочности, износостойкости изделий. Структура стали 45 – отпущенный мартенсит, стали У8 – отпущенный мартенсит + цементит (при доэвтектоидной концентрации углерода в стали У8 цементит выделяться не будет).
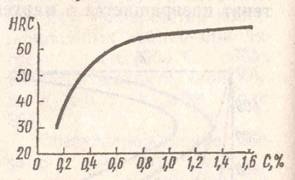
Рисунок 1 – Твердость мартенсита в зависимости от содержания углерода
Из рисунка 1 видно, что сталь У8 (0,8-0,9% С) после закалки имеет большую твердость, чем сталь 45 (0,42-0,50% С).
Металли́ческая связь — химическая связь между атомами в металлическом кристалле, возникающая за счёт перекрытия (обобществления) их валентных электронов. Металлическая связь описывается многими физическими свойствами металлов, такими как прочность, пластичность, теплопроводность, удельное электрическое сопротивление и проводимость, непрозрачность и блеск[1][2][3][4].
Механизм металлической связи[править | править код]
В узлах кристаллической решётки расположены положительные ионы металла. Между ними беспорядочно, подобно молекулам газа, движутся электроны проводимости, происходящие из атомов металлов при образовании ионов. Эти электроны играют роль «цемента», удерживая вместе положительные ионы; в противном случае решётка распалась бы под действием сил отталкивания между ионами. Вместе с тем и электроны удерживаются ионами в пределах кристаллической решётки и не могут её покинуть. Когда металл принимает какую-либо форму или растягивается, он не разрушается, потому что ионы в его кристаллической структуре довольно легко смещаются относительно друг друга[5]. Силы связи не локализованы и не направлены. В металлах в большинстве случаев проявляются высокие координационные числа (например, 12 или 8).
Рис. 1. Расположение ионов в кристалле щелочного металла
Так, щелочные металлы кристаллизуются в кубической объёмно-центрированной решётке, и каждый положительно заряженный ион щелочного металла имеет в кристалле по восемь ближайших соседей — положительно заряженных ионов щелочного металла (рис. 1). Кулоновское отталкивание одноимённо заряженных частиц (ионов) компенсируется электростатическим притяжением к электронам связывающих звеньев, имеющих форму искажённого сплющенного октаэдра — квадратной бипирамиды, высота которой и рёбра базиса равны величине постоянной решётки aw кристалла щелочного металла (рис. 2).
Связывающие электроны становятся общими для системы из шести положительных ионов щелочных металлов и удерживают последние от кулоновского отталкивания.
Величина постоянной трансляционной решётки aw кристалла щелочного металла значительно превышает длину ковалентной связи молекулы щелочного металла, поэтому принято считать, что электроны в металле находятся в свободном состоянии:
| Щелочной металл | Li | Na | K | Rb | Cs |
|---|---|---|---|---|---|
| Постоянная решётки aw, Å[6] | 3,502 | 4,282 | 5,247 | 5,690 | 6,084 |
| Длина ковалентной связи для Me2, Å[7] | 2,67 | 3,08 | 3,92 | 4,10 | 4,30 |
Математическое построение, связанное со свойствами свободных электронов в металле, обычно отождествляют с «поверхностью Ферми», которую следует рассматривать как геометрическое место в k-пространстве, где пребывают электроны, обеспечивая основное свойство металла — проводить электрический ток[8]. Таким образом, электрический ток в металлах — это движение сорванных с орбитального радиуса электронов в поле положительно заряженных ионов, находящихся в узлах кристаллической решётки металла. Выход и вход свободных электронов в связывающее звено кристалла осуществляется через точки «0», равноудалённые от положительных ионов атомов (рис. 2).
Свободное движение электронов в металле подтверждено в 1916 году опытом Толмена и Стюарта по резкому торможению быстро вращающейся катушки с проводом — свободные электроны продолжали двигаться по инерции, в результате чего гальванометр регистрировал импульс электрического тока. Свободное движение электронов в металле обусловливает высокую теплопроводность металла и склонность металлов к термоэлектронной эмиссии, происходящей при умеренной температуре.
Колебание ионов кристаллической решётки создаёт сопротивление движению электронов по металлу, сопровождающееся разогревом металла. В настоящее время важнейшим признаком металлов считается положительный температурный коэффициент электрической проводимости, то есть понижение проводимости с ростом температуры. С понижением температуры электросопротивление металлов уменьшается, вследствие уменьшения колебаний ионов в кристаллической решётке. В процессе исследования свойств материи при низких температурах Камерлинг-Оннес открывает явление сверхпроводимости. В 1911 году ему удаётся обнаружить уменьшение электросопротивления ртути при температуре кипения жидкого гелия (4,2 К) до нуля. В 1913 году Камерлинг-Оннесу присуждается Нобелевская премия по физике со следующей формулировкой: «За исследование свойств веществ при низких температурах, которые привели к производству жидкого гелия».
Однако теория сверхпроводимости была создана позднее. В её основе лежит концепция куперовской электронной пары — коррелированного состояния связывающих электронов с противоположными спинамии и импульсами, и, следовательно, сверхпроводимость можно рассматривать как сверхтекучесть электронного газа, состоящего из куперовских пар электронов, через ионную кристаллическую решётку. В 1972 году авторам теории БКШ — Бардину, Куперу и Шрифферу присуждена Нобелевская премия по физике «За создание теории сверхпроводимости, обычно называемой БКШ-теорией».
Характерные кристаллические решётки[править | править код]
Большинство металлов образует одну из следующих высокосимметричных решёток с плотной упаковкой атомов: кубическую объемно центрированную, кубическую гранецентрированную и гексагональную.
В кубической объемно центрированной решётке (ОЦК) атомы расположены в вершинах куба и один атом в центре объёма куба. Кубическую объемно центрированную решётку имеют металлы: Pb, K, Na, Li, β-Ti, β-Zr, Ta, W, V, α-Fe, Cr, Nb, Ba и др.
В кубической гранецентрированной решётке (ГЦК) атомы расположены в вершинах куба и в центре каждой грани. Решётку такого типа имеют металлы: α-Ca, Ce, α-Sr, Pb, Ni, Ag, Au, Pd, Pt, Rh, γ-Fe, Cu, α-Co и др.
В гексагональной решётке атомы расположены в вершинах и центре шестигранных оснований призмы, а три атома — в средней плоскости призмы. Такую упаковку атомов имеют металлы: Mg, α-Ti, Cd, Re, Os, Ru, Zn, β-Co, Be, β-Ca и др.
Другие свойства[править | править код]
Свободно движущиеся электроны обусловливают высокую электро- и теплопроводность. Многие металлы обладают высокой твёрдостью, например хром, молибден, тантал, вольфрам и др. Вещества, обладающие металлической связью, часто сочетают прочность с пластичностью, так как при смещении атомов друг относительно друга не происходит разрыв связей.
