Какими химическими свойствами обладают амфотерные гидроксиды
Прежде чем рассуждать о химических свойствах оснований и амфотерных гидроксидов, давайте четко определим, что же это такое?
1) К основаниями или основным гидроксидам относят гидроксиды металлов в степени окисления +1 либо +2, т.е. формулы которых записываются либо как MeOH , либо как Me(OH)2. Однако существуют исключения. Так, гидроксиды Zn(OH)2, Be(OH)2, Pb(OH)2, Sn(OH)2 к основаниям не относятся.
2) К амфотерным гидроксидам относят гидроксиды металлов в степени окисления +3,+4, а также в качестве исключений гидроксиды Zn(OH)2, Be(OH)2, Pb(OH)2, Sn(OH)2. Гидроксиды металлов в степени окисления +4, в заданиях ЕГЭ не встречаются, поэтому рассмотрены не будут.
Химические свойства оснований
Все основания подразделяют на:
Напомним, что бериллий и магний к щелочноземельным металлам не относятся.
Помимо того, что щелочи растворимы в воде, они также очень хорошо диссоциируют в водных растворах, в то время как нерастворимые основания имеют низкую степень диссоциации.
Такое отличие в растворимости и способности к диссоциации у щелочей и нерастворимых гидроксидов приводит, в свою очередь, к заметным отличиям в их химических свойствах. Так, в частности, щелочи являются более химически активными соединениями и нередко способны вступать в те реакции, в которые не вступают нерастворимые основания.
Взаимодействие оснований с кислотами
Щелочи реагируют абсолютно со всеми кислотами, даже очень слабыми и нерастворимыми. Например:
Нерастворимые основания реагируют практически со всеми растворимыми кислотами, не реагируют с нерастворимой кремниевой кислотой:
Следует отметить, что как сильные, так и слабые основания с общей формулой вида Me(OH)2 могут образовывать основные соли при недостатке кислоты, например:
Взаимодействие с кислотными оксидами
Щелочи реагируют со всеми кислотными оксидами, при этом образуются соли и часто вода:
Нерастворимые основания способны реагировать со всеми высшими кислотными оксидами, соответствующими устойчивым кислотам, например, P2O5, SO3, N2O5, с образованием средних солей:
<.p>
Нерастворимые основания вида Me(OH)2 реагируют в присутствии воды с углекислым газом исключительно с образованием основных солей. Например:
Cu(OH)2 + CO2 = (CuOH)2CO3 + H2O
С диоксидом кремния, ввиду его исключительной инертности, реагируют только самые сильные основания — щелочи. При этом образуются нормальные соли. С нерастворимыми основаниями реакция не идет. Например:
Взаимодействие оснований с амфотерными оксидами и гидроксидами
Все щелочи реагируют с амфотерными оксидами и гидроксидами. Если реакцию проводят, сплавляя амфотерный оксид либо гидроксид с твердой щелочью, такая реакция приводит к образованию безводородных солей:
Если же используют водные растворы щелочей, то образуются гидроксокомплексные соли:
В случае алюминия при действии избытка концентрированной щелочи вместо соли Na[Al(OH)4] образуется соль Na3[Al(OH)6]:
Взаимодействие оснований с солями
Какое-либо основание реагирует с какой-либо солью только при соблюдении одновременно двух условий:
1) растворимость исходных соединений;
2) наличие осадка или газа среди продуктов реакции
Например:
Термическая устойчивость оснований
Все щелочи, кроме Ca(OH)2, устойчивы к нагреванию и плавятся без разложения.
Все нерастворимые основания, а также малорастворимый Ca(OH)2 при нагревании разлагаются. Наиболее высокая температура разложения у гидроксида кальция – около 1000oC:
Нерастворимые гидроксиды имеют намного более низкие температуры разложения. Так, например, гидроксид меди (II) разлагается уже при температуре выше 70 oC:
Химические свойства амфотерных гидроксидов
Взаимодействие амфотерных гидроксидов с кислотами
Амфотерные гидроксиды реагируют с кислотами:
Амфотерные гидроксиды металлов в степени окисления +3, т.е. вида Me(OH)3, не реагируют с такими кислотами, как H2S, H2SO3 и H2СO3 ввиду того, что соли, которые могли бы образоваться в результате таких реакций, подвержены необратимому гидролизу до исходного амфотерного гидроксида и соответствующей кислоты:
Взаимодействие амфотерных гидроксидов с кислотными оксидами
Амфотерные гидроксиды реагируют с высшими оксидами, которым соответствуют устойчивые кислоты (SO3, P2O5, N2O5):
Амфотерные гидроксиды металлов в степени окисления +3, т.е. вида Me(OH)3, не реагируют с кислотными оксидами SO2 и СO2.
Взаимодействие амфотерных гидроксидов с основаниями
Из оснований амфотерные гидроксиды реагируют только с щелочами. При этом, если используется водный раствор щелочи, то образуются гидроксокомплексные соли:
А при сплавлении амфотерных гидроксидов с твердыми щелочами получаются их безводные аналоги:
Взаимодействие амфотерных гидроксидов с основными оксидами
Амфотерные гидроксиды реагируют при сплавлении с оксидами щелочных и щелочноземельных металлов:
Термическое разложение амфотерных гидроксидов
Все амфотерные гидроксиды не растворимы в воде и, как любые нерастворимые гидроксиды, разлагаются при нагревании на соответствующий оксид и воду:
Определение
Амфотерность (от др.-греч. амфотеро — «двойственный», «обоюдный») — способность некоторых соединений проявлять в зависимости от условий как кислотные, так и основные свойства.
Понятие амфотерность как характеристика двойственного поведения вещества было введено в 1814 г. Ж. Гей-Люссаком и Л. Тенаром.
А. Ганч в рамках общей химической теории кислотно-основных взаимодействий (1917-1927 г.г.) предложил следующее определение:
Определение
Амфотерность — способность некоторых соединений проявлять как кислотные, так и основные свойства в зависимости от условий и природы реагентов, участвующих в кислотно-основном взаимодействии, особенно в зависимости от свойств растворителя.
Амфотерными называют соединения, которые в зависимости от условий могут быть как донорами катионов водорода и проявлять кислотные свойства, так и их акцепторами, то есть проявлять основные свойства.
Запомнить! Амфотерными свойствами обладают оксиды и гидроксиды
элементов главных подгрупп — бериллий, алюминий, галлий, мышьяк, сурьма, селен и др.,
элементов побочных подгрупп — хром, цинк, медь (II), железо (III), молибден, вольфрам и др.
Обычно в химическом поведении гидроксидов преобладает или кислотный, или основный характер. Амфотерными свойствами обладают также некоторые органические соединения. Например, аминокислоты $(NH_2)R-COOH$, содержат в своей структуре одновременно карбоксильную группу -СООН, обуславливающую кислотные свойства, то есть являющуюся донором протона водорода, и амино-группу $NH_2$, обеспечивающую основные свойства, то есть являющуюся акцептором протонов водорода за счет неподеленной электронной пары азота.
Получение амфотерных гидроксидов
Общим способом получения амфотерных гидроксидов является осаждение разбавленной щёлочью из растворов солей соответствующего амфотерного элемента, например:
$ZnSO_4 + 2NaOH longrightarrow Zn(OH)_2 downarrow+ Na_2SO_4$
В ряде случаев при осаждении образуется не гидроксид, а гидрат оксида соответствующего элемента (например, гидраты оксидов железа(III), хрома(III), олова(II) и др.). Химические свойства таких гидратов по большей части аналогичны свойствам соответствующих гидроксидов.
Общие химические свойства амфотерных гидроксидов
Все амфотерные гидроксиды являются твёрдыми веществами. Нерастворимы в воде, в основном являются слабыми электролитами.
1. При нагревании разлагаются с образованием соответствующего амфотерного оксида, например:
$2Fe(OH)_3 xrightarrow{150-200^0 C} Fe_2O_3 + 3H_2O$
2. При взаимодействии с кислотами образуют растворимые соли, содержащие амфотерный катион, например:
$Zn(OH)_2 downarrow + 2HCl longrightarrow ZnCl_2 + 2H_2O$
3. При взаимодействии со щёлочью образуют растворимые соли с амфотерным элементом в анионе, например:
$Zn(OH)_2 downarrow + 2NaOH rightarrow Na_2[Zn(OH)_4]$
При сплавлении со щелочами образуют средние соли с амфотерным элементом в ионе кислотного остатка:
$Zn(OH)_2 downarrow + 2NaOH xrightarrow[]{t, ^circ C} Na_2ZnO_2 + 2H_2O$
Химические свойства амфотерных гидроксидов
Амфотерность может проявляться как способность вещества к взаимодействию как с кислотами, так и с основаниями.
Это характерно для оксидов, гидроксидов и комплексных соединений некоторых p-элементов и большинства d-элементов в промежуточных степенях окисления. Амфотерность в той или иной степени является общим свойством гидроксидов. Например, для соединений хрома (III) характерны следующие реакции:
$Cr(OH)_3$ (тв) + $3HCl$ (р-р) $ longrightarrow CrCl_3$ (р-р) + $3H_2O$
$Cr(OH)_3$ (тв) + NaOH (р-р) + $2H_2O longrightarrow Na[Cr(OH)_4(H_2O)_2]$ (р-р)
$Cr_2O_3$ (тв) + 6HCl (р-р) $ longrightarrow 2CrCl_3$ (р-р) + $3H_2O$
$Cr_2O_3$ (тв) + $Na_2CO_3$ (плавл)$ longrightarrow 2NaCrO_2 + CO_2$ (газ)
Традиционные представления о проявлении амфотерности гидроксидов как диссоциации по кислотному и основному типам не являются достаточно точными. В общем виде амфотерное поведение нерастворимых гидроксидов хрома (III), алюминия, цинка может быть описано как реакции ионного обмена гидратированных комплексов с ионами гидроксония и гидроксил-анионами $H_3O^+$ и $OH^–$. Например, для $Al(OH_3)$ ионные равновесия могут быть записаны следующим образом:
$[Al(OH)_3(H_2O)_3] + 3H_3O^+ leftrightarrow [Al(H_2O)_6]^{3+} + 3H_2O$ (в кислой среде)
$[Al(OH)_3(H_2O)_3] + 3OH^- leftrightarrow [Al(OH)_6]^{3-}$ (в щелочной среде)
В ряде случаев важным косвенным признаком амфотерности является способность элемента образовывать два ряда солей, катионного и анионного типа. Например, для цинка:
$ZnCl_2$ и $[Zn(H_2O)_4]SO_4$ (катионные))
$Na_2ZnO_2$ и $Na_2]Zn(OH)_4]$ (анионные).
Ключевые слова конспекта: амфотерность, амфотерные оксиды, амфотерные гидроксиды,
ГИДРОКСИДЫ
Гидроксиды – это неорганические соединения, образованные тем или иным элементом, кислородом и водородом. В гидроксидах обязательно имеется водород, связанный с кислородом (связь О–Н). В некоторых гидроксидах водород может непосредственно соединяться с атомами элемента. Например, в H3РO3 два атома водорода связаны с атомами кислорода, а один – с атомом фосфора.
В ряде случаев гидроксиды являются продуктами гидратации (соединения с водой) соответствующих оксидов, хотя многие оксиды непосредственно с водой не взаимодействуют. В результате дегидратации гидроксидов образуются соответствующие оксиды.
Гидроксиды могут быть основными (основания), кислотными (кислородсодержащие кислоты) и амфотерными. Примерами основных гидроксидов являются NaOH, Ва(ОН)2, Mg(OH)2. Примерами кислотных гидроксидов являются НСlO4 (хлорная кислота, высший гидроксид хлора), H3РO4 (ортофосфорная кислота, высший гидроксид фосфора), H2SO4 (серная кислота, высший гидроксид серы).
Графические формулы перечисленных гидроксидов приведены ниже. Во всех гидроксидах имеется связь О–Н:
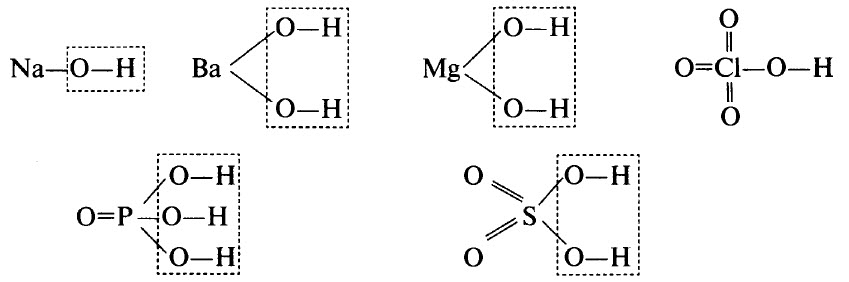
ПОНЯТИЕ ОБ АМФОТЕРНЫХ ОКСИДАХ И ГИДРОКСИДАХ
Амфотерность (от греч. amphoteros – и тот, и другой) – способность химических соединений проявлять и кислотные, и основные свойства в зависимости от природы реагента, с которым амфотерное вещество вступает в кислотно-основное взаимодействие.
Амфотерные оксиды и гидроксиды – оксиды и гидроксиды, проявляющие как основные, так и кислотные свойства. Они реагируют как с кислотами, так и с основаниями. Амфотерным оксидам соответствуют амфотерные гидроксиды, например: ВeО – Вe(ОН)2, Сr2O3 – Сr(ОН)3.
Амфотерные гидроксиды практически нерастворимы в воде. Их основные и кислотные свойства выражены слабо, они являются слабыми кислотами и слабыми основаниями.
Амфотерными оксидами и гидроксидами являются, как правило, оксиды и гидроксиды металлов, в которых степень окисления металла +3, +4, иногда +2.
Среди оксидов элементов главных подгрупп амфотерными являются: BeO, Al2O3, SnO, SnO2, PbO, Sb2O3.
Амфотерными гидроксидами являются следующие гидроксиды элементов главных подгрупп: Ве(ОН)2, Al(ОН)3, Рb(ОН)2 и некоторые другие.
Оксиды и гидроксиды элементов побочных подгрупп, соответствующие высоким степеням окисления, как правило, являются кислотными, например: СrO3 (ему соответствует H2СrO4), Мn2O7 (ему соответствует НМnO4).
Для низших оксидов и гидроксидов характерно преобладание основных свойств, например: СrO и Сr(ОН)2, МnО и Мn(ОН)2.
Оксиды и гидроксиды, в которых степени окисления элементов +3 и +4, являются, как правило, амфотерными: Сг2O3 и Cr(OH)3, Fe2O3 и Fe(OH)3. Однако последние элементы в декадах d–элементов (например, Zn) образуют амфотерные оксиды и гидроксиды даже в низких степенях окисления, например ZnO и Zn(OH)2.
ХИМИЧЕСКИЕ СВОЙСТВА АМФОТЕРНЫХ ОКСИДОВ И ГИДРОКСИДОВ
Рассмотрим амфотерные свойства оксида и гидроксида цинка – ZnO и Zn(OH)2. Оба вещества реагируют с кислотами:
ZnO + 2HNO3 = Zn(NO3)2 + H2O
Zn(OH)2 + H2SO4 = ZnSO4 + 2H2O
Оксид и гидроксид цинка реагируют также и со щелочами:
В результате реакций со щелочами в растворах образуются комплексные ионы – тетрагидроксоцинкаты (например, Na2[Zn(OH)4]), а при сплавлении – цинкаты (например, Na2ZnO2). Чтобы составить формулы цинкатов, запишите формулу гидроксида цинка Zn(OH)2 как формулу кислоты – H2ZnO2. Кислотным остатком такой кислоты является ион ZnO22–.
При диссоциации этих солей в растворах образуются ионы, в которых цинк входит в состав анионов, поэтому говорят, что в этих соединениях «цинк в анионной форме».
Докажем амфотерность оксида и гидроксида алюминия Al(ОН)3. Он растворяется в кислотах с образованием солей, где алюминий находится в катионной форме:
Al(ОН)3 + 3Н+ = Al3+ + 3H2O
Но гидроксид алюминия взаимодействует и со щелочами. При сплавлении со щелочами образуются алюминаты (метаалюминаты):
Al(ОН)3 + NaOH = NaAlO2 + 2H2O
Чтобы составить формулы алюминатов, запишите формулу гидроксида алюминия Al(ОН)3 как H3AlO3. Теперь представьте, что от 1 моль этого соединения отщепляется 1 моль воды. Образуется соединение НАlO2, в котором кислотным остатком будет ион AlO2–.
В образовавшейся соли алюминий образует анион AlO2– (алюминий в анионной форме). В растворах в результате реакции со щёлочью образуется комплексный тетрагидроксоалюминат-ион [Al(ОН)4]–:
Al(ОН)3 + NaOH = Na[Al(OH)4] (тетрагидроксоалюминат натрия)
Некоторые амфотерные оксиды и гидроксиды не проявляют амфотерность в обычных условиях и в растворах ведут себя как основные. Амфотерность таких соединений проявляется в более жёстких условиях. Например, гидроксид железа (III) Fe(OH)3 легко реагирует с кислотами:
Fe(OH)3 + 3НCl = FeCl3 + 3H2O
Fe(OH)3 + NaOH = NaFeO2 + 2H2O
Признаком этой реакции будет растворение бурого осадка. А вот при добавлении раствора щёлочи гидроксид железа (III) не растворяется. Тогда, может быть, считать его основанием, не растворимым в воде? Дело в том, что в данном случае соль образуется при плавлении со щёлочью.
Естественно, что в ходе плавления происходит разложение гидроксида на оксид и воду, и в действительности реакция идёт между оксидом и щёлочью:
Fe2O3 + 2NaOH = 2NaFeO2 + H2O
Таким образом, гидроксид железа (III) можно отнести к амфотерным гидроксидам, хотя основные свойства у него преобладают.
Конспект урока «Амфотерные оксиды и гидроксиды».
Следующая тема: «».
6.3.
Амфотерные гидроксиды, их свойства
Амфотерные гидроксиды – электролиты,
образующие при диссоциации одновременно катионы Н+и анионы ОН–:
X+ + OH– ⇌ ХOH = HXO ⇌ H++ XO–.
Амфотерные гидроксиды в кислой среде ведут
себя как основания, а в щелочной – как кислоты.
K амфотерным гидроксидам относятся Be(OH)2,
Zn(OH)2, Pb(OH)2, Sn(OH)2, Al(OH)3,
Fe(OH)3,
Cr(OH)3 и некоторые
другие, им соответствуют амфотерные оксиды. Практически все они нерастворимы в
воде, являются слабыми электролитами и диссоциируют ступенчато.
Химические свойства
амфотерных гидроксидов
Например:
2Al(OH)3 + Na2O 2NaAlO2 + 3H2O↑.
Некоторые
амфотерные гидроксиды (Be(OH)2, Zn(OH)2, Pb(OH)2)
реагируют с кислотным оксидом СО2 с образованием осадков
основных солей и воды. Например:
2Be(OH)2 +
CO2 = (BeOH)2CO3 +
H2O.
Например:
Zn(OH)2 +
2KOH (тв.) K2ZnO2 + 2H2O↑,
Zn(OH)2 + 2KOH = K2[Zn(OH)4].
Например:
Al(OH)3 +
3HCl = AlCl3 + 3H2O.
Все
амфотерные гидроксиды (как и большинство оснований) разлагаются при нагревании
на оксид и воду. Например:
2Al(OH)3 Al2O3 +
3H2O.
В связи с
этим нужно учитывать, что фактически в процессе сплавления их со щелочами и
оксидами участвует не сам амфотерный гидроксид, а соответствующий ему оксид.
УПРАЖНЕНИЯ
1) СО2 и
HCl 2) Н2 и NaOH 3) NО
и NaNO3 4) H2SO4 и NaOH
Решение: Гидроксид хрома –
амфотерный гидроксид. Амфотерные гидроксиды реагируют с кислотами и щелочами, с
кислотыми и основными оксидами. Поэтому нам подходит вариант 4 –серная кислота
и гидроксид натрия (щелочь):
2Cr(OH)3 + 3H2SO4 = Cr2(SO4)3 + 6H2O
Cr(OH)3 + NaOH
= Na[Cr(OH)4]
Ответ: 4
________________________________________________________________
2.
Гидроксид калия взаимодействует с каждым из
двух веществ
1) нитратом натрия и нитратом серебра
2) гидроксидом алюминия и нитратом серебра
3) гидроксидом цинка и оксидом меди(I)
4) хлоридом бария и оксидом фосфора(V)
Решение:
Гидроксид калия это щелочь. она взаимодействует
с кислотами,кислотными оксидами, амфотерными оксидами и гидроксидами,растворами
солей при условии, если есть признак необратимости реакции (осадок,
газ, слабый электролит). Данному условию соответствует набор веществ
в варианте 2 — амфотерный гидроксид и соль.
________________________________________________________________
3.
Осуществить превращения:
Al-1-
Al2O3 -2— NaAlO2 -3—
Al (OH)3 -4— Al2O3
1. 4Al + 3O2 = 2Al2O3
2. Al2O3 + Na2O 2NaAlO2
3. NaAlO2 + HCl + H2O = NaCl + Al(OH)3
4. 2Al(OH)3 Al2O3 +3H2O
________________________________________________________________
4.
Осуществить превращения:
AlCl3 —1—
Al(OH)3 -2— Na[Al (OH)4] —3—
AlCl3
1. AlCl3 + 3NaOH = 3NaCl + Al(OH)3 |
2. Al(OH)3 + NaOH = Na[ Al(OH)4 ]
3. Na[ Al(OH)4 ]+ 4HCl = NaCl + AlCl3 + 4H2O
________________________________________________________________
ЗАДАНИЯ ДЛЯ САМОСТОЯТЕЛЬНОГО
РЕШЕНИЯ
1.
Закончите уравнения реакций:
Cr(OH)3 +
6HCl = ?
Cr(OH)3 +
NaOH = ?
2.
Напишите уравнения реакций, описывающие следующие
химические превращения:
а)
ZnCl2 + KOH(избыток) → осадок → растворение осадка;
б)
Cr(NO3)2 +
NaOH(избыток) → осадок
→ растворение осадка.
3.
Закончи уравнения реакций:
4. В предложенных рядах исключи (вычеркни) одну лишнюю
формулу – такую, которая не образует с остальными однородную группу. Объясни
свой выбор.
а)
HClO4, H2SO3, HNO3, H3PO4;
б) KOH, Mg(OH)2, Al(OH)3;
в)
HBr, HCl, HF; г) Mg(OH)2, Ca(OH)2, Zn(OH)2,
Ba(OH)2;
д) H2CO3,
H2SO3, HNO3; е) ZnO, BeO, MgO.
5. Составь уравнения реакций, соответствующие схемам:
1) Zn Na2→ZnO2 → ZnSO4 → Zn(OH)2 → ZnO;
2) Al2O3 → X → Al(OH)3 → Y → AlCl3;
6. Предложи cпособ разделения смеси KOH,
Mg(OH)2, Fe(OH)3. Напиши уравнения реакций.
………………………………………………………………………………………
……………………………………………………………………………………..
………………………………………………………………………………………
7.
Осуществите следующие превращения:
Al2O3 → Al → Al2O3 → NaAlO2 → AlCl3
8. Из порошкообразной смеси, содержащей
Na2CO3, Fe, Al и
BaSO4, выделите химическим путем все соединения в чистом виде.
Напишите уравнения реакций и последовательность их проведения (опишите
технологию всей работы).
9. Напишите схему диссоциации
гидроксида хрома (III), а также молекулярное и ионное уравнения реакций
растворения его в:
а) азотной кислоте;
б) растворе гидроксида натрия.
10. Заполни таблицу по химическим свойствам амфотерных гидроксидов
(укажи продукты реакций). Напиши уравнения реакций на примере Zn(OH)2.
Вещества-реагенты | Продукты реакции с амфотерными | |
Основный оксид | щелочных/ щелочно-земельных металлов | ………………………………………………………….. |
остальных металлов | ………………………………………………………….. | |
Амфотерный оксид | ………………………………………………………….. | |
Kислотный оксид | ………………………………………………………….. | |
Основание | растворимое (щелочь) | ………………………………………………………….. |
нерастворимое | ………………………………………………………….. | |
Амфотерный гидроксид | ………………………………………………………….. | |
Kислота | ………………………………………………………….. | |
Соль | ………………………………………………………….. | |
Металл | ………………………………………………………….. | |
Неметалл | ………………………………………………………….. | |
Термическое разложение | ………………………………………………………….. | |
1. В отличие от гидроксида калия гидроксид алюминия | |
а) хлоридом натрия | б) соляной кислотой |
в) гидроксидом натрия (р-р) | г) серной кислотой |
2. Гидроксид меди (II) | |
а) | б) меди с водой |
в) водных растворов хлорида меди (II) и гидроксида натрия | г) меди и водного раствора гидроксида |
3. В каких группах указаны формулы веществ, все из | |
а) Al, | б) P2O5, Al, |
в) Mn2O7, ZnO, | г) CO2, |
4. Действием каких веществ из гидроксида калия нельзя | |
а) нитрат натрия | б) азотная кислота |
в) нитрат меди (II) | г) оксид азота (V) |
5. Укажите схемы реакций, в результате протекания | |
а)Al2O3 + H2O → | б)Al2O3 + KOH (р-р)→ |
в)AlCl3 + K→ | г) Al2(SO4)3 + |
6. В каких парах между веществами при определенных | |
а) гидроксид калия и оксид кремния (IV) | б) хлорид калия и гидроксид бария |
в) железа и гидроксид натрия | г) гидроксид кальция и оксид углерода |
7. Щелочи могут реагировать: | |
а) только с сильными кислотами | б) все ответы верны |
в) только с кислотными оксидами | г) как с кислотными, так и с |
8. Укажите формулы веществ, с водными растворами | |
а)NaOH (разб.) | б) HCl |
в)все ответы | г) KCl |
9. Основание не образуется при взаимодействии избытка | |
а) сульфатом алюминия | б) хлоридом железа (II) |
в) нитратом аммония | г) все ответы верны |
10. Гидроксид алюминия проявляет кислотные свойства, | |
а) соляной кислотой | б) гироксидом калия |
в) серной кислотой | г) нет верного ответа |
Ответы:
1 | в |
2 | в |
3 | г |
4 | а |
5 | г |
6 | а |
7 | г |
8 | б |
9 | а |
10 | б |
