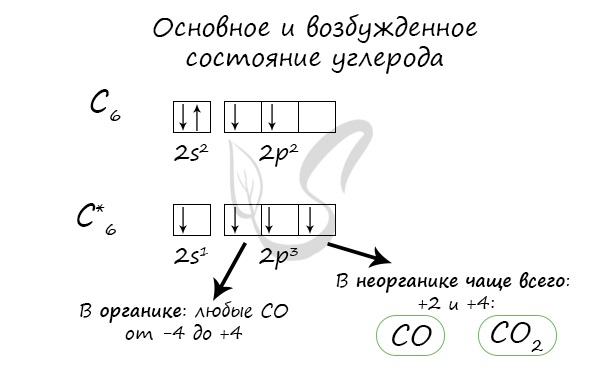
Какими химическими свойствами обладает углерод

Óãëåðîä (Ñ) íàõîäèòñÿ â IV ïîäãðóïïå ïåðèîäè÷åñêîé òàáëèöû Ä.È. Ìåíäåëååâà. Íà âíåøíåì óðîâíå 4 íåñïàðåííûõ ýëåêòðîíà. Óãëåðîä – íåìåòàëë. Îáëàäàåò âîññòàíîâèòåëüíûìè ñâîéñòâàìè.
Àëëîòðîïèÿ óãëåðîäà.
Óãëåðîä ñóùåñòâóåò â íåñêîëüêèõ àëëîòðîïíûõ ìîäèôèêàöèÿõ:
— ãðàôèò (èìååò ñëîèñòóþ ñòðóêòóðó, î÷åíü ïëàñòè÷åí),
— àëìàç (ñàìîå òâåðäîå ñîåäèíåíèå),
— Ñ60 (ôóëëåðåí).
Èç ãðàôèòà ìîæíî ïîëó÷èòü àëìàç ïóòåì äëèòåëüíîãî íàãðåâà ïðè âûñîêèì äàâëåíèåì. È àëìàç è ãðàôèò èìåþò ðàçëè÷íûå êðèñòàëëè÷åñêèå ðåøåòêè, âñëåäñòâèå ÷åãî íàáëþäàþòñÿ ðàçëè÷èÿ â ñâîéñòâàõ.
Õèìè÷åñêèå ñâîéñòâà óãëåðîäà.
1. Âçàèìîäåéñòâèå ñ êèñëîðîäîì:
Ñ + Î2 + ÑÎ2,
 íåäîñòàòêå êèñëîðîäà îáðàçóþòñÿ ìîíîîêñèäû:
2Ñ +Î2 = 2ÑÎ,
2. Ñî ñëîæíûìè âåùåñòâàìè:
Ñ + Î2 = 2ÑÎ,
Ñ + ÑÎ2 = 2ÑÎ,
3. Ïðè îáû÷íîé òåìïåðàòóðå âçàèìîäåéñòâóåò ñî ôòîðîì, ïðè íàãðåâàíèè – ñ õëîðîì, ñåðîé è àçîòîì:
4C + S8 = 4CS2,
2C + N2 = C2N2,
Ñ êðåìíèåì óãëåðîä îáðàçóåò êàáðîðóíä – ñîåäèíåíèå ïî òâåðäîñòè ñðàâíèìîå ñ àëìàçîì:
Si + C = SiC,
4. Ðàçáàâëåííûå êèñëîòû íå äåéñòâóþò íà óãëåðîä, à êîíöåíòðèðîâàííûå îêèñëÿþò:
C + 2H2SO4 = CO2 + 2SO2 + 2H2O,
5. Óãëåðîä ó÷àñòâóåò â ðåàêöèÿõ â êà÷åñòâå âîññòàíîâèòåëÿ:
CuO + C = C + CO,
6. Ïðè íàãðåâå âçàèìîäåéñòâóåò ñ îêñèäàìè àêòèâíûõ ìåòàëëîâ, îáðàçóÿ êàðáèäû:
CaO + 3C = CaC2 + CO,
7. Ïðè âçàèìîäåéñòâèè ñ ìåòàëëàìè óãëåðîä âûñòóïàåò â êà÷åñòâå îêèñëèòåëÿ:
Ca + 2C = CaC2.
Êàëüêóëÿòîðû ïî õèìèè | |
| Õèìèÿ îíëàéí íà íàøåì ñàéòå äëÿ ðåøåíèÿ çàäà÷ è óðàâíåíèé. | |
| Êàëüêóëÿòîðû ïî õèìèè | |
Õèìè÷åñêèå ýëåìåíòû | |
| Õèìè÷åñêèå ýëåìåíòû Ïåðèîäè÷åñêîé ñèñòåìû Ìåíäåëååâà, ñâîéñòâà, âàëåíòíîñòü õèìè÷åñêèõ ýëåìåíòîâ | |
| Õèìè÷åñêèå ýëåìåíòû | |
Õèìèÿ 7,8,9,10,11 êëàññ, ÅÃÝ, ÃÈÀ | |
| Îñíîâíàÿ èíôîðìàöèÿ ïî êóðñó õèìèè äëÿ îáó÷åíèÿ è ïîäãîòîâêè â ýêçàìåíàì, ÃÂÝ, ÅÃÝ, ÎÃÝ, ÃÈÀ | |
| Õèìèÿ 7,8,9,10,11 êëàññ, ÅÃÝ, ÃÈÀ | |
Ñîåäèíåíèÿ õèìè÷åñêèõ ýëåìåíòîâ | |
| Àëêàíû, âîäà, ãàëîãåíû, ìûëà, æèðû, ãèäðîêñèäû; îêñèäû, õëîðèäû, ïðîèçâîäíûå õèìè÷åñêèõ ýëåìåíòîâ òàáëèöû Ìåíäåëååâà | |
| Ñîåäèíåíèÿ õèìè÷åñêèõ ýëåìåíòîâ | |
Âîäà. Ñâîéñòâà âîäû. | |
| Âîäà íàèáîëåå øèðîêî ðàñïðîñòðàí¸ííîå ñîåäèíåíèå íà íàøåé ïëàíåòå. | |
| Âîäà. Ñâîéñòâà âîäû. | |
Éîä. Ñâîéñòâà éîäà. | |
| Éîä ( I 2 ) íàõîäèòñÿ â 7-îé ãðóïïå ïåðèîäè÷åñêîé òàáëèöû Ä. | |
| Éîä. Ñâîéñòâà éîäà. | |
Углерод
Углерод — неметаллический элемент IV группы периодической таблицы Д.И. Менделеева, является важнейшей частью всех органических
веществ в природе.

Общая характеристика элементов IVa группы
От C к Pb (сверху вниз в периодической таблице) происходит увеличение: атомного радиуса, металлических, основных, восстановительных свойств.
Уменьшается электроотрицательность, энергия ионизация, сродство к электрону.
Из элементов IVа группы углерод и кремний относятся к неметаллам, германий, олово и свинец — металлы.
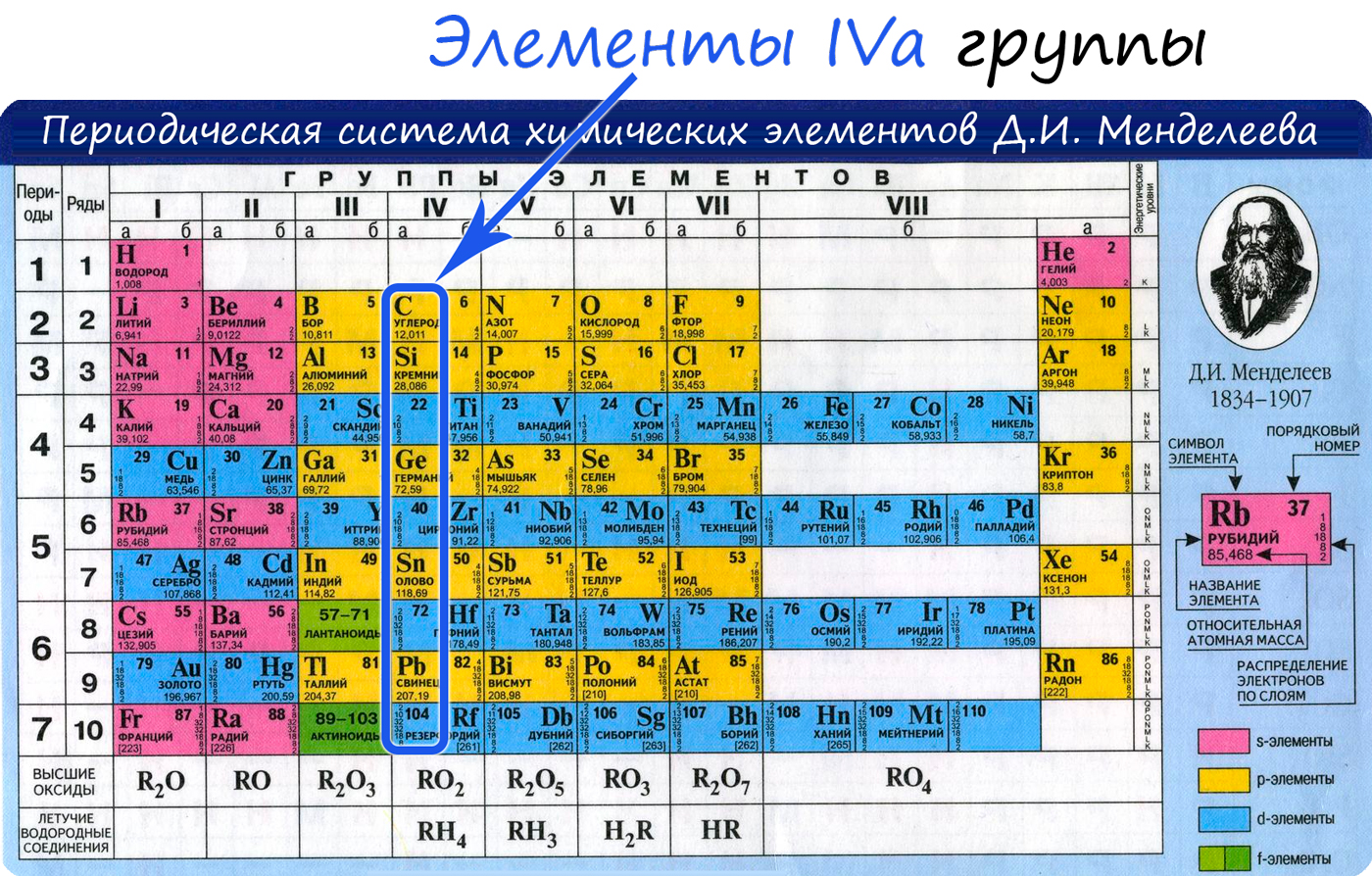
Электронные конфигурации у данных элементов схожи, так как они находятся в одной группе (главной подгруппе!), общая формула ns2np2:
- C — 2s22p2
- Si — 3s23p2
- Ge — 4s24p2
- Sn — 5s25p2
- Pb — 6s26p2
Природные соединения
В природе углерод встречается в виде следующих соединений:
- Аллотропных модификаций — графит, алмаз, фуллерен
- MgCO3 — магнезит
- CaCO3 — кальцит (мел, мрамор)
- CaCO3*MgCO3 — доломит

Получение
Углерод получают в ходе пиролиза углеводородов (пиролиз — нагревание без доступа кислорода). Также применяется получение углеродистых соединений:
древесины и каменного угля.
C2H6 → (t) C + H2 (пиролиз этана)
Химические свойства
- Реакции с неметаллами
- Реакции с металлами
- Восстановительные свойства
- Реакция с водой
- Реакции с кислотами
При нагревании углерод реагирует со многими неметаллами: водородом, кислородом, фтором.
C + H2 → (t) CH4 (метан)
2С + O2 → (t) 2CO (угарный газ — продукт неполного окисления углерода, образуется при недостатке кислорода)
С + O2 → (t) CO2 (углекислый газ — продукт полного окисления углерода, образуется при достаточном количестве кислорода)
С + F2 → (t) CF4
При нагревании углерод реагирует с металлами, проявляя свои окислительные свойства. Напомню, что металлы могут принимать только положительные
степени окисления.
Ca + C → CaC2 (карбид кальция, СО углерода = -1)
Al + C → Al4C3 (карбид алюминий, СО углерода -4)
Очевидно, что степень окисления углерода в соединении с различными металлами может отличаться.

Углерод — хороший восстановитель. С помощью него металлургическая промышленность справляется с задачей получения чистых металлов из их
оксидов:
Fe2O3 + C → Fe + CO2
ZnO + C → Zn + CO
FeO + C → Fe + CO
Углерод восстанавливает не только металлы из их оксидов, но и неметаллы подобным образом:
SiO2 + C → (t) Si + CO
Может восстановить и собственный оксид:
CO2 + C → CO

Известная реакция взаимодействия угля с водяным паром, называемая также газификацией угля, торфа, сланца — крайне важна в промышленности:
C + H2O → CO↑ + H2↑
В реакциях с кислотами углерод проявляет себя как восстановитель:
C + HNO 3(конц.) → (t) CO2 + NO2 + H2
C + HNO3 → CO2 + NO + H2O
C + H2SO4(конц.) → CO2 + SO2 + H2O

Оксид углерода II — СO
Оксид углерода II — продукт неполного окисления углерода. Несолеобразующий оксид. Это чрезвычайно опасное вещество часто образуется
при пожарах в замкнутых помещениях, при прогревании машины в гараже.
Растворяясь в крови угарный газ (имеющий в 300 раз большее сродство к гемоглобину, чем кислород) легко выигрывает конкуренцию у кислорода
и занимает его место в эритроцитах. Отравление угарным газом нередко заканчивается летальным исходом.
Получение
В промышленности угарный газ получают восстановлением оксида углерода IV или газификацией угля (t = 1000 °С).
CO2 + C → (t) CO
C + H2O → (t) CO + H2
В лаборатории угарный газ получают при разложении муравьиной кислоты в присутствии серной:
HCOOH → (H2SO4) CO + H2O
Химические свойства
Полностью окисляется до углекислого газа в реакции с кислородом, восстанавливает оксиды металлов.
CO + O2 → CO2
Fe2O3 + CO → Fe + CO2
FeO + CO → Fe + CO2
Образование карбонилов — чрезвычайно токсичных веществ.
Fe + CO → (t) Fe(CO)5

Оксид углерода IV — CO2
Продукт полного окисления углерода. Относится к кислотным оксидам, соответствует угольной кислоте H2CO3. Бесцветный газ,
без запаха.
Получение
В промышленности углекислый газ получают при разложении известняка, в ходе производства алкоголя, при спиртовом брожении глюкозы.
CaCO3 → (t) CaO + CO2↑
C6H12O6 → C2H5OH + CO2↑
В лабораторных условиях используют реакцию мела (мрамора) с соляной кислотой.
CaCO3 + HCl → CaCl2 + H2O + CO2↑
Углекислый газ образуется при горении органических веществ:
C3H8 + O2 → CO2 + H2O

Химические свойства
- Реакция с водой
- Реакции с основными оксидами и основаниями
- Окислительные свойства
В результате реакции с водой образуется нестойкая угольная кислота, которая сразу же распадается на воду и углекислый газ.
CO2 + H2O ⇄ H2CO3
В ходе реакций с основаниями и основными оксидами углекислый газ образует соли угольной кислоты: средние — карбонаты (при избытке основания),
кислые — гидрокарбонаты (при избытке кислотного оксида).
2KOH + CO2 → K2CO3 + H2O (соотношение основание — кислотный оксид 2:1)
KOH + CO2 → KHCO3 (соотношение основание — кислотный оксид 1:1)
Na2O + CO2 → Na2CO3
При нагревании способен окислять металлы до их оксидов.
Zn + CO2 → (t) ZnO + CO

Угольная кислота
Слабая двухосновная кислота, существующая только в растворах, разлагается на воду и углекислый газ.

Химические свойства
- Качественная реакция
- Средние и кислые соли
- Нагревание солей угольной кислоты
Определить наличие карбонат-иона можно с помощью кислоты: такая реакция сопровождается «закипанием» — появлением пузырьков бесцветного
газа без запаха.
MgCO3 + HCl → MgCl2 + CO2↑ + H2O
Я не раз встречал описание реакций, связанных с этой кислотой, которое заслуживает нашего внимания. В задании было сказано, что
при добавлении к раствору гидроксида кальция углекислого газа осадок появлялся, при дальнейшем пропускании углекислого газа —
помутнение исчезало.
Это можно легко объяснить, вспомнив про способность угольной кислоты образовывать кислые соли, которые растворимы.
Ca(OH)2 + CO2 → CaCO3 (осадок выпадает)
CaCO3 + H2O + CO2 → Ca(HCO3)2 (осадок растворяется)

Чтобы сделать из средней соли (карбоната) — кислую соль (гидрокарбонат) нужно добавить угольную кислоту. Однако написать ее формулу
H2CO3 — ошибка. Ее следует записать в виде воды и углекислого газа.
Li2CO3 + CO2 + H2O → LiHCO3 (средняя соль + кислота = кислая соль)
Чтобы вернуть среднюю соль, следует добавить к кислой соли щелочь.
LiHCO3 + LiOH → Li2CO3 + H2O
При нагревании карбонаты распадаются на соответствующий оксид металла и углекислый газ, гидрокарбонаты — на соответствующий оксид
металла, углекислый газ и воду.
MgCO3 → (t) MgO + CO2
KHCO3 → (t) K2CO3 + CO2↑ + H2O
© Беллевич Юрий Сергеевич 2018-2020
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение
(в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов
без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования,
обратитесь, пожалуйста, к Беллевичу Юрию.
Углерод — это, пожалуй, основной и самый удивительный химический элемент на Земле, ведь с его помощью формируется колоссальное количество разнообразных соединений, как неорганических, так и органических. Углерод является основой всех живых существ, можно сказать, что углерод, наравне с водой и кислородом, — основа жизни на нашей планете! Углерод имеет разнообразие форм, которые не похожи ни по своим физико-химическим свойствам, ни по внешнему виду. Но всё это углерод!
История открытия углерода
Углерод был известен человечеству ещё с глубокой древности. Графит и уголь использовались ещё древними греками, а алмазы нашли применение в Индии. Правда, за графит частенько принимали похожие по внешнему виду соединения. Тем не менее, графит имел широкое применение в древности, в частности для письма. Даже его название происходит от греческого слова «графо» — «пишу». Графит сейчас используется в карандашах. Алмазами начали впервые торговать в Бразилии в первой половине 18 века, с этого времени открыто множество месторождений, а в 1970 году была разработана технология получения алмазов искусственным путём. Такие искусственные алмазы применяются в промышленности, натуральные же, в свою очередь, в ювелирном деле.
Углерод в природе
Содержание углерода в земной коре составляет всего около 0,15%. Казалось бы, один из основных элементов, а так мало… На самом деле, углерод подвержен постоянному круговороту из земной коры через биосферу в атмосферу и наоборот. Из углерода состоят природный газ, нефть, уголь, торф, известняки и многие другие соединения.
Наиболее значимое количество углерода собрано в атмосфере и гидросфере в виде углекислого газа. В атмосфере углерода содержится около 0,046%, а еще больше — в растворенном виде в Мировом Океане.
Кроме того, как мы видели выше, углерод является основой живых организмов. Например, в теле человека массой 70 кг содержится около 13 кг углерода! Это только в одном человеке! А углерод содержится также во всех растениях и животных. Вот и считайте…
 Круговорот углерода в природе
Круговорот углерода в природе
Аллотропные модификации углерода
Углерод — уникальный химический элемент, который образует так называемые аллотропные модификации, или, проще говоря, различные формы. Эти модификации подразделяются кристаллические, аморфные и в виде кластеров.
Кристаллические модификации имеют правильную кристаллическую решётку. К этой группе относятся: алмаз, фуллерит, графит, лонсдейлит, углеродные волокна и трубки. Подавляющее большинство кристаллических модификаций углерода на первых местах в рейтинге «Самые твёрдые материалы в мире» .
 Аллотропные формы углерода: a) лонсдейлит; б) алмаз;
Аллотропные формы углерода: a) лонсдейлит; б) алмаз;
в) графит; г) аморфный углерод; д) C60 (фуллерен); е) графен;
ж) однослойная нанотрубка
Аморфные формы образованы углеродом с небольшими примесями других химических элементов. Основные представители этой группы: уголь (каменный, древесный, активированный), сажа, антрацит.
Самыми сложными и высокотехнологичными являются соединения углерода в виде кластеров. Кластеры — это особая структура, при которой атомы углерода расположены таким образом, что образуют полую форму, которая заполнена изнутри атомами других элементов, например, воды. В этой группе не так уж и много представителей, в неё входят углеродные наноконусы, астралены и диуглерод.
 Графит — «тёмная сторона» алмаза
Графит — «тёмная сторона» алмаза
Применение углерода
Углерод и его соединения имеют огромное значение в жизнедеятельности человека. Из углерода образованы главные виды топлива на Земле — природный газ и нефть. Соединения углерода широко применяются в химической и металлургической промышленности, в строительстве, в машиностроении и медицине. Аллотропные модификации в виде алмазов используют в ювелирном деле, фуллерит и лонсдейлит в ракетостроении. Из соединений углерода изготавливаются различные смазки для механизмов, техническое оборудование и многое другое. Промышленность в настоящее время не может обойтись без углерода, он используется везде!
Углерод С находится в периодической таблице Менделеева под номером 6. Еще первобытные люди обратили внимание, что после сжигания древесины образуется уголь, которым можно рисовать на стенах пещеры. В составе любых органических соединений есть углерод. Наиболее изучены две аллотропные модификации углерода: графит и алмаз.
Графит — мягкое черное вещество, которое легко оставляет следы на бумаге, имеет металлический блеск.
Помимо этого, графит является отличным проводником тепла и электрического тока. Графит используют в промышленности для изготовления графитных смазок, а также для производства карандашей.
Графитовый сланец
[Deposit Photos]
В отличие от графита, структура алмаза (другой аллотропной модификации) напоминает тетраэдр. Кроме углерода, в состав алмаза также входят хром, кремний, алюминий, марганец, титан, железо. Наибольшую долю в составе алмаза углерод делит с азотом. Благодаря своей структуре он не проводит электрический ток и обладает слабой теплопроводностью. Алмазы используют для изготовления драгоценных камней — бриллиантов. Искусственно созданные алмазы используют для изготовления режущих инструментов, абразивных материалов.
[Wikipedia]
Еще одной аллотропной модификацией углерода признан фуллерен. Он состоит из множества атомов углерода, соединенных ковалентными связями. Молекулы в сложной структуре фуллерена удерживаются электростатическими и вандерваальсовыми силами. Свойства фуллерена еще не до конца изучены. Но уже известно, что благодаря своей способности поглощать свободные радикалы эта аллотропная модификация углерода может применяться при изготовлении лекарств.
Молекула фуллерена
[Deposit Photos]
Химические свойства углерода
1. Углерод является неметаллом и способен взаимодействовать с металлами и образовывать карбиды:
Ca + 2C = CaC₂
2. В кислородной среде углерод сгорает в два этапа:
2С + O₂ = 2CO
2СO₂ + О₂ = 2СО₂
3. При взаимодействии углерода и водорода получается органическое вещество — метан:
С + 2H₂ = CH₄
4. При испарении воды под раскаленным углем образуются угарный газ и водород:
C + H₂O = CO + H₂
5. Углерод не реагирует с хлором, бромом и йодом, но взаимодействует со фтором:
С + 2F₂ = CF₄
6. Реагирует с серой:
С + 2S = CS₂
7. Углерод способен восстанавливать металлы из их оксидов:
2ZnO + C = 2Zn + CO₂
8. При повышении температуры реакции углерод взаимодействует с серной кислотой:
C + 2H₂SO₄ = CO₂ + 2SO₂ + 2H₂O
Чтобы лучше изучить свойства этого элемента, рекомендуем провести несколько наглядных экспериментов.
Углерод в органической химии
Углерод занимает особое место в периодической cистеме. Благодаря своему строению он образует длинные цепочки связей линейной или циклической структуры. Известно более 10 миллионов органических соединений. Несмотря на свое разнообразие, на воздухе и под действием температуры они всегда будут превращаться в углекислый газ и воду.
[Deposit Photos]
Роль углерода в нашей повседневной жизни огромна. Без углекислого газа не будет происходить фотосинтез — один из основных биологических процессов.
Применение углерода
Углерод широко применяется в медицине для создания различных лекарств органической природы. Изотопы углерода позволяют проводить радиоуглеродный анализ. Без углерода невозможна работа металлургической промышленности. Уголь, сгорающий в твердотопливных пиролизных котлах, служит источником энергии. В нефтеперерабатывающей промышленности из органических соединений углерода производят бензин и дизельное топливо. В значительной мере углерод необходим для производства сахара. Также он применяется в синтезе органических соединений, важных для всех сфер повседневной жизни.
