Какими физическими и химическими свойствами обладают металлы
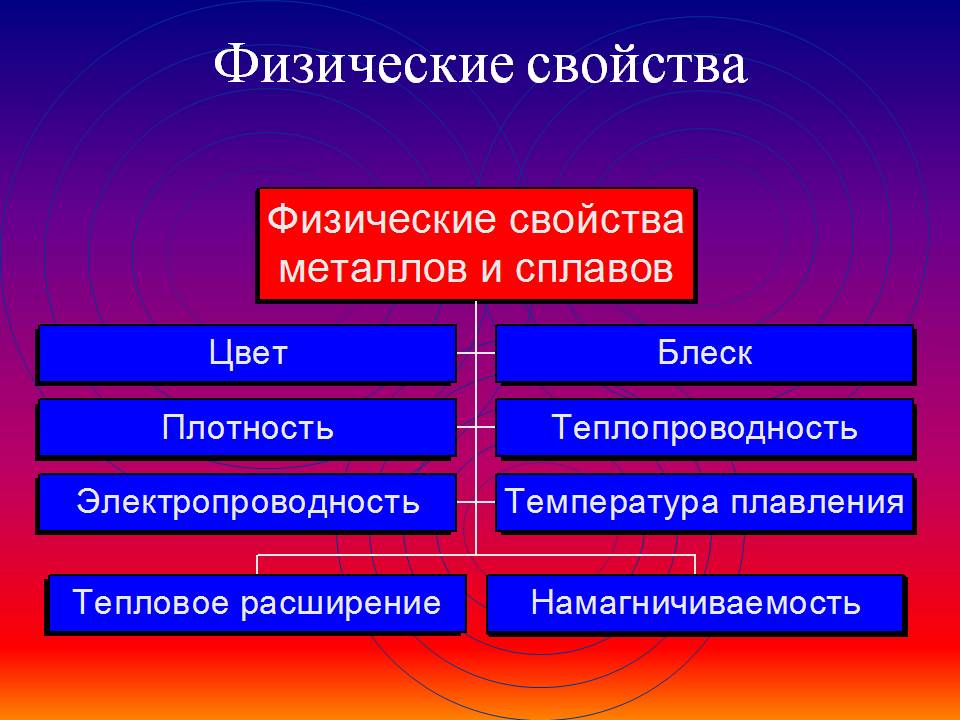
Общие физические свойства металлов
Благодаря наличию свободных электронов (“электронного газа”) в кристаллической решетке все металлы проявляют следующие характерные общие свойства:
1) Пластичность – способность легко менять форму, вытягиваться в проволоку, прокатываться в тонкие листы.
2) Металлический блеск и непрозрачность. Это связано со взаимодействием свободных электронов с падающими на металл светом.
3) Электропроводность. Объясняется направленным движением свободных электронов от отрицательного полюса к положительному под влиянием небольшой разности потенциалов. При нагревании электропроводность уменьшается, т.к. с повышением температуры усиливаются колебания атомов и ионов в узлах кристаллической решетки, что затрудняет направленное движение “электронного газа”.
4) Теплопроводность. Обусловлена высокой подвижностью свободных электронов, благодаря чему происходит быстрое выравнивание температуры по массе металла. Наибольшая теплопроводность – у висмута и ртути.
5) Твердость. Самый твердый – хром (режет стекло); самые мягкие – щелочные металлы – калий, натрий, рубидий и цезий – режутся ножом.
6) Плотность. Она тем меньше, чем меньше атомная масса металла и больше радиус атома. Самый легкий – литий (ρ=0,53 г/см3); самый тяжелый – осмий (ρ=22,6 г/см3). Металлы, имеющие плотность менее 5 г/см3 считаются “легкими металлами”.
7) Температуры плавления и кипения. Самый легкоплавкий металл – ртуть (т.пл. = -39°C), самый тугоплавкий металл – вольфрам (t°пл. = 3390°C). Металлы с t°пл. выше 1000°C считаются тугоплавкими, ниже – низкоплавкими.
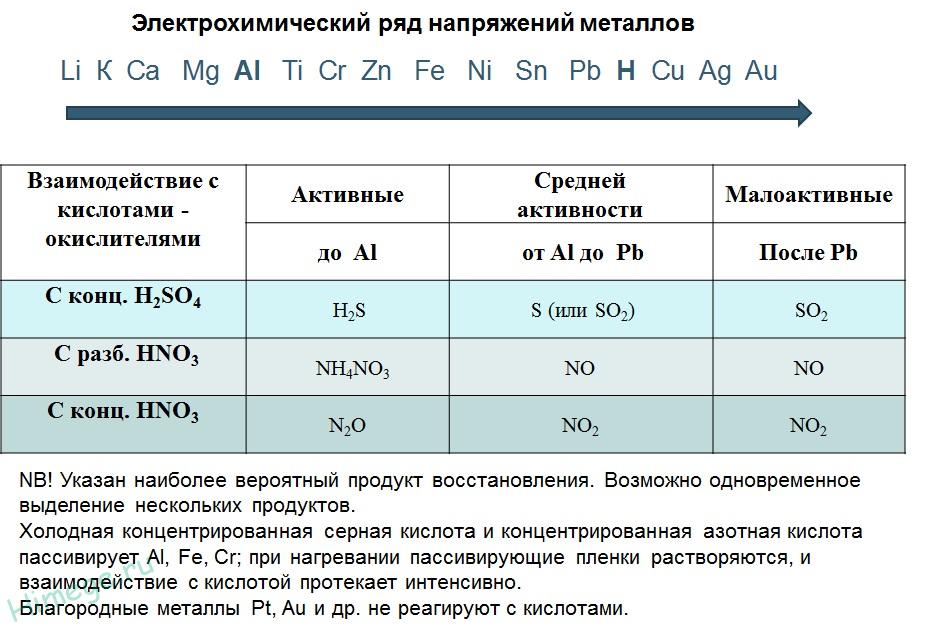
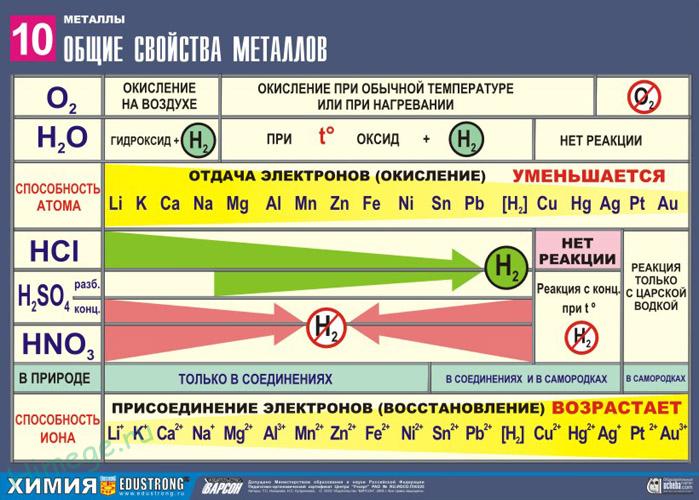
Общие химические свойства металлов
Сильные восстановители: Me0 – nē → Men+
Ряд напряжений характеризует сравнительную активность металлов в окислительно-восстановительных реакциях в водных растворах.
1. Реакции металлов с неметаллами
1) С кислородом:
2Mg + O2 → 2MgO
2) С серой:
Hg + S → HgS
3) С галогенами:
Ni + Cl2 –t°→ NiCl2
4) С азотом:
3Ca + N2 –t°→ Ca3N2
5) С фосфором:
3Ca + 2P –t°→ Ca3P2
6) С водородом (реагируют только щелочные и щелочноземельные металлы):
2Li + H2 → 2LiH
Ca + H2 → CaH2
2. Реакции металлов с кислотами
1) Металлы, стоящие в электрохимическом ряду напряжений до H восстанавливают кислоты-неокислители до водорода:
Mg + 2HCl → MgCl2 + H2
2Al+ 6HCl → 2AlCl3 + 3H2
6Na + 2H3PO4 → 2Na3PO4 + 3H2
2) С кислотами-окислителями:
При взаимодействии азотной кислоты любой концентрации и концентрированной серной с металлами водород никогда не выделяется!

Zn + 2H2SO4(К) → ZnSO4 + SO2 + 2H2O
4Zn + 5H2SO4(К) → 4ZnSO4 + H2S + 4H2O
3Zn + 4H2SO4(К) → 3ZnSO4 + S + 4H2O
2H2SO4(к) + Сu → Сu SO4 + SO2 + 2H2O
10HNO3 + 4Mg → 4Mg(NO3)2 + NH4NO3 + 3H2O
4HNO3(к) + Сu → Сu (NO3)2 + 2NO2 + 2H2O
3. Взаимодействие металлов с водой
1) Активные (щелочные и щелочноземельные металлы) образуют растворимое основание (щелочь) и водород:
2Na + 2H2O → 2NaOH + H2
Ca+ 2H2O → Ca(OH)2 + H2
2) Металлы средней активности окисляются водой при нагревании до оксида:
Zn + H2O –t°→ ZnO + H2
3) Неактивные (Au, Ag, Pt) – не реагируют.
4. Вытеснение более активными металлами менее активных металлов из растворов их солей:
Cu + HgCl2 → Hg+ CuCl2
Fe+ CuSO4 → Cu+ FeSO4
В промышленности часто используют не чистые металлы, а их смеси — сплавы, в которых полезные свойства одного металла дополняются полезными свойствами другого. Так, медь обладает невысокой твердостью и малопригодна для изготовления деталей машин, сплавы же меди с цинком (латунь) являются уже достаточно твердыми и широко используются в машиностроении. Алюминий обладает высокой пластичностью и достаточной легкостью (малой плотностью), но слишком мягок. На его основе готовят сплав с магнием, медью и марганцем – дуралюмин (дюраль), который, не теряя полезных свойств алюминия, приобретает высокую твердость и становится пригодным в авиастроении. Сплавы железа с углеродом (и добавками других металлов) – это широко известные чугун и сталь.
Металлы в свободном виде являются восстановителями. Однако реакционная способность некоторых металлов невелика из-за того, что они покрыты поверхностной оксидной пленкой, в разной степени устойчивой к действию таких химических реактивов, как вода, растворы кислот и щелочей.
Например, свинец всегда покрыт оксидной пленкой, для его перехода в раствор требуется не только воздействие реактива (например, разбавленной азотной кислоты), но и нагревание. Оксидная пленка на алюминии препятствует его реакции с водой, но под действием кислот и щелочей разрушается. Рыхлая оксидная пленка (ржавчина), образующаяся на поверхности железа во влажном воздухе, не мешает дальнейшему окислению железа.
Под действием концентрированных кислот на металлах образуется устойчивая оксидная пленка. Это явление называется пассивацией. Так, в концентрированной серной кислоте пассивируются (и после этого не реагируют с кислотой) такие металлы, как Ве, Вi, Со, Fе, Мg и Nb, а в концентрированной азотной кислоте – металлы А1, Ве, Вi, Со, Сг, Fе, Nb, Ni, РЬ, Тh и U.
При взаимодействии с окислителями в кислых растворах большинство металлов переходит в катионы, заряд которых определяется устойчивой степенью окисления данного элемента в соединениях (Nа+, Са2+,А13+,Fе2+ и Fе3+)
Восстановительная активность металлов в кислом растворе передается рядом напряжений. Большинство металлов переводится в раствор соляной и разбавленной серной кислотами, но Сu, Аg и Нg – только серной (концентрированной) и азотной кислотами, а Рt и Аи – «царской водкой».
Коррозия металлов
Нежелательным химическим свойством металлов является их коррозия, т. е. активное разрушение (окисление) при контакте с водой и под воздействием растворенного в ней кислорода (кислородная коррозия). Например, широко известна коррозия железных изделий в воде, в результате чего образуется ржавчина, и изделия рассыпаются в порошок.
Коррозия металлов протекает в воде также из-за присутствия растворенных газов СО2 и SО2; создается кислотная среда, и катионы Н+ вытесняются активными металлами в виде водорода Н2 (водородная коррозия).
Особенно коррозионно-опасным может быть место контакта двух разнородных металлов (контактная коррозия). Между одним металлом, например Fе, и другим металлом, например Sn или Сu, помещенными в воду, возникает гальваническая пара. Поток электронов идет от более активного металла, стоящего левее в ряду напряжений (Ре), к менее активному металлу (Sn, Сu), и более активный металл разрушается (корродирует).
Именно из-за этого ржавеет луженая поверхность консервных банок (железо, покрытое оловом) при хранении во влажной атмосфере и небрежном обращении с ними (железо быстро разрушается после появления хотя бы небольшой царапины, допускающей контакт железа с влагой). Напротив, оцинкованная поверхность железного ведра долго не ржавеет, поскольку даже при наличии царапин корродирует не железо, а цинк (более активный металл, чем железо).
Сопротивление коррозии для данного металла усиливается при его покрытии более активным металлом или при их сплавлении; так, покрытие железа хромом или изготовление сплава железа с хромом устраняет коррозию железа. Хромированное железо и сталь, содержащая хром (нержавеющая сталь), имеют высокую коррозионную стойкость.
Различают технологические, физические, механические и химические свойства металлов. К физическим относят удельный вес, цвет, электропроводность. К характеристикам этой группы относятся также теплопроводность, плавкость и плотность металла.
К механическим характеристикам относят пластичность, упругость, твердость, прочность, вязкость.
Химические свойства металлов включают в себя коррозийную стойкость, растворимость и окисляемость.
Такие характеристики, как «жидкотекучесть», прокаливаемость, свариваемость, ковкость, являются технологическими.
Физические свойства
- Цвет. Металлы не пропускают свет сквозь себя, то есть непрозрачны. В отраженном свете каждый элемент обладает своим собственным оттенком – цветом. Среди технических металлов окраску имеет только медь и сплавы с ней. Для остальных элементов характерным является оттенок от серебристо-белого до серо-стального.
- Плавкость. Эта характеристика указывает на способность элемента под воздействием температуры переходить в жидкое состояние из твердого. Плавкость считается важнейшим свойством металлов. В процессе нагревания все металлы из твердого состояния переходят в жидкое. При охлаждении же расплавленного вещества происходит обратный переход – из жидкого в твердое состояние.
- Электропроводность. Данная характеристика свидетельствует о способности переноса свободными электронами электричества. Электропроводность металлических тел в тысячи раз больше, чем неметаллических. При увеличении температуры показатель проводимости электричества снижается, а при уменьшении температуры, соответственно, повышается. Необходимо отметить, что электропроводность сплавов будет всегда ниже, нежели какого-либо металла, составляющего сплав.
- Магнитные свойства. К явно магнитным (ферромагнитным) элементам относят только кобальт, никель, железо, а также ряд их сплавов. Однако в процессе нагревания до определенной температуры указанные вещества теряют магнитность. Отдельные сплавы железа при комнатной температуре не относятся к ферромагнитным.
- Теплопроводность. Эта характеристика указывает на способность перехода тепла к менее нагретому от более нагретого тела без видимого перемещения составляющих его частиц. Высокий уровень теплопроводности позволяет равномерно и быстро нагревать и охлаждать металлы. Среди технических элементов наибольшим показателем обладает медь.
Металлы в химии занимают отдельное место. Наличие соответствующих характеристик позволяет применять то или иное вещество в определенной области.
Химические свойства металлов
- Коррозийная стойкость. Коррозией называют разрушение вещества в результате электрохимического или химического взаимоотношения с окружающей средой. Самым распространенным примером считается ржавление железа. Коррозийная стойкость относится к важнейшим природным характеристикам ряда металлов. В связи с этим такие вещества, как серебро, золото, платина получили название благородных. Обладает высокой коррозийной сопротивляемостью никель и прочие цветные металлы. Черные металлы подвержены разрушению быстрее и сильнее, нежели цветные.
- Окисляемость. Эта характеристика указывает на способность элемента вступать в реакцию с О2 под влиянием окислителей.
- Растворимость. Металлы, обладающие в жидком состоянии неограниченной растворимостью, при затвердении могут формировать твердые растворы. В этих растворах атомы от одного компонента встраиваются в кристаллическую решетку другого составляющего только в определенных пределах.
Необходимо отметить, что физические и химические свойства металлов являются одними из основных характеристик этих элементов.

Металлы (от лат. metallum — шахта, рудник) — группа элементов, в виде простых веществ обладающих характерными металлическими свойствами, такими как высокие тепло- и электропроводность, положительный температурный коэффициент сопротивления, высокая пластичность и металлический блеск.
Из 118 химических элементов, открытых на данный момент (из них не все официально признаны), к металлам относят:
- 6 элементов в группе щелочных металлов,
- 6 в группе щёлочноземельных металлов,
- 38 в группе переходных металлов,
- 11 в группе лёгких металлов,
- 7 в группе полуметаллов,
- 14 в группе лантаноиды + лантан,
- 14 в группе актиноиды (физические свойства изучены не у всех элементов) + актиний,
- вне определённых групп бериллий и магний.
Таким образом, к металлам, возможно, относится 96 элементов из всех открытых.
В астрофизике термин «металл» может иметь другое значение и обозначать все химические элементы тяжелее гелия
Характерные свойства металлов
- Металлический блеск (характерен не только для металлов: его имеют и неметаллы иод и углерод в виде графита)
- Хорошая электропроводность
- Возможность лёгкой механической обработки
- Высокая плотность (обычно металлы тяжелее неметаллов)
- Высокая температура плавления (исключения: ртуть, галлий и щелочные металлы)
- Большая теплопроводность
- В реакциях чаще всего являются восстановителями.
Физические свойства металлов
Все металлы (кроме ртути и, условно, франция) при нормальных условиях находятся в твёрдом состоянии, однако обладают различной твёрдостью. Ниже приводится твёрдость некоторых металлов по шкале Мооса.
Температуры плавления чистых металлов лежат в диапазоне от −39 °C (ртуть) до 3410 °C (вольфрам). Температура плавления большинства металлов (за исключением щелочных) высока, однако некоторые «нормальные» металлы, например олово и свинец, можно расплавить на обычной электрической или газовой плите.
В зависимости от плотности, металлы делят на лёгкие (плотность 0,53 ÷ 5 г/см³) и тяжёлые (5 ÷ 22,5 г/см³). Самым лёгким металлом является литий (плотность 0.53 г/см³). Самый тяжёлый металл в настоящее время назвать невозможно, так как плотности осмия и иридия — двух самых тяжёлых металлов — почти равны (около 22.6 г/см³ — ровно в два раза выше плотности свинца), а вычислить их точную плотность крайне сложно: для этого нужно полностью очистить металлы, ведь любые примеси снижают их плотность.
Большинство металлов пластичны, то есть металлическую проволоку можно согнуть, и она не сломается. Это происходит из-за смещения слоёв атомов металлов без разрыва связи между ними. Самыми пластичными являются золото, серебро и медь. Из золота можно изготовить фольгу толщиной 0.003 мм, которую используют для золочения изделий. Однако не все металлы пластичны. Проволока из цинка или олова хрустит при сгибании; марганец и висмут при деформации вообще почти не сгибаются, а сразу ломаются. Пластичность зависит и от чистоты металла; так, очень чистый хром весьма пластичен, но, загрязнённый даже незначительными примесями, становится хрупким и более твёрдым. Некоторые металлы такие как золото, серебро, свинец, алюминий, осмий могут срастаться между собой, но на это может уйти десятки лет.
Все металлы хорошо проводят электрический ток; это обусловлено наличием в их кристаллических решётках подвижных электронов, перемещающихся под действием электрического поля. Серебро, медь и алюминий имеют наибольшую электропроводность; по этой причине последние два металла чаще всего используют в качестве материала для проводов. Очень высокую электропроводность имеет также натрий, в экспериментальной аппаратуре известны попытки применения натриевых токопроводов в форме тонкостенных труб из нержавеющей стали, заполненных натрием. Благодаря малому удельному весу натрия, при равном сопротивлении натриевые «провода» получаются значительно легче медных и даже несколько легче алюминиевых.
Высокая теплопроводность металлов также зависит от подвижности свободных электронов. Поэтому ряд теплопроводностей похож на ряд электропроводностей и лучшим проводником тепла, как и электричества, является серебро. Натрий также находит применение как хороший проводник тепла; широко известно, например, применение натрия в клапанах автомобильных двигателей для улучшения их охлаждения.
Цвет у большинства металлов примерно одинаковый — светло-серый с голубоватым оттенком. Золото, медь и цезий соответственно жёлтого, красного и светло-жёлтого цвета.
Химические свойства металлов
На внешнем электронном уровне у большинства металлов небольшое количество электронов (1-3), поэтому они в большинстве реакций выступают как восстановители (то есть «отдают» свои электроны)
Реакции с простыми веществами
- С кислородом реагируют все металлы, кроме золота, платины. Реакция с серебром происходит при высоких температурах, но оксид серебра(II) практически не образуется, так как он термически неустойчив. В зависимости от металла на выходе могут оказаться оксиды, пероксиды, надпероксиды:
оксид лития
пероксид натрия
надпероксид калия
Чтобы получить из пероксида оксид, пероксид восстанавливают металлом:
Со средними и малоактивными металлами реакция происходит при нагревании:
- С азотом реагируют только самые активные металлы, при комнатной температуре взаимодействует только литий, образуя нитриды:
При нагревании:
- С серой реагируют все металлы, кроме золота и платины:
Железо взаимодействует с серой при нагревании, образуя сульфид:
- С водородом реагируют только самые активные металлы, то есть металлы IA и IIA групп кроме Be. Реакции осуществляются при нагревании, при этом образуются гидриды. В реакциях металл выступает как восстановитель, степень окисления водорода −1:
- С углеродом реагируют только наиболее активные металлы. При этом образуются ацетилениды или метаниды. Ацетилениды при взаимодействии с водой дают ацетилен, метаниды — метан.
Взаимодействие кислот с металлами
Взаимодействие неокисляющих кислот с металлами, стоящими в электрическом ряду активности металлов до водорода
Происходит реакция замещения, которая также является окислительно-восстановительной:
Взаимодействие серной кислоты H2SO4 с металлами
Окисляющие кислоты могут взаимодействовать и с металлами, стоящими в ЭРАМ после водорода:
Очень разбавленная кислота реагирует с металлом по классической схеме:
При увеличении концентрации кислоты образуются различные продукты:
Реакции для азотной кислоты (HNO3)
При взаимодействии с активными металлами вариантов реакций ещё больше:
Когда-то пресловутая фраза «люди гибнут за сталь» была символом важности данного материала в жизни людей. Да и сегодня он не потерял своей актуальности. Он активно используется в самых разных областях жизнедеятельности человека, начиная со строительства и производства высокотехнологичных изделий, заканчивая предметами роскоши и украшениями. По этой причине свойства интенсивно исследовались и сейчас изучаются ведущими умами и крупнейшими корпорациями.
Что же это такое?
На сегодняшний день известно огромное количество различных металлов. Каждый из них обладает определенными характеристиками, отличающим его от других химических элементов или материалов. Может ли стекло быть прочнее стали? Кажется вопрос глупый и ответ на него более чем однозначный – нет. Но те, кто думает, что стекло материал хрупкий, ошибаются и не знают современных технологий сжатия стекла, которые делают его в 7 раз крепче стали. Поэтому, если выбираете стеклянные банки от производителя, стоит об этом знать.
Однако существуют определенные признаки, которые однозначно говорят, что мы имеем дело с металлическим компонентом:
- Высокая теплопроводность и низкое электрическое сопротивление. Другие составы не обладают таким сочетанием. К примеру, графит проводит электричество, но не тепло.
- Присутствие блеска в области излома.
- Подверженность ковке.
- Кристаллы в структуре.
Какие виды встречаются?
Свойства металлов во многом зависят от того, к какому виду тот или иной ингредиент относится. В этом ракурсе стоит выделить черные и цветные компоненты.

Чермет
Данная группа считается самой распространенной и востребованной в объемном ракурсе. Свое название они получили благодаря своему цвету – темному. При этом отличительной особенностью черных руд считается низкая стоимость.
В свою очередь, классифицируется на:
- железные – сюда стоит отнести железосодержащие материалы и основы, а также никелевые и кобальтовые сплавы;
- тугоплавкие основания для сплавов (имеют температуру плавления равную или превышающую 1600 градусов Цельсия, что является достаточно высоким показателем);
- низкопрочностные редкоземельные элементы, такие как церий, неодим и другие (активно используются в производстве микроэлектроники).

Цветмет
Принято считать, что эта группа элементов отличается меньшими прочностными характеристиками, температурой плавления, устойчивостью к механическим нагрузкам, но более солидной стоимостью. Понятно, что по всем этим позициям встречаются исключения.
Цветные ранжируют на следующие категории:
- Легкие – литий, натрий и так далее. Они характеризуются небольшой плотностью – до 5 тонн на метр кубический. Это всего в 5 раз больше воды.
- Тяжелые – свинец, серебро, золото. Их плотность в разы выше легких.
- Благородные – те же золото и серебро, а также платина, плутоний.
Также поделить «цветные» разновидности можно на тугоплавкие и легкоплавкие.
Сплавы – основная форма представления
В чистом виде подобного рода элементы в природе и жизнедеятельности человека не встречаются. Да и без примесей они не просто неустойчивы, но бесполезны. Даже золотые и серебряные мерные слитки в банках имеют определенный процент добавок, в том числе и для увеличения прочностных характеристик. Кстати, они в буквальном смысле меняются кардинальным образом от варианта метсплава.
Физические свойства металлов
В данном случае речь идет о различных визуальных аспектах, а также параметрах, связанных с физикой. Можно привести сравнительную таблицу:
| Показатели | Категории | Примеры |
| Электрическая проводность | проводник диэлектрик | железо магний |
| Температура плавления | низкая высокая | ртуть хром |
| Удельный вес | малый большой | берилий осьмий |
| твердость | мягкий высокотвердый | натрий вольфрам |
На практике знание физических свойств металла описывает сферу использования того или иного мономатериала. В частности, электропроводность определяет область применения в электронике, как вариант, германий – полупроводники, серебро – дорожки микросхем.
К физ. характеристикам также относят цветопередачу – зрительный параметр, который может изменяться под воздействием различных факторов, например, температуры или наличия-отсутствия защитного покрытия. Многие цвета, кстати, были названы в честь хим. элементов – золотой, серебристый, медный и так далее.
Химические свойства металлов
Таблица Менделеева на треть состоит из рассматриваемых в данной статье моноэлементов. С практической точки для обывателя, да и специалиста, эти аспекты определяют их взаимодействие с окружающими агрессивными средами, такими как реагенты из воздушной массы, влажность, перепады температурных показателей, как суточных, так и годовых.
В этом ракурсе металлопозиции утрировано разделяются на следующие группы:
- Активные. В качестве примеров можно привести литий, калий, барий, кальций, натрий.
- Среднеактивные – магний, алюминий, марганец, цинк, хром, железо, никель, серебро.
- Малоактивные. Речь идет о меди, золотых слитках, платине и иных инертных компонентах.
Соединение с простыми веществами
Самым популярным в мире соединением, которое формируется между двумя одинаковыми элементами – это, безусловно, оксид. Ярким примером, который считается весьма распространенным и не очень приятным с практической точки зрения, считается окись железа – ржавчина (каждый из нас сталкивался с коррозионными процессами):
2FE + O2 = 2FEO.
Важно знать, что благородные металлоэлементы, такие как серебро, золото и платина, оксиды в обычных условиях не образуют. Это и является одной из основных причин их высокой стоимости.
О взаимодействии с галогенами (фтором, хлором и другими позициями, которые присутствуют в окружающей среде) также не стоит забывать. Вариант: образование солей:
2Na + Cl2 = 2 NaCl.
Реакции со сложными соединениями
Здесь в первую очередь необходимо отметить взаимодействие щелочей с водой. Такие реакции всегда сопровождаются выделение водорода, что на практике чревато формированием взрывоопасной среды.
Среднеактивные также могут реагировать с H2O. Однако происходит это при достаточно высоких температурах, поэтому в обычных условиях повышения концентрации водорода не стоит.
Механические свойства металлов
Данные сведения не рассматриваются как расчетные величины. Они определяются в процессе экспериментальных изысканий, в частности, деформации заготовок на растяжение и сжатие с применением специализированного оборудования.
Основными называют:
- Прочность. Под этим аспектом принято понимать способность сохранять кристалическую целостность под воздействием мех. нагрузок различного типа, как статических, так и динамических, в том числе ударного формата. Чем прочнее монометалл, тем он долговечнее в тех конструкциях, где материал подвергается серьезным перегрузкам. Особенно это бывает актуально в тех областях, где от прочностных показателей зависит жизнь и здоровье человека, например, на транспорте.
- Пластичность – характеристика, отражающая потенциал того или иного моноэлемента либо сплава под усилиями от внешних сил изменять свою геометрию и объем. При этом, опять же, физического разрушения кристаллической решетки не должно быть.
- Твердость. Понятно, что подавляющее большинство металлических брусков руками не проверишь – для железа и алюминия ощущения будут одинаковыми. Для этого используются специальные приспособления – приборы Бриннеля или изобретение Роквелла. В первом случае в образец пытаются «впихнуть» сильнозакаленный шар, во втором – алмазную пирамиду. По размеру следа от давления и устанавливается плотность того или иного состава.
Здесь важно понимать, что прочность и твердость – это разные механические свойства металлов, порой, даже не взаимозначимые. Твердые образцы могут быть хрупкими.
- Ударная вязкость. Как следует из названия речь идет о возможности противостоять нагрузкам при целенаправленных ударах. Измеряется в джоулях на сантиметр кубический.
- Упругость. Под действием различного рода сил образец изменяет свою форму и объем. Способность восстановить свои начальные параметры и определяют упругость.
Также к механике относятся конструкторские особенности – надежность, живучесть, долговечность.
Технологические характеристики
При оценке целесообразности выбора того или иного металла для решения конкретных практических, производственных задач, необходимо учитывать:
- Ковкость. Под давлением производится обработка изделий. При этом полного разрушения не наблюдается, однако структура кристаллической решетки изменяется. В результате могут меняться механические, физические и даже химические факторы изделий.
- Свариваемость. Возможность формирования сварных соединений с применением стандартных технологий.
- Усадка – определяется соответствующим коэффициентом. При нагреве любой объект расширяется, после охлаждения – уменьшается. Так вот соотношение и определяет данное свойство. Кстати, далеко не всегда малое усадочное значение являет собой благо. К примеру, ртутные термометры работают именно за счет предельно большого коэффициента расширения.
- Податливость режущим инструментам. С технологической точки зрения производственную ценность имеет только тот компонент, который можно сравнительно просто обработать или изготовить этот самый технический инструментарий.
Рассматриваемые направления характеризуют поведение уже готовых производственных изделий, товаров в процессе эксплуатации.
Таким образом, металлы – весьма распространенный материал, который активно используется в самых разных областях жизнедеятельности. Это обусловлено широкой вариативностью физических, химических, механических параметров продукции.
